1 . 二氧化碳与氢气催化合成乙烯具有重要的意义。将 和
和 按物质的量之比1:3加入VL的密闭容器中,压强为0.1MPa,反应达到平衡状态时,各组分的物质的量分数x随温度T的变化如下图所示。
按物质的量之比1:3加入VL的密闭容器中,压强为0.1MPa,反应达到平衡状态时,各组分的物质的量分数x随温度T的变化如下图所示。
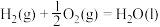
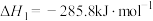
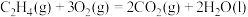
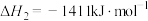

下列说法不正确 的是
 和
和 按物质的量之比1:3加入VL的密闭容器中,压强为0.1MPa,反应达到平衡状态时,各组分的物质的量分数x随温度T的变化如下图所示。
按物质的量之比1:3加入VL的密闭容器中,压强为0.1MPa,反应达到平衡状态时,各组分的物质的量分数x随温度T的变化如下图所示。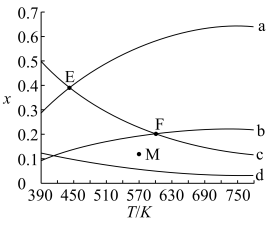
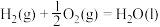
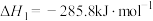
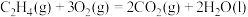
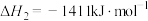

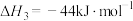
下列说法
A. 与 与 合成 合成 反应的热化学方程式: 反应的热化学方程式: 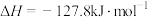 |
B.图中b、d分别表示 、 、 的变化曲线 的变化曲线 |
C.570K、0.2MPa反应达到平衡状态时,M点显示的可能是 的物质的量分数 的物质的量分数 |
D. 与 与 合成 合成 反应的 反应的 |
您最近一年使用:0次
22-23高三上·北京朝阳·期中
名校
2 . 2022北京冬奥会采用氢气作为火炬燃料,选择氢能汽车作为赛事交通服务用车,充分体现了绿色奥运的理念。已知:
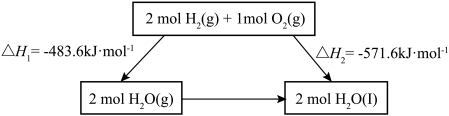
下列说法不正确 的是

下列说法
| A.氢气既可以通过燃烧反应提供热能,也可以设计成燃料电池提供电能 |
B. 的过程中, 的过程中, , , |
C.断裂2mol 和1mol 和1mol 中化学键所需能量大于断裂2mol 中化学键所需能量大于断裂2mol 中化学键所需能量 中化学键所需能量 |
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关 ,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
2022-11-04更新
|
616次组卷
|
9卷引用:北京市第四中学2022-2023学年高三上学期阶段测试2化学试题
名校
3 . 二甲醚( )是重要的化工原料,可用水煤气(主要成分为CO和
)是重要的化工原料,可用水煤气(主要成分为CO和 )合成。其主要反应原理如下(a、b、c均为正值):
)合成。其主要反应原理如下(a、b、c均为正值):
①
 kJ⋅mol
kJ⋅mol
②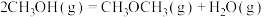
 kJ·mol
kJ·mol
③
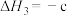 kJ⋅mol
kJ⋅mol
回答下列问题:
(1)总反应的热化学方程式: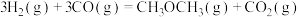

_______ kJ/mol。
(2)以下说法能说明反应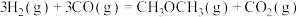 达到化学平衡状态的有
达到化学平衡状态的有_______ 。
a.恒温恒容条件下,气体的密度保持不变
b.恒温恒压条件下,气体的平均摩尔质量保持不变
c.绝热体系中,体系的温度保持不变
(3)生产二甲醚的过程中存在副反应: ,与甲醇脱水反应:
,与甲醇脱水反应: 形成竞争。将水煤气按一定进料比通入反应装置,选择合适的催化剂。在保持温度一定改变压强条件下测得二甲醚的选择性如下图所示。
形成竞争。将水煤气按一定进料比通入反应装置,选择合适的催化剂。在保持温度一定改变压强条件下测得二甲醚的选择性如下图所示。
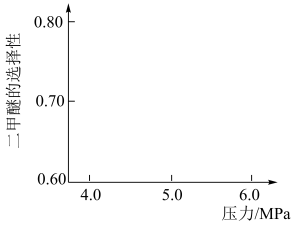
资料:二甲醚的选择性是指转化为二甲醚的CO在全部CO反应物中所占的比例。
分析:温度一定,随压强增大,二甲醚选择性增大的原因是_______ 。
 )是重要的化工原料,可用水煤气(主要成分为CO和
)是重要的化工原料,可用水煤气(主要成分为CO和 )合成。其主要反应原理如下(a、b、c均为正值):
)合成。其主要反应原理如下(a、b、c均为正值):①

 kJ⋅mol
kJ⋅mol
②
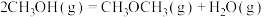
 kJ·mol
kJ·mol
③

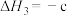 kJ⋅mol
kJ⋅mol
回答下列问题:
(1)总反应的热化学方程式:
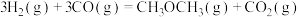

(2)以下说法能说明反应
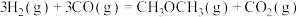 达到化学平衡状态的有
达到化学平衡状态的有a.恒温恒容条件下,气体的密度保持不变
b.恒温恒压条件下,气体的平均摩尔质量保持不变
c.绝热体系中,体系的温度保持不变
(3)生产二甲醚的过程中存在副反应:
 ,与甲醇脱水反应:
,与甲醇脱水反应: 形成竞争。将水煤气按一定进料比通入反应装置,选择合适的催化剂。在保持温度一定改变压强条件下测得二甲醚的选择性如下图所示。
形成竞争。将水煤气按一定进料比通入反应装置,选择合适的催化剂。在保持温度一定改变压强条件下测得二甲醚的选择性如下图所示。
资料:二甲醚的选择性是指转化为二甲醚的CO在全部CO反应物中所占的比例。
分析:温度一定,随压强增大,二甲醚选择性增大的原因是
您最近一年使用:0次
名校
4 . 中国科学家在淀粉人工光合成方面取得重大突破性进展,该实验方法首先将CO2催化还原为CH3OH。已知CO2催化加氢的主要反应有:
① CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
② CO2(g) + H2(g) CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
其他条件不变时,在相同时间内温度对CO2催化加氢的影响如下图。下列说法不正确 的是
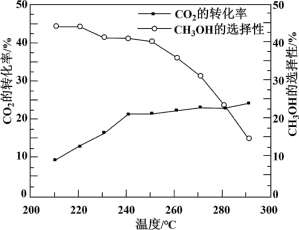
【注】CH3OH的选择性=
① CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol② CO2(g) + H2(g)
 CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol其他条件不变时,在相同时间内温度对CO2催化加氢的影响如下图。下列说法

【注】CH3OH的选择性=

A.CO(g) + 2H2(g) CH3OH(g) ΔH=- 90.6 kJ/mol CH3OH(g) ΔH=- 90.6 kJ/mol |
| B.使用催化剂,能降低反应的活化能,增大活化分子百分数 |
| C.其他条件不变,增大压强,有利于反应向生成CH3OH的方向进行 |
| D.220~240 ℃,升高温度,对反应②速率的影响比对反应①的小 |
您最近一年使用:0次
2023-02-16更新
|
613次组卷
|
13卷引用:北京市西城区2021~2022学年高三上学期期末考试化学试题
北京市西城区2021~2022学年高三上学期期末考试化学试题北京市第一六一中学2022-2023学年高三上学期10月月考化学试题北京市北京师范大学附属中学2022-2023学年高二上学期期中考试化学试题 北京市回民学校2023-2024学年高三上学期统练二化学试题北京市第十五中学2023-2024学年高二上学期期中考试化学试题北京一零一中学2022-2023学年高三上学期统练六化学试题北京市第二十中学2022-2023学年高三下学期开学检测化学试题北京市一0一中学2022-2023学年高二下学期期中考试化学试题新疆阿克苏地区等2地新疆生产建设兵团第一师第二高级中学等2校2022-2023学年高三下学期2月月考化学试题福建省南平第一中学2023-2024学年高三上学期10月月考化学试题广东省广州市实验外语学校2023-2024学年高二上学期11月期中考试化学试题北京市育才学校2023-2024学年高一上学期化学期中试题北京师范大学附属实验中学2023-2024学年高二下学期开学检测化学试题
5 . 二氧化碳捕获技术用于去除气流中的二氧化碳或者分离出二氧化碳作为气体产物,其中CO2催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有催化剂时的能量变化。

(1)从图可知,有催化剂存在的是过程_______ (填“Ⅰ”或“Ⅱ”)。
(2)写出图中CO2催化合成甲醇的热化学方程式:_______ 。
(3)已知:1mol液态甲醇完全气化需吸热37.4kJ,1mol液态水完全气化需吸热44.0kJ,由CO2合成1mol液态甲醇和1mol液态水将_______ (填“吸收”或“放出”)_______ kJ热量。
(4)关于CO2催化合成甲醇的反应,下列说法中,合理的是_______(填字母序号)。

(1)从图可知,有催化剂存在的是过程
(2)写出图中CO2催化合成甲醇的热化学方程式:
(3)已知:1mol液态甲醇完全气化需吸热37.4kJ,1mol液态水完全气化需吸热44.0kJ,由CO2合成1mol液态甲醇和1mol液态水将
(4)关于CO2催化合成甲醇的反应,下列说法中,合理的是_______(填字母序号)。
| A.该反应中所有原子都被用于合成甲醇 |
| B.该反应可用于CO2的转化,有助于缓解温室效应 |
| C.使用催化剂可以降低该反应的ΔH,从而使反应放出更多热量 |
| D.降温分离出液态甲醇和水,将剩余气体重新通入反应器,可以提高CO2与H2的利用率 |
您最近一年使用:0次
名校
解题方法
6 . 25℃ 101 kPa时,反应S(s) + O2(g) = SO2(g) ΔH = -297.23kJ/mol。下列说法中正确的是
| A.S(g) + O2(g) = SO2(g) 放出的热量大于297.23kJ |
| B.S的燃烧热为297.23kJ |
| C.相同条件下,S具有的能量高于SO2具有的能量 |
| D.形成1mol SO2的化学键释放的总能量小于断裂1mol S(g) 和1mol O2(g) 的化学键所吸收的总能量 |
您最近一年使用:0次
名校
解题方法
7 .  捕获技术用于去除气流中的
捕获技术用于去除气流中的 或者分离出
或者分离出 作为气体产物,其中
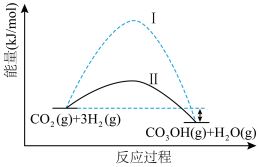
作为气体产物,其中 催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
(1)温度为523 K时,测得上述反应中生成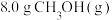 放出的热量为12.3 kJ。反应的热化学方程式为
放出的热量为12.3 kJ。反应的热化学方程式为___________ 。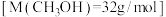
(2)从图可知,有催化剂存在的是过程___________ (填“Ⅰ”或“Ⅱ”)。
(3)一定温度下(各物质均为气态),向体积为2 L的恒容密闭容器中充入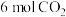 和
和 ,加入合适催化剂进行反应。某时刻测得
,加入合适催化剂进行反应。某时刻测得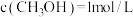 ,此时反应
,此时反应___________ (填“正向移动”、“逆向移动”或“达到平衡)。已知该温度下反应的化学平衡常数值为1/40.
(4)关于 催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
(5)制备过程中存在副反应: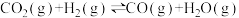
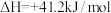 将混合气按进料比
将混合气按进料比 通入反应装置,选择合适催化剂发生反应。不同温度和压强下,
通入反应装置,选择合适催化剂发生反应。不同温度和压强下, 平衡产率和
平衡产率和 平衡转化率分别如图1、图2。
平衡转化率分别如图1、图2。
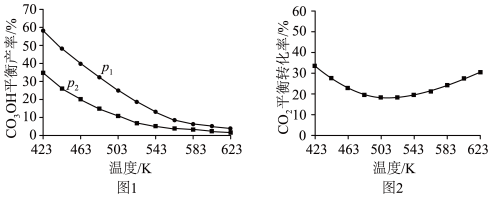
①图1中,压强
___________  (填“>”“=”或“<”),推断的依据是
(填“>”“=”或“<”),推断的依据是___________ 。
②图2中,压强为 ,温度高于503 K后,
,温度高于503 K后, 平衡转化率随温度升高而增大的原因是
平衡转化率随温度升高而增大的原因是___________ 。
 捕获技术用于去除气流中的
捕获技术用于去除气流中的 或者分离出
或者分离出 作为气体产物,其中
作为气体产物,其中 催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
(1)温度为523 K时,测得上述反应中生成
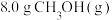 放出的热量为12.3 kJ。反应的热化学方程式为
放出的热量为12.3 kJ。反应的热化学方程式为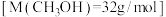
(2)从图可知,有催化剂存在的是过程
(3)一定温度下(各物质均为气态),向体积为2 L的恒容密闭容器中充入
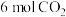 和
和 ,加入合适催化剂进行反应。某时刻测得
,加入合适催化剂进行反应。某时刻测得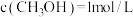 ,此时反应
,此时反应(4)关于
 催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。| A.该反应原子转化率为100% |
B.该反应可用于 的转化,有助于缓解温室效应 的转化,有助于缓解温室效应 |
C.使用催化剂可以降低该反应的 ,从而使反应放出更多热量 ,从而使反应放出更多热量 |
D.降温分离液态甲醇和水,将剩余气体重新通入反应器,可提高 与 与 的利用率 的利用率 |
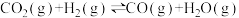
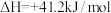 将混合气按进料比
将混合气按进料比 通入反应装置,选择合适催化剂发生反应。不同温度和压强下,
通入反应装置,选择合适催化剂发生反应。不同温度和压强下, 平衡产率和
平衡产率和 平衡转化率分别如图1、图2。
平衡转化率分别如图1、图2。
①图1中,压强

 (填“>”“=”或“<”),推断的依据是
(填“>”“=”或“<”),推断的依据是②图2中,压强为
 ,温度高于503 K后,
,温度高于503 K后, 平衡转化率随温度升高而增大的原因是
平衡转化率随温度升高而增大的原因是
您最近一年使用:0次
2021-11-15更新
|
181次组卷
|
2卷引用:北京市北师大附属实验中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
8 . CO2催化加氢制取甲醇、乙醇等低碳醇的研究,对于环境问题和能源文体都具有非常重要的意义。已知一定条件下的如下反应:
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=﹣49.0kJ•mol-1
2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(g) △H=﹣173.6kJ•mol-1
下列说法不正确的是
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=﹣49.0kJ•mol-1
2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(g) △H=﹣173.6kJ•mol-1
下列说法不正确的是
| A.CH3OH(g)+CO2(g)+3H2(g)⇌CH3CH2OH(g)+2H2O(g) △H<0 |
| B.增大压强,有利于反应向生成低碳醇的方向移动,平衡常数增大 |
| C.升高温度,可加快生成低碳醇的速率,但反应限度减小 |
| D.增大氢气浓度可以提高二氧化碳的转化率 |
您最近一年使用:0次
2021-11-07更新
|
375次组卷
|
9卷引用:北京师范大学附属中学2022-2-2023学年高三上学期统练(V)(月考)化学试题
9 . 依据图示关系,下列说法不正确 的是
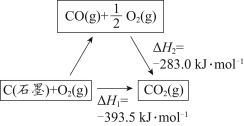

| A.石墨燃烧是放热反应 |
| B.C(石墨)+CO2(g)=2CO(g) △H=△H1-△H2 |
| C.1 mol C(石墨)和1 mol CO分别在足量O2中燃烧,全部转化为CO2,前者放热多 |
| D.化学反应的△H,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
2022-12-05更新
|
244次组卷
|
2卷引用:北京市第四十三中学2021-2022学年高二上学期12月月考化学试题
名校
解题方法
10 . 回收利用CO2是目前解决长期载人航天舱内(如空间站)供氧问题的有效途径,其物质转化如图:

(1)反应A为CO2(g)+4H2(g) CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ•mol-1
CH4(g)+2O2(g)=2H2O(g)+CO2(g) ΔH=-802.3kJ•mol-1
反应A的ΔH=____ kJ•mol-1。
(2)将原料气按n(CO2):n(H2)=1:4置于恒容密闭容器中发生反应A,在相同时间内测得H2O的物质的量分数与温度的变化曲线如图所示(虚线为平衡时的曲线)。

①理论上,能提高CO2平衡转化率的措施有____ (写出一条即可)。
②空间站的反应器内,通常采用反应器前段加热,后段冷却的方法来提高CO2的转化效率,原因是_____ 。
(3)下列关于空间站内物质和能量变化的说法中,不正确 的是_____ (填字母)。
a.反应B的能量变化是电能→化学能或光能→化学能
b.物质转化中O、H原子的利用率均为100%
c.不用Na2O2作供氧剂的原因可能是Na2O2不易实现循环利用
(4)用CO2(g)+2H2(g) C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是_____ 。

(1)反应A为CO2(g)+4H2(g)
 CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
CH4(g)+2H2O(g),是回收利用CO2的关键步骤。已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ•mol-1
CH4(g)+2O2(g)=2H2O(g)+CO2(g) ΔH=-802.3kJ•mol-1
反应A的ΔH=
(2)将原料气按n(CO2):n(H2)=1:4置于恒容密闭容器中发生反应A,在相同时间内测得H2O的物质的量分数与温度的变化曲线如图所示(虚线为平衡时的曲线)。

①理论上,能提高CO2平衡转化率的措施有
②空间站的反应器内,通常采用反应器前段加热,后段冷却的方法来提高CO2的转化效率,原因是
(3)下列关于空间站内物质和能量变化的说法中,
a.反应B的能量变化是电能→化学能或光能→化学能
b.物质转化中O、H原子的利用率均为100%
c.不用Na2O2作供氧剂的原因可能是Na2O2不易实现循环利用
(4)用CO2(g)+2H2(g)
 C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
您最近一年使用:0次
2022-09-02更新
|
316次组卷
|
4卷引用:北京市西城区2021—2022学年高二上学期期末化学试题



