1 .  资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使
资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使 转化为
转化为 。反应体系中主要反应的热化学方程式为:
。反应体系中主要反应的热化学方程式为:
反应I:

反应II: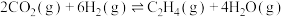

(1)基态镍原子核外电子的轨道表示式为____________
(2)将反应后气体通入______ (填试剂名称),可证明反应II发生。
(3)计算

______ (用 和
和 表示)
表示)
(4)相同投料比时,体系内 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为________ 。
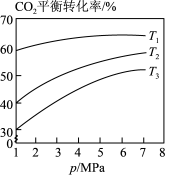
(5)向1 L恒压、密闭容器中通入1 mol 和4 mol
和4 mol  ,测得有关物质的物质的量随温度变化如图。
,测得有关物质的物质的量随温度变化如图。
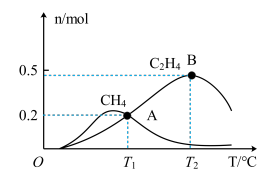
①催化剂在较低温度时主要选择______ (填“反应I”或“反应II”)
② 时
时 的转化率为
的转化率为______ ,反应I的平衡常数
______ 。
(6)镍氢催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:
 +75 kJ/mol
+75 kJ/mol
消碳反应:
 -173 kJ/mol
-173 kJ/mol
其他条件相同时,催化剂表面积碳量与温度的关系如图所示, ℃之后,温度升高积碳量减小的主要原因是
℃之后,温度升高积碳量减小的主要原因是______ 。

 资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使
资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使 转化为
转化为 。反应体系中主要反应的热化学方程式为:
。反应体系中主要反应的热化学方程式为:反应I:


反应II:
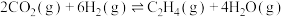

(1)基态镍原子核外电子的轨道表示式为
(2)将反应后气体通入
(3)计算


 和
和 表示)
表示)(4)相同投料比时,体系内
 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
(5)向1 L恒压、密闭容器中通入1 mol
 和4 mol
和4 mol  ,测得有关物质的物质的量随温度变化如图。
,测得有关物质的物质的量随温度变化如图。
①催化剂在较低温度时主要选择
②
 时
时 的转化率为
的转化率为
(6)镍氢催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:

 +75 kJ/mol
+75 kJ/mol消碳反应:

 -173 kJ/mol
-173 kJ/mol其他条件相同时,催化剂表面积碳量与温度的关系如图所示,
 ℃之后,温度升高积碳量减小的主要原因是
℃之后,温度升高积碳量减小的主要原因是
您最近一年使用:0次
名校
解题方法
2 . 工业上制硫酸的主要反应之一为: ,反应过程中能量的变化如图所示。
,反应过程中能量的变化如图所示。
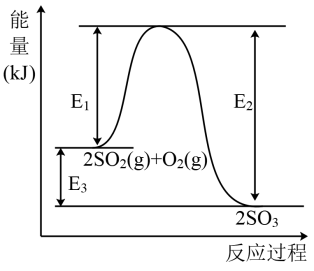
(1)向反应体系中加入催化剂后,图中
_______ (填“增大”、“减小”或“不变”,下同),
_______ 。
(2)已知:
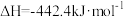

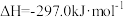
若 与
与 反应产生
反应产生 和
和 ,则反应的热化学方程式为
,则反应的热化学方程式为_______ 。
(3)某温度下,反应的起始浓度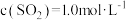 ,
,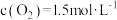 ,达到平衡后,
,达到平衡后, 的转化率为50%,则此温度下该反应的平衡常数K的数值为
的转化率为50%,则此温度下该反应的平衡常数K的数值为_______ 。
(4)在 温度时,该反应的平衡常数
温度时,该反应的平衡常数 ,若在此温度下,向
,若在此温度下,向 的恒容密闭容器中,充入
的恒容密闭容器中,充入 、
、 和
和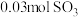 ,则反应开始时正反应速率
,则反应开始时正反应速率_______ (填“>”、“=”或“<”)逆反应速率。
(5)恒温恒容条件下,下列叙述能证明该反应已达化学平衡状态的是_______。(填字母)
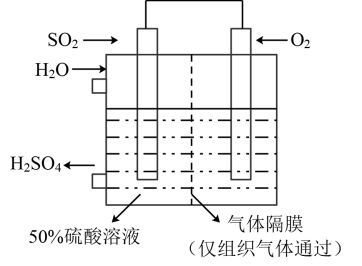
(6)若以如图所示装置生产硫酸,将 、
、 以一定压强喷到活性电极上反应。负极的电极反应式为
以一定压强喷到活性电极上反应。负极的电极反应式为_______ 。
 ,反应过程中能量的变化如图所示。
,反应过程中能量的变化如图所示。
(1)向反应体系中加入催化剂后,图中


(2)已知:

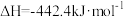

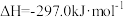
若
 与
与 反应产生
反应产生 和
和 ,则反应的热化学方程式为
,则反应的热化学方程式为(3)某温度下,反应的起始浓度
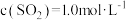 ,
,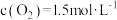 ,达到平衡后,
,达到平衡后, 的转化率为50%,则此温度下该反应的平衡常数K的数值为
的转化率为50%,则此温度下该反应的平衡常数K的数值为(4)在
 温度时,该反应的平衡常数
温度时,该反应的平衡常数 ,若在此温度下,向
,若在此温度下,向 的恒容密闭容器中,充入
的恒容密闭容器中,充入 、
、 和
和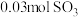 ,则反应开始时正反应速率
,则反应开始时正反应速率(5)恒温恒容条件下,下列叙述能证明该反应已达化学平衡状态的是_______。(填字母)
A. 的体积分数不再发生变化 的体积分数不再发生变化 |
| B.恒容时,容器内压强不再发生变化 |
| C.容器内,气体原子总数不再发生变化 |
D.相同时间内消耗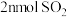 的同时生成 的同时生成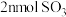 |
 、
、 以一定压强喷到活性电极上反应。负极的电极反应式为
以一定压强喷到活性电极上反应。负极的电极反应式为
您最近一年使用:0次
2022-01-21更新
|
283次组卷
|
2卷引用:北京市丰台区2021~2022学年高二上学期期末考试化学试题
3 .  和
和 是两种造成温室效应的主要气体,高温下可发生干重整反应进行综合利用,反应过程的能量变化如图所示:
是两种造成温室效应的主要气体,高温下可发生干重整反应进行综合利用,反应过程的能量变化如图所示:
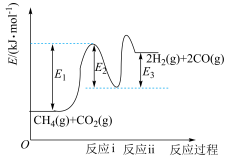
(1)干重整主反应的热化学方程式为_____ (用 、
、 、
、 表示反应热),反应速率由反应决定
表示反应热),反应速率由反应决定_____ (填“ⅰ”或“ⅱ”)。
(2)反应器中还同时存在副反应: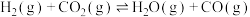
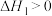
①下图表示投料比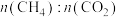 为
为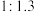 时,不同温度下的反应结果,下列说法中正确的是
时,不同温度下的反应结果,下列说法中正确的是_____ 。(填字母)
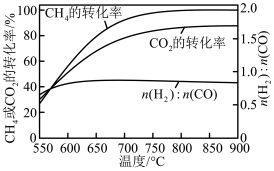
A.加压有利于增大 和
和 反应的速率但不利于提高二者的平衡转化率
反应的速率但不利于提高二者的平衡转化率
B.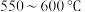 ,升温更有利于主反应,主反应先达到平衡
,升温更有利于主反应,主反应先达到平衡
C.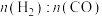 始终低于
始终低于 ,与副反应有关
,与副反应有关
②体系中会发生积炭反应
 ,为研究其热效应,还需要利用反应
,为研究其热效应,还需要利用反应_____ 的 。
。
③添加一定量的载氧剂 ,可避免积炭反应发生,增大
,可避免积炭反应发生,增大 的值,推测可能发生的反应,写出化学反应方程式
的值,推测可能发生的反应,写出化学反应方程式_____ 。
(3)文献中指出 和
和 可以发生反应生成
可以发生反应生成 和
和 ,且反应进行程度较大,但干重整反应器中进行程度小。结合键能数据,从平衡角度阐明理由
,且反应进行程度较大,但干重整反应器中进行程度小。结合键能数据,从平衡角度阐明理由_____ 。
 和
和 是两种造成温室效应的主要气体,高温下可发生干重整反应进行综合利用,反应过程的能量变化如图所示:
是两种造成温室效应的主要气体,高温下可发生干重整反应进行综合利用,反应过程的能量变化如图所示:
(1)干重整主反应的热化学方程式为
 、
、 、
、 表示反应热),反应速率由反应决定
表示反应热),反应速率由反应决定(2)反应器中还同时存在副反应:
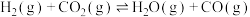
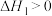
①下图表示投料比
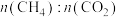 为
为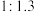 时,不同温度下的反应结果,下列说法中正确的是
时,不同温度下的反应结果,下列说法中正确的是
A.加压有利于增大
 和
和 反应的速率但不利于提高二者的平衡转化率
反应的速率但不利于提高二者的平衡转化率B.
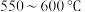 ,升温更有利于主反应,主反应先达到平衡
,升温更有利于主反应,主反应先达到平衡C.
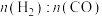 始终低于
始终低于 ,与副反应有关
,与副反应有关②体系中会发生积炭反应

 ,为研究其热效应,还需要利用反应
,为研究其热效应,还需要利用反应 。
。③添加一定量的载氧剂
 ,可避免积炭反应发生,增大
,可避免积炭反应发生,增大 的值,推测可能发生的反应,写出化学反应方程式
的值,推测可能发生的反应,写出化学反应方程式(3)文献中指出
 和
和 可以发生反应生成
可以发生反应生成 和
和 ,且反应进行程度较大,但干重整反应器中进行程度小。结合键能数据,从平衡角度阐明理由
,且反应进行程度较大,但干重整反应器中进行程度小。结合键能数据,从平衡角度阐明理由| 化学键 | 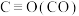 |  |  |  |
键能 | 1072 | 436 | 413 | 464 |
您最近一年使用:0次
解题方法
4 . 研究CO2的回收和综合利用对航天建设有重要意义。
Ⅰ.载人航天器中,利用萨巴蒂尔反应可将航天员呼出的CO2转化为 H2O,再通过电解H2O 获得 O2,实现O2的再生,同时还能制备CH4。已知:
反应①:CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H = −252.9kJ/mol
反应②:2H2O(l)=2H2(g)+O2(g) ∆H = +571.6kJ/mol
请回答下列问题:
(1)反应①属于___________ (填“吸热”或“放热”)反应。
(2)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
已知2CH4(g)=C2H4(g)+2H2(g) ΔH =+167kJ/mol,则a=___________ 。
Ⅱ.回收利用CO2是目前解决长期载人航天舱内(如空间站)供氧问题的有效途径,科研人员研究出其物质转化途径如下图:
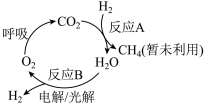
(3)反应A为CO2(g)+4H2(g) CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
已知:2H2(g) + O2(g) = 2H2O(g) ΔH = −483.6 kJ·mol−1
CH4(g) + 2O2(g) = 2H2O(g) + CO2(g) ΔH = −802.3 kJ·mol−1
反应A的ΔH =___________ kJ·mol−1
(4)将原料气按n(CO2):n(H2)=1:4置于恒容密闭容器中发生反应A,在相同时间内测得H2O的物质的量分数与温度的变化曲线如图所示(虚线为平衡时的曲线)。
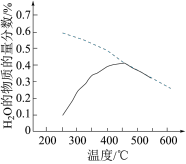
①理论上,能提高CO2平衡转化率的措施有___________ (写出一条即可)。
②空间站的反应器内,通常采用反应器前段加热,后段冷却的方法来提高CO2的转化效率,原因是___________ 。
(5)下列关于空间站内物质和能量变化的说法中,不正确 的是___________ (填字母)。
a.反应B的能量变化是电能→化学能或光能→化学能
b.物质转化中O、H原子的利用率均为100%
c.不用Na2O2作供氧剂的原因可能是Na2O2不易实现循环利用
(6)用CO2(g)+2H2(g) C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是___________ 。
Ⅰ.载人航天器中,利用萨巴蒂尔反应可将航天员呼出的CO2转化为 H2O,再通过电解H2O 获得 O2,实现O2的再生,同时还能制备CH4。已知:
反应①:CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H = −252.9kJ/mol
反应②:2H2O(l)=2H2(g)+O2(g) ∆H = +571.6kJ/mol
请回答下列问题:
(1)反应①属于
(2)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
Ⅱ.回收利用CO2是目前解决长期载人航天舱内(如空间站)供氧问题的有效途径,科研人员研究出其物质转化途径如下图:

(3)反应A为CO2(g)+4H2(g)
 CH4(g)+2H2O(g),是回收利用CO2的关键步骤。
CH4(g)+2H2O(g),是回收利用CO2的关键步骤。已知:2H2(g) + O2(g) = 2H2O(g) ΔH = −483.6 kJ·mol−1
CH4(g) + 2O2(g) = 2H2O(g) + CO2(g) ΔH = −802.3 kJ·mol−1
反应A的ΔH =
(4)将原料气按n(CO2):n(H2)=1:4置于恒容密闭容器中发生反应A,在相同时间内测得H2O的物质的量分数与温度的变化曲线如图所示(虚线为平衡时的曲线)。

①理论上,能提高CO2平衡转化率的措施有
②空间站的反应器内,通常采用反应器前段加热,后段冷却的方法来提高CO2的转化效率,原因是
(5)下列关于空间站内物质和能量变化的说法中,
a.反应B的能量变化是电能→化学能或光能→化学能
b.物质转化中O、H原子的利用率均为100%
c.不用Na2O2作供氧剂的原因可能是Na2O2不易实现循环利用
(6)用CO2(g)+2H2(g)
 C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
C(s)+2H2O(g)代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
您最近一年使用:0次
名校
解题方法
5 . 过渡金属氧化物离子(以MO+表示)在烃类的选择性氧化等方面应用广泛。MO+与CH4反应的过程如下图所示。不正确 的是
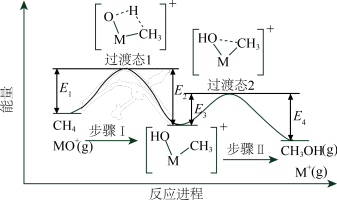
| A.反应速率:步骤I<步骤II |
| B.CH3OH分子中,键角:H—C—H>H—O—C |
| C.若MO+与CH3D反应,生成的氘代甲醇有2种 |
D.CH4(g) + MO+(g)=CH3OH(g) + M+(g)  = E2+E4-E1-E3 = E2+E4-E1-E3 |
您最近一年使用:0次
2024-04-01更新
|
572次组卷
|
5卷引用:北京市丰台区2023-2024学年高三下学期综合练习(一)化学试题
北京市丰台区2023-2024学年高三下学期综合练习(一)化学试题(已下线)通关练08 聚焦反应热、速率及化学平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)江苏省常州市第一中学2023-2024学年高二下学期4月期中考试化学试题(已下线)化学(天津卷03)-2024年高考化学押题预测卷(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
解题方法
6 . 工业上可以利用水煤气( 、
、 )合成二甲醚(
)合成二甲醚( ),同时生成
),同时生成 。合成过程中,主要发生三个反应,
。合成过程中,主要发生三个反应, ℃时,有关反应及相关数据如下。
℃时,有关反应及相关数据如下。

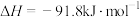
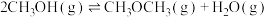
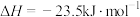


保持原料气组成、压强、反应时间等因素不变,进行实验,测得 转化率随温度变化曲线如下图。下列说法不正确的是
转化率随温度变化曲线如下图。下列说法不正确的是
 、
、 )合成二甲醚(
)合成二甲醚( ),同时生成
),同时生成 。合成过程中,主要发生三个反应,
。合成过程中,主要发生三个反应, ℃时,有关反应及相关数据如下。
℃时,有关反应及相关数据如下。
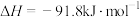
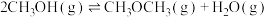
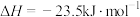


保持原料气组成、压强、反应时间等因素不变,进行实验,测得
 转化率随温度变化曲线如下图。下列说法不正确的是
转化率随温度变化曲线如下图。下列说法不正确的是
A. ℃时,水煤气合成二甲醚的热化学方程式: ℃时,水煤气合成二甲醚的热化学方程式:  |
B. ℃时,增大压强、加入催化剂均可提高 ℃时,增大压强、加入催化剂均可提高 的平衡转化率 的平衡转化率 |
C.220℃~240℃时,温度升高反应速率加快, 转化率升高 转化率升高 |
D.温度高于240℃时,温度升高 转化率降低的原因可能是平衡逆向移动 转化率降低的原因可能是平衡逆向移动 |
您最近一年使用:0次
名校
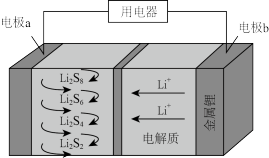
7 . 氧、硫、硒( )、碲(
)、碲( )、钋(
)、钋(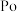 )是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
)是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
(1) 在周期表中的位置为
在周期表中的位置为_______ 。
(2)某温度时,该族单质与 反应生成气态
反应生成气态 的热化学方程式如下:
的热化学方程式如下:
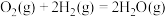

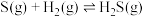


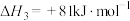
①硫和硒的氢化物的热稳定性:H2S_____ H2Se (填>、=或<);用原子结构知识解释你的判断结果_______ 。
②写出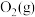 与
与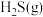 反应生成
反应生成 和
和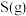 的热化学方程式
的热化学方程式_______ 。
(3)生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如图。

①步骤I反应的离子方程式为_______ 。
②生物浸出时的总反应的氧化剂是_______ 。
(4)全固态锂硫电池能量密度高,其工作原理如图所示,其中电极 常用掺有石墨烯的
常用掺有石墨烯的 材料,电池反应为:
材料,电池反应为: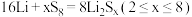 。下列说法
。下列说法错误 的是_______
 )、碲(
)、碲( )、钋(
)、钋(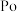 )是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
)是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:(1)
 在周期表中的位置为
在周期表中的位置为(2)某温度时,该族单质与
 反应生成气态
反应生成气态 的热化学方程式如下:
的热化学方程式如下: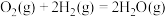

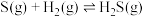


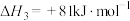
①硫和硒的氢化物的热稳定性:H2S
②写出
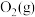 与
与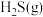 反应生成
反应生成 和
和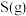 的热化学方程式
的热化学方程式(3)生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如图。

①步骤I反应的离子方程式为
②生物浸出时的总反应的氧化剂是
(4)全固态锂硫电池能量密度高,其工作原理如图所示,其中电极
 常用掺有石墨烯的
常用掺有石墨烯的 材料,电池反应为:
材料,电池反应为: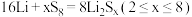 。下列说法
。下列说法
A.电池工作时,正极可发生反应: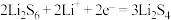 |
B.电池工作时,外电路中流过 电子,负极材料减重 电子,负极材料减重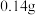 |
C.石墨烯的作用主要是提高电极 的导电性 的导电性 |
D.电池充电时间越长,电池中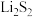 的量越多 的量越多 |
您最近一年使用:0次
2022-07-05更新
|
130次组卷
|
2卷引用:北京市第十二中学2021-2022学年高一下学期6月月考化学试题
8 . 依据图示关系,下列说法不正确 的是


| A.反应①是吸热反应 |
| B.△H3=△H1+△H2 |
| C.反应③是一个熵增的反应 |
| D.数据表明:V2O5(s)的能量比V2O4(s)低,更稳定 |
您最近一年使用:0次
2021-05-03更新
|
512次组卷
|
5卷引用:北京市丰台区2021届高三第二次模拟考试化学试题
北京市丰台区2021届高三第二次模拟考试化学试题(已下线)第17讲 化学能与热能(精练)-2022年高考化学一轮复习讲练测2020年北京高考化学真题变式题11-19江苏省宿迁市泗阳县2022-2023学年高二上学期11月期中化学试题山东省威海大光华学校2023-2024学年高二11月月考化学试题
名校
解题方法
9 .  催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。

下列说法不正确 的是
 催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。
下列说法
| A.由图1推知反应物断键吸收的能量小于生成物成键释放的能量 |
B.图2中,若生成的 为液态,则能量变化曲线为① 为液态,则能量变化曲线为① |
C. |
D.制备 的反应使用催化剂时,其 的反应使用催化剂时,其 不变 不变 |
您最近一年使用:0次
2021-05-10更新
|
792次组卷
|
8卷引用:北京市第十二中学2023-2024学年高二上学期期中考试化学试题
北京市第十二中学2023-2024学年高二上学期期中考试化学试题北京市海淀区2021届高三二模化学试题(已下线)2021年高考化学押题预测卷(北京卷)(02)北京一零一中学2020-2021学年高一下学期期末考试化学试题湖南省五市十校教研教改共同体2021-2022学年高一下学期期末考试化学试题河南省中原名校2022-2023学年高二上学期第一次联考化学试题(已下线)题型14 从吸热与放热角度突破反应热图像北京交通大学附属中学2023-2024学年高三上学期12月月考化学试题
名校
解题方法
10 . 依据图示关系,下列说法不正确 的是


A. |
| B.1 mol S(g)完全燃烧释放的能量小于2968 kJ |
C. |
| D.16 g S(s)完全燃烧释放的能量为1484 kJ |
您最近一年使用:0次
2022-03-25更新
|
1022次组卷
|
10卷引用:北京市丰台区2022届高三一模化学试题
北京市丰台区2022届高三一模化学试题辽宁省沈阳市第四十中学2021-2022年高一下学期4月份线上教学效果检测化学试题(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)(已下线)秘籍15 反应热、盖斯定律应用及图象分析-备战2022年高考化学抢分秘籍(全国通用)上海市上海中学2021-2022学年高一下学期期末考试化学试题北京市北京师范大学附属实验中学2022-2023学年高二上学期期中考试化学试题(已下线)第2讲 盖斯定律 反应热的计算北京市第二十二中学2023-2024学年高二上学期10月月考化学试题北京市中关村中学2023-2024学年高二上学期期中考试化学试题河南省郑州学森实验学校2023-2024学年高二上学期期中考试 化学试题



