1 . 下列叙述或表示方法不正确的是
| A.盖斯定律实质上是能量守恒定律的体现 |
B.在稀溶液中: ,含0.5 mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ ,含0.5 mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
| C.相同条件下,如果1mol氧原子所具有的能量为E1,1mol氧分子所具有的能量为E2,则2E1= E2 |
| D.化学键的断裂和形成是化学反应中能量变化的根本原因 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法或表示方法不正确的是
| A.盖斯定律实质上是能量守恒定律的体现 |
| B.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) △H = -57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ |
| C.由一定条件下石墨合成金刚石吸热,可知石墨比金刚石稳定 |
| D.在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) △H = –285.8kJ/mol |
您最近一年使用:0次
2020-11-12更新
|
326次组卷
|
17卷引用:山西省晋中市平遥县第二中学2018-2019学年高二上学期期中考试化学试题
山西省晋中市平遥县第二中学2018-2019学年高二上学期期中考试化学试题安徽省池州市第一中学2019-2020学年高二上学期期中考试化学试题山西大学附属中学2019-2020学年高二10月月考化学试题河北省唐山市河北唐山外国语学校2020-2021学年高二上学期期中考试(理科)化学试题河北省尚义县第一中学2020-2021学年高二上学期期中考试化学试题湖北省巴东县第二高级中学2020-2021学年高二上学期期中考试化学试题河北省唐山市遵化市2021-2022学年高二上学期期中考试化学试题2014-2015学年山东省微山一中高二下学期期末考试化学试卷云南省曲靖市罗平县第三中学2020届高二下学期开学考试化学试题四川省成都外国语学校2020-2021学年高二10月月考化学试题(已下线)小题必刷24 盖斯定律及反应热计算——2021年高考化学一轮复习小题必刷(通用版)甘肃省天水市第六中学2019-2020学年高二上学期期末考试化学试题(普通班)内蒙古自治区第二地质中学2020-2021学年高二下学期第二次阶段检测化学试题陕西省宝鸡市金台区2021-2022学年高二上学期期末考试化学(理)试题吉林省辽源市等2地高中友好学校2022-2023学年高二上学期期末联考化学试题安徽省安庆市怀宁县第二中学2022-2023学年高二上学期期末考试化学试题吉林省辽源、通化等2市2022-2023学年高二上学期1月期末考试化学试题
名校
3 . 我国学者研究了均相 NO- CO 的反应历程,反应路径中每一阶段内各驻点的能最均为相对于此阶段内反应物能量的能量之差,下列说法正确的是
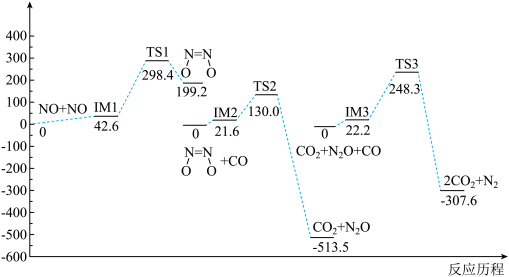

A.2NO(g)+ 2CO(g)  N2(g) +2CO2(g) ΔH>O N2(g) +2CO2(g) ΔH>O |
| B.均相NO—CO反应经历了三个过渡态和六个中间体 |
| C.整个反应分为三个基元反应阶段,总反应速率由第一阶段反应决定 |
D.NO二聚体(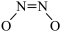 )比N2O分子更难与CO发生反应 )比N2O分子更难与CO发生反应 |
您最近一年使用:0次
4 . 1mol白磷转化为红磷放热18.39kJ,已知:
P4(白磷,s)+5O2(g)=2P2O5(s) ΔH= -akJ·mol-1(a>0);
4P(红磷,s)+5O2(g)=2P2O5(s) ΔH=-bkJ·mol-1(b>0);
则a和b的关系是( )
P4(白磷,s)+5O2(g)=2P2O5(s) ΔH= -akJ·mol-1(a>0);
4P(红磷,s)+5O2(g)=2P2O5(s) ΔH=-bkJ·mol-1(b>0);
则a和b的关系是( )
| A.a<b | B.a>b | C.a=b | D.无法确定 |
您最近一年使用:0次
2020-09-11更新
|
232次组卷
|
29卷引用:2014-2015学年山西省曲沃中学校高二上学期期中化学试卷
2014-2015学年山西省曲沃中学校高二上学期期中化学试卷(已下线)2011-2012学年天津一中高二上学期期中考试化学试卷(已下线)2011-2012学年辽宁省抚顺县高级中学高一下学期期中考试化学试卷(已下线)2011-2012学年天津市天津一中高二上学期期中考试化学试卷山西省运城市康杰中学2017-2018学年高二上学期第一次月考化学试题山西省汾阳市第二高级中学2018-2019学年高二上学期第二次半月考化学试题江西省上饶市第二中学2018-2019学年高二上学期期中考试化学试题内蒙古呼和浩特开来中学2019-2020学年高二上学期期中考试化学试题吉林省长春市第二十九中学2019-2020学年高一下学期期中考试化学试题(理)甘肃省庆阳市第六中学2020-2021学年高二上学期期中考试化学(理)试题(已下线)2011-2012学年吉林省长春外国语学校高二第二次月考化学试卷(已下线)2011-2012学年云南大理云龙一中高二上学期期末考试化学试卷(已下线)2011-2012学年安徽省安工大附中、红星中学高二3月联考化学试卷(已下线)2011-2012学年安徽省舒城晓天中学高二下学期质量测试2化学试卷2014-2015河北省正定中学高一下学期第一次月考化学试卷2016-2017学年山东省德州市陵城一中高二上10月月考化学试卷河北省安平中学2016-2017学年高一下学期升级考试化学试题山东省枣庄市第八中学南校区高二10月份月考化学试题山东省枣庄市第八中学东校区2017-2018学年高二10月月考化学试题福建省三明市第一中学2017-2018学年高二上学期第一次月考化学试题河北省邢台第三中学2017-2018学年高二9月月考化学试题山东省锦泽技工学校2017-2018学年高二10月月考化学试题陕西煤铜川市炭建设公司第一中学2018-2019学年高二上学期10月月考化学试题(已下线)2018年10月20日 《每日一题》人教选修4-周末培优吉林省实验中学2019-2020学年高二上学期第一次月考化学试题广东省惠来县葵潭中学2019-2020学年高二上学期第二次月考化学试题新疆吾尔自治区哈密市第十五中学2019-2020学年高一下学期期末考试化学试题甘肃省临夏中学2019-2020学年高二上学期第一次月考化学试题安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题
名校
解题方法
5 . (1)写出下列物质在水溶液中的电离方程式:
CH3COOH____ HClO4_____
Fe(OH)3____ Ba(OH)2_____
NaHSO4____
(2)常温下2.3g乙醇和一定量的氧气混合,点燃恰好完全燃烧,生成液态水和CO2放出68.35kJ热量,则该反应的热化学方程式为:___ 。
(3)根据下列热化学方程式分析,C(s)的燃烧热△H等于___ 。
C(s)+H2O(l)=CO(g)+H2(g) △H1=+175.3kJ·mol-1
2CO(g) + O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g) + O2(g)=2H2O(l) △H3=-571.6kJ·mol-1
CH3COOH
Fe(OH)3
NaHSO4
(2)常温下2.3g乙醇和一定量的氧气混合,点燃恰好完全燃烧,生成液态水和CO2放出68.35kJ热量,则该反应的热化学方程式为:
(3)根据下列热化学方程式分析,C(s)的燃烧热△H等于
C(s)+H2O(l)=CO(g)+H2(g) △H1=+175.3kJ·mol-1
2CO(g) + O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g) + O2(g)=2H2O(l) △H3=-571.6kJ·mol-1
您最近一年使用:0次
6 . 反应A(g)+B(g)  C(g)+D(g)过程中能量变化如图,下列说法正确的是( )
C(g)+D(g)过程中能量变化如图,下列说法正确的是( )
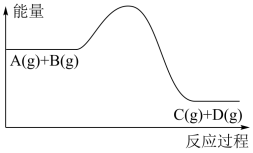
 C(g)+D(g)过程中能量变化如图,下列说法正确的是( )
C(g)+D(g)过程中能量变化如图,下列说法正确的是( ) 
| A.该反应为吸热反应 |
| B.升高温度,利于A的转化率增大 |
| C.加入催化剂时,可以降低反应热 |
| D.增大压强,能够缩短反应达到平衡状态的时间 |
您最近一年使用:0次
名校
7 . 根据下列热化学方程式
C(s) + O2(g) = CO2(g) △H1=–393.5 kJ·mol-1
2H2(g) + O2(g) =2H2O(l) △H2=–571.6 kJ·mol-1
CH3COOH(l) +2O2(g)=2CO2 (g) + 2H2O(l) △H3=–870.3 kJ·mol-1
可以计算出2C(s) + 2H2(g)+ O2(g)=CH3COOH(l)的反应热为:
C(s) + O2(g) = CO2(g) △H1=–393.5 kJ·mol-1
2H2(g) + O2(g) =2H2O(l) △H2=–571.6 kJ·mol-1
CH3COOH(l) +2O2(g)=2CO2 (g) + 2H2O(l) △H3=–870.3 kJ·mol-1
可以计算出2C(s) + 2H2(g)+ O2(g)=CH3COOH(l)的反应热为:
| A.△H=+244.1 kJ·mol-1 | B.△H=-488.3 kJ·mol-1 |
| C.△H=-996.6 kJ·mol-1 | D.△H=+996.6 kJ·mol-1 |
您最近一年使用:0次
2019-05-06更新
|
276次组卷
|
3卷引用:山西省吕梁市汾阳中学、孝义中学、文水中学2020-2021学年高二上学期期中测评考试化学试题
10-11高二上·福建厦门·期中
名校
8 . 已知下列热化学方程式,且b>a。Hg(l)+1/2O2(g)===HgO(s) △H=-a kJ·mol-1; Zn(s)+1/2O2(g)===ZnO(s) △H=-b kJ·mol-1由此可知反应Zn(s)+HgO(s)  ZnO(s)+Hg(l)的焓变为
ZnO(s)+Hg(l)的焓变为
 ZnO(s)+Hg(l)的焓变为
ZnO(s)+Hg(l)的焓变为| A.-(b-a) kJ·mol-1 | B.+(b-a) kJ·mol-1 |
| C.(b-a) kJ·mol-1 | D.(b+a)kJ·mol-1 |
您最近一年使用:0次
2016-12-09更新
|
1072次组卷
|
3卷引用:山西省康杰中学2017-2018学年高二上学期期中考试化学试题
名校
9 . 已知:C(s)+O2(g)=CO2(g) △H1=-395kJ/mol,
CO(g)+1/2O2(g)=CO2(g) △H2=-283kJ/mol,
则反应C(s)+1/2O2(g)=CO(g)的反应热△H3等于
CO(g)+1/2O2(g)=CO2(g) △H2=-283kJ/mol,
则反应C(s)+1/2O2(g)=CO(g)的反应热△H3等于
| A.-112 kJ/mol | B.-395 kJ/mol | C.+ 112 kJ/mol | D.-283 kJ/mol |
您最近一年使用:0次
2016-11-29更新
|
255次组卷
|
3卷引用:山西省阳泉二中2018-2019学年高二上学期期中考试化学试题



