解题方法
1 . 央广网消息:2020年大庆油田生产天然气46.6亿立方米,实现了“十连增”,在大战大考中交出了“当好标杆旗帜、建设百年油田”的新答卷。天然气的主要成分甲烷是一种重要的化工原料,广泛应用于民用和化工业生产中。回答下列问题:
(1)利用CH4超干重整CO2技术可得到富含CO的化工原料。
已知:①CH4(g)+H2O(g)=CO(g)+3H2(g)。∆H1=+196 kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) ∆H2=-484 kJ·mol-1
③2CO(g)+O2(g)=2CO2(g) ∆H3=-566 kJ·mol-1
则CH4(g)+CO2(g)=2CO(g)+2H2(g) ∆H=_______ 。
(2)在两个相同钢性密闭容器中充入CH4和CO2发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g),CH4和CO2的分压均为20 kPa,加入催化剂Ni/α-Al2O3,分别在T1℃和T2℃下进行反应,测得CH4转化率随时间变化如图1所示。
2CO(g)+2H2(g),CH4和CO2的分压均为20 kPa,加入催化剂Ni/α-Al2O3,分别在T1℃和T2℃下进行反应,测得CH4转化率随时间变化如图1所示。

图1
①A点处v正_______ B点处v逆(填“<”、“>”或“=”)。
②用单位时间内气体分压的变化来表示反应速率,即v= ,T2℃下,上述反应0~2min内平均反应速率v(CH4)=
,T2℃下,上述反应0~2min内平均反应速率v(CH4)=_______ kPa·min-1。(分压=总压×物质的量分数)
③上述反应达到平衡后,下列变化一定能使平衡向正向移动的是_____
A.通入惰性气体使容器内压强增大 B.正反应速率加快
C.平衡常数K变大 D.增大催化剂表面积
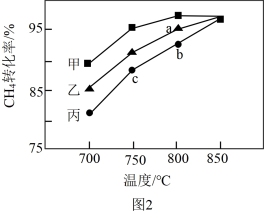
(3)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得甲烷转化率随温度变化如图2所示。三种催化剂作用下,反应活化能最大的是_______ (填“甲”、“乙”或“丙”);CH4的转化率b点高于c点的原因是_______ 。
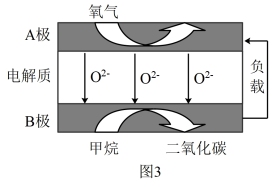
(4)我国科学家设计的新型甲烷燃料电池能量密度高、成本低,其工作原理如图3所示。B极电极反应式为_______ 。
(1)利用CH4超干重整CO2技术可得到富含CO的化工原料。
已知:①CH4(g)+H2O(g)=CO(g)+3H2(g)。∆H1=+196 kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) ∆H2=-484 kJ·mol-1
③2CO(g)+O2(g)=2CO2(g) ∆H3=-566 kJ·mol-1
则CH4(g)+CO2(g)=2CO(g)+2H2(g) ∆H=
(2)在两个相同钢性密闭容器中充入CH4和CO2发生反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g),CH4和CO2的分压均为20 kPa,加入催化剂Ni/α-Al2O3,分别在T1℃和T2℃下进行反应,测得CH4转化率随时间变化如图1所示。
2CO(g)+2H2(g),CH4和CO2的分压均为20 kPa,加入催化剂Ni/α-Al2O3,分别在T1℃和T2℃下进行反应,测得CH4转化率随时间变化如图1所示。
图1
①A点处v正
②用单位时间内气体分压的变化来表示反应速率,即v=
 ,T2℃下,上述反应0~2min内平均反应速率v(CH4)=
,T2℃下,上述反应0~2min内平均反应速率v(CH4)=③上述反应达到平衡后,下列变化一定能使平衡向正向移动的是
A.通入惰性气体使容器内压强增大 B.正反应速率加快
C.平衡常数K变大 D.增大催化剂表面积
(3)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得甲烷转化率随温度变化如图2所示。三种催化剂作用下,反应活化能最大的是

(4)我国科学家设计的新型甲烷燃料电池能量密度高、成本低,其工作原理如图3所示。B极电极反应式为

您最近一年使用:0次
名校
解题方法
2 . 工业合成氨的反应N2+3H2=2NH3的能量变化如图所示,请回答有关问题:
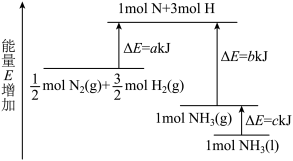
(1)合成1molNH3(l)___________ (填“吸收”或“放出”)___________ kJ的热量。(用字母表示)
(2)已知:拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则1molN2(g)完全反应生成NH3(g)产生的能量变化为___________ kJ。
(3)推测反应2NH3(l)=N2(g)+3H2(g)比反应2NH3(g)=N2(g)+3H2(g)___________ (填“吸收”或“放出”)的热量___________ (填“多”或“少”)。

(1)合成1molNH3(l)
(2)已知:拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则1molN2(g)完全反应生成NH3(g)产生的能量变化为
(3)推测反应2NH3(l)=N2(g)+3H2(g)比反应2NH3(g)=N2(g)+3H2(g)
您最近一年使用:0次
2021-05-03更新
|
300次组卷
|
8卷引用:黑龙江省齐齐哈尔市第八中学校2020-2021学年高一下学期期中考试化学试题
黑龙江省齐齐哈尔市第八中学校2020-2021学年高一下学期期中考试化学试题江西省南昌市八一中学、洪都中学等七校2020-2021学年高一下学期期中联考化学试题安徽省滁州市定远县育才学校2020-2021学年高一下学期期中考试化学试题江西省赣州市南康区第三中学2020-2021学年高一下学期期中考试化学试题山西省朔州市应县第一中学校2019-2020学年高一下学期期中考试化学试题(已下线)练习3 化学反应热的计算-2020-2021学年【补习教材·寒假作业】高二化学(人教版)云南省昌宁县第一中学2021-2022学年高一 3月月考化学试题陕西省渭南市华州区咸林中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
3 . 甲醇是重要的化工原料。回答下列问题:
(1)以甲醇为原料制备甲醛,同时生成副产物H2等,已知以下热化学方程式:
I.CH3OH(g) CO(g)+2H2(g) △H1=a kJ·mol-1
CO(g)+2H2(g) △H1=a kJ·mol-1
II.CO(g)+H2(g) HCHO(g) △H2=b kJ·mol-1
HCHO(g) △H2=b kJ·mol-1
III.CH3OH(g) HCHO(g)+H2(g) △H3=c kJ·mol-1
HCHO(g)+H2(g) △H3=c kJ·mol-1
则b=___________ (用含有a、c的代数式表示)。
(2)以Na2CO3固体为催化剂,甲醇脱氢可制得甲醛。反应机理如下:
(i)CH3OH(g) ·H(g)+·CH2OH(g);
·H(g)+·CH2OH(g);
(ii)·CH2OH(g) HCHO(g)+·H(g);
HCHO(g)+·H(g);
(iii)·H(g)十·H(g) H2(g)
H2(g)
①(i)中反应物的总能量___________ (填“>”“=”或“<”)生成物的总能量。
②某温度时反应(i)、(ii)、(ii)的平衡常数依次为K1、K2、K3,CH3OH(g) H2(g)+HCHO(g)的平衡常数为K,则K=
H2(g)+HCHO(g)的平衡常数为K,则K=___________ (用含K1、K2、K3的代数式表示)。
(3)向体积为1 L恒容反应器中加入2 mol CH3OH及适量催化剂,发生反应CH3OH(g) HCHO(g)+H2(g) △H,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
HCHO(g)+H2(g) △H,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
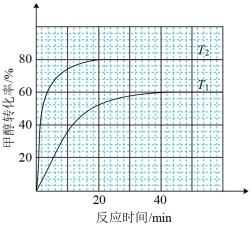
①T2温度下,20min时甲醇的体积分数为___________ %(保留三位有效数字),前20min平均反应速率 (HCHO)=
(HCHO)=___________ mol·L-1·min-1。
②T1温度下该反应的平衡常数Kp=___________ kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,反应器内的初始压强为103kPa)。
(4)固体氧化物甲醇燃料电池是能效高、环境友好地转化成电能的全固态电源,工作原理如图所示。
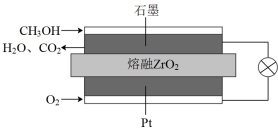
①石墨极上的反应式为___________ 。
②若通过用电器的电子的物质的量为1.2 mol,则消耗标准状况下O2的体积为___________ L。
(1)以甲醇为原料制备甲醛,同时生成副产物H2等,已知以下热化学方程式:
I.CH3OH(g)
 CO(g)+2H2(g) △H1=a kJ·mol-1
CO(g)+2H2(g) △H1=a kJ·mol-1II.CO(g)+H2(g)
 HCHO(g) △H2=b kJ·mol-1
HCHO(g) △H2=b kJ·mol-1III.CH3OH(g)
 HCHO(g)+H2(g) △H3=c kJ·mol-1
HCHO(g)+H2(g) △H3=c kJ·mol-1则b=
(2)以Na2CO3固体为催化剂,甲醇脱氢可制得甲醛。反应机理如下:
(i)CH3OH(g)
 ·H(g)+·CH2OH(g);
·H(g)+·CH2OH(g);(ii)·CH2OH(g)
 HCHO(g)+·H(g);
HCHO(g)+·H(g);(iii)·H(g)十·H(g)
 H2(g)
H2(g)①(i)中反应物的总能量
②某温度时反应(i)、(ii)、(ii)的平衡常数依次为K1、K2、K3,CH3OH(g)
 H2(g)+HCHO(g)的平衡常数为K,则K=
H2(g)+HCHO(g)的平衡常数为K,则K=(3)向体积为1 L恒容反应器中加入2 mol CH3OH及适量催化剂,发生反应CH3OH(g)
 HCHO(g)+H2(g) △H,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
HCHO(g)+H2(g) △H,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
①T2温度下,20min时甲醇的体积分数为
 (HCHO)=
(HCHO)=②T1温度下该反应的平衡常数Kp=
(4)固体氧化物甲醇燃料电池是能效高、环境友好地转化成电能的全固态电源,工作原理如图所示。

①石墨极上的反应式为
②若通过用电器的电子的物质的量为1.2 mol,则消耗标准状况下O2的体积为
您最近一年使用:0次
2021-04-22更新
|
293次组卷
|
2卷引用:黑龙江省齐齐哈尔市2021届高三第二次模拟考试理综化学试题
名校
解题方法
4 . 用 催化还原
催化还原 可以消除氮氧化物的污染。
可以消除氮氧化物的污染。
已知:①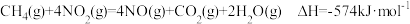
②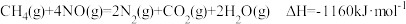
若在一定条件下,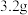 的
的 恰好与一定量的
恰好与一定量的 反应生成
反应生成 、
、 和
和 ,则整个过程中放出的热量为
,则整个过程中放出的热量为
 催化还原
催化还原 可以消除氮氧化物的污染。
可以消除氮氧化物的污染。已知:①
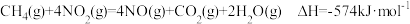
②
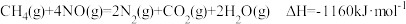
若在一定条件下,
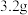 的
的 恰好与一定量的
恰好与一定量的 反应生成
反应生成 、
、 和
和 ,则整个过程中放出的热量为
,则整个过程中放出的热量为A. | B. | C. | D.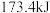 |
您最近一年使用:0次
名校
5 . 室温下,将 溶于水会使溶液温度降低,热效应为
溶于水会使溶液温度降低,热效应为 ,将
,将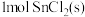 溶于水会使溶液温度升高,热效应为
溶于水会使溶液温度升高,热效应为 ;
; 受热分解的化学方程式为
受热分解的化学方程式为 ,热效应为
,热效应为 。则下列判断正确的是
。则下列判断正确的是
 溶于水会使溶液温度降低,热效应为
溶于水会使溶液温度降低,热效应为 ,将
,将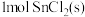 溶于水会使溶液温度升高,热效应为
溶于水会使溶液温度升高,热效应为 ;
; 受热分解的化学方程式为
受热分解的化学方程式为 ,热效应为
,热效应为 。则下列判断正确的是
。则下列判断正确的是A. | B.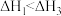 | C. | D. |
您最近一年使用:0次
名校
解题方法
6 . 在食品行业中,N2O 可用作发泡剂和密封剂。
(1)N2O 在金粉表面发生热分解反应:2N2O(g)=2N2(g)+O2(g) ΔH
已知:2NH3(g)+3N2O(g)=4N2(g)+3H2O(l) ΔH1=-1010 kJ•mol-1
4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH2=-1531 kJ•mol-1
则 ΔH=_______ 。
(2)N2O和CO是环境污染性气体,研究表明,CO与N2O在Fe+作用下发生反应 N2O(g)+CO(g)⇌CO2(g)+N2(g)的能量变化及反应历程如图所示。
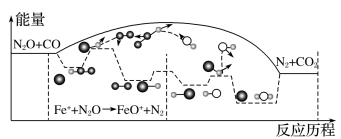
两步反应分别为:反应①Fe++N2O⇌FeO++N2,反应②_______ 。由图可知两步反应均为_______ (填“放热”或“吸热”)反应,由_______ (填“反应①”或“反应②”)决定反应达到平衡所用时间。
(3)在固定体积的密闭容器中,发生反应 N2O(g)+CO(g) ⇌CO2(g)+N2(g),改变原料气配比进行多组实验(各次实验的温度可能不同,也可能相同),测定 N2O 的平衡转化率。部分实验结果如图所示。
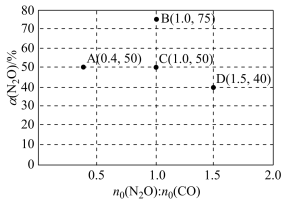
①如果要将图中 C 点的平衡状态改变为B 点的平衡状态,应采取的措施是_______ 。
②图中 C、D 两点对应的实验温度分别为 Tc和TD,通过计算判断Tc_______ (填“>”“=”或“<”)TD
(4)在某温度下,向1 L 密闭容器中充入CO与N2O,发生反应:N2O(g)+CO(g)⇌CO2(g)+N2(g),随着反应的进行,容器内 CO 的物质的量分数变化如表所示:
则该温度下反应的平衡常数 K=_______ 。
(1)N2O 在金粉表面发生热分解反应:2N2O(g)=2N2(g)+O2(g) ΔH
已知:2NH3(g)+3N2O(g)=4N2(g)+3H2O(l) ΔH1=-1010 kJ•mol-1
4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH2=-1531 kJ•mol-1
则 ΔH=
(2)N2O和CO是环境污染性气体,研究表明,CO与N2O在Fe+作用下发生反应 N2O(g)+CO(g)⇌CO2(g)+N2(g)的能量变化及反应历程如图所示。

两步反应分别为:反应①Fe++N2O⇌FeO++N2,反应②
(3)在固定体积的密闭容器中,发生反应 N2O(g)+CO(g) ⇌CO2(g)+N2(g),改变原料气配比进行多组实验(各次实验的温度可能不同,也可能相同),测定 N2O 的平衡转化率。部分实验结果如图所示。

①如果要将图中 C 点的平衡状态改变为B 点的平衡状态,应采取的措施是
②图中 C、D 两点对应的实验温度分别为 Tc和TD,通过计算判断Tc
(4)在某温度下,向1 L 密闭容器中充入CO与N2O,发生反应:N2O(g)+CO(g)⇌CO2(g)+N2(g),随着反应的进行,容器内 CO 的物质的量分数变化如表所示:
| 时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 物质的量分数 | 50.0% | 40.25% | 32.0% | 26.2% | 24.0% | 24.0% |
则该温度下反应的平衡常数 K=
您最近一年使用:0次
名校
7 . 甲醇是结构最为简单的饱和一元醇,又称“木醇”或“木精”。甲醇是一碳化学基础的原料和优质的燃料,主要应用于精细化工、塑料、能源等领域。已知甲醇制备的有关化学反应如下:
反应①:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=﹣92kJ/mol
反应②:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2
反应③:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH3=﹣49kJ/mol
(1)反应②的ΔH2=_______ kJ/mol
(2)500℃时三个反应的平衡常数依次为K1、K2与K3,则K3=_______ (用K1、K2表示)。已知500℃时,K1=2.5,K2=1.0,并测得该温度下反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol/L)分别为1.0、0.2、0.6、1.5,则此时 v正_______ v逆(填“>”、“=”或“<”)
反应①:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=﹣92kJ/mol
反应②:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2
反应③:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH3=﹣49kJ/mol
(1)反应②的ΔH2=
(2)500℃时三个反应的平衡常数依次为K1、K2与K3,则K3=
您最近一年使用:0次
8 . 某温度时,ⅥA元素单质与H2反应生成气态H2X的热化学方程式如下:
①H2(g)+ O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1
②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
请回答:
(1)上述反应中属于放热反应的是___________ (填序号,下同),属于吸热反应的是___________ 。
(2)2g H2完全燃烧生成气态水,放出的热量为___________ 。
(3)请写出O2与H2S反应生成S的热化学方程式___________ 。
(4)根据下图写出热化学方程式___________ 。
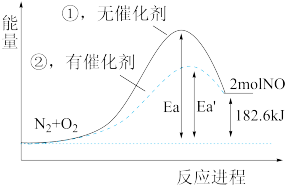
(5)加入催化剂该反应的反应热 H是否发生了改变
H是否发生了改变___________ (填“是”或“否”)。
①H2(g)+
 O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
请回答:
(1)上述反应中属于放热反应的是
(2)2g H2完全燃烧生成气态水,放出的热量为
(3)请写出O2与H2S反应生成S的热化学方程式
(4)根据下图写出热化学方程式

(5)加入催化剂该反应的反应热
 H是否发生了改变
H是否发生了改变
您最近一年使用:0次
2021-03-11更新
|
1408次组卷
|
4卷引用:黑龙江省大庆中学2020—2021学年高二上学期期末考试化学试题
9 . 中科院大连化物所研发的甲醇制乙烯技术能有效解决化工生产依赖进口石油的问题。该技术涉及如下反应:
甲醇制乙烯:2CH3OH(g)⇌C2H4(g)+2H2O(g)ΔH1
甲醇脱水:2CH3OH(g)⇌CH3OCH3(g)+H2O(g)ΔH2=-24.0kJ·mol-1
已知:C2H5OH(g)⇌CH3OCH3(g)ΔH3=+50.8kJ·mol-1
C2H4(g)+H2O(g)⇌C2H5OH(g)ΔH4=-45.8kJ·mol-1
下列说法不正确 的是
甲醇制乙烯:2CH3OH(g)⇌C2H4(g)+2H2O(g)ΔH1
甲醇脱水:2CH3OH(g)⇌CH3OCH3(g)+H2O(g)ΔH2=-24.0kJ·mol-1
已知:C2H5OH(g)⇌CH3OCH3(g)ΔH3=+50.8kJ·mol-1
C2H4(g)+H2O(g)⇌C2H5OH(g)ΔH4=-45.8kJ·mol-1
下列说法
| A.ΔH1>0 |
| B.甲醇脱水是放热反应 |
| C.减小压强,利于提高甲醇的平衡转化率 |
| D.加入选择性催化剂可抑制甲醇脱水反应的发生 |
您最近一年使用:0次
2021-03-08更新
|
358次组卷
|
5卷引用:黑龙江省哈尔滨市第一六二中学2021-2022学年高三上学期第三次月考化学试题
黑龙江省哈尔滨市第一六二中学2021-2022学年高三上学期第三次月考化学试题北京市昌平区2021届高三上学期期末考试化学试题(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)化学-2022年高考押题预测卷01(北京卷)
名校
解题方法
10 . 已知,在25℃、101 kPa时: ① C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
② 2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol
③ 2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol
下列判断不正确的是
② 2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol
③ 2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol
下列判断不正确的是
| A.6 g碳完全燃烧时放出热量196.8 kJ |
| B.反应②可以自发进行 |
| C.H2的燃烧热ΔH=-241.8 kJ/mol |
| D.制备水煤气的反应热ΔH=+131.3 kJ/mol |
您最近一年使用:0次
2021-03-05更新
|
147次组卷
|
2卷引用:黑龙江省佳木斯学校(佳木斯市实验中学)2021-2022学年高二上学期第二次月考化学试题



