1 . 研发二氧化碳的利用技术具有重要意义。
(1) 还原
还原 是实现“双碳”经济的有效途径之一,相关反应有:
是实现“双碳”经济的有效途径之一,相关反应有:
反应Ⅰ:


反应Ⅱ:


反应Ⅲ:


则反应 的
的
___________ 。
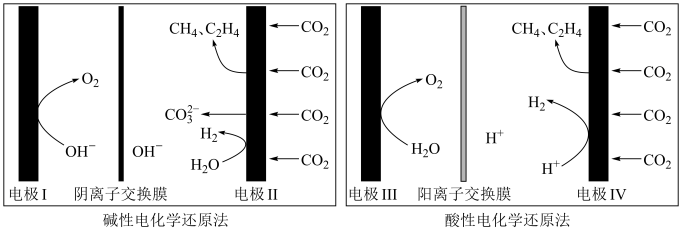
(2)利用电解法在碱性或酸性条件下将 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示:
已知:选择性(S)和法拉第效率(FE)的定义(X代表 或
或 )如下:
)如下:
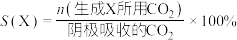
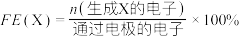
①写出碱性条件下 生成
生成 的电极反应式:
的电极反应式:___________ 。
②实验测得,碱性条件生成 、
、 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是___________ 。
③实验测得,酸性条件生成 、
、 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是___________ 。
④碱性条件下反应一段时间,实验测得 、
、 的选择性及
的选择性及 的法拉第效率如下表所示。则
的法拉第效率如下表所示。则 的法拉第效率
的法拉第效率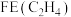 为
为___________ 。
(1)
 还原
还原 是实现“双碳”经济的有效途径之一,相关反应有:
是实现“双碳”经济的有效途径之一,相关反应有:反应Ⅰ:



反应Ⅱ:



反应Ⅲ:



则反应
 的
的
(2)利用电解法在碱性或酸性条件下将
 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示:
已知:选择性(S)和法拉第效率(FE)的定义(X代表
 或
或 )如下:
)如下: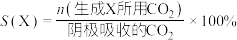
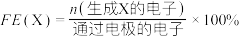
①写出碱性条件下
 生成
生成 的电极反应式:
的电极反应式:②实验测得,碱性条件生成
 、
、 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是③实验测得,酸性条件生成
 、
、 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是④碱性条件下反应一段时间,实验测得
 、
、 的选择性及
的选择性及 的法拉第效率如下表所示。则
的法拉第效率如下表所示。则 的法拉第效率
的法拉第效率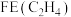 为
为 |  | |
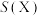 | 2% | 8% |
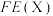 | 12.5% |
您最近一年使用:0次
2024-02-24更新
|
255次组卷
|
2卷引用:江苏省 徐州市第七中学2023-2024学年高三上学期12月月考化学试题
2 . 氢能是一种绿色能源,也是重要的还原剂。目前有多种方法可以制氢并储氢。催化加氢反应可以用于重要化工原料的转化。
Ⅰ.电解法制氢
(1)甲醇电解可制得 ,其原理如图所示。
,其原理如图所示。___________ 。
Ⅱ.催化重整法制氢
(2)已知:反应1:

反应2:
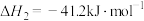
则反应3: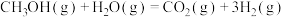
 =
=______ 
(3)以 催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及
催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及 选择性的影响如图所示。
选择性的影响如图所示。 的选择性=
的选择性=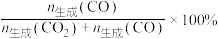
当水、甲醇比大于0.8时, 选择性下降的原因是
选择性下降的原因是___________ 。
(4)铜基催化剂(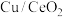 )能高效进行甲醇重整制氢,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。甲醇中混有少量的甲硫醇(
)能高效进行甲醇重整制氢,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。甲醇中混有少量的甲硫醇(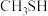 ),重整制氢时加入
),重整制氢时加入 可有效避免铜基催化剂失活且平衡产率略有上升,其原理用化学反应方程式表示为
可有效避免铜基催化剂失活且平衡产率略有上升,其原理用化学反应方程式表示为___________ 。
Ⅲ.催化加氢还原反应的应用 单原子位点对4-硝基苯乙烯有较好吸附效果。
单原子位点对4-硝基苯乙烯有较好吸附效果。
①使用双单原子催化剂可以大大提高4-乙烯基苯胺的产率,原因是_______ 。
Ⅰ.电解法制氢
(1)甲醇电解可制得
 ,其原理如图所示。
,其原理如图所示。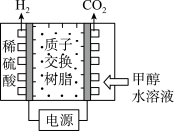
Ⅱ.催化重整法制氢
(2)已知:反应1:


反应2:

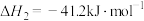
则反应3:
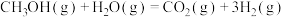
 =
=
(3)以
 催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及
催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及 选择性的影响如图所示。
选择性的影响如图所示。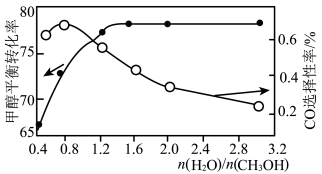
 的选择性=
的选择性=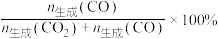
当水、甲醇比大于0.8时,
 选择性下降的原因是
选择性下降的原因是(4)铜基催化剂(
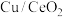 )能高效进行甲醇重整制氢,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。甲醇中混有少量的甲硫醇(
)能高效进行甲醇重整制氢,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。甲醇中混有少量的甲硫醇(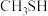 ),重整制氢时加入
),重整制氢时加入 可有效避免铜基催化剂失活且平衡产率略有上升,其原理用化学反应方程式表示为
可有效避免铜基催化剂失活且平衡产率略有上升,其原理用化学反应方程式表示为Ⅲ.催化加氢还原反应的应用
 能将
能将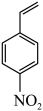 在特定条件下转化为4-乙烯基苯胺
在特定条件下转化为4-乙烯基苯胺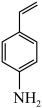 。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图所示。
。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图所示。

 单原子位点对4-硝基苯乙烯有较好吸附效果。
单原子位点对4-硝基苯乙烯有较好吸附效果。①使用双单原子催化剂可以大大提高4-乙烯基苯胺的产率,原因是
②请描述4-硝基苯乙烯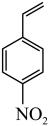 在单原子催化剂下与
在单原子催化剂下与 发生反应的过程
发生反应的过程
您最近一年使用:0次
解题方法
3 . 回收利用含硫化合物有利于节约资源、保护环境。
(1)一种由含 的烟气回收硫磺的工艺为:将一部分含
的烟气回收硫磺的工艺为:将一部分含 的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到单质硫
的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到单质硫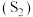 ,该工艺中涉及反应为:
,该工艺中涉及反应为:
反应1: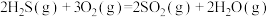

反应2: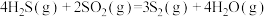
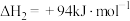
反应3: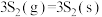
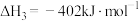
①反应
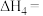
________ 。
②如果上述反应均能完全进行,为提高硫磺的产率,该工艺中需要控制反应1和反应2的烟气的体积比是________ 。
(2)一种以 为原料,循环吸收烟气中
为原料,循环吸收烟气中 的物质转化关系如下,写出转化中由
的物质转化关系如下,写出转化中由 制
制 同时生成硫酸铵的化学反应方程式:
同时生成硫酸铵的化学反应方程式:________ 。

(3)一种以 为催化剂载体、
为催化剂载体、 为催化剂的
为催化剂的 还原烟气中
还原烟气中 制S的反应机理如题图1和题图2所示:
制S的反应机理如题图1和题图2所示:
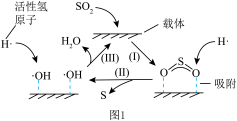
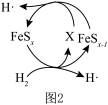
①图1中所示转化可以描述为 分解为活性氢原子,
分解为活性氢原子,________ 。
②图2中X的电子式为________ 。
③其他条件一定,改变起始时 与
与 的比例,反应相同时间,测得S的产率与温度和
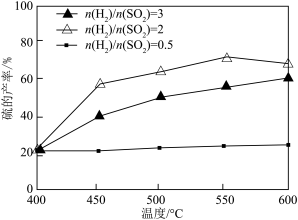
的比例,反应相同时间,测得S的产率与温度和 比值的关系如题图所示,500℃时,
比值的关系如题图所示,500℃时, 比值为3时硫的产率小于比值为2时的原因是
比值为3时硫的产率小于比值为2时的原因是________ 。
(1)一种由含
 的烟气回收硫磺的工艺为:将一部分含
的烟气回收硫磺的工艺为:将一部分含 的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到单质硫
的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到单质硫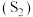 ,该工艺中涉及反应为:
,该工艺中涉及反应为:反应1:
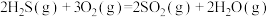

反应2:
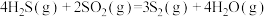
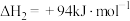
反应3:
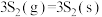
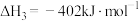
①反应

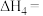
②如果上述反应均能完全进行,为提高硫磺的产率,该工艺中需要控制反应1和反应2的烟气的体积比是
(2)一种以
 为原料,循环吸收烟气中
为原料,循环吸收烟气中 的物质转化关系如下,写出转化中由
的物质转化关系如下,写出转化中由 制
制 同时生成硫酸铵的化学反应方程式:
同时生成硫酸铵的化学反应方程式:
(3)一种以
 为催化剂载体、
为催化剂载体、 为催化剂的
为催化剂的 还原烟气中
还原烟气中 制S的反应机理如题图1和题图2所示:
制S的反应机理如题图1和题图2所示:

①图1中所示转化可以描述为
 分解为活性氢原子,
分解为活性氢原子,②图2中X的电子式为
③其他条件一定,改变起始时
 与
与 的比例,反应相同时间,测得S的产率与温度和
的比例,反应相同时间,测得S的产率与温度和 比值的关系如题图所示,500℃时,
比值的关系如题图所示,500℃时, 比值为3时硫的产率小于比值为2时的原因是
比值为3时硫的产率小于比值为2时的原因是
您最近一年使用:0次
名校
4 . 气态含氮化合物是把双刃剑,既是固氮的主要途径,也是大气污染物。气态含氮化合物及相关反应是新型科研热点。回答下列问题:
(1)还原法:①用 催化还原
催化还原 可以消除氮氧化物的污染。已知:
可以消除氮氧化物的污染。已知:
ⅰ:
ⅱ:
写出 还原
还原 至
至 和水蒸气的热化学方程式
和水蒸气的热化学方程式_______ 。
②尿素水溶液热解产生的 可去除尾气中的
可去除尾气中的 ,流程如下:
,流程如下:

a.尿素 中氮元素的化合价为
中氮元素的化合价为_______ 。
b.若氧化处理后的尾气中混有 ,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低
,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低 的去除率。试分析硫酸盐的产生过程
的去除率。试分析硫酸盐的产生过程_______ 。
③某脱硝反应机理如图-1所示, 参与Ⅰ的反应方程式为
参与Ⅰ的反应方程式为_______ 。

(2)氧化法: 氧化性强于
氧化性强于 ,能更有效地氧化
,能更有效地氧化 。
。
Ⅰ:
Ⅱ: (活化能
(活化能 )
)
Ⅲ: (活化能
(活化能 )
)
 可经
可经 处理后再用碱液吸收而实现脱除。为分析氧化时温度对
处理后再用碱液吸收而实现脱除。为分析氧化时温度对 脱除率的影响,将
脱除率的影响,将 与
与 混合反应一段时间,再用碱液吸收氧化后的气体。其他条件相同时,脱除率随
混合反应一段时间,再用碱液吸收氧化后的气体。其他条件相同时,脱除率随 与
与 混合反应温度变化如图-2所示。试分析在
混合反应温度变化如图-2所示。试分析在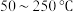 范围内,随着温度的升高
范围内,随着温度的升高 脱除率先几乎不变后下降的可能原因是
脱除率先几乎不变后下降的可能原因是_______ 。

(3)研究表明氮氧化物的脱除率除了与还原剂、氧化剂、催化剂相关外,还取决于催化剂表面氧缺位的密集程度。以 (A、B均为过渡元素)为催化剂,用
(A、B均为过渡元素)为催化剂,用 还原
还原 的机理如下:
的机理如下:
第一阶段: (不稳定)
(不稳定) 低价态的金属离子(还原前后催化剂中金属原子的个数不变)
低价态的金属离子(还原前后催化剂中金属原子的个数不变)
第二阶段:Ⅰ.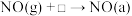 Ⅱ.
Ⅱ.
Ⅲ. Ⅳ.
Ⅳ.
Ⅴ.
注:表示催化剂表面的氧缺位,g表示气态,a表示吸附态
第一阶段用氢气还原 得到低价态的金属离子越多,第二阶段反应的速率越快,原因是
得到低价态的金属离子越多,第二阶段反应的速率越快,原因是_______ 。
(1)还原法:①用
 催化还原
催化还原 可以消除氮氧化物的污染。已知:
可以消除氮氧化物的污染。已知:ⅰ:

ⅱ:

写出
 还原
还原 至
至 和水蒸气的热化学方程式
和水蒸气的热化学方程式②尿素水溶液热解产生的
 可去除尾气中的
可去除尾气中的 ,流程如下:
,流程如下:
a.尿素
 中氮元素的化合价为
中氮元素的化合价为b.若氧化处理后的尾气中混有
 ,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低
,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低 的去除率。试分析硫酸盐的产生过程
的去除率。试分析硫酸盐的产生过程③某脱硝反应机理如图-1所示,
 参与Ⅰ的反应方程式为
参与Ⅰ的反应方程式为
(2)氧化法:
 氧化性强于
氧化性强于 ,能更有效地氧化
,能更有效地氧化 。
。Ⅰ:

Ⅱ:
 (活化能
(活化能 )
)Ⅲ:
 (活化能
(活化能 )
) 可经
可经 处理后再用碱液吸收而实现脱除。为分析氧化时温度对
处理后再用碱液吸收而实现脱除。为分析氧化时温度对 脱除率的影响,将
脱除率的影响,将 与
与 混合反应一段时间,再用碱液吸收氧化后的气体。其他条件相同时,脱除率随
混合反应一段时间,再用碱液吸收氧化后的气体。其他条件相同时,脱除率随 与
与 混合反应温度变化如图-2所示。试分析在
混合反应温度变化如图-2所示。试分析在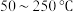 范围内,随着温度的升高
范围内,随着温度的升高 脱除率先几乎不变后下降的可能原因是
脱除率先几乎不变后下降的可能原因是
(3)研究表明氮氧化物的脱除率除了与还原剂、氧化剂、催化剂相关外,还取决于催化剂表面氧缺位的密集程度。以
 (A、B均为过渡元素)为催化剂,用
(A、B均为过渡元素)为催化剂,用 还原
还原 的机理如下:
的机理如下:第一阶段:
 (不稳定)
(不稳定) 低价态的金属离子(还原前后催化剂中金属原子的个数不变)
低价态的金属离子(还原前后催化剂中金属原子的个数不变)第二阶段:Ⅰ.
 Ⅱ.
Ⅱ.
Ⅲ.
 Ⅳ.
Ⅳ.
Ⅴ.

注:表示催化剂表面的氧缺位,g表示气态,a表示吸附态
第一阶段用氢气还原
 得到低价态的金属离子越多,第二阶段反应的速率越快,原因是
得到低价态的金属离子越多,第二阶段反应的速率越快,原因是
您最近一年使用:0次
2022-12-17更新
|
562次组卷
|
3卷引用:江苏省徐州市第七中学2023-2024学年高三上学期10月月考化学试题
名校
解题方法
5 . 工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为: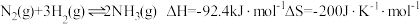
回答下列问题:
(1)合成氨反应在常温下___________ (填“能”或“不能”)自发。
(2)___________ 温(填“高”或“低”,下同)有利于提高反应速率,___________ 温有利于提高平衡转化率,综合考虑催化剂(铁触媒)活性等因素,工业常采用 。
。
针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
(3)方案二: 复合催化剂。
复合催化剂。
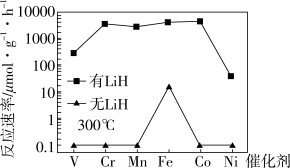
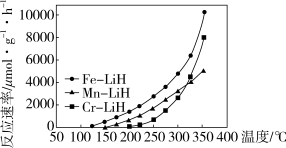
下列说法正确的是___________ 。
a. 时,复合催化剂比单一催化剂效率更高
时,复合催化剂比单一催化剂效率更高
b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(4)某合成氨速率方程为: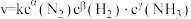 ,根据表中数据,
,根据表中数据,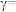
___________ ;
在合成氨过程中,需要不断分离出氨的原因为___________ 。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
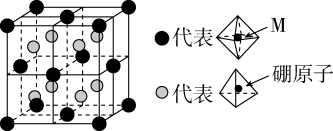
(5)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为 配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为
配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为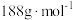 ,则M元素为
,则M元素为___________ (填元素符号);在该化合物中,M离子的价电子排布式为___________ 。
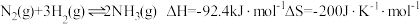
回答下列问题:
(1)合成氨反应在常温下
(2)
 。
。针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
(3)方案二:
 复合催化剂。
复合催化剂。

下列说法正确的是
a.
 时,复合催化剂比单一催化剂效率更高
时,复合催化剂比单一催化剂效率更高b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(4)某合成氨速率方程为:
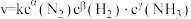 ,根据表中数据,
,根据表中数据,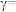
| 实验 | 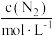 | 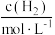 |  | 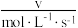 |
| 1 | m | n | p | q |
| 2 | 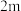 | n | p |  |
| 3 | m | n |  | 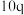 |
| 4 | m |  | p | 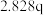 |
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
(5)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为
 配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为
配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为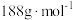 ,则M元素为
,则M元素为
您最近一年使用:0次
6 . SO2、NOx是空气的主要污染物,有效去除大气中的SO2、NOx可以保护大气环境。含氮废水氨态氮(以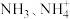 存在)和硝态氨(以
存在)和硝态氨(以 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。
(1)用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中SO2的相关反应的热化学方程式如下:



反应 的∆H=
的∆H=_____ 
(2)已知拆开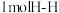 键,
键,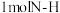 键,
键, 键分别需要的能量是
键分别需要的能量是 、
、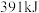 、
、 ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为
,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为_______
(3)SO2和NOx是主要大气污染物,利用如图装置可同时吸收SO2和NO。

①a是直流电源的_______ 极
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为_______
③写出电解池中发生反应的离子方程式:_______
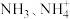 存在)和硝态氨(以
存在)和硝态氨(以 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。(1)用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中SO2的相关反应的热化学方程式如下:



反应
 的∆H=
的∆H=
(2)已知拆开
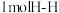 键,
键,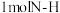 键,
键, 键分别需要的能量是
键分别需要的能量是 、
、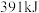 、
、 ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为
,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为(3)SO2和NOx是主要大气污染物,利用如图装置可同时吸收SO2和NO。

①a是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
③写出电解池中发生反应的离子方程式:
您最近一年使用:0次
名校
解题方法
7 . CH4—CO2重整反应能够有效去除大气中 CO2,是实现“碳中和”的重要途径之一,发生的反应如下:
重整反应 CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH
积炭反应Ⅰ 2CO(g)=CO2(g)+C(s) ΔH1=―172 kJ·mol-1
积炭反应Ⅱ CH4(g)=C(s)+2H2(g) ΔH2=+75kJ·mol-1
在恒压、起始投料比 =1条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
=1条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
重整反应 CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH
积炭反应Ⅰ 2CO(g)=CO2(g)+C(s) ΔH1=―172 kJ·mol-1
积炭反应Ⅱ CH4(g)=C(s)+2H2(g) ΔH2=+75kJ·mol-1
在恒压、起始投料比
 =1条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
=1条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
| A.重整反应的反应热ΔH=-247 kJ·mol-1 |
| B.曲线B表示CH4平衡时物质的量随温度的变化 |
| C.积炭会导致催化剂失活,降低CH4的平衡转化率 |
| D.低于600℃时,降低温度有利于减少积炭的量并去除CO2气体 |
您最近一年使用:0次
2022-06-08更新
|
803次组卷
|
7卷引用:江苏省徐州市第七中学2022-2023学年高三上学期10月学情调研化学试题
江苏省徐州市第七中学2022-2023学年高三上学期10月学情调研化学试题江苏省南通市海安高级中学2022-2023学年高三上学期第二次月考化学试题江苏省常熟中学2023-2024学年高三上学期阶段性抽测一化学试题2024届江苏省常熟市中学高三上学期阶段性抽测一 化学试题江苏省泰州市2021-2022学年高三下学期第四次调研测试化学试题(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)FHgkyldyjhx11
解题方法
8 . 关于反应CO2(g)+CH4(g)=2CO(g)+2H2(g);ΔH1=247kJ·mol-1说法正确的是
| A.该反应在任何温度下都可自发进行 |
| B.反应CO2(s)+CH4(g)=2CO(g)+2H2(g);ΔH2<247kJ·mol-1 |
| C.反应中每生成1molH2,转移电子的数目为3×6.02×1023 |
| D.在过渡元素区域内选择高效催化剂可以降低反应的焓变,提高化学反应速率 |
您最近一年使用:0次
解题方法
9 .  是自然界中的重要碳源,
是自然界中的重要碳源, 综合利用是日前的研究热点.
综合利用是日前的研究热点.
(1)工业上已经实现 与
与 反应合成甲醇.在一恒温、恒容密闭容器中充入
反应合成甲醇.在一恒温、恒容密闭容器中充入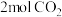 和
和 ,一定条件下发生反应:
,一定条件下发生反应: 。测得
。测得 和
和 的浓度随时间变化如图所示。请回答:
的浓度随时间变化如图所示。请回答:

① 内,用
内,用 表示的平均反应速率
表示的平均反应速率
_______ 
②能够判断该反应达到平衡状态的是_______ (填选项)
a. 和
和 的浓度相等
的浓度相等
b.混合气体的总物质的量不再改变
c.消耗 同时生成
同时生成
d.
(2)中科院大连化学物理研究所的科研人员在新型纳米催化剂 和
和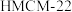 的表面将
的表面将 转化为烷烃
转化为烷烃
①已知在纳米催化剂 表面,
表面, 与
与 完全反应生成CO和气态
完全反应生成CO和气态 时吸收
时吸收 的能量,则该反应的热化学方程式为
的能量,则该反应的热化学方程式为_______
②催化剂中 的制备方法如下:将一定比例的
的制备方法如下:将一定比例的 和
和 溶于盐酸,然后在
溶于盐酸,然后在 下逐滴加入
下逐滴加入 溶液,继续搅拌,得
溶液,继续搅拌,得 ,写出该反应的离子方程式
,写出该反应的离子方程式_______
 是自然界中的重要碳源,
是自然界中的重要碳源, 综合利用是日前的研究热点.
综合利用是日前的研究热点.(1)工业上已经实现
 与
与 反应合成甲醇.在一恒温、恒容密闭容器中充入
反应合成甲醇.在一恒温、恒容密闭容器中充入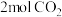 和
和 ,一定条件下发生反应:
,一定条件下发生反应: 。测得
。测得 和
和 的浓度随时间变化如图所示。请回答:
的浓度随时间变化如图所示。请回答:
①
 内,用
内,用 表示的平均反应速率
表示的平均反应速率

②能够判断该反应达到平衡状态的是
a.
 和
和 的浓度相等
的浓度相等b.混合气体的总物质的量不再改变
c.消耗
 同时生成
同时生成
d.

(2)中科院大连化学物理研究所的科研人员在新型纳米催化剂
 和
和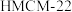 的表面将
的表面将 转化为烷烃
转化为烷烃①已知在纳米催化剂
 表面,
表面, 与
与 完全反应生成CO和气态
完全反应生成CO和气态 时吸收
时吸收 的能量,则该反应的热化学方程式为
的能量,则该反应的热化学方程式为②催化剂中
 的制备方法如下:将一定比例的
的制备方法如下:将一定比例的 和
和 溶于盐酸,然后在
溶于盐酸,然后在 下逐滴加入
下逐滴加入 溶液,继续搅拌,得
溶液,继续搅拌,得 ,写出该反应的离子方程式
,写出该反应的离子方程式
您最近一年使用:0次
解题方法
10 .  是重要的化工原料,工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成
是重要的化工原料,工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成 ,生成的一氧化氮与残余的氧气继续反应生成二氧化氮:
,生成的一氧化氮与残余的氧气继续反应生成二氧化氮: 。下列说法正确的是
。下列说法正确的是
 是重要的化工原料,工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成
是重要的化工原料,工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成 ,生成的一氧化氮与残余的氧气继续反应生成二氧化氮:
,生成的一氧化氮与残余的氧气继续反应生成二氧化氮: 。下列说法正确的是
。下列说法正确的是A. 和 和 都是常用的化肥 都是常用的化肥 |
B. 和 和 受热时都易分解 受热时都易分解 |
C.工业利用 的还原性与 的还原性与 合成尿素 合成尿素 |
D. |
您最近一年使用:0次



