名校
1 . 金属矿物常以硫化物形式存在,如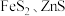 等。
等。
Ⅰ.掺烧 和
和 ,用于制铁精粉和硫酸
,用于制铁精粉和硫酸
(1)已知: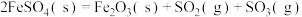 为吸热反应。
为吸热反应。 时,
时, 固体在
固体在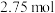 氧气中完全燃烧生成气态
氧气中完全燃烧生成气态 和
和 固体,放出
固体,放出 热量。
热量。
① 与
与 反应的热化学方程式为
反应的热化学方程式为_________ 。
②将 与
与 掺烧(混合燃烧),其目的包括
掺烧(混合燃烧),其目的包括_________ (填字母)。
 节约燃料和能量
节约燃料和能量  为制备硫酸提供原料
为制备硫酸提供原料  减少空气污染
减少空气污染
(2) 常带一定量的结晶水。
常带一定量的结晶水。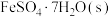 分解脱水反应的能量变化如图所示。
分解脱水反应的能量变化如图所示。
_________  。
。
②为维持炉内温度基本不变, 所带结晶水越多,掺烧比
所带结晶水越多,掺烧比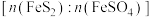 应
应_________ 。(填“增大”“减小”或“不变”)。
Ⅱ.浸出法处理
(3) 难溶于水,处理
难溶于水,处理 常使用酸浸法,两步反应依次为:
常使用酸浸法,两步反应依次为:
ⅰ.
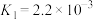
ⅱ.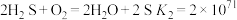
①平衡常数 的表达式为
的表达式为_________ 。
②仅发生反应ⅰ时, 酸浸效果不好,结合平衡常数说明原因:
酸浸效果不好,结合平衡常数说明原因:_________ 。
(4)从平衡移动角度解释通入 在
在 酸浸过程中的作用:
酸浸过程中的作用:_________ 。
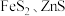 等。
等。Ⅰ.掺烧
 和
和 ,用于制铁精粉和硫酸
,用于制铁精粉和硫酸(1)已知:
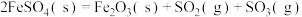 为吸热反应。
为吸热反应。 时,
时, 固体在
固体在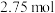 氧气中完全燃烧生成气态
氧气中完全燃烧生成气态 和
和 固体,放出
固体,放出 热量。
热量。①
 与
与 反应的热化学方程式为
反应的热化学方程式为②将
 与
与 掺烧(混合燃烧),其目的包括
掺烧(混合燃烧),其目的包括 节约燃料和能量
节约燃料和能量  为制备硫酸提供原料
为制备硫酸提供原料  减少空气污染
减少空气污染(2)
 常带一定量的结晶水。
常带一定量的结晶水。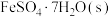 分解脱水反应的能量变化如图所示。
分解脱水反应的能量变化如图所示。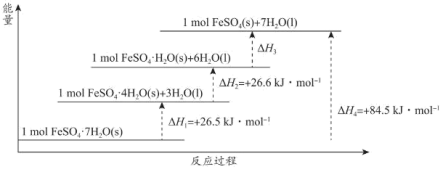

 。
。②为维持炉内温度基本不变,
 所带结晶水越多,掺烧比
所带结晶水越多,掺烧比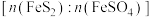 应
应Ⅱ.浸出法处理

(3)
 难溶于水,处理
难溶于水,处理 常使用酸浸法,两步反应依次为:
常使用酸浸法,两步反应依次为:ⅰ.

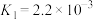
ⅱ.
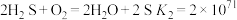
①平衡常数
 的表达式为
的表达式为②仅发生反应ⅰ时,
 酸浸效果不好,结合平衡常数说明原因:
酸浸效果不好,结合平衡常数说明原因:(4)从平衡移动角度解释通入
 在
在 酸浸过程中的作用:
酸浸过程中的作用:
您最近半年使用:0次
2 .  与
与 能发生反应:
能发生反应: 。
。
已知:①该反应由两个基元反应分步完成,第一步为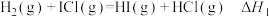
②两步反应的活化能分别为 、
、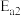 ,且
,且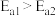
下列判断不正确 的是
 与
与 能发生反应:
能发生反应: 。
。已知:①该反应由两个基元反应分步完成,第一步为
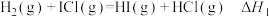
②两步反应的活化能分别为
 、
、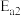 ,且
,且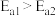
下列判断
| A.第一步为非氧化还原反应 |
| B.第一步的化学反应速率小于第二步的化学反应速率 |
C.已知键能: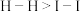 ,可推知键能: ,可推知键能: |
D.第二步的热化学方程式为 |
您最近半年使用:0次
3 . 我国力争于2030年前完成碳达峰,2060年前实现碳中和。 含量的控制和
含量的控制和 资源利用具有重要的研究价值和现实意义。
资源利用具有重要的研究价值和现实意义。
(1)燃煤烟气中的 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。
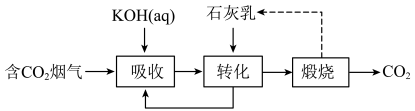
写出
充分 吸收 的化学方程式为
的化学方程式为________________ 。
(2)合成尿素 是利用
是利用 的途径之一。通过两步反应实现,其能量变化示意图所示:
的途径之一。通过两步反应实现,其能量变化示意图所示:
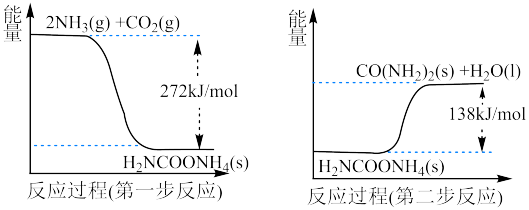
① 与
与 反应生成尿素的热化学方程式为
反应生成尿素的热化学方程式为________________ 。
②工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有________ .(填序号)
a.升高温度 b.加入催化剂
c.将尿素及时分离出去 d.增大反应体系的压强
(3)用 充分吸收
充分吸收 后,将溶液进行电解,可实现
后,将溶液进行电解,可实现 转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的
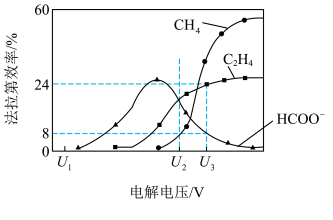
转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率 (FE%)随电解电压的变化如图所示。
已知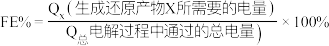
其中,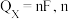 表示电解生成还原产物
表示电解生成还原产物 所转移电子的物质的量,
所转移电子的物质的量, 表示法拉第常数。
表示法拉第常数。
①当电解电压为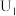 时,电解过程中含碳还原产物的
时,电解过程中含碳还原产物的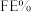 为0,阴极主要还原产物为
为0,阴极主要还原产物为________ (填化学式)。
②当电解电压为 时,阴极生成
时,阴极生成 的电极反应式为
的电极反应式为________________ .
③当电解电压为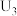 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为________ .
 含量的控制和
含量的控制和 资源利用具有重要的研究价值和现实意义。
资源利用具有重要的研究价值和现实意义。(1)燃煤烟气中的
 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。
写出

 的化学方程式为
的化学方程式为(2)合成尿素
 是利用
是利用 的途径之一。通过两步反应实现,其能量变化示意图所示:
的途径之一。通过两步反应实现,其能量变化示意图所示:
①
 与
与 反应生成尿素的热化学方程式为
反应生成尿素的热化学方程式为②工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有
a.升高温度 b.加入催化剂
c.将尿素及时分离出去 d.增大反应体系的压强
(3)用
 充分吸收
充分吸收 后,将溶液进行电解,可实现
后,将溶液进行电解,可实现 转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的
转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的
已知
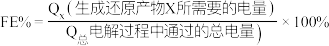
其中,
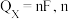 表示电解生成还原产物
表示电解生成还原产物 所转移电子的物质的量,
所转移电子的物质的量, 表示法拉第常数。
表示法拉第常数。①当电解电压为
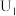 时,电解过程中含碳还原产物的
时,电解过程中含碳还原产物的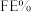 为0,阴极主要还原产物为
为0,阴极主要还原产物为②当电解电压为
 时,阴极生成
时,阴极生成 的电极反应式为
的电极反应式为③当电解电压为
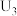 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
名校
4 . 完成下列问题
(1)消除汽车尾气中的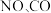 ,有利于减少
,有利于减少 的排放。已知如下信息:
的排放。已知如下信息:
Ⅰ.
Ⅱ.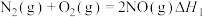

①
___________ 。
②在催化剂作用下 和
和 转化为无毒气体,写出反应的热化学方程式
转化为无毒气体,写出反应的热化学方程式___________ 。
(2)测定汽车尾气常用的方法有两种。
①方法1:电化学气敏传感器法。其中 传感器的工作原理如图所示,则工作电极的电极反应式为
传感器的工作原理如图所示,则工作电极的电极反应式为___________ 。
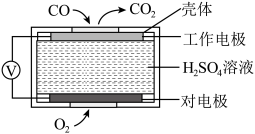
②方法2:氧化还原滴定法。用 溶液吸收尾气,将氮氧化物转化为硝酸,用酸碱中和滴定法测定硝酸浓度。写出
溶液吸收尾气,将氮氧化物转化为硝酸,用酸碱中和滴定法测定硝酸浓度。写出 与
与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(3)中药在世界医学界越来越受到关注。中药药剂砒霜(主要成分 )可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注。查文献得知,可以从硫化砷(As2S3)废渣中提取
)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注。查文献得知,可以从硫化砷(As2S3)废渣中提取 ,提取的工艺流程简图如下:
,提取的工艺流程简图如下:

①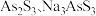 中的S均为-2价,碱浸过程中发生的反应
中的S均为-2价,碱浸过程中发生的反应___________ (填“是”或“是”)氧化还原反应。
②写出过程Ⅲ的离子方程式___________ 。
(4)亚砷酸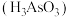 也可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液
也可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液 关系如下图所示。
关系如下图所示。
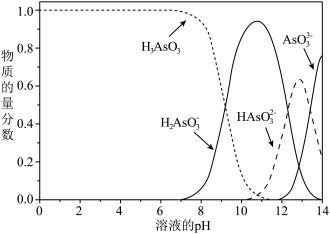
①人体血液的 在
在 之间,用药后人体中含砷元素的主要微粒是
之间,用药后人体中含砷元素的主要微粒是___________ 。
②将 溶液滴入亚砷酸溶液,当
溶液滴入亚砷酸溶液,当 调至11时发生反应的离子方程式是
调至11时发生反应的离子方程式是___________ 。
(1)消除汽车尾气中的
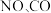 ,有利于减少
,有利于减少 的排放。已知如下信息:
的排放。已知如下信息:Ⅰ.

Ⅱ.
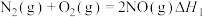

①

②在催化剂作用下
 和
和 转化为无毒气体,写出反应的热化学方程式
转化为无毒气体,写出反应的热化学方程式(2)测定汽车尾气常用的方法有两种。
①方法1:电化学气敏传感器法。其中
 传感器的工作原理如图所示,则工作电极的电极反应式为
传感器的工作原理如图所示,则工作电极的电极反应式为
②方法2:氧化还原滴定法。用
 溶液吸收尾气,将氮氧化物转化为硝酸,用酸碱中和滴定法测定硝酸浓度。写出
溶液吸收尾气,将氮氧化物转化为硝酸,用酸碱中和滴定法测定硝酸浓度。写出 与
与 溶液反应的离子方程式
溶液反应的离子方程式(3)中药在世界医学界越来越受到关注。中药药剂砒霜(主要成分
 )可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注。查文献得知,可以从硫化砷(As2S3)废渣中提取
)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注。查文献得知,可以从硫化砷(As2S3)废渣中提取 ,提取的工艺流程简图如下:
,提取的工艺流程简图如下:
①
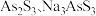 中的S均为-2价,碱浸过程中发生的反应
中的S均为-2价,碱浸过程中发生的反应②写出过程Ⅲ的离子方程式
(4)亚砷酸
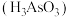 也可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液
也可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液 关系如下图所示。
关系如下图所示。
①人体血液的
 在
在 之间,用药后人体中含砷元素的主要微粒是
之间,用药后人体中含砷元素的主要微粒是②将
 溶液滴入亚砷酸溶液,当
溶液滴入亚砷酸溶液,当 调至11时发生反应的离子方程式是
调至11时发生反应的离子方程式是
您最近半年使用:0次
名校
解题方法
5 . 利用 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。
(1)20世纪初,工业上以 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
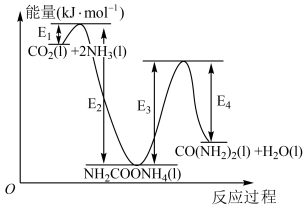
①反应物液氨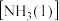 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在___________ (填作用力名称)。
②写出在该条件下由 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:___________ 。
(2)近年研究发现,电催化 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
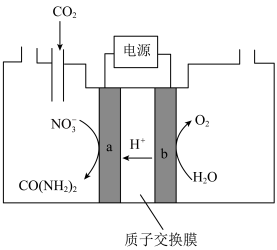
①电解过程中生成尿素的电极反应式为___________ 。
②目前以 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到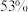 的法拉第效率
的法拉第效率 。已知:
。已知: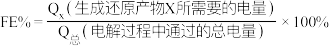 ,其中,
,其中,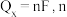 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下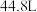 的
的 ,可获得尿素的质量为
,可获得尿素的质量为___________ 。(尿素的相对分子质量:60)
(3)尿素样品含氮量的测定方法如下。
已知:溶液中 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。

①消化液中的含氮粒子是___________ 。
②步骤ⅳ中标准 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有___________ 。
 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。(1)20世纪初,工业上以
 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
①反应物液氨
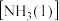 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在②写出在该条件下由
 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:(2)近年研究发现,电催化
 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
①电解过程中生成尿素的电极反应式为
②目前以
 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到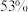 的法拉第效率
的法拉第效率 。已知:
。已知: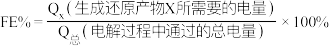 ,其中,
,其中,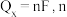 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下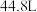 的
的 ,可获得尿素的质量为
,可获得尿素的质量为(3)尿素样品含氮量的测定方法如下。
已知:溶液中
 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。
①消化液中的含氮粒子是
②步骤ⅳ中标准
 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
您最近半年使用:0次
名校
解题方法
6 . 用甲烷制高纯氢气是目前研究热点之一、
(1)一定条件下,CH4(g) C(s) + 2H2(g) 反应历程如图1所示,其中化学反应速率最慢的反应过程为
C(s) + 2H2(g) 反应历程如图1所示,其中化学反应速率最慢的反应过程为___________ 。

(2)甲烷水蒸气催化重整可制得较高纯度的氢气,相关反应如下。
反应Ⅰ CH4(g) + H2O(g) CO(g) + 3H2(g) ∆H1 = +206 kJ·mol-1
CO(g) + 3H2(g) ∆H1 = +206 kJ·mol-1
反应Ⅱ CO(g) + H2O(g) CO2(g) + H2(g) ΔH2= -41 kJ·mol-1
CO2(g) + H2(g) ΔH2= -41 kJ·mol-1
① 总反应:CH4(g) + 2H2O(g) CO2(g) + 4H2(g) ΔH =
CO2(g) + 4H2(g) ΔH = ___________
② 1000 ℃恒容密闭容器(2L)中发生反应Ⅰ,已知1000 ℃时,反应I的平衡常数K=2,请结合K、Q关系判断:若容器中 n(CH4) =n(H2O)= n(H2)= 1 mol 、n(CO)=2 mol 时,反应处于___________ 状态(正向进行、逆向进行、平衡)。
③ 已知830 ℃时,反应II的平衡常数K=1。在容积不变的密闭容器中,将2 mol CO与8 mol H2O混合加热到830 ℃,反应达平衡时CO的转化率为___________ 。
④ 在常压、600 ℃条件下,甲烷制备氢气的总反应中H2平衡产率为82%。若加入适量生石灰后H2的产率可提高到95%,应用化学平衡移动原理解释原因___________ 。
(3)科学家研究将CH4、H2O与CH4、CO2联合重整制备氢气:
反应Ⅰ:CH4(g) + H2O(g) CO(g) + 3H2(g) ∆H1 = +206 kJ·mol-1
CO(g) + 3H2(g) ∆H1 = +206 kJ·mol-1
反应Ⅲ:CH4(g) + CO2(g) 2CO(g) + 2H2(g) ΔH3= +247 kJ·mol-1
2CO(g) + 2H2(g) ΔH3= +247 kJ·mol-1
常压下,将CH4、H2O和CO2按一定比例混合置于密闭容器中,相同时间不同温度下测得体系中n(H2): n(CO)变化如图2所示。
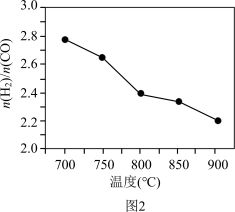
① 已知700℃、NiO催化剂条件下,向反应体系中加入少量O2可增加H2产率,此条件下还原性CO___________ H2(填“>”“<”或“=”)。
② 随着温度升高n(H2) : n(CO)变小的原因可能是___________ 。
(1)一定条件下,CH4(g)
 C(s) + 2H2(g) 反应历程如图1所示,其中化学反应速率最慢的反应过程为
C(s) + 2H2(g) 反应历程如图1所示,其中化学反应速率最慢的反应过程为
(2)甲烷水蒸气催化重整可制得较高纯度的氢气,相关反应如下。
反应Ⅰ CH4(g) + H2O(g)
 CO(g) + 3H2(g) ∆H1 = +206 kJ·mol-1
CO(g) + 3H2(g) ∆H1 = +206 kJ·mol-1反应Ⅱ CO(g) + H2O(g)
 CO2(g) + H2(g) ΔH2= -41 kJ·mol-1
CO2(g) + H2(g) ΔH2= -41 kJ·mol-1① 总反应:CH4(g) + 2H2O(g)
 CO2(g) + 4H2(g) ΔH =
CO2(g) + 4H2(g) ΔH = ② 1000 ℃恒容密闭容器(2L)中发生反应Ⅰ,已知1000 ℃时,反应I的平衡常数K=2,请结合K、Q关系判断:若容器中 n(CH4) =n(H2O)= n(H2)= 1 mol 、n(CO)=2 mol 时,反应处于
③ 已知830 ℃时,反应II的平衡常数K=1。在容积不变的密闭容器中,将2 mol CO与8 mol H2O混合加热到830 ℃,反应达平衡时CO的转化率为
④ 在常压、600 ℃条件下,甲烷制备氢气的总反应中H2平衡产率为82%。若加入适量生石灰后H2的产率可提高到95%,应用化学平衡移动原理解释原因
(3)科学家研究将CH4、H2O与CH4、CO2联合重整制备氢气:
反应Ⅰ:CH4(g) + H2O(g)
 CO(g) + 3H2(g) ∆H1 = +206 kJ·mol-1
CO(g) + 3H2(g) ∆H1 = +206 kJ·mol-1反应Ⅲ:CH4(g) + CO2(g)
 2CO(g) + 2H2(g) ΔH3= +247 kJ·mol-1
2CO(g) + 2H2(g) ΔH3= +247 kJ·mol-1常压下,将CH4、H2O和CO2按一定比例混合置于密闭容器中,相同时间不同温度下测得体系中n(H2): n(CO)变化如图2所示。

① 已知700℃、NiO催化剂条件下,向反应体系中加入少量O2可增加H2产率,此条件下还原性CO
② 随着温度升高n(H2) : n(CO)变小的原因可能是
您最近半年使用:0次
7 . 已知: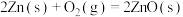
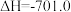 kJ·mol-1
kJ·mol-1

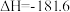 kJ·mol-1
kJ·mol-1
则反应 的
的 为
为
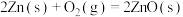
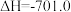 kJ·mol-1
kJ·mol-1
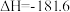 kJ·mol-1
kJ·mol-1则反应
 的
的 为
为| A.+519.4kJ⋅mol-1 | B.-259.7kJ⋅mol-1 | C.+259.7kJ⋅mol-1 | D.-519.4kJ⋅mol-1 |
您最近半年使用:0次
2024-02-07更新
|
324次组卷
|
90卷引用:北京市顺义区第一中学2022-2023学年高二上学期10月月考化学试题
北京市顺义区第一中学2022-2023学年高二上学期10月月考化学试题北京市和平街第一中学2023-2024学年高二上学期10月阶段性练习化学试题北京市首都师范大学附属中学2023-2024学年高二上学期9月检测化学试题(已下线)2012届山东省济宁一中高三上学期第二次定时练习化学试卷(已下线)2012-2013学年江苏省如皋中学高二10月阶段练习化学试卷(已下线)2012-2013学年陕西省三原县北城中学高二第四次月考化学试卷(已下线)2013届广东省佛山一中高三第二次段考化学试卷(已下线)2015届吉林省汪清县第六中学高三第三次月考化学试卷2014-2015学年内蒙古巴市一中高二10月月考化学试卷2015-2016学年山西太原五中高二上第一周考理科化学试卷2016届福建省三明一中高三上学期第二次月考化学试卷2015-2016学年四川省南充市老林中学高二上学期9月月考化学试卷2017届山东省枣庄三中高三上学期9月质检化学试卷2016-2017学年贵州省湄潭县湄江中学高二上第一次月考化学试卷2016-2017学年河南省南阳市宛东五校高二上第一次联考化学试卷2017届河北邯郸市大名一中高三上学期第二次月考化学试卷2016-2017学年安徽省合肥一中高二上月考一化学试卷2017届福建省柘荣一中、宁德中学高三上联考一化学卷宁夏育才中学2017-2018学年高二9月月考化学试题山东省垦利第一中学2017-2018学年高二上学期第一次月考化学试题河北省邢台第三中学2017-2018学年高二9月月考化学试题【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题北京四中2018-2019学年高一下学期期末考试化学试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(学考)试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(选考)试题河南省周口中英文学校2019-2020学年高二上学期第一次月考化学试题河南省郑州市106中学2019-2020学年高二9月月考化学(理)试题云南省曲靖市会泽县茚旺高级中学2020届高三上学期11月月考化学试题安徽省涡阳县第一中学2019-2020学年高二12月月考化学试题辽宁省凌源市第三中学2019-2020学年高二下学期第一次月考化学试题宁夏银川市宁夏大学附属中学2019-2020学年高二下期第二次月考化学试题广东省揭阳市揭西县河婆中学2020-2021学年高二上学期第一次月考化学试题黑龙江省牡丹江市第三高级中学2021-2022学年高三上学期第四次月考化学试题四川省峨眉第二中学校2021-2022学年高二下学期5月月考化学试题四川省广安第二中学校2021-2022学年高二上学期第一次月考化学试题辽宁省阜新市第二高级中学2022-2023学年高二上学期9月月考化学试题云南省宣威市第三中学2023-2024学年高二上学期第四次月考化学试题山东省菏泽市外国语学校2023-2024学年高二上学期化学10月份月考试题(已下线)2011-2012学年黑龙江省牡丹江一中高二上学期期末考试化学试卷(已下线)2011-2012学年浙江省杭州十四中高二上学期期末化学试卷(已下线)2011-2012学年天津一中高二上学期期中考试化学试卷(已下线)2012届陕西省兴平市秦岭中学高三上学期期末练习化学试卷(已下线)2011-2012学年浙江省嘉兴一中高一下学期期中考试化学试卷(已下线)2011-2012学年天津市天津一中高二上学期期中考试化学试卷(已下线)2012-2013学年江苏泰州二中高二上学期期中考试化学(选修)试卷(已下线)2013-2014学年天津市红桥区高二上学期期末考试化学试卷(已下线)2014陕西省西安中学高三上学期第三次质量检测化学试卷(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷(已下线)2014秋安徽省宿州市高二上学期期中化学(理)试卷2014-2015学年黑龙江省伊春市伊春二中高二上学期期中化学试卷2014-2015学年云南省景洪市第四中学高二下学期期中考试化学试卷2015-2016学年福建省宁德市霞浦七中高二上期中(理)化学试卷2015-2016学年山东省淄博市淄川一中等三校高二上期末联考化学试卷2015-2016学年河北省沧州一中高一下期末化学试卷2015-2016学年福建省福州市文博中学高二上期中化学试卷黑龙江省大庆市第十中学2016-2017学年高一下学期期末考试化学试题湖北省武汉市武昌区2017_2018学年高二化学上学期期中化学试题黑龙江省哈尔滨市第三中学2017-2018届高二上学期模块考试(期末)化学试题安徽省滁州市(九校)2017-2018学年高二上学期期末考试化学试题【全国百强校】黑龙江省哈尔滨师范大学附属中学2017-2018学年高一下学期期末考试(理)化学试题人教版高二化学选修四专题:化学反应热的计算同步练习卷【全国百强校】贵州省铜仁市第一中学2018-2019学年高二上学期期中考试化学试题福建省莆田市第八中学2018-2019学年高二(理)上学期期中考试化学试题海南省海口市第四中学2020届高三上学期摸底考试化学试题甘肃省永昌四中2019-2020学年高二上学期期中考试化学试题步步为赢 高二化学寒假作业:作业一 化学反应中的能量变化西藏自治区日喀则市南木林高级中学2019-2020学年高二上学期期中化学试题黑龙江省牡丹江市第三高级中学2019-2020学年高二上学期期末考试化学试题河南省周口市扶沟县包屯高中2019---2020学年高二上期期末考试化学试题甘肃省张掖市高台县第一中学2018-2019学年高二上学期期末考试理科化学试题(已下线)1.3.2 反应热的计算(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)山东省滕州市第一中学2020-2021学年高二9月开学收心考试化学试题四川省成都市蓉城高中教育联盟2019-2020学年高二上学期期中联考化学试题福建省漳州市平和县第一中学2021届高三上学期期中考试化学试题吉林油田第十一中学2020-2021学年高二上学期期中考试化学试题四川省达州市宣汉县第二中学2020-2021学年高二上学期期中考试理综化学试题广东省江门市第二中学2020-2021学年高二上学期第二次考试(期中)化学试题河北省张家口市宣化一中2020-2021学年高二上学期期末考试化学试题海南省海南鑫源高级中学2019-2020学年高二上学期期中考试化学试题2011年普通高等学校招生全国统一考试化学(海南卷)海南省鑫源中学2021-2022学年高二上学期期中考试化学试题新疆喀什第二中学2022-2023学年高二上学期期中考试化学试题青海省西宁市海湖中学2022-2023学年高二上学期期末考试化学试题海南省临高县新盈中学2021-2022学年高二上学期(1-4班)期中考试化学试题第3课时 反应焓变的计算第一章 第二节 反应热的计算四川省眉山市仁寿第一中学校(北校区)2023-2024学年高二上学期11月期中化学试题宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】广东省江门市新会第一中学2023-2024学年高二上学期期末考试化学试题四川省泸州市泸县第四中学2023-2024学年高二下学期开学化学试题
名校
解题方法
8 . 氢能是一种清洁能源,按照生产过程中的碳排放情况分为灰氢、蓝氢和绿氢。
(1)煤的气化制得灰氢 :C(s) + H2O(g)  CO(g) + H2(g)。该反应的平衡常数表达式K=
CO(g) + H2(g)。该反应的平衡常数表达式K=_____ 。在恒容容器中发生上述反应,下列说法正确的是_______ 。
a. 升高温度,可提高活化分子百分数
b. 将煤粉碎可提高反应速率
c. 断裂2mol H-O的同时断裂1molH-H,反应达到化学平衡状态
d. 容器内混合气体平均摩尔质量不变时,反应达到化学平衡状态
(2)甲烷水蒸气催化重整制得蓝氢 ,步骤如下。
I.H2的制取:CH4(g) + H2O(g) CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0
①为提高CH4的平衡转化率,可采取的措施有___________ (写出两条即可)。
Ⅱ.H2的富集:CO(g) + H2O(g) CO2(g) + H2(g) ΔH<0
CO2(g) + H2(g) ΔH<0
②已知830 ℃时,该反应的平衡常数K=1.在容积不变的的密闭容器中,将2 mol CO与8 mol H2O混合加热到830 ℃。利用三段式 计算反应达平衡时CO的转化率(书写过程) _______ 。
Ⅲ.用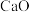 吸收
吸收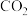 实现低碳排放。
实现低碳排放。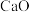 消耗率随时间变化关系如图所示。
消耗率随时间变化关系如图所示。
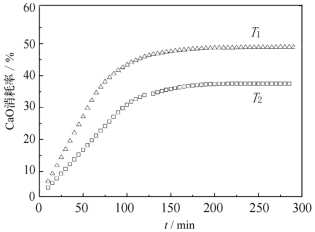
③比较温度高低:T1_____ T2(填“>”或“<”)。
(3)热化学硫碘循环分解水制得绿氢 ,全程零碳排放。反应如下:
反应i:SO2(g) + I2(g) + 2H2O(g) = H2SO4(l) + 2HI(g) ∆H1=-82 kJ·mol−1。
反应ii:2H2SO4(l) = 2SO2(g) + O2(g) + 2H2O(g) ∆H2=+544 kJ·mol−1。
反应iii:∙∙∙∙∙∙
反应ⅰ~iii循环实现分解水:2H2O(g) = 2H2(g) + O2(g) ∆H=+484 kJ·mol−1。
写出反应iii的热化学方程式___________ 。
(1)煤的气化制得
 CO(g) + H2(g)。该反应的平衡常数表达式K=
CO(g) + H2(g)。该反应的平衡常数表达式K=a. 升高温度,可提高活化分子百分数
b. 将煤粉碎可提高反应速率
c. 断裂2mol H-O的同时断裂1molH-H,反应达到化学平衡状态
d. 容器内混合气体平均摩尔质量不变时,反应达到化学平衡状态
(2)甲烷水蒸气催化重整制得
I.H2的制取:CH4(g) + H2O(g)
 CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0①为提高CH4的平衡转化率,可采取的措施有
Ⅱ.H2的富集:CO(g) + H2O(g)
 CO2(g) + H2(g) ΔH<0
CO2(g) + H2(g) ΔH<0②已知830 ℃时,该反应的平衡常数K=1.在容积不变的的密闭容器中,将2 mol CO与8 mol H2O混合加热到830 ℃。利用
Ⅲ.用
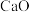 吸收
吸收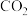 实现低碳排放。
实现低碳排放。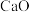 消耗率随时间变化关系如图所示。
消耗率随时间变化关系如图所示。
③比较温度高低:T1
(3)热化学硫碘循环分解水制得
反应i:SO2(g) + I2(g) + 2H2O(g) = H2SO4(l) + 2HI(g) ∆H1=-82 kJ·mol−1。
反应ii:2H2SO4(l) = 2SO2(g) + O2(g) + 2H2O(g) ∆H2=+544 kJ·mol−1。
反应iii:∙∙∙∙∙∙
反应ⅰ~iii循环实现分解水:2H2O(g) = 2H2(g) + O2(g) ∆H=+484 kJ·mol−1。
写出反应iii的热化学方程式
您最近半年使用:0次
名校
解题方法
9 . 研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义。
(1)NO2、SO2的任意排放均可导致酸雨的产生。请分别写出二者产生酸雨的化学方程式_______ 、____ 。
(2)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
① CO(g) + 1/2O2(g) = CO2(g) ΔH = -283.0 kJ/mol
② S(s) + O2(g) = SO2(g) ΔH = -296.0 kJ/mol
此方法涉及的热化学方程式是___________ 。
(3)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
① CO(g) + NO2(g) = NO(g) + CO2(g) ΔH = -a kJ/mol (a>0)
② 2CO(g) + 2NO(g) = N2(g) + 2CO2(g) ΔH = -b kJ/mol (b>0)
若用标准状况下 3.36 L CO 还原 NO2 至 N2(CO完全反应)的整个过程中转移电子的物质的量为_____ mol,放出的热量为___ kJ(用含有a和b的代数式表示)。
(1)NO2、SO2的任意排放均可导致酸雨的产生。请分别写出二者产生酸雨的化学方程式
(2)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
① CO(g) + 1/2O2(g) = CO2(g) ΔH = -283.0 kJ/mol
② S(s) + O2(g) = SO2(g) ΔH = -296.0 kJ/mol
此方法涉及的热化学方程式是
(3)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
① CO(g) + NO2(g) = NO(g) + CO2(g) ΔH = -a kJ/mol (a>0)
② 2CO(g) + 2NO(g) = N2(g) + 2CO2(g) ΔH = -b kJ/mol (b>0)
若用标准状况下 3.36 L CO 还原 NO2 至 N2(CO完全反应)的整个过程中转移电子的物质的量为
您最近半年使用:0次
名校
10 . 用甲烷制高纯氢气是目前研究热点之一。
(1)甲烷水蒸气催化重整可制得较高纯度的氢气,相关反应如下:
反应Ⅰ:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206kJ/mol
CO(g)+3H2(g) ΔH1=+206kJ/mol
反应Ⅱ:CO(g)+H2O(g) CO2(g)+H2(g) ΔH2= -41kJ/mol
CO2(g)+H2(g) ΔH2= -41kJ/mol
①总反应: CH4(g)+2H2O(g) CO2(g)+4H2(g) ΔH=
CO2(g)+4H2(g) ΔH=___________ 。
②已知830℃时,反应II的平衡常数K= 1,在容积不变的密闭容器中,将2molCO、8molH2O混合加热到830℃,反应达平衡时CO的转化率为_________ 。
③在常压、600℃条件下,甲烷制备氢气的总反应中H2平衡产率为82%。加入适量石灰后,H2的产率可提高到95%,利用平衡移动原理解释原因:________ 。
(2)科学家研究将CH4、H2O 与CH4、CO2联合重整制备氢气:
反应Ⅰ:CH4(g)+H2O(g) CO(g) + 3H2(g) ΔH1= +206kJ/mol
CO(g) + 3H2(g) ΔH1= +206kJ/mol
反应Ⅲ:CH4(g) +CO2(g) 2CO(g) + 2H2(g) ΔH3=+247kJ/mol
2CO(g) + 2H2(g) ΔH3=+247kJ/mol
常温下,将CH4、H2O和CO2按一定比例混合置于密闭容器中,相同时间不同温度下测得体系中 变化如图所示。
变化如图所示。

①已知700℃、NiO催化剂条件下,向反应体系中加入少量O2可增加H2产率,此条件下还原性CO______ H2 (填“>”“<"或“=”)。
②随着温度升高 变小的原因可能是
变小的原因可能是___________ 。
(1)甲烷水蒸气催化重整可制得较高纯度的氢气,相关反应如下:
反应Ⅰ:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+206kJ/mol
CO(g)+3H2(g) ΔH1=+206kJ/mol反应Ⅱ:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH2= -41kJ/mol
CO2(g)+H2(g) ΔH2= -41kJ/mol①总反应: CH4(g)+2H2O(g)
 CO2(g)+4H2(g) ΔH=
CO2(g)+4H2(g) ΔH=②已知830℃时,反应II的平衡常数K= 1,在容积不变的密闭容器中,将2molCO、8molH2O混合加热到830℃,反应达平衡时CO的转化率为
③在常压、600℃条件下,甲烷制备氢气的总反应中H2平衡产率为82%。加入适量石灰后,H2的产率可提高到95%,利用平衡移动原理解释原因:
(2)科学家研究将CH4、H2O 与CH4、CO2联合重整制备氢气:
反应Ⅰ:CH4(g)+H2O(g)
 CO(g) + 3H2(g) ΔH1= +206kJ/mol
CO(g) + 3H2(g) ΔH1= +206kJ/mol反应Ⅲ:CH4(g) +CO2(g)
 2CO(g) + 2H2(g) ΔH3=+247kJ/mol
2CO(g) + 2H2(g) ΔH3=+247kJ/mol常温下,将CH4、H2O和CO2按一定比例混合置于密闭容器中,相同时间不同温度下测得体系中
 变化如图所示。
变化如图所示。
①已知700℃、NiO催化剂条件下,向反应体系中加入少量O2可增加H2产率,此条件下还原性CO
②随着温度升高
 变小的原因可能是
变小的原因可能是
您最近半年使用:0次



