名校
解题方法
1 . 光催化是新发展的一个催化技术,TiO2是目前研究成功的应用广泛的光催化剂,它是由金红石矿(主要成分为TiO2)先制备为TiCl4,再转化为纯TiO2。
请根据表中数据作答:
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行___________ ?
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向___________ 。
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向___________ 。
| 物种 | TiO2(s) | TiCl4(g) | Cl2(g) | O2(g) | C(s) | CO(g) |
| ΔrΗΘm /kJ∙molˉ1 | –944.7 | –763.2 | 0 | 0 | 0 | –110.5 |
| SΘm/J∙molˉ1∙Kˉ1 | 55.02 | 354.9 | 223.1 | 205.1 | 5.74 | 197.7 |
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向
您最近半年使用:0次
2 . 为了实现“碳达峰”和“碳中和”的目标,将CO2转化成可利用的化学能源的“负碳”技术是世界各国关注的焦点。
方法Ⅰ:CO2催化加氢制甲醇。
以CO2、H2为原料合成CH3OH涉及的反应如下:
反应i:CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH1=-49.0 kJ·mol-1
CH3OH(g) + H2O(g) ΔH1=-49.0 kJ·mol-1
反应ii:CO2(g) + H2(g) CO(g) + H2O(g) ΔH2= +41.0 kJ·mol-1
CO(g) + H2O(g) ΔH2= +41.0 kJ·mol-1
反应iii:CO(g) + 2H2(g) CH3OH(g) ΔH3=
CH3OH(g) ΔH3=
(1)计算反应iii的ΔH3=___________ 。
(2)一定温度和催化剂条件下,0.73mol H2、0.24mol CO2和0.03mol N2(已知N2不参与反应)在总压强为3.0MPa的密闭容器中进行上述反应,平衡时CO2的转化率、CH3OH和CO的选择性随温度的变化曲线如图所示。
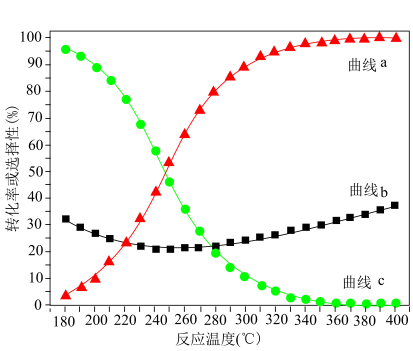
①图中曲线c表示物质___________ 的变化(填“CO2”“CH3OH”或“CO”)。
②上述反应体系在一定条件下建立平衡后,下列说法不正确 的有___________ (填字母)。
A.降低温度,反应i~iii的正、逆反应速率都减小
B.向容器中再通入少量N2,CO2的平衡转化率下降
C.移去部分H2O(g),反应iii向正反应方向衡移动
D.选择合适的催化剂能提高CO2的平衡转化率
③某温度下,t1 min反应到达平衡,测得容器中CH3OH的体积分数为12.5%。此时用CH3OH的分压表示0-t1时间内的反应速率v(CH3OH)=___________ MPa·min-1。设此时n(CO) = a mol,计算该温度下反应ii的平衡常数Kx=___________ (用含有a的代数式表示)。[已知:分压=总压 × 该组分物质的量分数;对于反应mA(g) + nB(g) pC(g) + qD(g),
pC(g) + qD(g),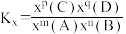 ,x为物质的量分数。]
,x为物质的量分数。]
方法Ⅱ:CO2电解法制甲醇
利用电解原理,可将CO2转化为CH3OH,其装置如图所示:
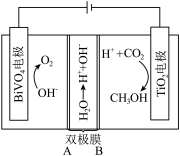
(3)双极膜B侧为___________ (填“阴离子”或“阳离子”)交换膜。
(4)TiO2电极上电极反应方程式:___________ 。
方法Ⅲ:CO2催化加氢制低碳烯烃(2~4个C的烯烃)
某研究小组使用Zn-Ga-O/SAPO-34双功能催化剂实现了CO2直接合成低碳烯烃,并给出了其可能的反应历程(如图所示)。H2首先在Zn-Ga-O表面解离成2个H*,随后参与到CO2的还原过程;SAPO-34则催化生成的甲醇转化为低碳烯烃。
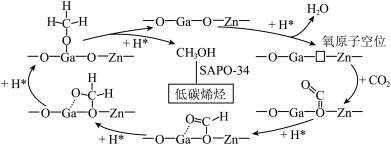
注:☐表示氧原子空位,*表示吸附在催化剂上的微粒。
(5)理论上,反应历程中消耗的H*与生成的甲醇的物质的量之比为___________ 。
方法Ⅰ:CO2催化加氢制甲醇。
以CO2、H2为原料合成CH3OH涉及的反应如下:
反应i:CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ΔH1=-49.0 kJ·mol-1
CH3OH(g) + H2O(g) ΔH1=-49.0 kJ·mol-1反应ii:CO2(g) + H2(g)
 CO(g) + H2O(g) ΔH2= +41.0 kJ·mol-1
CO(g) + H2O(g) ΔH2= +41.0 kJ·mol-1反应iii:CO(g) + 2H2(g)
 CH3OH(g) ΔH3=
CH3OH(g) ΔH3=(1)计算反应iii的ΔH3=
(2)一定温度和催化剂条件下,0.73mol H2、0.24mol CO2和0.03mol N2(已知N2不参与反应)在总压强为3.0MPa的密闭容器中进行上述反应,平衡时CO2的转化率、CH3OH和CO的选择性随温度的变化曲线如图所示。

①图中曲线c表示物质
②上述反应体系在一定条件下建立平衡后,下列说法
A.降低温度,反应i~iii的正、逆反应速率都减小
B.向容器中再通入少量N2,CO2的平衡转化率下降
C.移去部分H2O(g),反应iii向正反应方向衡移动
D.选择合适的催化剂能提高CO2的平衡转化率
③某温度下,t1 min反应到达平衡,测得容器中CH3OH的体积分数为12.5%。此时用CH3OH的分压表示0-t1时间内的反应速率v(CH3OH)=
 pC(g) + qD(g),
pC(g) + qD(g),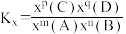 ,x为物质的量分数。]
,x为物质的量分数。] 方法Ⅱ:CO2电解法制甲醇
利用电解原理,可将CO2转化为CH3OH,其装置如图所示:

(3)双极膜B侧为
(4)TiO2电极上电极反应方程式:
方法Ⅲ:CO2催化加氢制低碳烯烃(2~4个C的烯烃)
某研究小组使用Zn-Ga-O/SAPO-34双功能催化剂实现了CO2直接合成低碳烯烃,并给出了其可能的反应历程(如图所示)。H2首先在Zn-Ga-O表面解离成2个H*,随后参与到CO2的还原过程;SAPO-34则催化生成的甲醇转化为低碳烯烃。

注:☐表示氧原子空位,*表示吸附在催化剂上的微粒。
(5)理论上,反应历程中消耗的H*与生成的甲醇的物质的量之比为
您最近半年使用:0次
3 . 利用1-甲基萘(1-MN)制备四氢萘类物质(MTLs,包括1-MTL和5-MTL)。反应过程中伴有生成十氢萘(1-MD)的副反应,涉及反应如图:
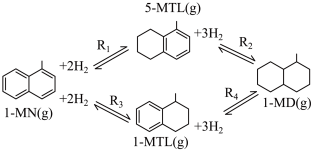
回答下列问题:
(1)1-甲基萘(1-MN)的组成元素电负性由小到大的顺序为___________ 。
(2)已知一定条件下反应 、
、 、
、 的焓变分别为
的焓变分别为 、
、 、
、 ,则反应
,则反应 的焓变为
的焓变为___________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(3)四个平衡体系的平衡常数与温度的关系如图甲所示。
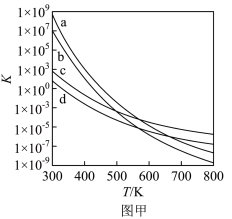
①c、d分别为反应 和
和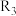 的平衡常数随温度变化的曲线,则表示反应
的平衡常数随温度变化的曲线,则表示反应 的平衡常数随温度变化曲线为
的平衡常数随温度变化曲线为___________ 。
②已知反应 的速率方程
的速率方程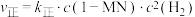 ,
,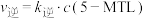 (
( 、
、 分别为正、逆反应速率常数,只与温度、催化剂有关)。温度
分别为正、逆反应速率常数,只与温度、催化剂有关)。温度 下反应达到平衡时
下反应达到平衡时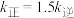 ,温度
,温度 下反应达到平衡时
下反应达到平衡时 。由此推知,
。由此推知,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③下列说法不正确的是___________ (填标号)。
A.四个反应均为放热反应
B.反应体系中1-MD最稳定
C.压强越大,温度越低越有利于生成四氢萘类物质
D.由上述信息可知,400K时反应 速率最快
速率最快
(4)1-MN在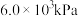 的高压
的高压 氛围下反应(
氛围下反应( 压强近似等于总压)。不同温度下达平衡时各产物的选择性
压强近似等于总压)。不同温度下达平衡时各产物的选择性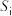 (某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数
(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数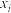 (
(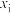 表示物种i与除
表示物种i与除 外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应
外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应 的平衡常数
的平衡常数
___________  (列出计算式)。
(列出计算式)。

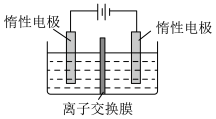
(5)利用膜电解技术(装置如图所示),以 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: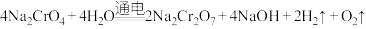 。则
。则 在
在___________ (填“阴”或“阳”)极室制得,电解时通过膜的离子主要为___________ 。

回答下列问题:
(1)1-甲基萘(1-MN)的组成元素电负性由小到大的顺序为
(2)已知一定条件下反应
 、
、 、
、 的焓变分别为
的焓变分别为 、
、 、
、 ,则反应
,则反应 的焓变为
的焓变为 、
、 、
、 的代数式表示)。
的代数式表示)。(3)四个平衡体系的平衡常数与温度的关系如图甲所示。

①c、d分别为反应
 和
和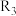 的平衡常数随温度变化的曲线,则表示反应
的平衡常数随温度变化的曲线,则表示反应 的平衡常数随温度变化曲线为
的平衡常数随温度变化曲线为②已知反应
 的速率方程
的速率方程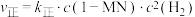 ,
,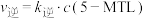 (
( 、
、 分别为正、逆反应速率常数,只与温度、催化剂有关)。温度
分别为正、逆反应速率常数,只与温度、催化剂有关)。温度 下反应达到平衡时
下反应达到平衡时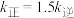 ,温度
,温度 下反应达到平衡时
下反应达到平衡时 。由此推知,
。由此推知,
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③下列说法不正确的是
A.四个反应均为放热反应
B.反应体系中1-MD最稳定
C.压强越大,温度越低越有利于生成四氢萘类物质
D.由上述信息可知,400K时反应
 速率最快
速率最快(4)1-MN在
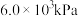 的高压
的高压 氛围下反应(
氛围下反应( 压强近似等于总压)。不同温度下达平衡时各产物的选择性
压强近似等于总压)。不同温度下达平衡时各产物的选择性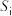 (某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数
(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数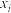 (
(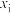 表示物种i与除
表示物种i与除 外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应
外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应 的平衡常数
的平衡常数
 (列出计算式)。
(列出计算式)。
(5)利用膜电解技术(装置如图所示),以
 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: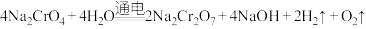 。则
。则 在
在
您最近半年使用:0次
4 . 已知: 与不足量的
与不足量的 反应时,生成S和
反应时,生成S和 。根据以下三个热化学方程式:
。根据以下三个热化学方程式:
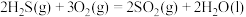
 ①
①

 ②
②

 ③
③
 、
、 、
、 三者大小关系正确的是
三者大小关系正确的是
 与不足量的
与不足量的 反应时,生成S和
反应时,生成S和 。根据以下三个热化学方程式:
。根据以下三个热化学方程式: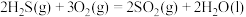
 ①
①
 ②
②
 ③
③ 、
、 、
、 三者大小关系正确的是
三者大小关系正确的是A.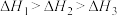 | B.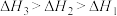 |
C.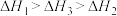 | D.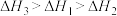 |
您最近半年使用:0次
2023-12-03更新
|
451次组卷
|
24卷引用:甘肃省古浪县第二中学2019-2020学年高二上学期基础知识竞赛化学试题
甘肃省古浪县第二中学2019-2020学年高二上学期基础知识竞赛化学试题江西省上饶县中学2017-2018学年高二上学期补考化学试题重庆市第三十中学2018-2019学年高二上学期第三次月考化学试题江苏省淮安市涟水县第一中学2020届高三上学期第二次月考化学试题福建省福州格致中学2021-2022学年高二上学期第一阶段测试化学试题(10月)山西省怀仁市2021-2022学年高二上学期期中化学试题广西钦州市2021-2022学年高二上学期期末考试化学试题第二节 反应热的计算 第2课时 反应热的计算甘肃省甘南藏族自治州合作第一中学2021-2022学年高二上学期期中考试化学试题(理)河南省濮阳市元龙高级中学2021-2022学年高二上学期期中考试化学试题贵州省部分学校2022-2023学年高二上学期10月联考化学试题贵州省“三新”改革联盟校联考2022-2023学年高二上学期期中考试化学试题陕西省咸阳市实验中学2021-2022学年高二上学期第三次月考化学试题湖南省怀化市雅礼实验学校2022-2023学年高二上学期第一次月考化学试题河南省洛阳市第一中学2022-2023学年高二上学期期末检测化学试题章末检测卷(一) 化学反应的热效应广东省广州市执信中学2023-2024学年高二上学期10月选考化学试题安徽省无为襄安中学2022-2023学年高二下学期开学考试化学试题山东省聊城市2023-2024学年高二上学期11月期中考试化学试题天津市南开区2023-2024学年高二上学期11月期中考试化学试题陕西省咸阳市兴平市西郊高级中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业01 化学反应的热效应-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)江西省抚州市资溪县第一中学2023-2024学年高二上学期11月期中化学试题安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题
5 . 已知下列反应的热化学方程式如下,则反应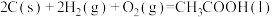 的
的 为
为
(1)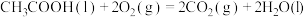
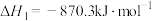
(2)
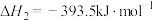
(3)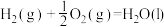
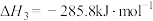
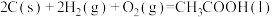 的
的 为
为(1)
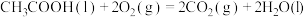
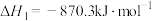
(2)

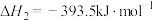
(3)
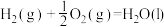
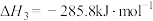
A.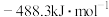 | B.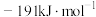 |
C. | D.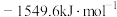 |
您最近半年使用:0次
2023-11-13更新
|
165次组卷
|
3卷引用:山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期元旦竞赛考试化学试题
解题方法
6 . 深入研究碳、氮元素的物质转化有着重要的实际意义。N2O、CO在Pt2O+的表面进行两步反应转化为无毒的气体,其相对能量、反应历程和熵值(298.15K,100Kpa时)如图甲、乙所示。
I: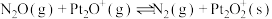
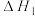
II:
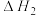
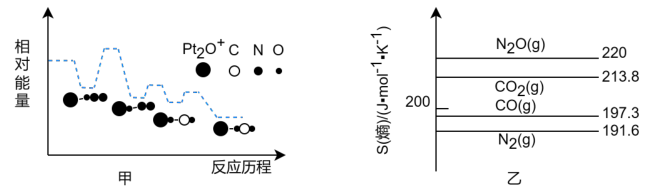
将等物质的量的N2O和CO充入一密闭容器中进行反应,请回答:
(1)总反应的热化学方程式为_______ ( 用含
用含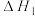 、
、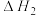 的式子表示)。
的式子表示)。
(2)下列说法正确的是_______。
(3)在T1℃,平衡时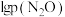 与
与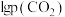 的关系如图丙所示,p为物质的分压强(单位为kPa)。若
的关系如图丙所示,p为物质的分压强(单位为kPa)。若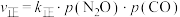 、
、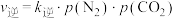 ,则
,则
_______ 。(分压=总压×物质的量分数)。

(4)若在相同时间内测得N2O的转化率随温度的变化曲线如图丁所示,N2O的转化率在400℃~900℃之间下降由缓到急的原因是_______ 。
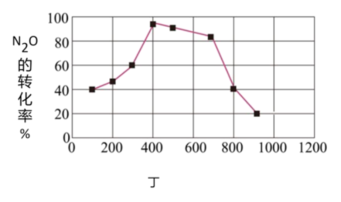
(5)在图丁中画出900℃以后,相同时间内N2O的转化率随温度的变化曲线_______ 。
I:
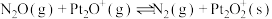
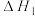
II:

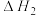

将等物质的量的N2O和CO充入一密闭容器中进行反应,请回答:
(1)总反应的热化学方程式为
 用含
用含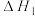 、
、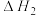 的式子表示)。
的式子表示)。(2)下列说法正确的是_______。
| A.在恒温,恒容时,混合气体的密度不再变化说明体系达到平衡状态 |
| B.该总反应高温下可能不自发 |
| C.反应过程中先是N2O中的O原子去进攻Pt2O+中的Pt原子 |
| D.研究表明,Pt2O+一步催化相对于上述反应历程具有更少的反应步骤和更低的活化能,所以平衡转化率更大 |
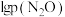 与
与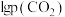 的关系如图丙所示,p为物质的分压强(单位为kPa)。若
的关系如图丙所示,p为物质的分压强(单位为kPa)。若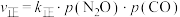 、
、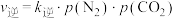 ,则
,则

(4)若在相同时间内测得N2O的转化率随温度的变化曲线如图丁所示,N2O的转化率在400℃~900℃之间下降由缓到急的原因是

(5)在图丁中画出900℃以后,相同时间内N2O的转化率随温度的变化曲线
您最近半年使用:0次
名校
7 . 丙烯是重要的化工原料,可以用于生产丙醇、卤代烃和塑料。回答下列问题:
(1)工业上用丙烯加成法制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:
①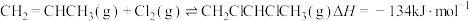
②
已知: 的活化能
的活化能 (逆)为
(逆)为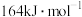 ,则该反应的活化能
,则该反应的活化能 (正)为
(正)为___________  。
。
(2)一定温度下,向恒容密闭容器中充入等物质的量的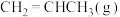 和
和 ,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
用单位时间内气体分压的变化来表示反应速率,即 ,则反应①前
,则反应①前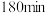 内平均反应速率
内平均反应速率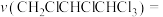
___________ kPa/min(保留小数点后2位)。
(3) 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图1所示。图中a、b、c、d代表丙烷或丙烯,则a、d代表
时,测得丙烷及丙烯的物质的量分数如图1所示。图中a、b、c、d代表丙烷或丙烯,则a、d代表___________ ,
___________  (填“大于”“小于”或“等于”);若
(填“大于”“小于”或“等于”);若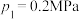 ,起始时充入一定量的丙烷在恒压条件下发生反应,计算
,起始时充入一定量的丙烷在恒压条件下发生反应,计算 点对应温度下丙烷的转化率为
点对应温度下丙烷的转化率为___________ (保留一位小数),该反应的平衡常数
___________  (用平衡分压代替平衡浓度计算,分压=总压
(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。

(4)丙烷氧化脱氢法制备丙烯还生成 等副产物,制备丙烯的反应:
等副产物,制备丙烯的反应: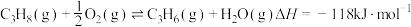 ,在催化剂的作用下
,在催化剂的作用下 的转化率和
的转化率和 的产率随温度变化关系如图2所示。图中
的产率随温度变化关系如图2所示。图中 的转化率随温度升高而上升的原因是
的转化率随温度升高而上升的原因是___________ ;观察图2,写出能提高 选择性的措施是
选择性的措施是___________ ( 的选择性
的选择性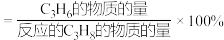 )。
)。

(1)工业上用丙烯加成法制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:
①
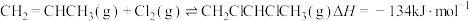
②

已知:
 的活化能
的活化能 (逆)为
(逆)为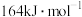 ,则该反应的活化能
,则该反应的活化能 (正)为
(正)为 。
。(2)一定温度下,向恒容密闭容器中充入等物质的量的
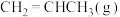 和
和 ,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。时间 | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强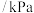 | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
 ,则反应①前
,则反应①前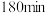 内平均反应速率
内平均反应速率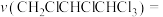
(3)
 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图1所示。图中a、b、c、d代表丙烷或丙烯,则a、d代表
时,测得丙烷及丙烯的物质的量分数如图1所示。图中a、b、c、d代表丙烷或丙烯,则a、d代表
 (填“大于”“小于”或“等于”);若
(填“大于”“小于”或“等于”);若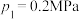 ,起始时充入一定量的丙烷在恒压条件下发生反应,计算
,起始时充入一定量的丙烷在恒压条件下发生反应,计算 点对应温度下丙烷的转化率为
点对应温度下丙烷的转化率为
 (用平衡分压代替平衡浓度计算,分压=总压
(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。
(4)丙烷氧化脱氢法制备丙烯还生成
 等副产物,制备丙烯的反应:
等副产物,制备丙烯的反应: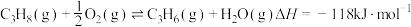 ,在催化剂的作用下
,在催化剂的作用下 的转化率和
的转化率和 的产率随温度变化关系如图2所示。图中
的产率随温度变化关系如图2所示。图中 的转化率随温度升高而上升的原因是
的转化率随温度升高而上升的原因是 选择性的措施是
选择性的措施是 的选择性
的选择性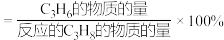 )。
)。
您最近半年使用:0次
2023-06-10更新
|
199次组卷
|
3卷引用:江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题
名校
解题方法
8 . 含氮化合物在生产生活中有重要的应用。请回答:
(1) 与含硫化合物的热化学方程式如下:
与含硫化合物的热化学方程式如下:
反应I: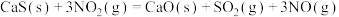
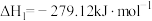

反应II:
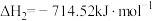

反应III:



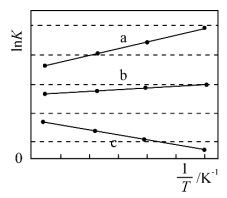
_______  ,三个反应的平衡常数的
,三个反应的平衡常数的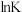 随温度变化关系如图所示,则表示
随温度变化关系如图所示,则表示 的曲线是
的曲线是_______ 。
(2)合成氨工厂以“水煤气”和 为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、
为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、 、
、 、
、 的混合气体,在反应器A进行合成氨,其催化剂III铁触媒,在500℃活性最大,反应器B中主要发生的反应为:
的混合气体,在反应器A进行合成氨,其催化剂III铁触媒,在500℃活性最大,反应器B中主要发生的反应为:
 ,装置如图。
,装置如图。
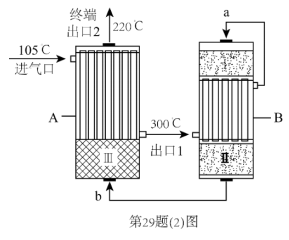
①温度比较:气流a_______ 气流b(填“>”“<”或“=”)。
②气体流速一定,经由催化剂I到催化剂II,原料转化率有提升,其可能原因是:_______ 。
③下列说法正确的是_______ 。
A.焦炭与水蒸气制水煤气时,适当加快通入水蒸气的流速,有利于水煤气的生成
B.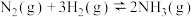
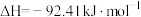 反应器温度越低,终端出口2收率越高
反应器温度越低,终端出口2收率越高
C.终端出口2得到的气体,通过水吸收,再加热水溶液,可分离出
D.反应原料气从进气口105℃到300℃出口1,已完成氨的合成
(3)已知水中存在电离平衡 ,称为自偶电离。-33℃液氨中也存在自偶电离,请写出液氨中的自偶电离方程式:
,称为自偶电离。-33℃液氨中也存在自偶电离,请写出液氨中的自偶电离方程式:_______ ,液氨自偶电离平衡常数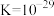 ,在100mL液氨中加入0.0001 mol
,在100mL液氨中加入0.0001 mol  固体,溶解,并完全电离(忽略体积变化),则
固体,溶解,并完全电离(忽略体积变化),则
_______  。金属钾能溶解于液氨中形成蓝色的液氨溶液,反应的化学方程式为
。金属钾能溶解于液氨中形成蓝色的液氨溶液,反应的化学方程式为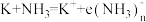 (电子的氨合物,显蓝色),加入
(电子的氨合物,显蓝色),加入 固体后生成氢气,请写出离子方程式
固体后生成氢气,请写出离子方程式_______ 。
(1)
 与含硫化合物的热化学方程式如下:
与含硫化合物的热化学方程式如下:反应I:
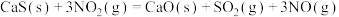
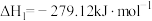

反应II:

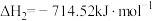

反应III:




 ,三个反应的平衡常数的
,三个反应的平衡常数的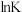 随温度变化关系如图所示,则表示
随温度变化关系如图所示,则表示 的曲线是
的曲线是
(2)合成氨工厂以“水煤气”和
 为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、
为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、 、
、 、
、 的混合气体,在反应器A进行合成氨,其催化剂III铁触媒,在500℃活性最大,反应器B中主要发生的反应为:
的混合气体,在反应器A进行合成氨,其催化剂III铁触媒,在500℃活性最大,反应器B中主要发生的反应为:
 ,装置如图。
,装置如图。
①温度比较:气流a
②气体流速一定,经由催化剂I到催化剂II,原料转化率有提升,其可能原因是:
③下列说法正确的是
A.焦炭与水蒸气制水煤气时,适当加快通入水蒸气的流速,有利于水煤气的生成
B.
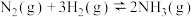
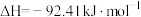 反应器温度越低,终端出口2收率越高
反应器温度越低,终端出口2收率越高C.终端出口2得到的气体,通过水吸收,再加热水溶液,可分离出

D.反应原料气从进气口105℃到300℃出口1,已完成氨的合成
(3)已知水中存在电离平衡
 ,称为自偶电离。-33℃液氨中也存在自偶电离,请写出液氨中的自偶电离方程式:
,称为自偶电离。-33℃液氨中也存在自偶电离,请写出液氨中的自偶电离方程式: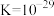 ,在100mL液氨中加入0.0001 mol
,在100mL液氨中加入0.0001 mol  固体,溶解,并完全电离(忽略体积变化),则
固体,溶解,并完全电离(忽略体积变化),则
 。金属钾能溶解于液氨中形成蓝色的液氨溶液,反应的化学方程式为
。金属钾能溶解于液氨中形成蓝色的液氨溶液,反应的化学方程式为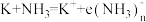 (电子的氨合物,显蓝色),加入
(电子的氨合物,显蓝色),加入 固体后生成氢气,请写出离子方程式
固体后生成氢气,请写出离子方程式
您最近半年使用:0次
9 . 金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石( )转化为
)转化为 ,再进一步还原得到钛。
,再进一步还原得到钛。
直接氯化:
反应Ⅰ:
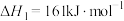
碳氯化:
反应Ⅱ: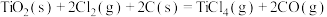
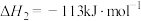
反应Ⅲ:

(1)直接氯化可以在___________ 下自发进行。
(2)反应Ⅳ 的
的 为
为___________ 
(3)科学家对以上反应做过热重分析,温度为1223K、氯气分压 的条件下,得到固体相对质量变化与时间的关系如下图所示:
的条件下,得到固体相对质量变化与时间的关系如下图所示:
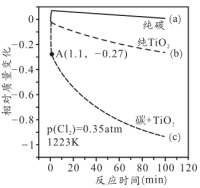
①用纯碳实验时,质量稍微有所增长,生成了含___________ 键的物质。
②用纯 实验时,所发生的化学方程式为
实验时,所发生的化学方程式为___________ ;该反应的活化能___________ (填“高”或“低”)。
③按照 混合,实验发现1.1min内质量迅速减少,经光谱分析证明有光气(
混合,实验发现1.1min内质量迅速减少,经光谱分析证明有光气( )生成,固体中含有C和
)生成,固体中含有C和 ,则x=
,则x=___________ 。
④1.1min之后,光气( )继续反应,有理论认为机理如下:
)继续反应,有理论认为机理如下:

决速步骤的反应方程式为___________ ,1.1min之后发生的总反应方程式为___________ 。
(4)按照 混合,平衡状态下不同物质的组成比与温度的关系如下图所示:
混合,平衡状态下不同物质的组成比与温度的关系如下图所示:
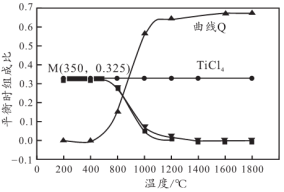
①曲线Q是___________ (填化学式)的变化图像。
②M点所发生的化学方程式是___________ 。
 )转化为
)转化为 ,再进一步还原得到钛。
,再进一步还原得到钛。直接氯化:
反应Ⅰ:

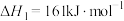
碳氯化:
反应Ⅱ:
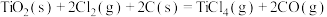
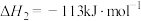
反应Ⅲ:


(1)直接氯化可以在
(2)反应Ⅳ
 的
的 为
为
(3)科学家对以上反应做过热重分析,温度为1223K、氯气分压
 的条件下,得到固体相对质量变化与时间的关系如下图所示:
的条件下,得到固体相对质量变化与时间的关系如下图所示:
①用纯碳实验时,质量稍微有所增长,生成了含
②用纯
 实验时,所发生的化学方程式为
实验时,所发生的化学方程式为③按照
 混合,实验发现1.1min内质量迅速减少,经光谱分析证明有光气(
混合,实验发现1.1min内质量迅速减少,经光谱分析证明有光气( )生成,固体中含有C和
)生成,固体中含有C和 ,则x=
,则x=④1.1min之后,光气(
 )继续反应,有理论认为机理如下:
)继续反应,有理论认为机理如下:
决速步骤的反应方程式为
(4)按照
 混合,平衡状态下不同物质的组成比与温度的关系如下图所示:
混合,平衡状态下不同物质的组成比与温度的关系如下图所示:
①曲线Q是
②M点所发生的化学方程式是
您最近半年使用:0次
10 . 甲醇制备原理如下:
反应Ⅰ

反应Ⅱ

某温度下,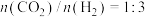 加入一恒压密闭容器中反应,达到平衡时,氢气、甲醇和一氧化碳的分压有如下关系:
加入一恒压密闭容器中反应,达到平衡时,氢气、甲醇和一氧化碳的分压有如下关系: ,下列说法正确的是
,下列说法正确的是
反应Ⅰ


反应Ⅱ


某温度下,
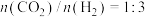 加入一恒压密闭容器中反应,达到平衡时,氢气、甲醇和一氧化碳的分压有如下关系:
加入一恒压密闭容器中反应,达到平衡时,氢气、甲醇和一氧化碳的分压有如下关系: ,下列说法正确的是
,下列说法正确的是A. 的平衡转化率为 的平衡转化率为 |
B.该温度下反应Ⅰ的平衡常数 之值为 之值为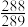 |
C.该温度下反应Ⅱ的平衡常数 为 为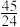 |
| D.平衡时,甲醇含量最高 |
您最近半年使用:0次



