1 . Ti、Na、Mg、C、N、O、Fe等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)已知C、CO的燃烧热分别为393.5kJ/mol和283.0kJ/mol,写出碳不完全燃烧生成CO的热化学方程式___________ 。
(2)Na、Mg、C、N、O的第一电离能由大到小的顺序为___________ 。
(3)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.原子吸收光谱 B.原子发射光谱
(4)钢铁发生吸氧腐蚀时正极的电极反应式为:___________ 。为防止钢铁输水管的腐蚀,可用导线将其与镁块连接,这种防护方法为___________ 。(电化学保护法中的一种)
(5)基态 原子最高能层的原子轨道形状为
原子最高能层的原子轨道形状为___________ ,其价电子轨道表示式为___________ 。
(6)用琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是___________ 。
(1)已知C、CO的燃烧热分别为393.5kJ/mol和283.0kJ/mol,写出碳不完全燃烧生成CO的热化学方程式
(2)Na、Mg、C、N、O的第一电离能由大到小的顺序为
(3)钠在火焰上灼烧产生的黄光是一种
A.原子吸收光谱 B.原子发射光谱
(4)钢铁发生吸氧腐蚀时正极的电极反应式为:
(5)基态
 原子最高能层的原子轨道形状为
原子最高能层的原子轨道形状为(6)用琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是
您最近一年使用:0次
名校
解题方法
2 . 完成下列问题
Ⅰ.氨是重要的化工原料,已知NH3(g)在纯氧中燃烧的能量变化如图。

(1)已知: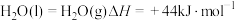 ,则NH3(g)的燃烧热的热化学方程式为
,则NH3(g)的燃烧热的热化学方程式为_______ 。
Ⅱ.火箭推进器中装有肼(N2H4)和过氧化氢。已知下列各物质反应的热化学方程式:
①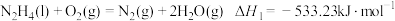
②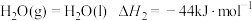
③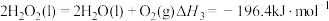
(2)以下选项中,是氮原子激发态的电子排布式,且其中能量较高的是_______ 。(填标号)
a.1s22s22p23s1 b.ls22s22p43d2 c.1s22s12p5 d.1s22s22p13p2
(3)N2H4晶体的晶胞结构_______ (填“是”或者“不”)符合分子密堆积,原因是_______ 。
(4)16g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出热量为:_______ (保留小数点后一位有效数字)。
(5)在高温下,N2H4可完全分解为NH3、N2及H2,实验测得分解产物中N2与H2的物质的量之比为3∶2,则该分解反应的化学方程式为_______ 。
(6)有以下物质:①碘、②金刚砂、③氨气、④氯化钠、⑤水晶、⑥肼,它们的熔点由高到低的顺序为_______ (用序号表示)。
Ⅰ.氨是重要的化工原料,已知NH3(g)在纯氧中燃烧的能量变化如图。

(1)已知:
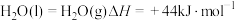 ,则NH3(g)的燃烧热的热化学方程式为
,则NH3(g)的燃烧热的热化学方程式为Ⅱ.火箭推进器中装有肼(N2H4)和过氧化氢。已知下列各物质反应的热化学方程式:
①
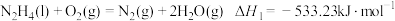
②
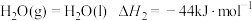
③
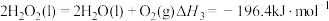
(2)以下选项中,是氮原子激发态的电子排布式,且其中能量较高的是
a.1s22s22p23s1 b.ls22s22p43d2 c.1s22s12p5 d.1s22s22p13p2
(3)N2H4晶体的晶胞结构
(4)16g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出热量为:
(5)在高温下,N2H4可完全分解为NH3、N2及H2,实验测得分解产物中N2与H2的物质的量之比为3∶2,则该分解反应的化学方程式为
(6)有以下物质:①碘、②金刚砂、③氨气、④氯化钠、⑤水晶、⑥肼,它们的熔点由高到低的顺序为
您最近一年使用:0次
名校
3 . I.回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态钴原子的价层电子排布式为_______ ;基态磷原子中,电子占据的最高能层符号为_______ 。
(2)基态Mn2+的价层电子轨道表示式为_______ ;银与铜位于同一族,银元素位于元素周期表的_______ 区。
(3)基态Ge原子核外简化电子排布式为_______ ,Ge原子的电子发生跃迁时会吸收或发出不同的光;可用光谱分析仪获得_______ 光谱(填“连续”或“线状”),鉴定Ge元素的存在。
(4)N、O、Mg元素的前3级电离能如表所示:
X、Y、Z中为N元素的是_______ 。
(5)根据对角线规则,元素周期表中Al元素左上方元素的最高价氧化物对应的水化物与NaOH反应的化学方程式为_______ 。
II.25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(6)下列反应不能发生的是_______ (填序号)。
a.CO +2CH3COOH=2CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
+2CH3COOH=2CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
c.CO +2HClO=2ClO-+CO2↑+ H2O d.2ClO-+CO2+H2O=CO
+2HClO=2ClO-+CO2↑+ H2O d.2ClO-+CO2+H2O=CO +2HClO
+2HClO
(7)用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是_______ (填序号)。
a.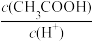 b.
b.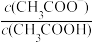 c.
c.
III.空气中的污染物主要来源为燃煤、机动车尾气等。因此,对CO、SO2、NOx等进行研究具有重要意义,请回答下列问题:
(8)为减少CO2、SO2污染的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
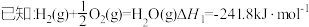
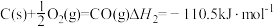
写出焦炭与水蒸气反应的热化学方程式:_______ 。
②在含硫燃料中加入石灰石,燃煤生成的SO2即可转化为CaSO4总反应化学方程式为_______ 。
(9)汽车尾气中NOx和CO的生成及转化,燃油不完全燃烧时产生CO,有人设想按下列反应除去:2CO(g)=2C(s)+O2(g)已知该反应的△H>0,简述该设想不能实现的理论依据:_______ 。
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态钴原子的价层电子排布式为
(2)基态Mn2+的价层电子轨道表示式为
(3)基态Ge原子核外简化电子排布式为
(4)N、O、Mg元素的前3级电离能如表所示:
| 元素 | I1/(kJ·mol-1) | I2/(kJ·mol-1) | I3/(kJ·mol-1) |
| X | 737.7 | 1450.7 | 7732.7 |
| Y | 1313.9 | 3388.3 | 5300.5 |
| Z | 1402.3 | 2856.0 | 4578.1 |
(5)根据对角线规则,元素周期表中Al元素左上方元素的最高价氧化物对应的水化物与NaOH反应的化学方程式为
II.25℃时,三种酸的电离平衡常数如下:
| 化学式 |  |  | HClO |
| 电离平衡常数 |  | 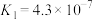 , ,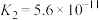 |  |
(6)下列反应不能发生的是
a.CO
 +2CH3COOH=2CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
+2CH3COOH=2CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClOc.CO
 +2HClO=2ClO-+CO2↑+ H2O d.2ClO-+CO2+H2O=CO
+2HClO=2ClO-+CO2↑+ H2O d.2ClO-+CO2+H2O=CO +2HClO
+2HClO(7)用蒸馏水稀释
 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是a.
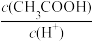 b.
b.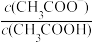 c.
c.
III.空气中的污染物主要来源为燃煤、机动车尾气等。因此,对CO、SO2、NOx等进行研究具有重要意义,请回答下列问题:
(8)为减少CO2、SO2污染的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
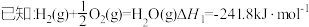
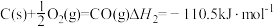
写出焦炭与水蒸气反应的热化学方程式:
②在含硫燃料中加入石灰石,燃煤生成的SO2即可转化为CaSO4总反应化学方程式为
(9)汽车尾气中NOx和CO的生成及转化,燃油不完全燃烧时产生CO,有人设想按下列反应除去:2CO(g)=2C(s)+O2(g)已知该反应的△H>0,简述该设想不能实现的理论依据:
您最近一年使用:0次



