解题方法
1 . 以钛铁矿(主要成分 ,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为:
,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为: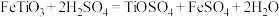 。
。
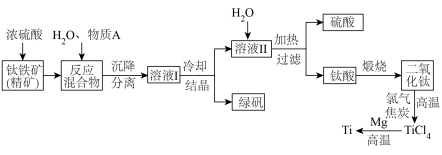
回答下列问题:
(1)钛铁矿和浓硫酸反应属于___________ (选填“氧化还原反应”或“非氧化还原反应”)。
(2)上述生产流程中加入物质A的目的是防止 被氧化,物质A是
被氧化,物质A是___________ ,上述制备 的过程中,所得到的副产物和可回收利用的物质分别是
的过程中,所得到的副产物和可回收利用的物质分别是___________ 、___________ 。
(3)反应 在Ar气氛中进行的理由是
在Ar气氛中进行的理由是___________ 。
(4)由二氧化钛制取四氯化钛所涉及的反应有:
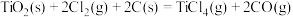
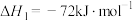

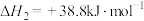

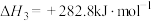
反应 的
的
___________ 。
 ,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为:
,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为: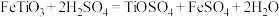 。
。
回答下列问题:
(1)钛铁矿和浓硫酸反应属于
(2)上述生产流程中加入物质A的目的是防止
 被氧化,物质A是
被氧化,物质A是 的过程中,所得到的副产物和可回收利用的物质分别是
的过程中,所得到的副产物和可回收利用的物质分别是(3)反应
 在Ar气氛中进行的理由是
在Ar气氛中进行的理由是(4)由二氧化钛制取四氯化钛所涉及的反应有:
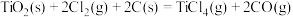
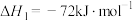

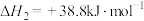

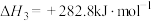
反应
 的
的
您最近一年使用:0次
2023-11-26更新
|
46次组卷
|
2卷引用:湖北省黄州中学(黄冈市外国语学校)2023-2024学年高二上学期9月月考化学试题
2 . 碳酸二甲脂( )是一种重要的化工原料,被广泛应用于制备锂离子电池和聚碳酸酯等。某科研小组以
)是一种重要的化工原料,被广泛应用于制备锂离子电池和聚碳酸酯等。某科研小组以 、
、 、
、 为原料合成碳酸二甲酯。
为原料合成碳酸二甲酯。
主反应: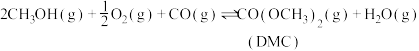

副反应: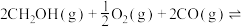
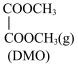

(1)在 作用下,主反应可分两步进行:
作用下,主反应可分两步进行:
ⅰ)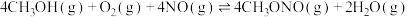
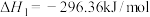
ⅱ)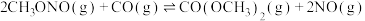
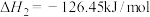
则主反应
_______ 。
(2)研究发理,合成 时易生成则产物草酸二甲脂(
时易生成则产物草酸二甲脂(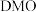 )。某温度下,在2L密闭容器中充入
)。某温度下,在2L密闭容器中充入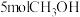 、
、 、
、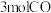 以及
以及 ,达平衡后,
,达平衡后, 和
和 的体积分数相等且为
的体积分数相等且为 体积分数的一半,则主反应的平衡常数
体积分数的一半,则主反应的平衡常数
_______ ;碳酸二甲酯( )的选择性=
)的选择性=_______ ( 的选择性
的选择性 )
)
(3)在200~300℃下,草酸二甲酯(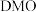 )容易被催化脱膜形成碳酸二甲酯(
)容易被催化脱膜形成碳酸二甲酯( ),某温度下,经过相同时间测得的部分数据如下表所示:
),某温度下,经过相同时间测得的部分数据如下表所示:
①由数据可知,催化效果最好的催化剂及其负载量是_______ 。
②将 、
、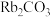 和
和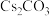 负载于活性炭上对其催化活性具有重要的促进作用,可能的原因是
负载于活性炭上对其催化活性具有重要的促进作用,可能的原因是_______ 。
(4)早在20世纪已有科学家设计通过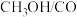 电化学氧化合成碳酸二甲酯(
电化学氧化合成碳酸二甲酯( ),阳极发生的反应分3步进行:
),阳极发生的反应分3步进行:

第一步: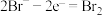
第二步: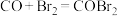
则第三步的方程式为_______ ; 在总反应中的作用是
在总反应中的作用是_______ 。
 )是一种重要的化工原料,被广泛应用于制备锂离子电池和聚碳酸酯等。某科研小组以
)是一种重要的化工原料,被广泛应用于制备锂离子电池和聚碳酸酯等。某科研小组以 、
、 、
、 为原料合成碳酸二甲酯。
为原料合成碳酸二甲酯。主反应:
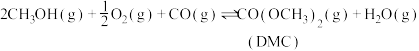

副反应:
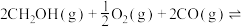
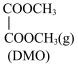

(1)在
 作用下,主反应可分两步进行:
作用下,主反应可分两步进行:ⅰ)
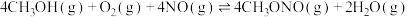
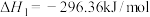
ⅱ)
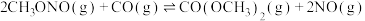
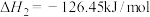
则主反应

(2)研究发理,合成
 时易生成则产物草酸二甲脂(
时易生成则产物草酸二甲脂(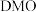 )。某温度下,在2L密闭容器中充入
)。某温度下,在2L密闭容器中充入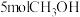 、
、 、
、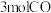 以及
以及 ,达平衡后,
,达平衡后, 和
和 的体积分数相等且为
的体积分数相等且为 体积分数的一半,则主反应的平衡常数
体积分数的一半,则主反应的平衡常数
 )的选择性=
)的选择性= 的选择性
的选择性 )
)(3)在200~300℃下,草酸二甲酯(
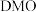 )容易被催化脱膜形成碳酸二甲酯(
)容易被催化脱膜形成碳酸二甲酯( ),某温度下,经过相同时间测得的部分数据如下表所示:
),某温度下,经过相同时间测得的部分数据如下表所示:| 催化剂 |  /活性炭 /活性炭 | 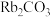 /活性炭 /活性炭 | 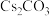 /活性炭 /活性炭 | ||||||
| 负载量 | 5% | 10% | 15% | 5% | 10% | 15% | 5% | 10% | 15% |
| 转化率% | 64 | 70 | 56 | 87 | 84 | 82 | 30 | 95 | 89 |
| 选择性% | 100 | 100 | 100 | 100 | 100 | 100 | 100 | 90 | 85 |
②将
 、
、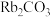 和
和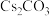 负载于活性炭上对其催化活性具有重要的促进作用,可能的原因是
负载于活性炭上对其催化活性具有重要的促进作用,可能的原因是(4)早在20世纪已有科学家设计通过
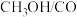 电化学氧化合成碳酸二甲酯(
电化学氧化合成碳酸二甲酯( ),阳极发生的反应分3步进行:
),阳极发生的反应分3步进行:
第一步:
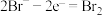
第二步:
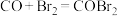
则第三步的方程式为
 在总反应中的作用是
在总反应中的作用是
您最近一年使用:0次
名校
解题方法
3 . 甲烷在工业上有很多用途。回答下列问题:
Ⅰ.利用甲烷催化还原 消除氮氧化物的污染:
消除氮氧化物的污染:
ⅰ.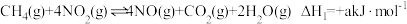 ;
;
ⅱ.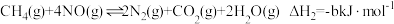 ;
;
ⅲ.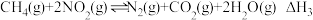 。
。
其中: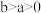 。
。
(1)
_______ (用含a、b的代数式表示)。
(2)在4L某恒容密闭容器中充入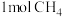 和
和 ,只发生反应ⅲ,
,只发生反应ⅲ, 的平衡转化率
的平衡转化率 随温度的变化关系如图所示。
随温度的变化关系如图所示。
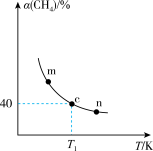
①曲线上m、n两点的正反应速率:
_______ (填“>”、“<”或“=”)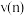 。
。
②T1时,若反应进行到 时达到平衡,此时测得混合气体的总压强为
时达到平衡,此时测得混合气体的总压强为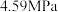 ,则
,则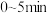 内,
内,
_______  ,反应平衡常数
,反应平衡常数
_______  (用分压表示,分压=物质的量分数×总压)。
(用分压表示,分压=物质的量分数×总压)。
③下列说法正确的是_______ (填标号)。
A.当混合气体的密度不再随时间改变时,该反应达到平衡
B.该反应的反应物的键能总和小于生成物的键能总和
C.降低温度,有利于提高 的转化率,反应平衡常数也增大
的转化率,反应平衡常数也增大
D.加入合适的催化剂, 的值增大
的值增大
(3)甲烷-氧气燃料电池的工作原理如图所示(L、K均为惰性电极,气体已换算成标准状况)。
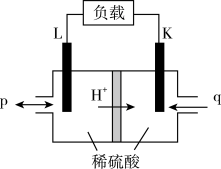
①电池工作时,K电极上发生_______ (填“还原反应”或“氧化反应”)。
②L电极上的电极反应式为_______ 。
③每消耗 ,电路中转移电子的物质的量为
,电路中转移电子的物质的量为_______ mol。
Ⅰ.利用甲烷催化还原
 消除氮氧化物的污染:
消除氮氧化物的污染:ⅰ.
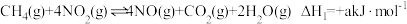 ;
;ⅱ.
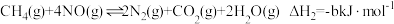 ;
;ⅲ.
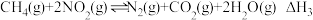 。
。其中:
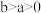 。
。(1)

(2)在4L某恒容密闭容器中充入
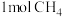 和
和 ,只发生反应ⅲ,
,只发生反应ⅲ, 的平衡转化率
的平衡转化率 随温度的变化关系如图所示。
随温度的变化关系如图所示。
①曲线上m、n两点的正反应速率:

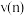 。
。②T1时,若反应进行到
 时达到平衡,此时测得混合气体的总压强为
时达到平衡,此时测得混合气体的总压强为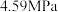 ,则
,则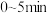 内,
内,
 ,反应平衡常数
,反应平衡常数
 (用分压表示,分压=物质的量分数×总压)。
(用分压表示,分压=物质的量分数×总压)。③下列说法正确的是
A.当混合气体的密度不再随时间改变时,该反应达到平衡
B.该反应的反应物的键能总和小于生成物的键能总和
C.降低温度,有利于提高
 的转化率,反应平衡常数也增大
的转化率,反应平衡常数也增大D.加入合适的催化剂,
 的值增大
的值增大(3)甲烷-氧气燃料电池的工作原理如图所示(L、K均为惰性电极,气体已换算成标准状况)。

①电池工作时,K电极上发生
②L电极上的电极反应式为
③每消耗
 ,电路中转移电子的物质的量为
,电路中转移电子的物质的量为
您最近一年使用:0次
2022-05-29更新
|
137次组卷
|
4卷引用:湖北省十堰市2021-2022学年高二下学期期末调研考试化学试题
名校
解题方法
4 . 习近平总书记在世界领导人气候峰会上指出,中国将在2030年前实现“碳达峰”、2060年前实现“碳中和”。这是中国基于推动构建人类命运共同体的责任担当和实现可持续发展的内在要求作出的重大战略决策。因此CO2的捕集、创新利用与封存成为科学家研究的重要课题。
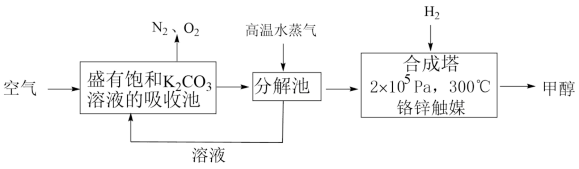
Ⅰ.最近有科学家提出“绿色自由”构想:先把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如图:
已知:
(1)上述工艺中采用气液逆流接触吸收(空气从吸收池底部进入,溶液从顶部喷淋),其目的是___ 。写出吸收池中反应的化学方程式___ 。
(2)根据表中键能写出合成塔中反应的热化学方程式 ___ 。
(3)合成塔中制备甲醇的反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ·mol-1
若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___ 。
(4)下列物质能作为CO2捕获剂的是___ (填标号)。
Ⅱ.CO2和H2合成甲烷也是CO2资源化利用的重要方法。
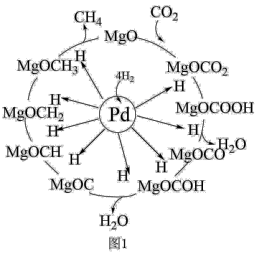
(5)一定条件下Pd—Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图1所示,该反应的化学方程式为___ ,反应过程中碳元素的化合价为-2价的中间体是___ 。
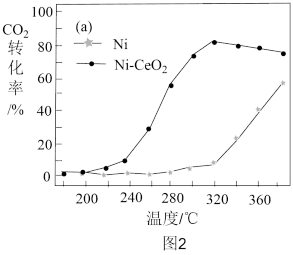
(6)催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率随温度变化的影响如图2所示。对比两种催化剂的催化性能,工业上应选择的催化剂是___ ,使用的合适温度为___ 。
Ⅰ.最近有科学家提出“绿色自由”构想:先把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如图:

已知:
| 化学键 | H—H | C—O | C=O | H—O | C—H |
| 键能/(kJ•mol-1) | 436 | 326 | 803 | 464 | 414 |
(2)根据表中键能写出合成塔中反应的
(3)合成塔中制备甲醇的反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ·mol-1
若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
A.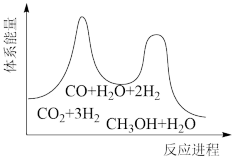 | B.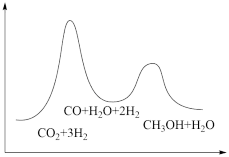 |
C.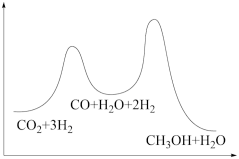 | D.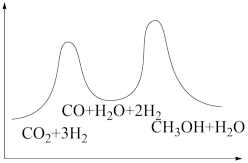 |
| A.NaOH溶液 | B.NH4Cl溶液 | C.CH3CH2OH | D.浓氨水 |
Ⅱ.CO2和H2合成甲烷也是CO2资源化利用的重要方法。
(5)一定条件下Pd—Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图1所示,该反应的化学方程式为

(6)催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率随温度变化的影响如图2所示。对比两种催化剂的催化性能,工业上应选择的催化剂是

您最近一年使用:0次
2021-12-02更新
|
445次组卷
|
6卷引用:湖北省沙市中学2022-2023学年高二上学期第一次月考化学试题
5 . I.以铝土矿的烧渣(主要成分为Al2O3、Fe2O3、SiO2)为原料,生产Fe3O4的工艺流程如下:
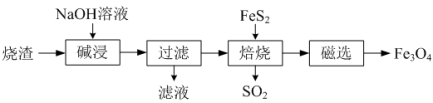
(1)“碱浸”时将烧渣粉碎的目的是_______
(2)“过滤”时用到的玻璃仪器除烧杯外,还有_______
(3)“滤液”中含有的溶质为_______ (填化学式),可以往滤液中通入过量二氧化碳,经过滤、灼烧生产氧化铝。
(4)“过滤”得到的滤渣中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,写出焙烧时发生反应的化学方程式_______
II.热化学铁氧化合物循环制H2具有成本低、产物易分离等优点。以太阳能为热源,经由铁氧化合物循环分解液态水的过程如下图所示:
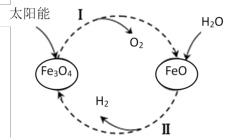
已知:①过程I:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
②2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
③H2O(g)=H2O(l) ΔH=-44kJ/mol
请回答下列问题3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ/mol
(5)氢气的燃烧热ΔH=_______
(6)过程II的热化学方程式_______ 。

(1)“碱浸”时将烧渣粉碎的目的是
(2)“过滤”时用到的玻璃仪器除烧杯外,还有
(3)“滤液”中含有的溶质为
(4)“过滤”得到的滤渣中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,写出焙烧时发生反应的化学方程式
II.热化学铁氧化合物循环制H2具有成本低、产物易分离等优点。以太阳能为热源,经由铁氧化合物循环分解液态水的过程如下图所示:

已知:①过程I:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
②2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
③H2O(g)=H2O(l) ΔH=-44kJ/mol
请回答下列问题3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ/mol
(5)氢气的燃烧热ΔH=
(6)过程II的热化学方程式
您最近一年使用:0次
解题方法
6 . 自热化学链重整制氢 工艺的原理如图所示:
工艺的原理如图所示:
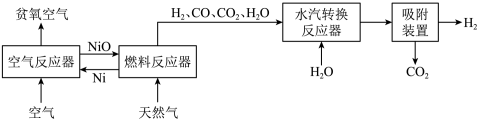
回答下列问题:
(1)25℃、101 时,5.9g
时,5.9g 与足量
与足量 反应生成
反应生成 放出47.2
放出47.2 的热量,则在“空气反应器”中发生反应的热化学方程式为
的热量,则在“空气反应器”中发生反应的热化学方程式为_______ 。
(2)“燃料反应器”中发生的部分反应有:
(Ⅰ)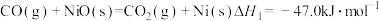
(Ⅱ)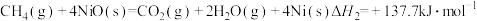
(Ⅲ)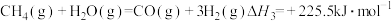
则反应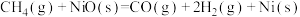 的
的
_______  。
。
(3)“水汽转换反应器”中发生的反应为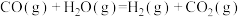 (平衡常数
(平衡常数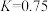 ),将天然气看作是纯净的
),将天然气看作是纯净的 (假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻
(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻 、
、 、
、 、
、 浓度之比为
浓度之比为 此时
此时
_______ 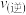 (填“>”、“=”或“<”),理由是
(填“>”、“=”或“<”),理由是_______ 。
(4)甲烷制氢传统工艺有水蒸气重整部分氧化重整以及联合重整等, 工艺重整是一种联合重整,涉及反应的热化学方程式如下:
工艺重整是一种联合重整,涉及反应的热化学方程式如下:
水蒸气重整反应: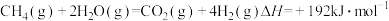
部分氧化重整反应: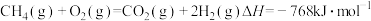
采用水蒸气重整的优点是_______ ;若上述两个反应在保持自热条件下(假设无热量损失),理论上1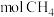 至多可获得
至多可获得 的物质的量为
的物质的量为_______ (结果保留1位小数)。
 工艺的原理如图所示:
工艺的原理如图所示:
回答下列问题:
(1)25℃、101
 时,5.9g
时,5.9g 与足量
与足量 反应生成
反应生成 放出47.2
放出47.2 的热量,则在“空气反应器”中发生反应的热化学方程式为
的热量,则在“空气反应器”中发生反应的热化学方程式为(2)“燃料反应器”中发生的部分反应有:
(Ⅰ)
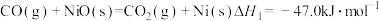
(Ⅱ)
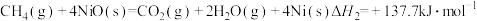
(Ⅲ)
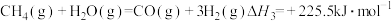
则反应
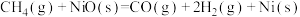 的
的
 。
。(3)“水汽转换反应器”中发生的反应为
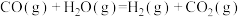 (平衡常数
(平衡常数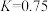 ),将天然气看作是纯净的
),将天然气看作是纯净的 (假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻
(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻 、
、 、
、 、
、 浓度之比为
浓度之比为 此时
此时
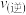 (填“>”、“=”或“<”),理由是
(填“>”、“=”或“<”),理由是(4)甲烷制氢传统工艺有水蒸气重整部分氧化重整以及联合重整等,
 工艺重整是一种联合重整,涉及反应的热化学方程式如下:
工艺重整是一种联合重整,涉及反应的热化学方程式如下:水蒸气重整反应:
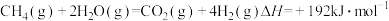
部分氧化重整反应:
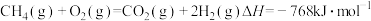
采用水蒸气重整的优点是
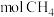 至多可获得
至多可获得 的物质的量为
的物质的量为
您最近一年使用:0次
7 . 硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是SO2的催化氧化:2SO2(g)+O2(g)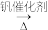 2SO3(g) ΔH=-196 kJ·mol-1。回答下列问题:
2SO3(g) ΔH=-196 kJ·mol-1。回答下列问题:
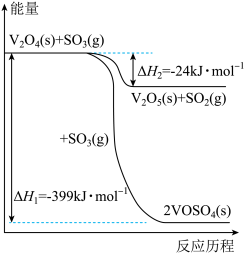
(1) 钒催化剂参与反应的能量变化如图所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:__________________________ 。
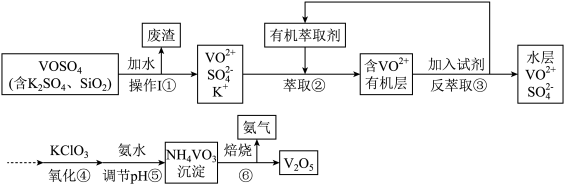
(2) 工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
请回答下列问题:
①步骤①所得废渣的成分是__________ (写化学式),操作I的名称______________ 。
②步骤②、③的变化过程表示为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n(水层)+2n HA(有机层) 2RAn(有机层)+n H2SO4(水层)
2RAn(有机层)+n H2SO4(水层)
②中萃取时必须加入适量碱,其原因是_________________________________ 。
③中X试剂为(写化学式)________________ 。
③④的离子方程式为_____________________________________ 。
 2SO3(g) ΔH=-196 kJ·mol-1。回答下列问题:
2SO3(g) ΔH=-196 kJ·mol-1。回答下列问题:(1) 钒催化剂参与反应的能量变化如图所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:

(2) 工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:

请回答下列问题:
①步骤①所得废渣的成分是
②步骤②、③的变化过程表示为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n(水层)+2n HA(有机层)
 2RAn(有机层)+n H2SO4(水层)
2RAn(有机层)+n H2SO4(水层)②中萃取时必须加入适量碱,其原因是
③中X试剂为(写化学式)
③④的离子方程式为
您最近一年使用:0次
名校
解题方法
8 . 饮用水的质量关系到关系到每个人的健康,因含有一定浓度的NO3-将对人类健康产生危害,NO3-能氧化人体血红蛋白中的Fe(II),使其失去携氧功能,为了降低饮用水中NO3-的浓度,某兴趣小组提出如图方案:
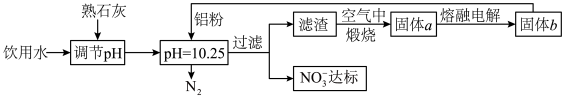
请回答下列问题:
(1)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。市场出售的某种麦片中含有微量、颗粒细小的还原铁粉,这些铁粉在人体胃酸(胃酸的主要成分是HCl)作用下转化成亚铁盐。写出该反应的离子方程式:____ 。
(2)已知过滤后得到的滤渣是一种混合物,则在溶液中铝粉和NO3-反应的离子方程式为__ 。
(3)该方案中选用熟石灰调节pH,理由是___ 、___ 。
(4)用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为___ 。
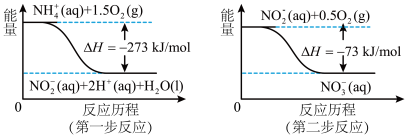
(5)饮用水中的NO3-主要来自于NH4+。已知在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如图,试写出1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是____ 。

请回答下列问题:
(1)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。市场出售的某种麦片中含有微量、颗粒细小的还原铁粉,这些铁粉在人体胃酸(胃酸的主要成分是HCl)作用下转化成亚铁盐。写出该反应的离子方程式:
(2)已知过滤后得到的滤渣是一种混合物,则在溶液中铝粉和NO3-反应的离子方程式为
(3)该方案中选用熟石灰调节pH,理由是
(4)用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为
(5)饮用水中的NO3-主要来自于NH4+。已知在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如图,试写出1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是

您最近一年使用:0次
9 . 钒是一种重要的合金元素,还用于催化剂和新型电池。从含钒固体废弃物(含有SiO2、Al2O3及其他残渣)中提取钒的一种新工艺主要流程如下:

部分含钒化合物在水中的溶解性如下表:
请回答下列问题:
(1)反应①所得溶液中除H+之外的阳离子有___________ 。
(2)反应②碱浸后滤出的固体主要成分是____________ (写化学式)。
(3)反应④的离子方程式为____________________ 。
(4)25℃、101 kPa时,4Al(s)+3O2(g)==2Al2O3(s) ΔH1=-a kJ/mol
4V(s)+5O2(g)==2V2O5(s) ΔH2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是_____________ 。
(5)钒液流电池(如右上图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过。电池放电时负极的电极反应式为__________ ,电池充电时阳极的电极反应式是_________ 。

(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2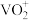 +H2C2O4+2H+=2VO2++2CO2↑+2H2O。取25.00 mL0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为
+H2C2O4+2H+=2VO2++2CO2↑+2H2O。取25.00 mL0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为______ g/L。

部分含钒化合物在水中的溶解性如下表:
| 物质 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
| 溶解性 | 难溶 | 难溶 | 可溶 | 易溶 |
(1)反应①所得溶液中除H+之外的阳离子有
(2)反应②碱浸后滤出的固体主要成分是
(3)反应④的离子方程式为
(4)25℃、101 kPa时,4Al(s)+3O2(g)==2Al2O3(s) ΔH1=-a kJ/mol
4V(s)+5O2(g)==2V2O5(s) ΔH2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是
(5)钒液流电池(如右上图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过。电池放电时负极的电极反应式为

(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2
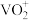 +H2C2O4+2H+=2VO2++2CO2↑+2H2O。取25.00 mL0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为
+H2C2O4+2H+=2VO2++2CO2↑+2H2O。取25.00 mL0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为
您最近一年使用:0次
2016-12-09更新
|
647次组卷
|
5卷引用:2015届湖北省武汉华中师大一附中高三5月适应性考试化学试卷



