名校
解题方法
1 . 为实现“碳中和”“碳达峰”,碳的循环利用是重要措施。利用氢气和CO反应生成甲烷,涉及的反应如下:
i.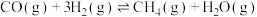

ii.

iii.

回答下列问题:
(1)在25℃和101kPa下, 转变为
转变为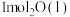 时放出44.0kJ热量,
时放出44.0kJ热量, 的燃烧热为
的燃烧热为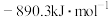 ,CO的燃烧热为
,CO的燃烧热为 ,
, 的燃烧热为
的燃烧热为 ,则
,则
________  。
。
(2)一定温度下,在恒容的密闭容器中进行上述反应,平衡时CO的转化率及 的选择性随
的选择性随 变化的情况如图所示[已知
变化的情况如图所示[已知 的选择性
的选择性 ]。
]。 选择性变化的曲线是
选择性变化的曲线是________ (填“甲”或“乙”),保持 不变,曲线甲由B点达到A点需要的条件为
不变,曲线甲由B点达到A点需要的条件为________ 。
②相同温度下,向恒容容器内加入 和1molCO,初始压强为10MPa,平衡时
和1molCO,初始压强为10MPa,平衡时 的物质的量为
的物质的量为________ mol,反应ii的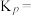
________ (保留小数点后一位)。
(3) 催化加氢制甲醇也是碳循环的重要途径。
催化加氢制甲醇也是碳循环的重要途径。 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共
在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共________ 种, 催化加氢制甲醇总反应的化学方程式为
催化加氢制甲醇总反应的化学方程式为________ 。
i.
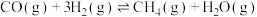

ii.


iii.


回答下列问题:
(1)在25℃和101kPa下,
 转变为
转变为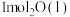 时放出44.0kJ热量,
时放出44.0kJ热量, 的燃烧热为
的燃烧热为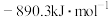 ,CO的燃烧热为
,CO的燃烧热为 ,
, 的燃烧热为
的燃烧热为 ,则
,则
 。
。(2)一定温度下,在恒容的密闭容器中进行上述反应,平衡时CO的转化率及
 的选择性随
的选择性随 变化的情况如图所示[已知
变化的情况如图所示[已知 的选择性
的选择性 ]。
]。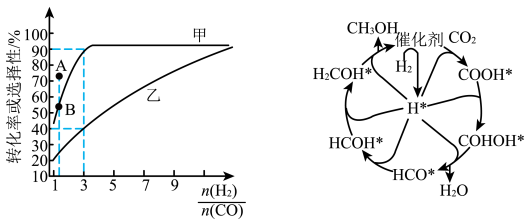
 选择性变化的曲线是
选择性变化的曲线是 不变,曲线甲由B点达到A点需要的条件为
不变,曲线甲由B点达到A点需要的条件为②相同温度下,向恒容容器内加入
 和1molCO,初始压强为10MPa,平衡时
和1molCO,初始压强为10MPa,平衡时 的物质的量为
的物质的量为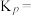
(3)
 催化加氢制甲醇也是碳循环的重要途径。
催化加氢制甲醇也是碳循环的重要途径。 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共
在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共 催化加氢制甲醇总反应的化学方程式为
催化加氢制甲醇总反应的化学方程式为
您最近一年使用:0次
7日内更新
|
217次组卷
|
7卷引用:2024届陕西省安康市安康市高新中学,安康中学高新分校高三下学期模拟预测理综试题-高中化学
解题方法
2 . 将 转化为
转化为 等燃料有助于降低大气中
等燃料有助于降低大气中 浓度,还能获得乙醇等高附加值化学品,是实现“碳中和”目标的一种有效途径。
浓度,还能获得乙醇等高附加值化学品,是实现“碳中和”目标的一种有效途径。
(1)已知下列反应的热化学方程式:
Ⅰ.2CO2(g)+2H2O(g)⇌2C2H4(g)+3O2(g) K1 ΔH1=+1323kJ/mol
Ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g) K2 ΔH2=+41kJ/mol
Ⅲ.C2H4(g)+H2O(g)⇌C2H5OH(g) K3 ΔH3=-45.5kJ/mol
反应2CO(g)+5H2O(g)⇌2C2H5OH(g)+3O2(g)+2H2(g)的
___________ ,平衡常数K=___________ (用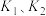 和
和 表示)。
表示)。
(2)将5mol 和20mol
和20mol 通入起始压强为p的某恒容密闭容器中发生反应Ⅳ:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) K4 ΔH4=-165kJ/mol(主反应)和反应Ⅱ(副反应),平衡时容器中含碳物质的物质的量随温度的变化如图1所示。
通入起始压强为p的某恒容密闭容器中发生反应Ⅳ:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) K4 ΔH4=-165kJ/mol(主反应)和反应Ⅱ(副反应),平衡时容器中含碳物质的物质的量随温度的变化如图1所示。 的产率,理论上应采用的措施是
的产率,理论上应采用的措施是___________ (填“低”或“高”,后同)温___________ 压。
②800K时,反应Ⅱ的平衡常数
___________ (用平衡分压代替物质的量浓度计算,保留两位有效数字)。
③500K时,若只发生反应Ⅳ,下列说法能判断反应达到平衡状态的是___________ (填标号)。
A.消耗1mol 的同时生成2mol
的同时生成2mol
B.混合气体的平均相对分子质量保持不变
C. 的体积分数不再变化
的体积分数不再变化
D.体系的温度不再发生变化
(3)我国科学家提出了一种用双催化剂协同催化 合成
合成 的路径。先利用催化剂将
的路径。先利用催化剂将 转化为*CO(*表示吸附态)和游离态的CO,再经过一系列的反应形成
转化为*CO(*表示吸附态)和游离态的CO,再经过一系列的反应形成 ,该过程能量与反应进程的关系如图2所示。
,该过程能量与反应进程的关系如图2所示。___________ (用“→”表示含碳物质间的转化)。
②游离态CO的自由能___________ (填“大于”或“小于”) *CO的自由能。
 转化为
转化为 等燃料有助于降低大气中
等燃料有助于降低大气中 浓度,还能获得乙醇等高附加值化学品,是实现“碳中和”目标的一种有效途径。
浓度,还能获得乙醇等高附加值化学品,是实现“碳中和”目标的一种有效途径。(1)已知下列反应的热化学方程式:
Ⅰ.2CO2(g)+2H2O(g)⇌2C2H4(g)+3O2(g) K1 ΔH1=+1323kJ/mol
Ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g) K2 ΔH2=+41kJ/mol
Ⅲ.C2H4(g)+H2O(g)⇌C2H5OH(g) K3 ΔH3=-45.5kJ/mol
反应2CO(g)+5H2O(g)⇌2C2H5OH(g)+3O2(g)+2H2(g)的

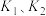 和
和 表示)。
表示)。(2)将5mol
 和20mol
和20mol 通入起始压强为p的某恒容密闭容器中发生反应Ⅳ:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) K4 ΔH4=-165kJ/mol(主反应)和反应Ⅱ(副反应),平衡时容器中含碳物质的物质的量随温度的变化如图1所示。
通入起始压强为p的某恒容密闭容器中发生反应Ⅳ:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) K4 ΔH4=-165kJ/mol(主反应)和反应Ⅱ(副反应),平衡时容器中含碳物质的物质的量随温度的变化如图1所示。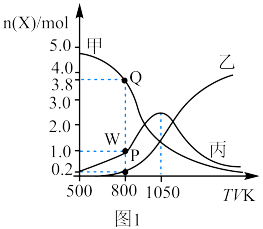
 的产率,理论上应采用的措施是
的产率,理论上应采用的措施是②800K时,反应Ⅱ的平衡常数

③500K时,若只发生反应Ⅳ,下列说法能判断反应达到平衡状态的是
A.消耗1mol
 的同时生成2mol
的同时生成2mol
B.混合气体的平均相对分子质量保持不变
C.
 的体积分数不再变化
的体积分数不再变化D.体系的温度不再发生变化
(3)我国科学家提出了一种用双催化剂协同催化
 合成
合成 的路径。先利用催化剂将
的路径。先利用催化剂将 转化为*CO(*表示吸附态)和游离态的CO,再经过一系列的反应形成
转化为*CO(*表示吸附态)和游离态的CO,再经过一系列的反应形成 ,该过程能量与反应进程的关系如图2所示。
,该过程能量与反应进程的关系如图2所示。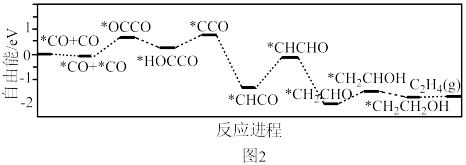
②游离态CO的自由能
您最近一年使用:0次
名校
解题方法
3 . 乙醇是燃料,也是重要的有机化工原料,二氧化碳加氢还原制乙醇已成为研究热点,相关的反应如下:
反应i:
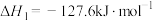
反应ii: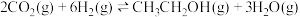
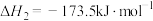
反应iii: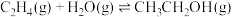
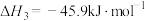
请回答下列问题:
(1)已知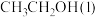 的燃烧热(
的燃烧热( )为
)为 ,表示
,表示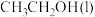 燃烧热的热化学方程式为
燃烧热的热化学方程式为________ 。
(2)在一定温度下,向2L恒容密闭容器中充入 和
和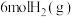 ,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如
,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如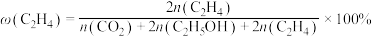 ]与时间的关系如图所示。
]与时间的关系如图所示。
①表示乙烯占比的曲线是________ (填“a”“b”或“c”)。
②若选择对反应i催化效果更好的催化剂,则A点可能移向________ (填“E”“E点上方”或“E点下方”)。
③已知C点、D点均为平衡点,则反应iii的平衡常数K=________ (保留小数点后一位)。
④设反应i和反应ii的化学平衡常数分别为 、
、 ,适当升温后,
,适当升温后,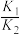
________ (填“增大”“减小”或“无法判断”),理由是________ 。
(3)近日,中国科学技术大学某课题组以Pd掺杂的 原子层为原型,在温和条件下,通过
原子层为原型,在温和条件下,通过 光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴(
光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴( )(
)(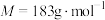 )在空气中受热时固体质量随温度变化的曲线如图所示。
)在空气中受热时固体质量随温度变化的曲线如图所示。________ ,CD段发生反应的化学方程式为________ 。
反应i:

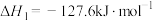
反应ii:
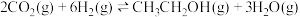
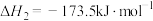
反应iii:
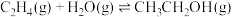
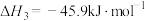
请回答下列问题:
(1)已知
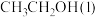 的燃烧热(
的燃烧热( )为
)为 ,表示
,表示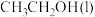 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)在一定温度下,向2L恒容密闭容器中充入
 和
和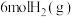 ,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如
,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如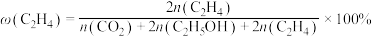 ]与时间的关系如图所示。
]与时间的关系如图所示。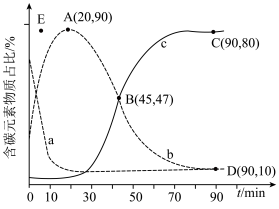
①表示乙烯占比的曲线是
②若选择对反应i催化效果更好的催化剂,则A点可能移向
③已知C点、D点均为平衡点,则反应iii的平衡常数K=
④设反应i和反应ii的化学平衡常数分别为
 、
、 ,适当升温后,
,适当升温后,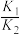
(3)近日,中国科学技术大学某课题组以Pd掺杂的
 原子层为原型,在温和条件下,通过
原子层为原型,在温和条件下,通过 光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴(
光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴( )(
)(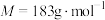 )在空气中受热时固体质量随温度变化的曲线如图所示。
)在空气中受热时固体质量随温度变化的曲线如图所示。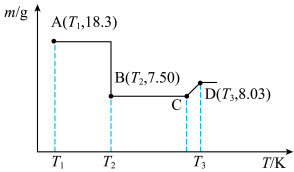
您最近一年使用:0次
解题方法
4 . 二氧化碳催化加氢制甲烷的反应受到人们广泛关注。回答下列问题:
(1)二氧化碳加氢制甲烷的过程中主要发生以下反应:
Ⅰ.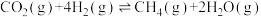
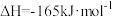
Ⅱ.

反应 的
的
_______  ,该反应在
,该反应在_______ (填“低温”“高温”或“任意温度”)条件下能自发进行。
(2)以Ni作催化剂,可选择 、
、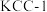 、
、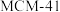 为载体。在密闭容器中,控制
为载体。在密闭容器中,控制 、加入
、加入 和
和 ,使用不同的催化剂载体,发生反应Ⅰ、Ⅱ,
,使用不同的催化剂载体,发生反应Ⅰ、Ⅱ, 的转化率及其平衡转化率随温度变化的情况如图所示。
的转化率及其平衡转化率随温度变化的情况如图所示。_______ 。
②在图中所示温度范围内,随温度升高, 的平衡转化率减小,原因可能是
的平衡转化率减小,原因可能是_______ 。研究表明,当温度升至600℃以上, 的平衡转化率随温度升高而增大,此时
的平衡转化率随温度升高而增大,此时 的产率随温度升高而
的产率随温度升高而_______ (填“升高”“降低”或“不变”)。
③525℃下达到平衡时, 的转化率为80%,
的转化率为80%, 的转化率为57.5%,
的转化率为57.5%, 的物质的量为
的物质的量为_______ mol,反应Ⅰ用摩尔分数表示的平衡常数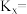
_______ (列出计算式,用摩尔分数代替平衡浓度计算,物质i的摩尔分数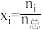 )。
)。
(3)若反应物中混入 ,会导致Ni催化剂失活。原因是
,会导致Ni催化剂失活。原因是 吸附在Ni活性位点,阻止了
吸附在Ni活性位点,阻止了 与
与 的反应。在Ni催化剂中添加Mn和Zn助剂,可避免Ni催化剂失活,其机理可能是
的反应。在Ni催化剂中添加Mn和Zn助剂,可避免Ni催化剂失活,其机理可能是_______ 。
(1)二氧化碳加氢制甲烷的过程中主要发生以下反应:
Ⅰ.
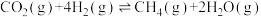
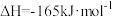
Ⅱ.


反应
 的
的
 ,该反应在
,该反应在(2)以Ni作催化剂,可选择
 、
、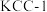 、
、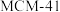 为载体。在密闭容器中,控制
为载体。在密闭容器中,控制 、加入
、加入 和
和 ,使用不同的催化剂载体,发生反应Ⅰ、Ⅱ,
,使用不同的催化剂载体,发生反应Ⅰ、Ⅱ, 的转化率及其平衡转化率随温度变化的情况如图所示。
的转化率及其平衡转化率随温度变化的情况如图所示。
②在图中所示温度范围内,随温度升高,
 的平衡转化率减小,原因可能是
的平衡转化率减小,原因可能是 的平衡转化率随温度升高而增大,此时
的平衡转化率随温度升高而增大,此时 的产率随温度升高而
的产率随温度升高而③525℃下达到平衡时,
 的转化率为80%,
的转化率为80%, 的转化率为57.5%,
的转化率为57.5%, 的物质的量为
的物质的量为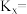
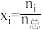 )。
)。(3)若反应物中混入
 ,会导致Ni催化剂失活。原因是
,会导致Ni催化剂失活。原因是 吸附在Ni活性位点,阻止了
吸附在Ni活性位点,阻止了 与
与 的反应。在Ni催化剂中添加Mn和Zn助剂,可避免Ni催化剂失活,其机理可能是
的反应。在Ni催化剂中添加Mn和Zn助剂,可避免Ni催化剂失活,其机理可能是
您最近一年使用:0次
解题方法
5 .  和
和 共活化处理的研究既有利于实现碳中和,又有利于处理某些环境中的有害气体.该研究过程主要涉及如下反应:
共活化处理的研究既有利于实现碳中和,又有利于处理某些环境中的有害气体.该研究过程主要涉及如下反应:
Ⅰ.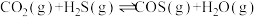
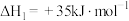
Ⅱ.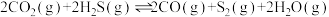
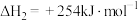
Ⅲ.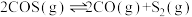

回答下列问题:
(1)反应Ⅲ的反应热
________ ,该反应在________ (填“高温”“低温”或“任意温度”)下能自发进行;
(2)向某密闭容器中投入等物质的量的 和
和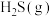 ,发生上述反应.其中
,发生上述反应.其中 的平衡转化率随温度或压强变化如图.L,X可分别代表压强或温度;
的平衡转化率随温度或压强变化如图.L,X可分别代表压强或温度;________ ,原因为________ ;
②若在恒温恒容密闭容器中发生上述反应,下列条件能说明上述反应均达到平衡状态的是________ (填字母);
A. 和
和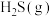 的物质的量之比不再发生变化时
的物质的量之比不再发生变化时
B. 和
和 的物质的量之比不再发生变化时
的物质的量之比不再发生变化时
C. 混合气体密度不再发生变化时
D. 容器内压强不再发生变化时
(3) 下,向起始压强为
下,向起始压强为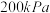 的恒容密闭容器中通入等物质的量的
的恒容密闭容器中通入等物质的量的 和
和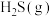 混合气体,发生上述反应,
混合气体,发生上述反应,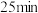 时达到平衡状态,测得此时体系总压强为
时达到平衡状态,测得此时体系总压强为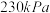 ,
, ;
;
①平衡时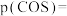
________ 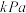 ;
;
② 的平均生成速率为
的平均生成速率为________  ;
;
③ 下反应Ⅲ的压力平衡常数
下反应Ⅲ的压力平衡常数
________  ;
;
 和
和 共活化处理的研究既有利于实现碳中和,又有利于处理某些环境中的有害气体.该研究过程主要涉及如下反应:
共活化处理的研究既有利于实现碳中和,又有利于处理某些环境中的有害气体.该研究过程主要涉及如下反应:Ⅰ.
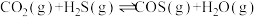
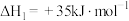
Ⅱ.
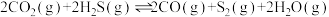
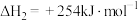
Ⅲ.
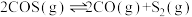

回答下列问题:
(1)反应Ⅲ的反应热

(2)向某密闭容器中投入等物质的量的
 和
和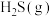 ,发生上述反应.其中
,发生上述反应.其中 的平衡转化率随温度或压强变化如图.L,X可分别代表压强或温度;
的平衡转化率随温度或压强变化如图.L,X可分别代表压强或温度;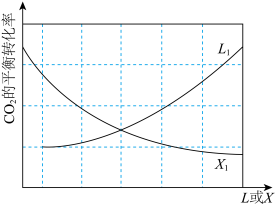
②若在恒温恒容密闭容器中发生上述反应,下列条件能说明上述反应均达到平衡状态的是
A.
 和
和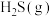 的物质的量之比不再发生变化时
的物质的量之比不再发生变化时B.
 和
和 的物质的量之比不再发生变化时
的物质的量之比不再发生变化时C. 混合气体密度不再发生变化时
D. 容器内压强不再发生变化时
(3)
 下,向起始压强为
下,向起始压强为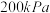 的恒容密闭容器中通入等物质的量的
的恒容密闭容器中通入等物质的量的 和
和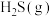 混合气体,发生上述反应,
混合气体,发生上述反应,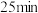 时达到平衡状态,测得此时体系总压强为
时达到平衡状态,测得此时体系总压强为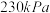 ,
, ;
;①平衡时
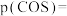
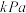 ;
;②
 的平均生成速率为
的平均生成速率为 ;
;③
 下反应Ⅲ的压力平衡常数
下反应Ⅲ的压力平衡常数
 ;
;
您最近一年使用:0次
6 . 2023年杭州亚运会主火炬塔首次使用废碳再生的“绿色甲醇”作为燃料,实现了循环内的零排放。“零碳甲醇”作为公认的新型清洁可再生能源,不易爆炸、储运安全便捷。
甲醇的制备方法有二氧化碳加氢法、电催化法、甲烷催化氧化法等。回答下列问题:
Ⅰ.二氧化碳加氢制甲醇:
①
 kJ/mol
kJ/mol
②
 kJ/mol
kJ/mol
③

已知:甲醇的选择性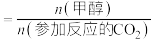
(1)
___________ ,该反应自发进行的条件是___________ 。
(2)一定温度下,在恒容密闭反应器中,反应③达到平衡,下列措施中能使平衡体系中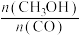 增大且加快化学反应速率的是___________ (填字母)。
增大且加快化学反应速率的是___________ (填字母)。
(3)恒温恒容条件下,原料气 、
、 以物质的量浓度之比为1∶3投料时,控制合适条件(不考虑反应③),甲醇的选择性为60%。已知初始压强为4MPa,
以物质的量浓度之比为1∶3投料时,控制合适条件(不考虑反应③),甲醇的选择性为60%。已知初始压强为4MPa, ,达到平衡时,
,达到平衡时,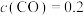 mol/L,则该过程中
mol/L,则该过程中 的平衡转化率为
的平衡转化率为___________ %,该条件下反应②的
___________ (保留三位有效数字)。
Ⅱ.电催化法
一种基于铜基金属簇催化剂电催化还原 制备甲醇的装置如左下图所示。控制其他条件相同,将一定量的
制备甲醇的装置如左下图所示。控制其他条件相同,将一定量的 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如右下图所示。
通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如右下图所示。 的电极反应式为
的电极反应式为___________ 。
(5)控制电压为0.8V,电解时转移电子的物质的量为___________ mol。
Ⅲ.甲烷催化氧化法
主反应: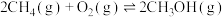
副反应: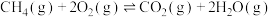
科学家将 、
、 和
和 (
( 是活性催化剂)按一定体积比在催化剂表面合成甲醇,部分反应历程如图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。
是活性催化剂)按一定体积比在催化剂表面合成甲醇,部分反应历程如图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。___________ kJ·mol ,写出该步骤反应的化学方程式:
,写出该步骤反应的化学方程式:___________ 。
甲醇的制备方法有二氧化碳加氢法、电催化法、甲烷催化氧化法等。回答下列问题:
Ⅰ.二氧化碳加氢制甲醇:
①

 kJ/mol
kJ/mol②

 kJ/mol
kJ/mol③


已知:甲醇的选择性
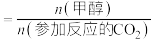
(1)

(2)一定温度下,在恒容密闭反应器中,反应③达到平衡,下列措施中能使平衡体系中
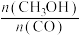 增大且加快化学反应速率的是___________ (填字母)。
增大且加快化学反应速率的是___________ (填字母)。| A.升高温度 | B.充入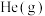 ,使体系压强增大 ,使体系压强增大 |
C.再充入1 mol | D.将 从体系中分离出去 从体系中分离出去 |
(3)恒温恒容条件下,原料气
 、
、 以物质的量浓度之比为1∶3投料时,控制合适条件(不考虑反应③),甲醇的选择性为60%。已知初始压强为4MPa,
以物质的量浓度之比为1∶3投料时,控制合适条件(不考虑反应③),甲醇的选择性为60%。已知初始压强为4MPa, ,达到平衡时,
,达到平衡时,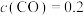 mol/L,则该过程中
mol/L,则该过程中 的平衡转化率为
的平衡转化率为
Ⅱ.电催化法
一种基于铜基金属簇催化剂电催化还原
 制备甲醇的装置如左下图所示。控制其他条件相同,将一定量的
制备甲醇的装置如左下图所示。控制其他条件相同,将一定量的 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如右下图所示。
通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如右下图所示。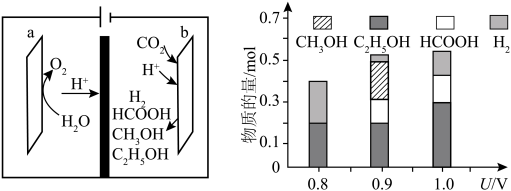
 的电极反应式为
的电极反应式为(5)控制电压为0.8V,电解时转移电子的物质的量为
Ⅲ.甲烷催化氧化法
主反应:
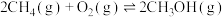
副反应:
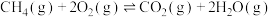
科学家将
 、
、 和
和 (
( 是活性催化剂)按一定体积比在催化剂表面合成甲醇,部分反应历程如图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。
是活性催化剂)按一定体积比在催化剂表面合成甲醇,部分反应历程如图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。
 ,写出该步骤反应的化学方程式:
,写出该步骤反应的化学方程式:
您最近一年使用:0次
7 . 为减小或消除CO2对环境的影响,科学家加强了对CO2创新利用的研究。回答下列问题:
(1)将CO2通过光热催化还原为高附加值碳氢燃料,包括以下反应:
反应I.

反应Ⅱ.

①已知反应Ⅲ.
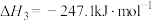 ,则
,则
___________ kJ·mol-1。
②350℃时,将0.5molCO2、1.5molH2通入恒压密闭容器中,在0.1gCo3O4催化下发生反应I和反应Ⅱ,10h后达到平衡,CO2转化率为75%,CO的产量为0.075mol,则CH4的产率为___________ mol·h-1·g-1(产率= ),CH4选择性为
),CH4选择性为___________ (选择性=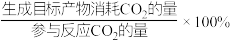 ),反应Ⅱ的
),反应Ⅱ的
___________ 。
(2)在催化剂的作用下,CO2高选择性转化为乙醇的反应原理为 。
。
①图1、图2是温度、压强对乙醇选择性的影响,则最佳温度和压强分别为___________ 。___________ 。
①写出在酸性介质中CO2转化为CH4的电极反应式:___________ 。
②理论上生成等物质的量的CH4和HCOOH时消耗的电能之比为___________ 。
(1)将CO2通过光热催化还原为高附加值碳氢燃料,包括以下反应:
反应I.


反应Ⅱ.


①已知反应Ⅲ.

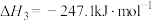 ,则
,则
②350℃时,将0.5molCO2、1.5molH2通入恒压密闭容器中,在0.1gCo3O4催化下发生反应I和反应Ⅱ,10h后达到平衡,CO2转化率为75%,CO的产量为0.075mol,则CH4的产率为
 ),CH4选择性为
),CH4选择性为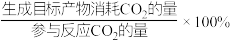 ),反应Ⅱ的
),反应Ⅱ的
(2)在催化剂的作用下,CO2高选择性转化为乙醇的反应原理为
 。
。①图1、图2是温度、压强对乙醇选择性的影响,则最佳温度和压强分别为
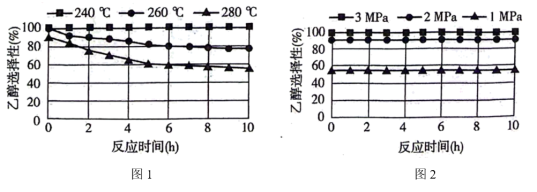
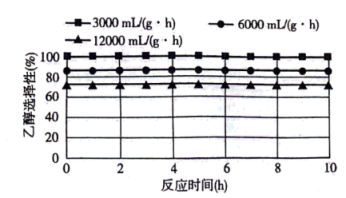
①写出在酸性介质中CO2转化为CH4的电极反应式:
②理论上生成等物质的量的CH4和HCOOH时消耗的电能之比为
您最近一年使用:0次
解题方法
8 . CO2资源化利用备受关注,研究CO2资源化综合利用有重要意义。已知:
反应Ⅰ:CO2(g)+H2(g)=CO(g)+H2O(g) H1=+41.2kJ/mol
H1=+41.2kJ/mol
反应Ⅱ:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) H2=-122.5kJ/mol
H2=-122.5kJ/mol
回答下列问题:
(1)反应2CO(g)+4H2(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)  H=
H=___________ kJ/mol。
(2)将4molCO、6molH2置于某密闭容器中,控制适当条件使其发生反应:2CO(g)+4H2(g) CH3OCH3(g)+H2O(g),测得CO的某种平衡量值(x)在不同压强下随温度的变化如图1所示:
CH3OCH3(g)+H2O(g),测得CO的某种平衡量值(x)在不同压强下随温度的变化如图1所示:___________ (填“体积分数”或“转化率”),为了提高反应速率的同时能提高H2的转化率,可采取的措施有___________ (填字母)。
a.使用高效催化剂 b.缩小容器的体积
c.升高温度 d.增大H2的浓度
②若p1=6MPa,B点表示反应从开始进行到10min时达到平衡状态,则v(H2)=___________ MPa·min-1,Kp=___________ MPa-4(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③若对D点状态的反应同时进行降温、缩小体积的操作,重新达到平衡状态可能是图中A~G点中的___________ 点。
(3)在恒压密闭容器中投入xmolCO2和ymolH2,发生上述反应Ⅰ和Ⅱ。测得CO2的平衡转化率和平衡时CO的选择性(CO的选择性=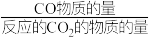 ×100%)随温度的变化曲线如图2所示。
×100%)随温度的变化曲线如图2所示。
①T℃达到平衡时,反应Ⅱ理论上消耗CO2的物质的量为___________ mol。
②合成二甲醚的适宜温度为260℃,其原因是___________ 。
反应Ⅰ:CO2(g)+H2(g)=CO(g)+H2O(g)
 H1=+41.2kJ/mol
H1=+41.2kJ/mol反应Ⅱ:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)
 H2=-122.5kJ/mol
H2=-122.5kJ/mol回答下列问题:
(1)反应2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)  H=
H=(2)将4molCO、6molH2置于某密闭容器中,控制适当条件使其发生反应:2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g),测得CO的某种平衡量值(x)在不同压强下随温度的变化如图1所示:
CH3OCH3(g)+H2O(g),测得CO的某种平衡量值(x)在不同压强下随温度的变化如图1所示: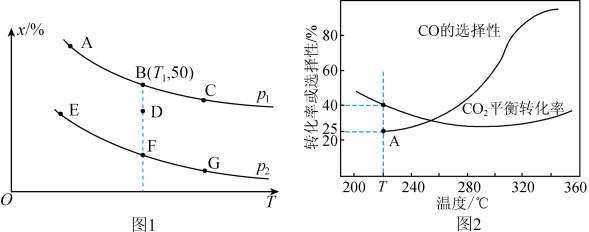
a.使用高效催化剂 b.缩小容器的体积
c.升高温度 d.增大H2的浓度
②若p1=6MPa,B点表示反应从开始进行到10min时达到平衡状态,则v(H2)=
③若对D点状态的反应同时进行降温、缩小体积的操作,重新达到平衡状态可能是图中A~G点中的
(3)在恒压密闭容器中投入xmolCO2和ymolH2,发生上述反应Ⅰ和Ⅱ。测得CO2的平衡转化率和平衡时CO的选择性(CO的选择性=
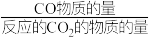 ×100%)随温度的变化曲线如图2所示。
×100%)随温度的变化曲线如图2所示。①T℃达到平衡时,反应Ⅱ理论上消耗CO2的物质的量为
②合成二甲醚的适宜温度为260℃,其原因是
您最近一年使用:0次
解题方法
9 . 我国力争于2030年前实现碳达峰,2060年前实现碳中和,因此 的综合利用成为研究热点。
的综合利用成为研究热点。
(1)通过捕捉空气中的 和电解水产生的H2可以合成“零碳甲醇”。已知H2(g)的燃烧热为286
和电解水产生的H2可以合成“零碳甲醇”。已知H2(g)的燃烧热为286 ,
, 的燃烧热为726
的燃烧热为726 ,反应
,反应 的
的
_______  。
。
(2)利用电喷雾电离等方法可得 ,
, 与
与 反应能高选择性地生成甲醇,反应机理如下图所示:
反应能高选择性地生成甲醇,反应机理如下图所示: 与
与 反应的能量变化曲线为
反应的能量变化曲线为_______ (填“c”或“d”),写出 与
与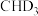 反应生成的氘代甲醇的结构简式:
反应生成的氘代甲醇的结构简式:_______ 或_______ 。
(3)氢气和碳氧化物反应生成甲烷,涉及反应如下:
反应Ⅰ:
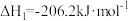
反应Ⅱ:
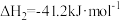
反应皿: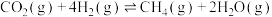
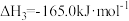
T℃时,向恒容密闭容器中充入一定量的 和1mol
和1mol  ,平衡时
,平衡时 和CO的转化率
和CO的转化率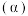 及
及 和
和 的物质的量
的物质的量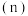 随
随 变化的情况如图所示。
变化的情况如图所示。 变化的曲线是
变化的曲线是_______ (填“a”、“b”、“c”或“d”);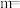
_______ ; 的选择性
的选择性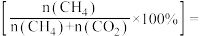
_______ 。
②已知起始充入1mol 和1mol
和1mol 进行上述反应时,起始压强为
进行上述反应时,起始压强为 。反应Ⅰ的分压平衡常数
。反应Ⅰ的分压平衡常数
_______ (用含 的代数式表示)。
的代数式表示)。
 的综合利用成为研究热点。
的综合利用成为研究热点。(1)通过捕捉空气中的
 和电解水产生的H2可以合成“零碳甲醇”。已知H2(g)的燃烧热为286
和电解水产生的H2可以合成“零碳甲醇”。已知H2(g)的燃烧热为286 ,
, 的燃烧热为726
的燃烧热为726 ,反应
,反应 的
的
 。
。(2)利用电喷雾电离等方法可得
 ,
, 与
与 反应能高选择性地生成甲醇,反应机理如下图所示:
反应能高选择性地生成甲醇,反应机理如下图所示: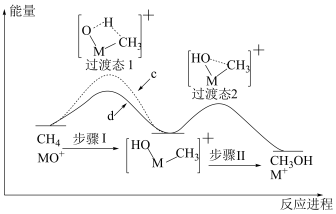
 与
与 反应的能量变化曲线为
反应的能量变化曲线为 与
与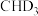 反应生成的氘代甲醇的结构简式:
反应生成的氘代甲醇的结构简式:(3)氢气和碳氧化物反应生成甲烷,涉及反应如下:
反应Ⅰ:

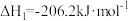
反应Ⅱ:

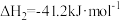
反应皿:
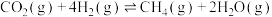
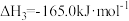
T℃时,向恒容密闭容器中充入一定量的
 和1mol
和1mol  ,平衡时
,平衡时 和CO的转化率
和CO的转化率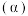 及
及 和
和 的物质的量
的物质的量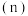 随
随 变化的情况如图所示。
变化的情况如图所示。
 变化的曲线是
变化的曲线是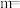
 的选择性
的选择性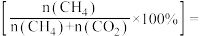
②已知起始充入1mol
 和1mol
和1mol 进行上述反应时,起始压强为
进行上述反应时,起始压强为 。反应Ⅰ的分压平衡常数
。反应Ⅰ的分压平衡常数
 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-04-29更新
|
136次组卷
|
2卷引用:2024届陕西省铜川市高三下学期第三次模拟考试理科综合试题-高中化学
10 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)已知: 、
、 和
和 键的键能分别为
键的键能分别为 、
、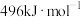 和
和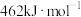 。
。

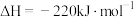

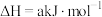
则
___________ 。
(2)已知: 在催化剂I和II的催化下的反应历程和能量变化如下图。
在催化剂I和II的催化下的反应历程和能量变化如下图。___________ (填I或II)时,反应过程中 所能达到的最高浓度更大。
所能达到的最高浓度更大。
②在相同条件下反应达到平衡状态,为提高 的平衡浓度和
的平衡浓度和 的平衡物质的量分数,可以采取的措施是
的平衡物质的量分数,可以采取的措施是___________ 。
(3)以 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
I.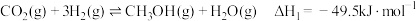
II.
在密闭容器中,压强恒为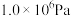 ,
,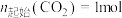 ,
,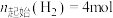 ,
, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率,随温度的变化如图所示。
实际转化率,随温度的变化如图所示。 的选择性可表示为
的选择性可表示为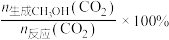 。
。
①反应的最佳温度___________ 。
②反应温度超过 时,
时, 平衡转化率逐渐增大的原因是
平衡转化率逐渐增大的原因是___________ 。
③反应温度超过 时,
时, 实际转化率逐渐减小的原因是
实际转化率逐渐减小的原因是___________ 。
④反应温度在 时,
时, 点
点 的选择性为
的选择性为 ,则平衡时
,则平衡时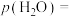
___________  (保留三位有效数字,后面相同),反应II的压强平衡常数
(保留三位有效数字,后面相同),反应II的压强平衡常数
___________ 。
(4)工业废气中含有的 和
和 可利用如下装置回收利用。
可利用如下装置回收利用。___________ 。
②装置b中,x和y为石墨电极,写出电极x的电极反应___________ 。
(1)已知:
 、
、 和
和 键的键能分别为
键的键能分别为 、
、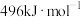 和
和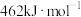 。
。
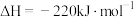

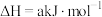
则

(2)已知:
 在催化剂I和II的催化下的反应历程和能量变化如下图。
在催化剂I和II的催化下的反应历程和能量变化如下图。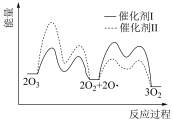
 所能达到的最高浓度更大。
所能达到的最高浓度更大。②在相同条件下反应达到平衡状态,为提高
 的平衡浓度和
的平衡浓度和 的平衡物质的量分数,可以采取的措施是
的平衡物质的量分数,可以采取的措施是(3)以
 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:I.
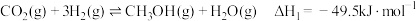
II.

在密闭容器中,压强恒为
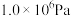 ,
,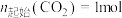 ,
,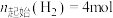 ,
, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率,随温度的变化如图所示。
实际转化率,随温度的变化如图所示。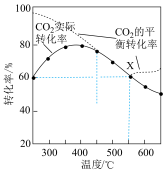
 的选择性可表示为
的选择性可表示为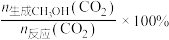 。
。①反应的最佳温度
②反应温度超过
 时,
时, 平衡转化率逐渐增大的原因是
平衡转化率逐渐增大的原因是③反应温度超过
 时,
时, 实际转化率逐渐减小的原因是
实际转化率逐渐减小的原因是④反应温度在
 时,
时, 点
点 的选择性为
的选择性为 ,则平衡时
,则平衡时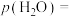
 (保留三位有效数字,后面相同),反应II的压强平衡常数
(保留三位有效数字,后面相同),反应II的压强平衡常数
(4)工业废气中含有的
 和
和 可利用如下装置回收利用。
可利用如下装置回收利用。
②装置b中,x和y为石墨电极,写出电极x的电极反应
您最近一年使用:0次



