1 . 甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。利用甲醇一定条件下直接脱氢可制甲醛,涉及的反应如下:
反应I:

反应II:

已知:①平衡状态下,甲醛选择性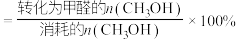 ;甲醛的收率
;甲醛的收率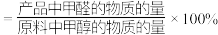 。
。
②几种物质的燃烧热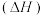 如下表:
如下表:
回答下列问题:
(1)
_______ ,HCHO的空间结构为_______ 形。
(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii: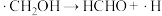
历程iii:
历程iv: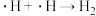
写出历程i的反应方程式:_______ 。
(3)将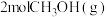 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示:_______ (填“I”或“II”),判断的依据是_______ 。
② ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为_______ ,
_______ ,反应I的平衡常数
_______  。
。
反应I:


反应II:


已知:①平衡状态下,甲醛选择性
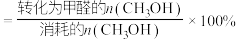 ;甲醛的收率
;甲醛的收率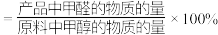 。
。②几种物质的燃烧热
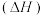 如下表:
如下表:| 物质 |  |  |  |  |
燃烧热 | -725.8 | -563.6 | -283.0 | -285.8 |
(1)

(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii:
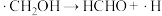
历程iii:

历程iv:
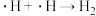
写出历程i的反应方程式:
(3)将
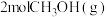 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示: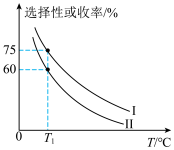
②
 ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为

 。
。
您最近一年使用:0次
7日内更新
|
178次组卷
|
3卷引用:2024届河南省周口市高三5月全真模拟理科综合试题-高中化学
解题方法
2 . 利用 为原料合成
为原料合成 的主要反应如下。
的主要反应如下。
Ⅰ.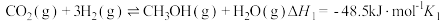
Ⅱ.
回答下列问题:
(1)已知反应Ⅲ的平衡常数 ,写出反应Ⅲ的热化学方程式
,写出反应Ⅲ的热化学方程式___________ 。
(2)一定条件下,向恒压密闭容器中以一定流速通入 和
和 混合气体,
混合气体, 平衡转化率和
平衡转化率和 选择性
选择性 随温度、投料比的变化曲线如图所示。
随温度、投料比的变化曲线如图所示。 选择性的曲线是
选择性的曲线是___________ (填“ ”或“
”或“ ”);
”); 平衡转化率随温度升高发生如图变化的原因是
平衡转化率随温度升高发生如图变化的原因是___________ 。
②生成 的最佳条件是
的最佳条件是___________ (填标号)。


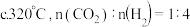

(3)一定温度下,向恒压密闭容器中通入 和
和 ,充分反应后,测得
,充分反应后,测得 平衡转化率为
平衡转化率为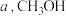 选择性为
选择性为 ,该温度下反应Ⅰ的平衡常数
,该温度下反应Ⅰ的平衡常数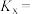
___________ ( 为以物质的量分数表示的平衡常数)。
为以物质的量分数表示的平衡常数)。
(4)向压强恒为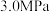 的密闭容器中通入反应混合气
的密闭容器中通入反应混合气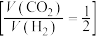 ,在
,在 催化作用下只发生反应Ⅰ,测得
催化作用下只发生反应Ⅰ,测得 时空收率(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度的变化曲线如图所示。
时空收率(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度的变化曲线如图所示。 时空收率随温度升高先增大后减小的原因是
时空收率随温度升高先增大后减小的原因是___________ 。
② 时,
时, 的平均反应速率
的平均反应速率
___________  。
。
③反应Ⅰ的速率方程可表示为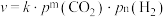 ,其中
,其中 为速率常数,
为速率常数, (单位:
(单位: )为各物质的起始分压,
)为各物质的起始分压,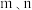 分别为
分别为 的反应级数。实验结果表明速率常数与反应级数均受温度影响,当反应温度由
的反应级数。实验结果表明速率常数与反应级数均受温度影响,当反应温度由 升高到
升高到 ,则
,则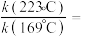
___________ 。
 为原料合成
为原料合成 的主要反应如下。
的主要反应如下。Ⅰ.
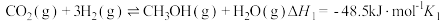
Ⅱ.

回答下列问题:
(1)已知反应Ⅲ的平衡常数
 ,写出反应Ⅲ的热化学方程式
,写出反应Ⅲ的热化学方程式(2)一定条件下,向恒压密闭容器中以一定流速通入
 和
和 混合气体,
混合气体, 平衡转化率和
平衡转化率和 选择性
选择性 随温度、投料比的变化曲线如图所示。
随温度、投料比的变化曲线如图所示。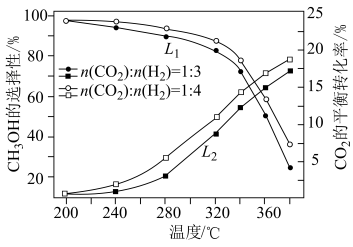
 选择性的曲线是
选择性的曲线是 ”或“
”或“ ”);
”); 平衡转化率随温度升高发生如图变化的原因是
平衡转化率随温度升高发生如图变化的原因是②生成
 的最佳条件是
的最佳条件是

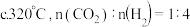

(3)一定温度下,向恒压密闭容器中通入
 和
和 ,充分反应后,测得
,充分反应后,测得 平衡转化率为
平衡转化率为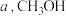 选择性为
选择性为 ,该温度下反应Ⅰ的平衡常数
,该温度下反应Ⅰ的平衡常数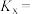
 为以物质的量分数表示的平衡常数)。
为以物质的量分数表示的平衡常数)。(4)向压强恒为
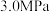 的密闭容器中通入反应混合气
的密闭容器中通入反应混合气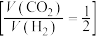 ,在
,在 催化作用下只发生反应Ⅰ,测得
催化作用下只发生反应Ⅰ,测得 时空收率(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度的变化曲线如图所示。
时空收率(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度的变化曲线如图所示。
 时空收率随温度升高先增大后减小的原因是
时空收率随温度升高先增大后减小的原因是②
 时,
时, 的平均反应速率
的平均反应速率
 。
。③反应Ⅰ的速率方程可表示为
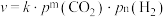 ,其中
,其中 为速率常数,
为速率常数, (单位:
(单位: )为各物质的起始分压,
)为各物质的起始分压,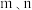 分别为
分别为 的反应级数。实验结果表明速率常数与反应级数均受温度影响,当反应温度由
的反应级数。实验结果表明速率常数与反应级数均受温度影响,当反应温度由 升高到
升高到 ,则
,则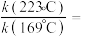
您最近一年使用:0次
3 . 氮氧化物( 、NO等)的处理和资源化利用具有重要意义。
、NO等)的处理和资源化利用具有重要意义。
(1)反应 分为三步基元反应完成。
分为三步基元反应完成。
第一步: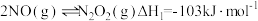 决速步骤)
决速步骤)
第二步: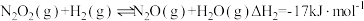
①活化能最高的是第___________ 步。
②为了提高总反应中NO的反应速率和转化率可采用的措施为___________ (写两条)。
(2)已知反应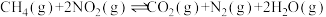 。某温度下向2.0L刚性密闭容器中充入
。某温度下向2.0L刚性密闭容器中充入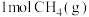 和
和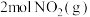 ,发生该反应,测得容器内气体总压强(p)与时间(t)的变化如下表所示:
,发生该反应,测得容器内气体总压强(p)与时间(t)的变化如下表所示:
①用 表示0~4min内平均反应速率为
表示0~4min内平均反应速率为___________ 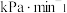 。
。
②该温度下的压强平衡常数
___________ kPa。
(3)NO催化分解ICl制取 和
和 的原理为:
的原理为:
反应I: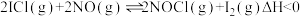 ;
;
反应Ⅱ: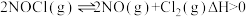 ;
; 。
。
反应的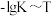 的关系如图所示。
的关系如图所示。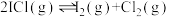 的
的
___________
(4)催化电解NO吸收液可生成多种物质,其中将NO还原为 的催化机理如图甲所示。在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率(FE%,法拉第效率之比等于转移电子的物质的量之比)随电解电压的变化如图乙所示。
的催化机理如图甲所示。在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率(FE%,法拉第效率之比等于转移电子的物质的量之比)随电解电压的变化如图乙所示。 的电极反应式为
的电极反应式为___________ 。
②当电解电压为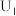 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为___________ 。
 、NO等)的处理和资源化利用具有重要意义。
、NO等)的处理和资源化利用具有重要意义。(1)反应
 分为三步基元反应完成。
分为三步基元反应完成。第一步:
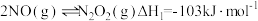 决速步骤)
决速步骤)第二步:
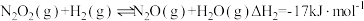
①活化能最高的是第
②为了提高总反应中NO的反应速率和转化率可采用的措施为
(2)已知反应
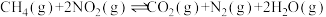 。某温度下向2.0L刚性密闭容器中充入
。某温度下向2.0L刚性密闭容器中充入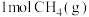 和
和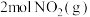 ,发生该反应,测得容器内气体总压强(p)与时间(t)的变化如下表所示:
,发生该反应,测得容器内气体总压强(p)与时间(t)的变化如下表所示:| 反应时间(t)/min | 0 | 2 | 4 | 6 | 8 | 10 |
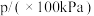 | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
 表示0~4min内平均反应速率为
表示0~4min内平均反应速率为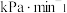 。
。②该温度下的压强平衡常数

(3)NO催化分解ICl制取
 和
和 的原理为:
的原理为:反应I:
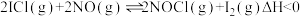 ;
;
反应Ⅱ:
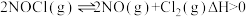 ;
; 。
。反应的
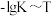 的关系如图所示。
的关系如图所示。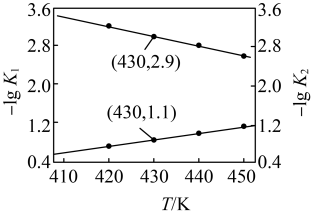
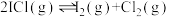 的
的
(4)催化电解NO吸收液可生成多种物质,其中将NO还原为
 的催化机理如图甲所示。在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率(FE%,法拉第效率之比等于转移电子的物质的量之比)随电解电压的变化如图乙所示。
的催化机理如图甲所示。在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率(FE%,法拉第效率之比等于转移电子的物质的量之比)随电解电压的变化如图乙所示。
 的电极反应式为
的电极反应式为②当电解电压为
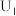 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
4 . 过硫酸钠(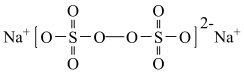 ),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对
),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对 制备和性质及用途进行探究。
制备和性质及用途进行探究。

工业制备过硫酸钠的反应原理:
主反应:

副反应:

实验室设计如图实验装置:
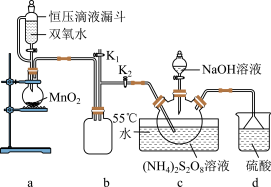
(2)装置b的作用是
(3)上述反应过程中,d装置中主要发生的化学反应方程式为
Ⅱ.探究
 的性质与用途
的性质与用途(4)
 用于废水中苯酚的降解
用于废水中苯酚的降解已知:a.
 具有强氧化性,
具有强氧化性, 浓度较高时会导致
浓度较高时会导致 淬灭。
淬灭。b.
 可将苯酚氧化,但反应速率较慢,加入
可将苯酚氧化,但反应速率较慢,加入 可加快反应。
可加快反应。过程为ⅰ.

ⅱ.
 将苯酚氧化为
将苯酚氧化为 气体
气体①
 氧化苯酚的离子方程式是
氧化苯酚的离子方程式是②将含
 的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。
的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。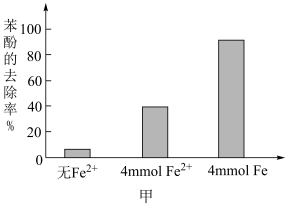
 ,可明显提高苯酚的降解率,主要原因是
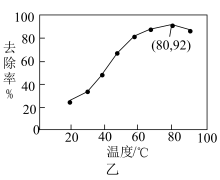
,可明显提高苯酚的降解率,主要原因是(5)工业上利用
 能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含
能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含 的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为
的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为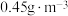 ,
, 达到最大去除率,NO去除的平均反应速率:
达到最大去除率,NO去除的平均反应速率:
 。
。
您最近一年使用:0次
解题方法
5 . 研究氮氧化物 (NOₓ)的还原处理方法是环保领域的主要方向之一。回答下列问题:
 .用H2还原NO的反应为
.用H2还原NO的反应为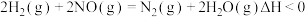

(1)该反应的正反应速率方程可表示为 ,某温度下,测得正反应速率v正与c(NO)或c(H
,某温度下,测得正反应速率v正与c(NO)或c(H )的变化关系如图1所示。
)的变化关系如图1所示。
___________ ,
___________ 。
(2)研究表明上述反应历程分两步基元反应:
i. ;
;
ii.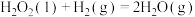 。
。
根据 (1)所给信息判断,H 还原 NO 总反应的速率由反应
还原 NO 总反应的速率由反应___________ (填“ i”或“ii” ) 决定。
(3)将一定量的H 和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H
和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H 的平衡转化率最大的是
的平衡转化率最大的是___________ 。
a. 恒温恒容 b.恒温恒压 c. 恒容绝热
 .脱除汽车尾气中 NO 和CO包括以下两个反应:
.脱除汽车尾气中 NO 和CO包括以下两个反应:
反应i. ;
;
反应ii. 。
。
反应过程中各物质相对能量如图 2 (TS表示过渡态): 的热化学方程式为
的热化学方程式为___________ 。
将恒定组成的NO和CO混合气体通入不同温度的反应器,相同时间内检测物质浓度,结果如图3。___________ (填“高温”或者“低温”)。
(6)实验过程中,高于340℃后N O浓度逐渐减小,试分析发生该变化的原因是
O浓度逐渐减小,试分析发生该变化的原因是___________ 。
(7)450℃时, 该时间段内NO的脱除率=___________ (保留2位有效数字, NO的脱除率
 .用H2还原NO的反应为
.用H2还原NO的反应为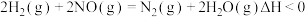

(1)该反应的正反应速率方程可表示为
 ,某温度下,测得正反应速率v正与c(NO)或c(H
,某温度下,测得正反应速率v正与c(NO)或c(H )的变化关系如图1所示。
)的变化关系如图1所示。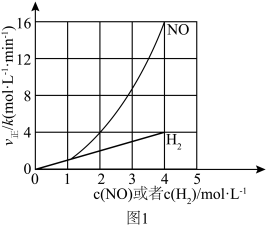


(2)研究表明上述反应历程分两步基元反应:
i.
 ;
;ii.
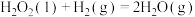 。
。根据 (1)所给信息判断,H
 还原 NO 总反应的速率由反应
还原 NO 总反应的速率由反应(3)将一定量的H
 和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H
和NO置于以下条件下发生反应(起始容器的体积、温度、压强均相同),到达平衡时,H 的平衡转化率最大的是
的平衡转化率最大的是a. 恒温恒容 b.恒温恒压 c. 恒容绝热
 .脱除汽车尾气中 NO 和CO包括以下两个反应:
.脱除汽车尾气中 NO 和CO包括以下两个反应:反应i.
 ;
;反应ii.
 。
。反应过程中各物质相对能量如图 2 (TS表示过渡态):
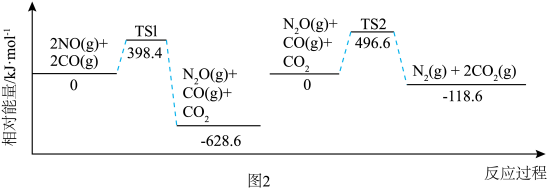
 的热化学方程式为
的热化学方程式为将恒定组成的NO和CO混合气体通入不同温度的反应器,相同时间内检测物质浓度,结果如图3。
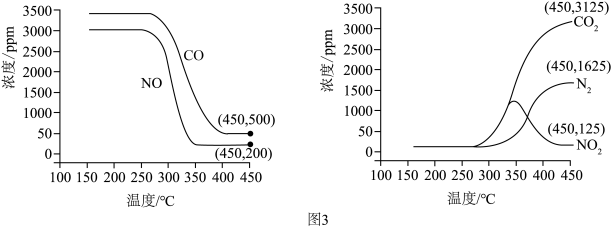
(6)实验过程中,高于340℃后N
 O浓度逐渐减小,试分析发生该变化的原因是
O浓度逐渐减小,试分析发生该变化的原因是(7)450℃时, 该时间段内NO的脱除率=

您最近一年使用:0次
解题方法
6 . 酯化反应可用通式表示为 。在酸性条件下,
。在酸性条件下, ,
, 。假设整个过程中无环酯生成,不出现分层现象。
。假设整个过程中无环酯生成,不出现分层现象。
将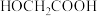 投入反应容器中,发生如下反应:
投入反应容器中,发生如下反应:
二聚: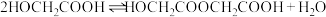
n聚: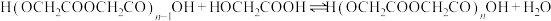
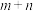 聚:
聚: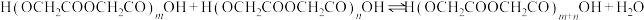 以上反应中每一步的速率常数近似认为相同,记平衡常数
以上反应中每一步的速率常数近似认为相同,记平衡常数 。
。
Ⅰ.反应平衡体系分析
(1)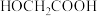 按系统命名法命名为
按系统命名法命名为______ 。
(2)定义反应程度 ,其中
,其中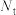 为时刻t时反应体系中-OH或者-COOH的数目,
为时刻t时反应体系中-OH或者-COOH的数目,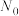 为初始反应体系中-OH或-COOH的数目。若
为初始反应体系中-OH或-COOH的数目。若 ,则
,则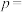
______ 。
(3)最终产物中存在多种聚合度的缩聚产物,平均聚合度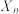 与平衡常数K的关系
与平衡常数K的关系
______ 。
(4)为了使平均聚合度增大,下列方法可行的是______ (填标号)。
A.及时移去 B.升高温度(
B.升高温度( )
)
C.提高 浓度 D.提高
浓度 D.提高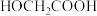 浓度
浓度
E.先将单体预聚合成低聚物,然后将低聚物进一步聚合
Ⅱ.在实际生产过程中,通常会将反应生成的水及时移去。
(5)加入少量 催化与不加入
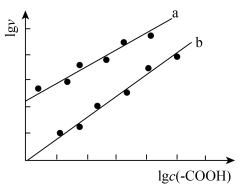
催化与不加入 催化两种情况下,初始阶段酯基的生成速率v与c(-COOH)的理论关系如图[图示为
催化两种情况下,初始阶段酯基的生成速率v与c(-COOH)的理论关系如图[图示为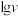 与
与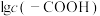 的关系]。
的关系]。
a、b两条曲线的理论斜率之比更接近______ 。 B.
B. C.
C.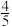 D.
D.
当温度升高时,b线斜率将______ (填“变大”、“变小”或“不变”)。
(6)加入少量 催化时,实验测得反应过程中平均聚合度
催化时,实验测得反应过程中平均聚合度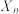 与反应时间t的关系为:
与反应时间t的关系为: ,其中
,其中 为反应初始时
为反应初始时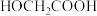 浓度,k为常数。0~t时,酯基生成的平均速率
浓度,k为常数。0~t时,酯基生成的平均速率
______ (用k、 、t表示,忽略移去水对溶液体积的影响)。
、t表示,忽略移去水对溶液体积的影响)。
 。在酸性条件下,
。在酸性条件下, ,
, 。假设整个过程中无环酯生成,不出现分层现象。
。假设整个过程中无环酯生成,不出现分层现象。将
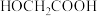 投入反应容器中,发生如下反应:
投入反应容器中,发生如下反应:二聚:
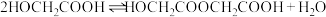
n聚:
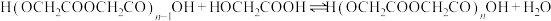
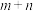 聚:
聚: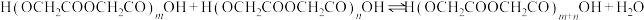 以上反应中每一步的速率常数近似认为相同,记平衡常数
以上反应中每一步的速率常数近似认为相同,记平衡常数 。
。Ⅰ.反应平衡体系分析
(1)
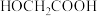 按系统命名法命名为
按系统命名法命名为(2)定义反应程度
 ,其中
,其中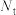 为时刻t时反应体系中-OH或者-COOH的数目,
为时刻t时反应体系中-OH或者-COOH的数目,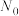 为初始反应体系中-OH或-COOH的数目。若
为初始反应体系中-OH或-COOH的数目。若 ,则
,则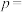
(3)最终产物中存在多种聚合度的缩聚产物,平均聚合度
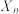 与平衡常数K的关系
与平衡常数K的关系
(4)为了使平均聚合度增大,下列方法可行的是
A.及时移去
 B.升高温度(
B.升高温度( )
)C.提高
 浓度 D.提高
浓度 D.提高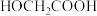 浓度
浓度E.先将单体预聚合成低聚物,然后将低聚物进一步聚合
Ⅱ.在实际生产过程中,通常会将反应生成的水及时移去。
(5)加入少量
 催化与不加入
催化与不加入 催化两种情况下,初始阶段酯基的生成速率v与c(-COOH)的理论关系如图[图示为
催化两种情况下,初始阶段酯基的生成速率v与c(-COOH)的理论关系如图[图示为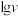 与
与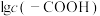 的关系]。
的关系]。a、b两条曲线的理论斜率之比更接近
 B.
B. C.
C.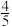 D.
D.
当温度升高时,b线斜率将
(6)加入少量
 催化时,实验测得反应过程中平均聚合度
催化时,实验测得反应过程中平均聚合度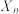 与反应时间t的关系为:
与反应时间t的关系为: ,其中
,其中 为反应初始时
为反应初始时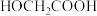 浓度,k为常数。0~t时,酯基生成的平均速率
浓度,k为常数。0~t时,酯基生成的平均速率
 、t表示,忽略移去水对溶液体积的影响)。
、t表示,忽略移去水对溶液体积的影响)。
您最近一年使用:0次
7 . 甲醛释氢对氢能源和含甲醛污水处理有重要意义。
(1) 电催化释氢
电催化释氢
催化电解含较低浓度的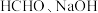 混合溶液,可获得
混合溶液,可获得 与
与 (如图所示)、其中电极b表面覆盖一种
(如图所示)、其中电极b表面覆盖一种 与P形成的化合物(晶胞结构如图所示)作催化剂。
与P形成的化合物(晶胞结构如图所示)作催化剂。 与
与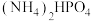 混合物与
混合物与 高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为
高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为___________ 。
②电解时,电极b上同时产生 与
与 的物质的量之比为
的物质的量之比为 、则电极b上的电极反应式为
、则电极b上的电极反应式为___________ ,此种情况下,电解过程中每产生 ,通过阴离子交换膜的
,通过阴离子交换膜的 为
为___________  。
。
(2) 水化释氧
水化释氧
45℃时,碱性条件下 作催化剂可将甲醛转化为
作催化剂可将甲醛转化为 ,反应的机理如图所示:
,反应的机理如图所示: 颗粒负载在
颗粒负载在 表面以防止纳米
表面以防止纳米 团聚,其他条件不变,反应相同时间,
团聚,其他条件不变,反应相同时间, 浓度对氢气产生快慢的影响如图所示:
浓度对氢气产生快慢的影响如图所示: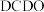 ,得到的氢气产物为
,得到的氢气产物为___________ (填化学式)。
②若 浓度过大,
浓度过大,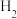 的产生迅速减慢的原因可能是
的产生迅速减慢的原因可能是___________ 。
(3)氢气在化学工业中应用广泛,一定条件下,在某恒容密闭容器中,按投料比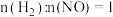 发生如下反应:
发生如下反应: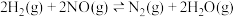
①下列能够说明该反应已达到化学平衡状态的是___________ (填标号)。
A. B.混合气体的密度不再变化
B.混合气体的密度不再变化
C.容器内总压强不再变化 D.混合气体的平均相对分子质量不再变化
②研究表明该反应速率方程式为 ,其中k为速率常数。与温度、活化能有关,若投料比
,其中k为速率常数。与温度、活化能有关,若投料比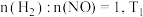 时的初始速率为
时的初始速率为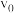 ,当
,当 转化率为
转化率为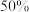 时,反应速率为
时,反应速率为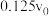 ,由此可知
,由此可知
___________ ;设此时反应的活化能为 ,不同温度
,不同温度 条件下对应的速率常数分别为
条件下对应的速率常数分别为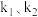 ,存在关系:
,存在关系: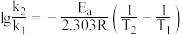 (R为常数),据此推测:升高一定温度,活化能越大,速率常数增大倍数
(R为常数),据此推测:升高一定温度,活化能越大,速率常数增大倍数___________ (填“越大”“越小”或“不变”)。
(1)
 电催化释氢
电催化释氢催化电解含较低浓度的
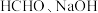 混合溶液,可获得
混合溶液,可获得 与
与 (如图所示)、其中电极b表面覆盖一种
(如图所示)、其中电极b表面覆盖一种 与P形成的化合物(晶胞结构如图所示)作催化剂。
与P形成的化合物(晶胞结构如图所示)作催化剂。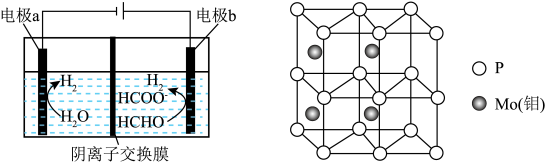
 与
与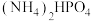 混合物与
混合物与 高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为
高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为②电解时,电极b上同时产生
 与
与 的物质的量之比为
的物质的量之比为 、则电极b上的电极反应式为
、则电极b上的电极反应式为 ,通过阴离子交换膜的
,通过阴离子交换膜的 为
为 。
。(2)
 水化释氧
水化释氧45℃时,碱性条件下
 作催化剂可将甲醛转化为
作催化剂可将甲醛转化为 ,反应的机理如图所示:
,反应的机理如图所示: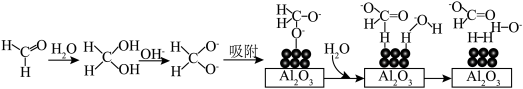
 颗粒负载在
颗粒负载在 表面以防止纳米
表面以防止纳米 团聚,其他条件不变,反应相同时间,
团聚,其他条件不变,反应相同时间, 浓度对氢气产生快慢的影响如图所示:
浓度对氢气产生快慢的影响如图所示: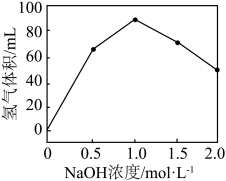
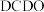 ,得到的氢气产物为
,得到的氢气产物为②若
 浓度过大,
浓度过大,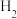 的产生迅速减慢的原因可能是
的产生迅速减慢的原因可能是(3)氢气在化学工业中应用广泛,一定条件下,在某恒容密闭容器中,按投料比
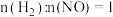 发生如下反应:
发生如下反应: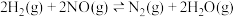
①下列能够说明该反应已达到化学平衡状态的是
A.
 B.混合气体的密度不再变化
B.混合气体的密度不再变化C.容器内总压强不再变化 D.混合气体的平均相对分子质量不再变化
②研究表明该反应速率方程式为
 ,其中k为速率常数。与温度、活化能有关,若投料比
,其中k为速率常数。与温度、活化能有关,若投料比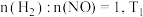 时的初始速率为
时的初始速率为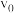 ,当
,当 转化率为
转化率为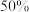 时,反应速率为
时,反应速率为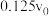 ,由此可知
,由此可知
 ,不同温度
,不同温度 条件下对应的速率常数分别为
条件下对应的速率常数分别为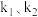 ,存在关系:
,存在关系: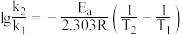 (R为常数),据此推测:升高一定温度,活化能越大,速率常数增大倍数
(R为常数),据此推测:升高一定温度,活化能越大,速率常数增大倍数
您最近一年使用:0次
解题方法
8 . 乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心,乙烯产品占石化产品的75%以上,在国民经济中占有重要的地位。利用乙烷裂解制乙烯的反应为C2H6(g) C2H4(g)+H2(g)△H。
C2H4(g)+H2(g)△H。
(1)298K时,乙烷的裂解反应历程如图1所示,可能发生反应的平衡常数的对数值(lgK)与温度的倒数( )的关系如图2所示。
)的关系如图2所示。_____ (填“反应a”或“反应b”),乙烷裂解制乙烯的△H=_____ 。
②工业上一般选择温度在1000K左右裂解乙烷,可能的原因是_____ 。
(2)在恒温恒容条件下,下列情况表明反应C2H6(g) C2H4(g)+H2(g)达到平衡状态的是_____(填标号)。
C2H4(g)+H2(g)达到平衡状态的是_____(填标号)。
(3)在106kPa下,分别按照反应气组成n(C2H6):n(H2O)为1:1、1:4、1:9投料,C2H6的平衡转化率随反应温度的变化关系如图:_____ (填曲线标号)。
②图中Y点正反应速率和Z点逆反应速率的大小关系为v(Y)_____ (填“>”、“=”或“<”)v(Z)。
③在T4℃,按n(C2H6):n(H2O)=1:9投料时,若达到平衡所需要的时间为20min,则乙烷分压平均变化速率为_____ kPa/min,该反应的平衡常数Kp=_____ kPa(Kp为用分压表示的平衡常数,分压=总压×体积分数)。
 C2H4(g)+H2(g)△H。
C2H4(g)+H2(g)△H。(1)298K时,乙烷的裂解反应历程如图1所示,可能发生反应的平衡常数的对数值(lgK)与温度的倒数(
 )的关系如图2所示。
)的关系如图2所示。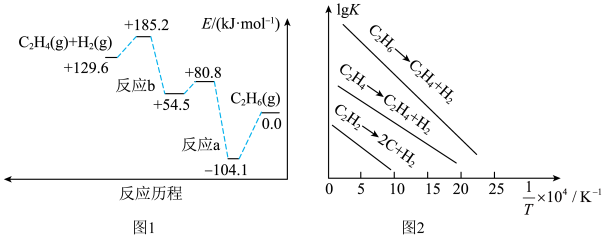
②工业上一般选择温度在1000K左右裂解乙烷,可能的原因是
(2)在恒温恒容条件下,下列情况表明反应C2H6(g)
 C2H4(g)+H2(g)达到平衡状态的是_____(填标号)。
C2H4(g)+H2(g)达到平衡状态的是_____(填标号)。| A.混合气体密度保持不变 | B.气体总压强保持不变 |
| C.气体平均摩尔质量保持不变 | D.产物浓度之比保持不变 |
(3)在106kPa下,分别按照反应气组成n(C2H6):n(H2O)为1:1、1:4、1:9投料,C2H6的平衡转化率随反应温度的变化关系如图:
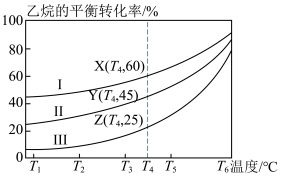
②图中Y点正反应速率和Z点逆反应速率的大小关系为v(Y)
③在T4℃,按n(C2H6):n(H2O)=1:9投料时,若达到平衡所需要的时间为20min,则乙烷分压平均变化速率为
您最近一年使用:0次
解题方法
9 . 以CO、 为原料进行资源化利用,对于环境、能源均具有重要意义。已知存在如下反应:
为原料进行资源化利用,对于环境、能源均具有重要意义。已知存在如下反应:
Ⅰ.

Ⅱ.

Ⅲ.

Ⅳ.

回答下列问题:
(1)已知某反应的平衡常数表达式为 ,则该反应的热化学方程式为
,则该反应的热化学方程式为__________ 。
(2)向一容积为2L的恒容密闭容器中通入1mol 和3mol
和3mol ,一定温度下发生反应Ⅰ.起始总压为pPa,20min时达到化学平衡状态,测得
,一定温度下发生反应Ⅰ.起始总压为pPa,20min时达到化学平衡状态,测得 的物质的量分数为12.5%。
的物质的量分数为12.5%。
①平衡时总压为________ Pa。
②0~20min内,用 表示的平均反应速率
表示的平均反应速率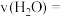
________  ,
, 的平衡浓度
的平衡浓度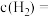
________ 
(3)在一定条件下发生反应Ⅰ、Ⅲ( 过量),若反应Ⅰ中
过量),若反应Ⅰ中 的转化率为90%,Ⅲ中
的转化率为90%,Ⅲ中 的转化率为40%,则
的转化率为40%,则 的产率为
的产率为________ .
(4)工业上,以一定比例混合的 与
与 的混合气体以一定流速分别通过填充有催化剂a、催化剂b的反应器,发生反应Ⅰ.
的混合气体以一定流速分别通过填充有催化剂a、催化剂b的反应器,发生反应Ⅰ. 转化率与温度的关系如图1所示.在催化剂b作用下,温度高于
转化率与温度的关系如图1所示.在催化剂b作用下,温度高于 时,
时, 转化率下降的原因可能是
转化率下降的原因可能是__________ 。 分别为1mol、2mol时,发生反应Ⅳ,平衡后混合物中
分别为1mol、2mol时,发生反应Ⅳ,平衡后混合物中 的体积分数(
的体积分数( )如图2所示。
)如图2所示。 、
、 和
和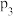 由大到小的顺序是
由大到小的顺序是________ 。
②若在250℃、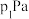 的条件下,反应达到平衡,则该反应的平衡常数
的条件下,反应达到平衡,则该反应的平衡常数
________ 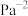 (分压
(分压 总压
总压 物质的量分数)。
物质的量分数)。
 为原料进行资源化利用,对于环境、能源均具有重要意义。已知存在如下反应:
为原料进行资源化利用,对于环境、能源均具有重要意义。已知存在如下反应:Ⅰ.


Ⅱ.


Ⅲ.


Ⅳ.


回答下列问题:
(1)已知某反应的平衡常数表达式为
 ,则该反应的热化学方程式为
,则该反应的热化学方程式为(2)向一容积为2L的恒容密闭容器中通入1mol
 和3mol
和3mol ,一定温度下发生反应Ⅰ.起始总压为pPa,20min时达到化学平衡状态,测得
,一定温度下发生反应Ⅰ.起始总压为pPa,20min时达到化学平衡状态,测得 的物质的量分数为12.5%。
的物质的量分数为12.5%。①平衡时总压为
②0~20min内,用
 表示的平均反应速率
表示的平均反应速率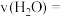
 ,
, 的平衡浓度
的平衡浓度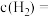

(3)在一定条件下发生反应Ⅰ、Ⅲ(
 过量),若反应Ⅰ中
过量),若反应Ⅰ中 的转化率为90%,Ⅲ中
的转化率为90%,Ⅲ中 的转化率为40%,则
的转化率为40%,则 的产率为
的产率为(4)工业上,以一定比例混合的
 与
与 的混合气体以一定流速分别通过填充有催化剂a、催化剂b的反应器,发生反应Ⅰ.
的混合气体以一定流速分别通过填充有催化剂a、催化剂b的反应器,发生反应Ⅰ. 转化率与温度的关系如图1所示.在催化剂b作用下,温度高于
转化率与温度的关系如图1所示.在催化剂b作用下,温度高于 时,
时, 转化率下降的原因可能是
转化率下降的原因可能是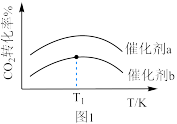
 分别为1mol、2mol时,发生反应Ⅳ,平衡后混合物中
分别为1mol、2mol时,发生反应Ⅳ,平衡后混合物中 的体积分数(
的体积分数( )如图2所示。
)如图2所示。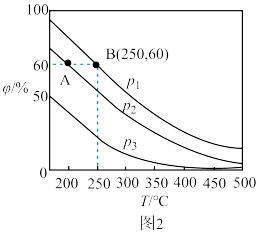
 、
、 和
和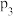 由大到小的顺序是
由大到小的顺序是②若在250℃、
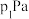 的条件下,反应达到平衡,则该反应的平衡常数
的条件下,反应达到平衡,则该反应的平衡常数
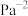 (分压
(分压 总压
总压 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
2024-05-21更新
|
68次组卷
|
2卷引用:江西省部分重点中学2024届高三下学期第二次联考化学试题
10 . 我国提出“CO2排放力争于2023年前达到峰值,努力争取2060年前实现碳中和”。研发CO2的利用技术,降低空气中CO2的含量是实现该目标的重要途径。
(1)下面是用H2捕捉CO2时发生的两个反应:
I.CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H1
CH4(g)+2H2O(g) ∆H1
II.CO2(g)+H2(g) CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2
①反应I、II的lnK随1/T的变化如图所示,则ΔH2___________ 0(填“>”“<”或“=”)0;有利于反应I自发进行的温度是___________ (填“高温”或“低温”)。___________ ,而速率仍然增大的可能原因是___________ ___________ ,反应II的平衡常数Kp为___________ (保留两位有效数字)。[已知:CH4的选择性=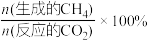 ]
]
(2)利用化学链将高炉废气中的CO2转化为CO的示意图如下。___________ ,该化学链的总反应是___________ 。
(1)下面是用H2捕捉CO2时发生的两个反应:
I.CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H1
CH4(g)+2H2O(g) ∆H1II.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2①反应I、II的lnK随1/T的变化如图所示,则ΔH2
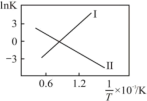
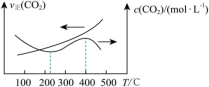
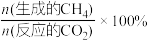 ]
](2)利用化学链将高炉废气中的CO2转化为CO的示意图如下。

您最近一年使用:0次



