名校
解题方法
1 . 中医药根植于中华传统文化。下列说法不正确 的是
| A.屠呦呦团队用乙醚从青蒿中提取了青蒿素,采用了萃取的方法 |
| B.中药甘草、金银花、石膏、明矾等的主要化学成分都是有机物 |
| C.汤药存放于冰箱中,可以减小其腐败变质的速率 |
| D.煎制草药不宜使用铁质容器,可能因为草药的有些成分能与铁发生反应影响药效 |
您最近一年使用:0次
2023-03-31更新
|
935次组卷
|
6卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题
宁夏平罗中学2022-2023学年高二下学期期中考试化学试题北京市西城区2023届一模考试化学试题(已下线)专题01 化学与STSE(已下线)专题05 元素及其化合物北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题广西柳州高级中学2023-2024学年高三上学期8月开学考试化学试题
名校
解题方法
2 . 为保护环境,充分利用钴资源,一种以废旧钴酸锂电池材料(正极材料主要含有LiCoO2、铝箔及金属钢壳)回收钴酸锂的工艺流程如下:
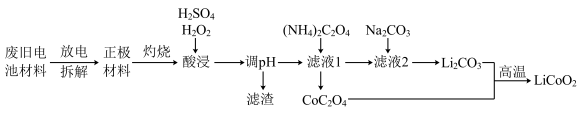
已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
请回答下列问题:
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理。放电方式为电化学放电,可以将废旧电池浸泡在_________ (填标号)中进行放电。粉碎的目的是_________ 。
A. Na2SO4溶液
B.98%的H2SO4溶液
C.酒精
(2)“酸浸”过程中,除加入H2SO4,还要加入H2O2。
①H2O2的作用是_________ (填标号)。
A.做氧化剂
B.做还原剂
C.既做氧化剂又做还原剂
②H2O2促进了LiCoO2在H2SO4中转化为CoSO4,该反应的离子方程式为_________ 。
③相同条件下,“酸浸”时钴的浸出率随温度变化如右图所示,此时温度控制在80°C左右的原因为_________ 。

(3)“调pH”时,溶液应控制的pH范围为_________ ,选用的最佳试剂是_________ (填标号)。
A. H2SO4 B. CoCO3 C.石灰乳 D. NaOH
(4)高温时,CoC2O4和Li2CO3生成LiCoO2的同时放出CO2。此反应的化学方程式为_________ 。

已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
| 离子 | Co3+ | Fe3+ | Co2+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 0.3 | 2.7 | 7.2 | 7.6 | 3.6 |
| 完全沉淀的pH | 1.1 | 3.2 | 9.2 | 9.6 | 5.2 |
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理。放电方式为电化学放电,可以将废旧电池浸泡在
A. Na2SO4溶液
B.98%的H2SO4溶液
C.酒精
(2)“酸浸”过程中,除加入H2SO4,还要加入H2O2。
①H2O2的作用是
A.做氧化剂
B.做还原剂
C.既做氧化剂又做还原剂
②H2O2促进了LiCoO2在H2SO4中转化为CoSO4,该反应的离子方程式为
③相同条件下,“酸浸”时钴的浸出率随温度变化如右图所示,此时温度控制在80°C左右的原因为

(3)“调pH”时,溶液应控制的pH范围为
A. H2SO4 B. CoCO3 C.石灰乳 D. NaOH
(4)高温时,CoC2O4和Li2CO3生成LiCoO2的同时放出CO2。此反应的化学方程式为
您最近一年使用:0次
2023-03-29更新
|
334次组卷
|
2卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题(重点班)
名校
解题方法
3 . 化学与生产、生活和社会发展密切相关,下列叙述不正确的是
| A.电热水器用镁棒防止金属内胆腐蚀,原理是牺牲阳极法 |
| B.西周的“酒曲”酿酒工艺,利用了催化剂使平衡正向移动的原理 |
| C.免洗洗手液的有效成分之一活性胶质银离子能使病毒蛋白质变性 |
| D.针对新冠疫情,可用医用酒精、次氯酸钠溶液等对场所杀菌消毒 |
您最近一年使用:0次
2023-03-02更新
|
252次组卷
|
5卷引用:宁夏石嘴山市平罗中学2022-2023学年高二下学期3月月考化学试题
名校
解题方法
4 . 已知化合物A与 在一定条件下反应生成化合物B与
在一定条件下反应生成化合物B与 ,其反应历程如图所示,其中
,其反应历程如图所示,其中 表示过渡态,I表示中间体。下列说法正确的是
表示过渡态,I表示中间体。下列说法正确的是

 在一定条件下反应生成化合物B与
在一定条件下反应生成化合物B与 ,其反应历程如图所示,其中
,其反应历程如图所示,其中 表示过渡态,I表示中间体。下列说法正确的是
表示过渡态,I表示中间体。下列说法正确的是
| A.两种中间体物质中较稳定的是中间体I2 |
B.该历程中的最大能垒(活化能)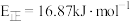 |
| C.有可能找到高效的催化剂将I1→I2的过程转变为放热反应 |
D.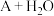 转化为Il是各步骤反应中较快的步骤 转化为Il是各步骤反应中较快的步骤 |
您最近一年使用:0次
2023-02-25更新
|
390次组卷
|
2卷引用:宁夏石嘴山市平罗中学2022-2023学年高二下学期3月月考化学试题
2022高三·全国·专题练习
真题
名校
5 . 某兴趣小组设计实验探究 ,催化空气氧化
,催化空气氧化 的效率。回答下列问题:
的效率。回答下列问题:
步骤Ⅰ 制备
在通风橱中用下图装置制备 (加热及夹持装置省略),反应方程式:
(加热及夹持装置省略),反应方程式: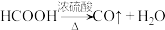

(1)装置A中盛放甲酸的仪器的名称是_______ 。
(2)从B、C、D中选择合适的装置收集 ,正确的接口连接顺序为a→_______→_______→_______→_______→h(每空填一个接口标号)。
,正确的接口连接顺序为a→_______→_______→_______→_______→h(每空填一个接口标号)。______
步骤Ⅱ 检验
将 通入新制银氨溶液中,有黑色沉淀生成。
通入新制银氨溶液中,有黑色沉淀生成。
(3)该反应的化学方程式为_______ 。
步骤Ⅲ 探究 催化空气氧化
催化空气氧化 的效率
的效率
将一定量 与空气混合,得到
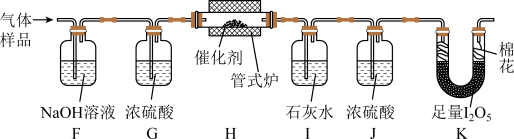
与空气混合,得到 体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),调节管式炉温度至
体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),调节管式炉温度至 ,按一定流速通入气体样品。(已知:
,按一定流速通入气体样品。(已知: 是白色固体,易吸水潮解:
是白色固体,易吸水潮解: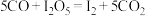 )
)
(4)通入 (已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了
(已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了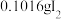 。
。
①能证明 被空气氧化的现象是
被空气氧化的现象是_______ ;
② 被催化氧化的百分率为
被催化氧化的百分率为_______ ;
③若未通入氮气,②的结果将_______ (填“偏大”“偏小”或“无影响”)。
(5)探究气体与催化剂接触时长对催化氧化效率的影响时,采用_______ 方法可以缩短接触时长。
(6)步骤Ⅲ装置存在的不足之处是_______ 。
 ,催化空气氧化
,催化空气氧化 的效率。回答下列问题:
的效率。回答下列问题:步骤Ⅰ 制备

在通风橱中用下图装置制备
 (加热及夹持装置省略),反应方程式:
(加热及夹持装置省略),反应方程式: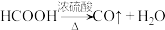

(1)装置A中盛放甲酸的仪器的名称是
(2)从B、C、D中选择合适的装置收集
 ,正确的接口连接顺序为a→_______→_______→_______→_______→h(每空填一个接口标号)。
,正确的接口连接顺序为a→_______→_______→_______→_______→h(每空填一个接口标号)。步骤Ⅱ 检验

将
 通入新制银氨溶液中,有黑色沉淀生成。
通入新制银氨溶液中,有黑色沉淀生成。(3)该反应的化学方程式为
步骤Ⅲ 探究
 催化空气氧化
催化空气氧化 的效率
的效率将一定量
 与空气混合,得到
与空气混合,得到 体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),调节管式炉温度至
体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),调节管式炉温度至 ,按一定流速通入气体样品。(已知:
,按一定流速通入气体样品。(已知: 是白色固体,易吸水潮解:
是白色固体,易吸水潮解: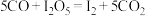 )
)
(4)通入
 (已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了
(已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了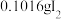 。
。①能证明
 被空气氧化的现象是
被空气氧化的现象是②
 被催化氧化的百分率为
被催化氧化的百分率为③若未通入氮气,②的结果将
(5)探究气体与催化剂接触时长对催化氧化效率的影响时,采用
(6)步骤Ⅲ装置存在的不足之处是
您最近一年使用:0次
2023-02-20更新
|
6816次组卷
|
15卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高三上学期期末考试理综试题-高中化学
宁夏回族自治区石嘴山市第三中学2023-2024学年高三上学期期末考试理综试题-高中化学(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编2022年福建省高考真题化学试题(已下线)2022年福建省高考真题变式题(实验探究题)(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试变式题(实验探究题)(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试举一反三(实验探究题)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题突破卷13 化学实验基础(二)-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省新泰市第一中学(弘文部)2023-2024学年高三上学期第二次月考化学试题福建省莆田第一中学2023-2024学年高一上学期期末考试化学试题天津市耀华中学2023-2024学年高三下学期开学验收考化学试卷
10-11高二上·江苏南通·期中
名校
解题方法
6 . 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,两位同学分别设计了如图甲、乙所示的实验。下列叙述不正确的是
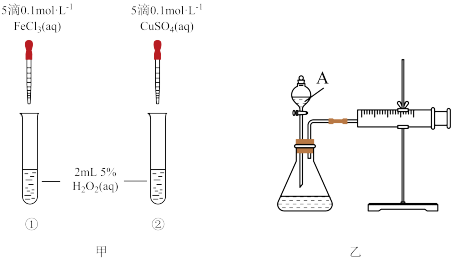

| A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 |
| B.若图甲中所示实验反应速率为①>②,则说明Fe3+一定比Cu2+对H2O2分解的催化效果好 |
| C.用图乙所示装置测定反应速率,可测定产生的一定体积气体所需要的时间 |
| D.为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
2022-11-02更新
|
163次组卷
|
85卷引用:宁夏石嘴山市平罗中学2021-2022学年高一下学期期中考试化学试题
宁夏石嘴山市平罗中学2021-2022学年高一下学期期中考试化学试题(已下线)2010年江苏省启东中学高二上学期期中考试化学卷(已下线)2010-2011学年江苏省启东中学高二上学期期中考试化学试题(理)2016届黑龙江省大庆实验中学高三上学期12月月考化学试卷2015-2016学年辽宁鞍山一中高一下期中化学试卷2015-2016学年浙江宁波效实中学高二下期中化学试卷2015-2016学年河北武邑中学高一下5.15周考化学试卷2015-2016学年湖南省娄底市双峰县高一下期中化学试卷2016-2017学年山东省烟台第二中学高二下学期开学考试化学试卷四川省南充高级中学2016-2017学年高一下学期期末考试化学试题甘肃省兰州第一中学2017-2018学年高二上学期第一次月考(9月)化学试题安徽省淮北市第一中学2017-2018学年高二上学期第四次月考(12月)化学试题四川省三台中学实验学校2017-2018学年高一下学期期末仿真模拟(二)化学试题安徽省定远重点中学2018-2019学年高二上学期第三次月考化学试题(已下线)2019年3月31日 《每日一题》 必修2 每周一测黑龙江省大庆中学2018-2019学年高一下学期期末考试化学试题四川省棠湖中学2018-2019学年高一下学期期末考试化学试题安徽省滁州市定远县育才学校2019-2020学年高二上学期入学考试化学试题贵州省贵阳市第二中学高一下学期期末考试化学试题辽宁省六校协作体2019-2020学年高二上学期10月月考化学试题广东省广州市第16中学2019-2020学年高二上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——气体制取流程的规范操作(提升练)2020届高三化学实验复习——气密性的检查【选择突破】四川省棠湖中学2019-2020学年高一下学期第二次月考化学试题第二章 化学反应与能量 第三节 化学反应的速率和限度安徽省阜阳市2019-2020学年高一下学期开学考化学试题吉林省辽源市田家炳高级中学2019-2020学年高一下学期期中考试化学试题安徽省定远县育才学校2019-2020学年高一6月月考化学试题(已下线)第15讲 化学反应速率-2021年高考化学一轮复习名师精讲练(已下线)2.1.2 影响化学反应速率的因素(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)(已下线)2.1.2 影响化学反应速率的因素(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)安徽省定远县育才学校2020-2021学年高二上学期开学考试化学试题鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第3节 化学反应的速率 课时2 影响化学反应速率的因素鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第3节 化学反应的速率高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第一节 化学反应速率 课时2 影响化学反应速率的因素山东省潍坊市临朐县实验中学2020-2021学年高二9月月考化学试题(已下线)易错11 影响化学反应速率的因素-备战2021年高考化学一轮复习易错题湖北省随州市曾都一中2020-2021学年高二上学期9月月考化学试题必修第二册RJ高效学习手册-第六章山西省长治市第二中学校2020-2021学年高二上学期第一次月考化学试题黑龙江省齐齐哈尔市第八中学2020-2021学年高二上学期期中考试化学试题黑龙江省哈尔滨市第六中学2020-2021学年高二10月月考化学试题四川省成都新津为明学校2020-2021学年高二上学期期中测试化学试题黑龙江省大庆中学2020-2021学年高二上学期期中考试化学试题安徽省桐城中学2020-2021学年高一上学期12月月考化学试题山西省吕梁市2020-2021学年高二上学期期末考试化学试题河北省张家口市宣化一中2020-2021学年高一下学期期初考试化学试题浙江省丽水市高中发展共同体2020-2021学年高二下学期期中联合测试化学试题福建省三明市三地三校2020-2021学年高一下学期期中联考化学试题2018年广东和广西高中学生化学竞赛试题选择性必修1 专题2 第一单元 课时2 影响化学反应速率的因素河北省任丘一中2021-2022学年高二上学期阶段考试(一)化学试题(已下线)专题21 化学反应速率(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练甘肃省庆阳市第六中学2021-2022学年高二上学期第一次月考化学(理)试题山西省长治市第二中学校2021-2022学年高二上学期第一次月考化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期第四次教学质量检测化学试题北京市石景山区第九中学2021-2022学年高二上学期期中考试化学试题(已下线)专题13 装置气密性的检查方法-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)湖北省武汉市部分普通高中联合体2021-2022学年高一下学期期中联考化学试题河南省南阳市第一中学校2021-2022学年高一下学期第三次月考化学试题四川省泸州市泸县第四中学2021-2022学年高一下学期期中考试化学试题湖南省长沙市实验中学2021-2022学年高一下学期期中考试化学试题甘肃省天水市秦安县第一中学2021-2022学年高一下学期期中考试化学试题 吉林省长春市东北师范大学附属中学2021-2022学年高一下学期期中考试化学试题广东省珠海市三校2021-2022学年高一下学期期中联考化学试题河南省实验中学2021-2022学年高一下学期期期中考试化学试题辽宁省营口市第二高级中学2021-2022学年高一6月月考化学试题宁夏永宁县永宁中学2021-2022学年高二上学期期中考试化学试题新疆乌鲁木齐市林肯外国语培训学校、第十二中学2021-2022学年高一下学期期中考试化学试题(已下线)2.3.3 化学反应速率综合分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)湖北省襄阳市第五中学2022-2023学年高二上学期9月化学试题福建省福州市第三中学2022-2023学年高一上学期10月月考化学试题黑龙江省佳木斯市第十二中学(佳木斯市建三江第一中学)2021-2022学年高一下学期期中考试化学试题广东省化州市第一中学2020-2021学年高二上学期10月月考化学试题甘肃省礼县第一中学2020-2021学年高一上学期期中测试化学试题福建省南平市浦城第一中学2022-2023学年高一下学期期中考试化学试题福建省南平市浦城县2022-2023学年高一下学期期中考试化学试题浙江省温州市环大罗山联盟2022-2023学年高二上学期11月期中考试化学试题作业(十四) 外界条件对化学反应速率的影响四川省南充高级中学2021-2022学年高一下学期第二次月考化学试题浙江省温州十校联合体2023-2024学年高二上学期期中考试化学试题江苏省苏州市吴江市高级中学2023-2024学年高二上学期10月月考化学试题湖北省武汉市新洲区第一中学2024届高二上学期期末联考化学试题湖北省武汉市新洲区第一中学2024届高二上学期11月阶段测试化学试题新疆实验中学2023-2024学年高二上学期期中考试化学试题
2022高二·上海·专题练习
名校
7 . 图1实验装置用于测定锌与稀硫酸反应的速率。 _______ 。
(2)分别取2 g颗粒大小相同的锌粒分别与体积均为40 mL的1 mol·L-1硫酸、4 mol·L-1硫酸反应,收集25 mL H2时所需时间后者比前者_______ 。 填“长”或“短”
填“长”或“短”
(3)某化学兴趣小组对教材实验装置进行图2所示改进。检查装置气密性后进行的实验操作有:
b. 在锥形瓶中加入40 mL的1 mol·L-1硫酸;
c. 塞好橡胶塞,_______ 时立即用秒表计时;
d. 注射器内每增加5mL气体时读取一次秒表。
(4)实验观察到锌与稀硫酸反应初期速率逐渐加快,其原因是_______ ,反应进行一定时间后速率逐渐减慢,原因是_______ 。
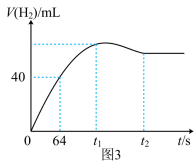
(5)测得产生H2的体积与反应时间的关系曲线如图3所示,t1~t2时间段氢气体积略有减小的原因是_______ ;在64 s内用H+浓度表示的平均反应速率v(H+) = _______ (此时,溶液体积仍为40 mL,气体摩尔体积为25 L·mol-1)。

(2)分别取2 g颗粒大小相同的锌粒分别与体积均为40 mL的1 mol·L-1硫酸、4 mol·L-1硫酸反应,收集25 mL H2时所需时间后者比前者
 填“长”或“短”
填“长”或“短”
(3)某化学兴趣小组对教材实验装置进行图2所示改进。检查装置气密性后进行的实验操作有:
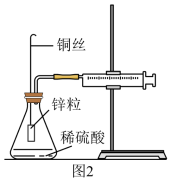
b. 在锥形瓶中加入40 mL的1 mol·L-1硫酸;
c. 塞好橡胶塞,
d. 注射器内每增加5mL气体时读取一次秒表。
(4)实验观察到锌与稀硫酸反应初期速率逐渐加快,其原因是
(5)测得产生H2的体积与反应时间的关系曲线如图3所示,t1~t2时间段氢气体积略有减小的原因是
您最近一年使用:0次
2022-09-28更新
|
276次组卷
|
4卷引用:宁夏石嘴山市平罗中学2023-2024学年高二下学期4月月考化学试题
宁夏石嘴山市平罗中学2023-2024学年高二下学期4月月考化学试题(已下线)2.3.1 化学反应速率的概念和测定-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)湖南省邵阳市武冈市2022-2023学年高二上学期期中考试化学试题(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)
名校
解题方法
8 . 能够加快少量铁粉与200mL0.5mol/L 溶液反应速率且不改变生成氢气的量的组合是
溶液反应速率且不改变生成氢气的量的组合是
①用同质量的铁块代替铁粉;②加入硫酸钠固体;③加入硝酸钠固体;④加入醋酸钠固体;⑤加入少量锌粒;⑥通入HCl气体;⑦加热;⑧再加入100mL0.5mol/L 溶液
溶液
 溶液反应速率且不改变生成氢气的量的组合是
溶液反应速率且不改变生成氢气的量的组合是①用同质量的铁块代替铁粉;②加入硫酸钠固体;③加入硝酸钠固体;④加入醋酸钠固体;⑤加入少量锌粒;⑥通入HCl气体;⑦加热;⑧再加入100mL0.5mol/L
 溶液
溶液| A.①②⑤⑥⑦⑧ | B.②③⑤⑦ | C.⑤⑥⑦ | D.⑥⑦ |
您最近一年使用:0次
2022-08-25更新
|
543次组卷
|
2卷引用:宁夏石嘴山第三中学2021-2022学年高一下学期期末考试化学试题
名校
解题方法
9 . 下列措施对增大反应速率明显有效的是
| A.Na与水反应时增大水的用量 |
| B.在K2SO4与BaCl2两溶液反应时,增大压强 |
| C.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| D.将铝片改为铝粉,做铝与氧气反应的实验 |
您最近一年使用:0次
23-24高一上·全国·假期作业
名校
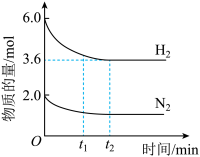
10 . 在2.0 L恒温恒容密闭容器中充入2.0 mol N2和6.0 mol H2,加入催化剂发生反应:N2(g)+3H2(g) 2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
 2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
| A.t1 min时,N2的生成速率等于N2的消耗速率 |
| B.使用催化剂可以缩短到达平衡时所需的时间 |
C.0~t2 min内,v(NH3)= mol·L−1·min−1 mol·L−1·min−1 |
| D.反应中通入足量的N2,可使H2完全转化为NH3 |
您最近一年使用:0次
2022-08-25更新
|
307次组卷
|
4卷引用:宁夏石嘴山第三中学2021-2022学年高一下学期期末考试化学试题
宁夏石嘴山第三中学2021-2022学年高一下学期期末考试化学试题(已下线)第10讲 化学反应限度(讲义)-【寒假自学课】2023年高一化学寒假精品课(人教版2019必修第二册)江苏省盐城市田家炳中学2021-2022学年高一下学期期中考试化学试题江西省萍乡市2022-2023学年高一下学期7月期末考试化学试题



