1 . 已知反应A2(g)+2B2(g) 2AB2(g)△H <0,升高温度,下列说法正确的
2AB2(g)△H <0,升高温度,下列说法正确的
 2AB2(g)△H <0,升高温度,下列说法正确的
2AB2(g)△H <0,升高温度,下列说法正确的| A.正向反应速率增大,逆向反应速率减小 |
| B.正向反应速率减小,逆向反应速率增大 |
| C.达到平衡后,升高温度有利于该反应平衡正向移动 |
| D.达到平衡后,升高温度有利于该反应平衡逆向移动 |
您最近一年使用:0次
2020-12-10更新
|
88次组卷
|
3卷引用:宁夏回族自治区石嘴山市平罗县平罗中学2020-2021学年高二上学期期中考试化学试题
名校
2 . 增大压强对下列反应的速率无影响的是
| A.CO2(g) + Ca(OH)2(aq)= CaCO3(s)↓+H2O(l) |
B.H2 (g) +I2(g) 2HI(g) 2HI(g) |
| C.NaCl(aq) +AgNO3(aq)=AgCl(s)↓+NaNO3(aq) |
D.N2(g)+3H2(g) 2NH3(g) 2NH3(g) |
您最近一年使用:0次
名校
3 . (1)向一体积不变的密闭容器中加入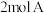 、
、 和一定量的B三种气体。一定条件下发生反应
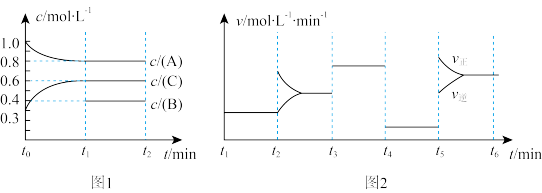
和一定量的B三种气体。一定条件下发生反应 ,各物质浓度随时间变化如图1所示。图2为
,各物质浓度随时间变化如图1所示。图2为 时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知
时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知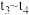 阶段为使用催化剂;图1中
阶段为使用催化剂;图1中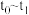 阶段
阶段 未画出。
未画出。
①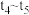 ,
, 阶段改变的条件为
阶段改变的条件为_________ ,________ B的起始物质的量为________ 。
②为使该反应的反应速率减慢且平衡向逆反应方向移动可以采取的措施有_________ 。
(2)某小组利用 溶液和硫酸酸化的
溶液和硫酸酸化的 溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性
溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性 溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知: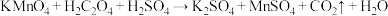 (未配平)。
(未配平)。
①表中
___________ mL,
___________ mL
②探究温度对化学反应速率影响的实验编号是________ (填编号,下同),可探究反应物浓度对反应速率影响的实验编号是____________ 。
③实验①测得 溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率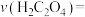
_______________ .
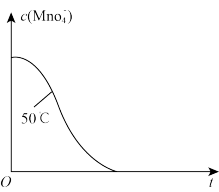
④已知50℃时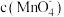 与反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25℃时
与反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25℃时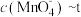 的变化曲线示意图。
的变化曲线示意图。_________
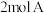 、
、 和一定量的B三种气体。一定条件下发生反应
和一定量的B三种气体。一定条件下发生反应 ,各物质浓度随时间变化如图1所示。图2为
,各物质浓度随时间变化如图1所示。图2为 时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知
时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知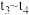 阶段为使用催化剂;图1中
阶段为使用催化剂;图1中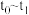 阶段
阶段 未画出。
未画出。①
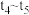 ,
,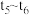 阶段改变的条件为
阶段改变的条件为②为使该反应的反应速率减慢且平衡向逆反应方向移动可以采取的措施有

(2)某小组利用
 溶液和硫酸酸化的
溶液和硫酸酸化的 溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性
溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性 溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知: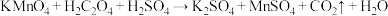 (未配平)。
(未配平)。| 实验编号 | 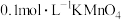 酸性溶液的体积 酸性溶液的体积 | 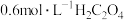 溶液的体积 溶液的体积 |  的体积 的体积 | 实验温度/℃ | 溶液褪色所需时间 |
| ① | 10 |  | 35 | 25 | |
| ② | 10 | 10 | 30 | 25 | |
| ③ | 10 | 10 |  | 50 |


②探究温度对化学反应速率影响的实验编号是
③实验①测得
 溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率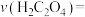
④已知50℃时
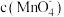 与反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25℃时
与反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25℃时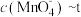 的变化曲线示意图。
的变化曲线示意图。
您最近一年使用:0次
名校
4 .  反应过程中的能量变化如图所示,图中
反应过程中的能量变化如图所示,图中 表示无催化剂时正反应的活化能,
表示无催化剂时正反应的活化能, 表示无催化剂时逆反应的活化能,下列有关叙述不正确的是
表示无催化剂时逆反应的活化能,下列有关叙述不正确的是

 反应过程中的能量变化如图所示,图中
反应过程中的能量变化如图所示,图中 表示无催化剂时正反应的活化能,
表示无催化剂时正反应的活化能, 表示无催化剂时逆反应的活化能,下列有关叙述不正确的是
表示无催化剂时逆反应的活化能,下列有关叙述不正确的是
| A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数 |
| B.有气体参加的化学反应,若增大压强即缩小反应容器的体积,可增加活化分子的百分数,从而使反应速率增大 |
| C.该反应中,反应物的总键能小于生成物的总键能 |
D.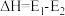 ,使用催化剂改变活化能,但不改变反应热 ,使用催化剂改变活化能,但不改变反应热 |
您最近一年使用:0次
名校
5 . 反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加C的量 ②保持体积不变,充入N2使体系压强增大
③将容器的体积缩小一半 ④保持压强不变,充入N2使容器体积变大
 CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是①增加C的量 ②保持体积不变,充入N2使体系压强增大
③将容器的体积缩小一半 ④保持压强不变,充入N2使容器体积变大
| A.①④ | B.②③ | C.①② | D.③④ |
您最近一年使用:0次
2020-11-11更新
|
504次组卷
|
16卷引用:宁夏石嘴山市第三中学2019-2020学年高二6月月考化学试题
宁夏石嘴山市第三中学2019-2020学年高二6月月考化学试题青海省西宁市第四高级中学2017-2018学年高二上学期第二次月考化学试题(已下线)2018年9月13日 《每日一题》人教选修4-影响化学平衡移动的因素(一)【全国百强校】黑龙江省大庆实验中学2018-2019学年高二上学期10月月考化学试题河南省安阳市第三十六中学2018-2019学年高二上学期第一次月考化学试题内蒙古翁牛特旗乌丹第二中学2019-2020学年高二上学期期中考试化学试题(已下线)2.3.2 压强变化对化学平衡的影响(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)广东省惠州市惠东中学2020-2021学年高二上学期期中考试化学试题辽宁省沈阳市郊联体2020-2021学年高二上学期期中考试化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时2 反应条件对化学平衡的影响内蒙古呼伦贝尔市阿荣旗第一中学2020-2021学年高二上学期月考化学试题甘肃省张掖市第二中学2021-2022学年高二上学期10月月考(B班)化学试题甘肃省张掖市第二中学2021-2022学年高二上学期10月月考(A班)化学试题辽宁省辽河油田第一高级中学2021-2022学年高二上学期月考化学试题(A部)第二节 化学平衡 第3课时 影响化学平衡的因素(已下线)化学反应速率与化学平衡——课时5影响化学平衡的因素
名校
6 . 工业上生产环氧乙烷的反应为:2 CH2=CH2 (g) + O2 (g) = 2 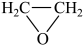 (g) ∆H = -106 kJ • mol−1,其反应机理如下:
(g) ∆H = -106 kJ • mol−1,其反应机理如下:
①Ag + O2=AgO2慢
②CH2=CH2+ AgO2 = + AgO 快
+ AgO 快
③CH2= CH2 + 6AgO =2CO2 + 2H2O + 6Ag 快
下列有关该反应的说法正确的是
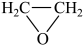 (g) ∆H = -106 kJ • mol−1,其反应机理如下:
(g) ∆H = -106 kJ • mol−1,其反应机理如下:①Ag + O2=AgO2慢
②CH2=CH2+ AgO2 =
 + AgO 快
+ AgO 快③CH2= CH2 + 6AgO =2CO2 + 2H2O + 6Ag 快
下列有关该反应的说法正确的是
| A.反应的活化能等于 106 kJ·mol−1 |
| B.工业上生产环氧乙烷的反应是一个焓减熵增的反应,所以能自发进行 |
| C.增大乙烯浓度能显著提高环氧乙烷的生成速率 |
| D.理论上 0.7 mol 乙烯参与反应最多可得到 0.6 mol 环氧乙烷 |
您最近一年使用:0次
2020-10-31更新
|
260次组卷
|
3卷引用:宁夏石嘴山市第三中学2022-2023学年高二下学期期末理科化学试题
名校
解题方法
7 . 一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成H2的总量,可采取的措施是( )
| A.加入少量稀NaOH溶液 | B.加入少量CH3COONa固体 |
| C.加入少量NH4HSO4固体 | D.加入少量CuSO4溶液 |
您最近一年使用:0次
2020-09-27更新
|
102次组卷
|
2卷引用:宁夏石嘴山市第三中学2020-2021学年高二上学期第一次月考化学试题
10-11高一下·内蒙古赤峰·期中
名校
解题方法
8 . 反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的容器中进行反应,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的容器中进行反应,下列条件的改变对其反应速率几乎无影响的是( )
 CO(g)+H2(g)在一可变容积的容器中进行反应,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的容器中进行反应,下列条件的改变对其反应速率几乎无影响的是( )| A.将容器的体积缩小一半 | B.增加C的量 |
| C.保持体积不变,升高温度 | D.压强不变,充入N2使体积增大 |
您最近一年使用:0次
2020-07-17更新
|
121次组卷
|
9卷引用:宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】
宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】(已下线)2010-2011学年内蒙古赤峰二中高一下学期期中考试化学试卷(已下线)2010—2011学年福建省三明二中高一下期期中考试化学试卷(已下线)2010-2011学年黑龙江省哈尔滨市第六中学高一下学期期末考试化学试卷2016-2017学年陕西省西安一中高二上10月月考化学卷安徽省蚌埠市第二中学2017-2018学年高二上学期开学考试化学试题贵州省六盘水市第七中学2019-2020学年高一上学期期末考试化学试题山东省泰安市新泰中学2019级高二上学期期中考试试题山东省新泰第一中学老校区(新泰中学)2020-2021学年高二上学期期中考试化学试题
名校
解题方法
9 . 按照要求填空:
(1) 在一可变的容积的密闭容器中进行
在一可变的容积的密闭容器中进行
①增加Fe的量,其反应速率的变化是______ (填增大、不变、减小,以下相同)
②将容器的体积缩小一半,反应速率______________
③保持体积不变,充入N2使体系压强增大,其反应速率________
④保持压强不变,充入N2使容器的体积增大,其反应速率__________
(2)2HI(g) ⇌H2(g)+I2(g)(正反应为吸热反应)改变下列条件:
①减小容器体积:平衡____ (填正移,逆移,不移动,以下相同)颜色___ (加深,变浅,不变,以下相同)
②加热升高温度:平衡____________
③体积不变,充入H2:平衡_____________ 颜色_______________
(3)可逆反应2NO2(g) N2O4(g),(正反应为放热反应),据图判断t2、t3时刻采取的措施t2:
N2O4(g),(正反应为放热反应),据图判断t2、t3时刻采取的措施t2:____ t3:_______

(1)
 在一可变的容积的密闭容器中进行
在一可变的容积的密闭容器中进行①增加Fe的量,其反应速率的变化是
②将容器的体积缩小一半,反应速率
③保持体积不变,充入N2使体系压强增大,其反应速率
④保持压强不变,充入N2使容器的体积增大,其反应速率
(2)2HI(g) ⇌H2(g)+I2(g)(正反应为吸热反应)改变下列条件:
①减小容器体积:平衡
②加热升高温度:平衡
③体积不变,充入H2:平衡
(3)可逆反应2NO2(g)
 N2O4(g),(正反应为放热反应),据图判断t2、t3时刻采取的措施t2:
N2O4(g),(正反应为放热反应),据图判断t2、t3时刻采取的措施t2:
您最近一年使用:0次
2020-05-27更新
|
115次组卷
|
2卷引用:宁夏石嘴山市第三中学2019-2020学年高一下学期期中考试化学试题
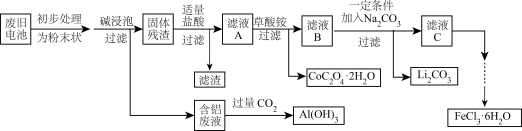
10 . 钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
已知:①还原性:Cl->Co2+;
②Fe3+和 结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
(1)废旧电池初步处理为粉末状的目的是________ 。
(2)从含铝废液得到Al(OH)3的离子方程式为___________
(3)滤液A中的溶质除HCl、LiCl外还有________ (填化学式)。写出LiCoO2和盐酸反应的化学方程式____________
(4)滤渣的主要成分为_______ (填化学式)。
(5)在空气中加热一定质量的CoC2O4·2H2O固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:①CoC2O4在空气中加热时的气体产物为CO2。
②固体失重率=对应温度下样品失重的质量/样品的初始质量。
(6)已知Li2CO3的溶度积常数Ksp=8.64×10-4,将浓度为0.02 mol·L-1的Li2SO4和浓度为0.02 mol·L-1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为________ mol·L-1。

已知:①还原性:Cl->Co2+;
②Fe3+和
 结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:(1)废旧电池初步处理为粉末状的目的是
(2)从含铝废液得到Al(OH)3的离子方程式为
(3)滤液A中的溶质除HCl、LiCl外还有
(4)滤渣的主要成分为
(5)在空气中加热一定质量的CoC2O4·2H2O固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:①CoC2O4在空气中加热时的气体产物为CO2。
②固体失重率=对应温度下样品失重的质量/样品的初始质量。
| 序号 | 温度范围/℃ | 化学方程式 | 固体失重率 |
| Ⅰ | 120~220 | CoC2O4·2H2O CoC2O4+2H2O | 19.67% |
| Ⅱ | 300~350 | 59.02% |
(6)已知Li2CO3的溶度积常数Ksp=8.64×10-4,将浓度为0.02 mol·L-1的Li2SO4和浓度为0.02 mol·L-1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为
您最近一年使用:0次
2020-03-27更新
|
783次组卷
|
5卷引用:宁夏石嘴山市第三中学2020届高三一模考试理综化学试题



