1 . 用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO等]制取CoCl2·6H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有,H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)①浸出过程中加入Na2SO3的目的是____ 。
②向浸出液中加入NaClO3的离子反应方程式为____ 。
③为提高浸取率除了适当增大NaClO3浓度,升高温度还可采取措施____ (答一条即可)。若不慎向“浸出液”中加入NaClO3过量时,可能会生成有毒气体,写出生成该有毒气体的离子方程式____ 。
(2)①“加Na2CO3调pH至a”,过滤所得到的沉淀成分为____ 。
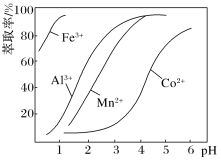
②萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是____ ;其使用的适宜pH范围是____ (填编号)。
A.2.0—2.5 B. 3.0—3.5 C.4.0—4.5 D.5.0—5.5
③“操作1”中包含的基本实验操作,它们依次是_______ 、____ 和过滤、减压烘干。
(3)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤,洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是____ (答一条即可)。

已知:①浸出液含有的阳离子主要有,H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe( OH)3 | Fe(OH)2 | Co(OH)2 | Al( OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
②向浸出液中加入NaClO3的离子反应方程式为
③为提高浸取率除了适当增大NaClO3浓度,升高温度还可采取措施
(2)①“加Na2CO3调pH至a”,过滤所得到的沉淀成分为
②萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是
A.2.0—2.5 B. 3.0—3.5 C.4.0—4.5 D.5.0—5.5

③“操作1”中包含的基本实验操作,它们依次是
(3)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤,洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
您最近半年使用:0次
2018-02-06更新
|
619次组卷
|
2卷引用:新疆乌鲁木齐地区2018届高三第一次诊断测试化学试题
2 . 钛是航空、军工、电力等领域重要的金属材料。一种由钛铁矿[主要成分是钛酸亚铁(FeTiO3),还含有少量 等杂质]制备金属钛同时获得
等杂质]制备金属钛同时获得 的工艺流程如图:
的工艺流程如图:
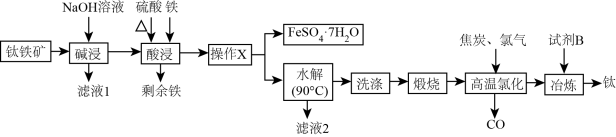
已知:“酸浸”后钛主要以 的形式存在;“水解”后钛以
的形式存在;“水解”后钛以 的形式存在。
的形式存在。
回答下列问题:
(1)基态 的最外层电子排布式为
的最外层电子排布式为_______ 。
(2)写出“水解( )”时发生反应的离子方程式:
)”时发生反应的离子方程式:_______ ;验证“洗涤”达到目的的操作为_______ 。
(3)“高温氯化”时发生反应的化学方程式为_______ ;有利于该过程中“气—固—固”接触的措施是_______ (写一种)。某科研小组模拟“高温氯化”反应理论计算结果显示,在 条件下达到平衡时,
条件下达到平衡时, 几乎完全转化为
几乎完全转化为 ,但实际生产中反应温度却远高于
,但实际生产中反应温度却远高于 ,其原因是
,其原因是_______ (写一种)。
(4)每次取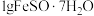 样品,加适量水溶解并加入
样品,加适量水溶解并加入 溶液和
溶液和 溶液,再用
溶液,再用 标准溶液滴定至终点,平行滴定3次,平均消耗标准溶液
标准溶液滴定至终点,平行滴定3次,平均消耗标准溶液 。
。
已知: (黄色)
(黄色)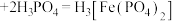 (无色)
(无色)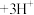 。
。
滴定终点溶液颜色变为_______ ;该样品中 的质量分数为
的质量分数为_______ (填含c,a的表达式)。
 等杂质]制备金属钛同时获得
等杂质]制备金属钛同时获得 的工艺流程如图:
的工艺流程如图:
已知:“酸浸”后钛主要以
 的形式存在;“水解”后钛以
的形式存在;“水解”后钛以 的形式存在。
的形式存在。回答下列问题:
(1)基态
 的最外层电子排布式为
的最外层电子排布式为(2)写出“水解(
 )”时发生反应的离子方程式:
)”时发生反应的离子方程式:(3)“高温氯化”时发生反应的化学方程式为
 条件下达到平衡时,
条件下达到平衡时, 几乎完全转化为
几乎完全转化为 ,但实际生产中反应温度却远高于
,但实际生产中反应温度却远高于 ,其原因是
,其原因是(4)每次取
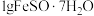 样品,加适量水溶解并加入
样品,加适量水溶解并加入 溶液和
溶液和 溶液,再用
溶液,再用 标准溶液滴定至终点,平行滴定3次,平均消耗标准溶液
标准溶液滴定至终点,平行滴定3次,平均消耗标准溶液 。
。已知:
 (黄色)
(黄色)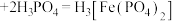 (无色)
(无色)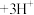 。
。滴定终点溶液颜色变为
 的质量分数为
的质量分数为
您最近半年使用:0次
名校
解题方法
3 . 黄铁矿的主要成分是FeS2,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:
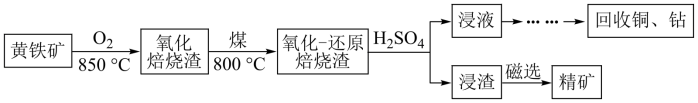
(1)黄铁矿焙烧之前需要粉碎,其目的是:_______
(2)①黄铁矿的氧化焙烧是制硫酸工艺的重要一步,其产物之一是 ,反应的化学方程式为:
,反应的化学方程式为:_______ ;
②制硫酸工艺中涉及反应2SO2+O2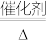 2SO3 ΔH<0,该反应需将温度控制在400-500℃,温度不宜过低的原因是
2SO3 ΔH<0,该反应需将温度控制在400-500℃,温度不宜过低的原因是_______ 。
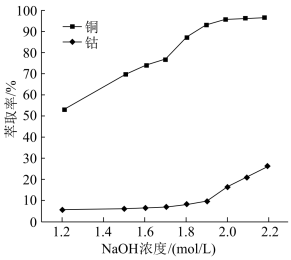
(3)用硫酸浸取后的浸渣能用磁选法分离,则该氧化物为_______ (填化学式);浸液通过加入萃取剂可实现铜和钴的分离,在萃取前加入NaOH溶液乳化可提高分离效率,不同浓度的溶液对萃取率的影响如图,则NaOH溶液最佳的浓度为_______ 。
已知黄铁矿氧化焙烧前后主要元素质量分数如表,为测定铜的浸出率,取50 g焙烧后的烧渣,经处理后测得Cu2+物质的量为5×10-3 mol,则铜离子的浸出率为_______ (结果保留三位有效数字)。

(1)黄铁矿焙烧之前需要粉碎,其目的是:
(2)①黄铁矿的氧化焙烧是制硫酸工艺的重要一步,其产物之一是
 ,反应的化学方程式为:
,反应的化学方程式为:②制硫酸工艺中涉及反应2SO2+O2
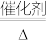 2SO3 ΔH<0,该反应需将温度控制在400-500℃,温度不宜过低的原因是
2SO3 ΔH<0,该反应需将温度控制在400-500℃,温度不宜过低的原因是(3)用硫酸浸取后的浸渣能用磁选法分离,则该氧化物为

已知黄铁矿氧化焙烧前后主要元素质量分数如表,为测定铜的浸出率,取50 g焙烧后的烧渣,经处理后测得Cu2+物质的量为5×10-3 mol,则铜离子的浸出率为
| 项目 | Fe | S | Cu | Co |
| 焙烧前(%) | 40.28 | 42.55 | 0.53 | 0.022 |
| 焙烧后(%) | 53.08 | 0.96 | 0.76 | 0.047 |
您最近半年使用:0次
4 . 废弃物回收再利用是环境保护的重要课题。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)、锌灰(主要成分为Zn、ZnO,杂质为Fe及其氧化物)回收Cu并制备ZnO,其部分实验过程如下图所示:
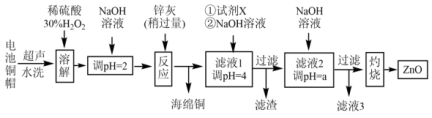
(1)铜帽溶解前需剪碎,其目的是_______ ,写出“溶解”过程中主要化学方程式_______ ,此过程不能加热的原因是_______ 。
(2)“反应”步骤为确定锌灰用量,以碘量法测定溶液中Cu2+含量:向含Cu2+待测液中加入过量KI溶液,再用Na2S2O3标准溶液滴定生成的 至终点,滴定原理如下:2Cu2++4I-=2CuI(白色)↓+I2;
至终点,滴定原理如下:2Cu2++4I-=2CuI(白色)↓+I2; 。
。
①滴定选用的指示剂为_______ ,滴定终点的现象是_______ 。
②若待测液中H2O2没有除尽,所测Cu2+含量将_______ (填“偏高”、“偏低”或“不变”)。
(3)已知:①滤液1中主要含有的金属离子有Zn2+、Fe2+;
②pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-;
③几种金属离子生成氧氧化物沉淀pH见下表。
利用滤液1制取ZnO,试剂X为_______ (填序号A.30% H2O2;B.1.0 mol/LHNO3),a的范围是_______ 。

(1)铜帽溶解前需剪碎,其目的是
(2)“反应”步骤为确定锌灰用量,以碘量法测定溶液中Cu2+含量:向含Cu2+待测液中加入过量KI溶液,再用Na2S2O3标准溶液滴定生成的
 至终点,滴定原理如下:2Cu2++4I-=2CuI(白色)↓+I2;
至终点,滴定原理如下:2Cu2++4I-=2CuI(白色)↓+I2; 。
。①滴定选用的指示剂为
②若待测液中H2O2没有除尽,所测Cu2+含量将
(3)已知:①滤液1中主要含有的金属离子有Zn2+、Fe2+;
②pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-;
③几种金属离子生成氧氧化物沉淀pH见下表。
| 开始沉淀pH | 沉淀完全pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
您最近半年使用:0次
5 . 一定温度下, 的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是
的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是
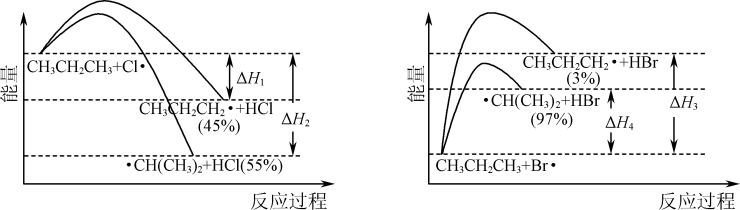
 的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是
的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是 
A. |
| B.升高温度,体系中n(1-氯丙烷)∶n(2-氯丙烷)的值增大 |
| C.以丙烷为原料合成丙醇时,“先溴代再水解”有利于提高2-丙醇的含量 |
| D.由图可知,丙烷中碳氢键的键能不完全相同 |
您最近半年使用:0次
2022-05-19更新
|
856次组卷
|
2卷引用:浙江省Z20名校联盟(名校新高考研究联盟)2022届高三第三次联考化学试题
名校
解题方法
6 . MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式如下所示:
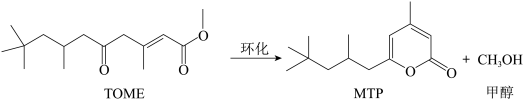
为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计,发生的其他副反应忽略不计。

已知:转化率= ,也可以用百分数表示。下列说法错误的是
,也可以用百分数表示。下列说法错误的是

为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计,发生的其他副反应忽略不计。

已知:转化率=
 ,也可以用百分数表示。下列说法错误的是
,也可以用百分数表示。下列说法错误的是| A.X、Y两点消耗反应物TOME的速率v正(X)<v正(Y) |
| B.X、Z两点该化学反应的瞬时速率大小为v(X)>v(Z) |
C.210℃时,0~150 min之间用MTP表示该化学反应的速率为 |
D.若Z点处于化学平衡,则平衡时溶液体系中甲醇的百分含量为 |
您最近半年使用:0次
名校
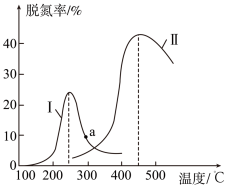
7 . 某研究小组探究催化剂对CO、NO转化的影响。将含NO和CO的尾气以一定的流速通过两种不同的催化剂进行反应:2NO(g)+2CO(g)  N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
①两种催化剂均能降低活化能,但ΔH不变
②相同条件下,改变压强对脱氮率没有影响
③曲线Ⅱ中的催化剂适用于450 ℃左右脱氮
④曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中的高
⑤ a 点是对应温度下的平衡脱氮率
⑥若低于200 ℃,图中曲线Ⅰ脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高
 N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
①两种催化剂均能降低活化能,但ΔH不变
②相同条件下,改变压强对脱氮率没有影响
③曲线Ⅱ中的催化剂适用于450 ℃左右脱氮
④曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中的高
⑤ a 点是对应温度下的平衡脱氮率
⑥若低于200 ℃,图中曲线Ⅰ脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高
| A.①③⑥ | B.①③④ | C.②③④ | D.①③⑤ |
您最近半年使用:0次



