名校
解题方法
1 . 科学家对汽车尾气进行无害化处理反应为:2CO+2NO⇌2CO2+N2。一定条件下,在1L密闭容器中充入2.00molCO和2.00molNO,一段时间后测得CO、CO2浓度随时间变化如图1所示,CO的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比m= ,完成问题:
,完成问题:
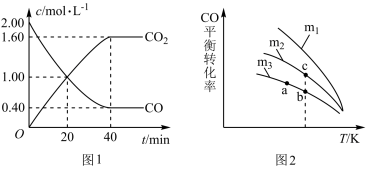
(1)该反应的化学平衡常数表达式是___________ ,根据图1,用N2表示该反应达平衡过程中的平均反应速率是___________ 。
(2)该反应的正反应是___________ 反应(填“吸热”或“放热”)。图2中a、b、c三点对应的平衡常数Ka、Kb、Kc相对大小关系是___________ 。
(3)关于该可逆反应的说法正确的是___________ 。
a.加入催化剂可提高NO的平衡转化率
b.当体系中c(CO2):c(N2)=2:1时,该反应达到平衡状态
c.保持其他条件不变,若充入N2,则达到新平衡时,正、逆反应速率均增大
d.投料比:m1>m2>m3
(4)随着温度的升高,不同投料比下CO的平衡转化率趋于相近的原因为___________ 。
 ,完成问题:
,完成问题:
(1)该反应的化学平衡常数表达式是
(2)该反应的正反应是
(3)关于该可逆反应的说法正确的是
a.加入催化剂可提高NO的平衡转化率
b.当体系中c(CO2):c(N2)=2:1时,该反应达到平衡状态
c.保持其他条件不变,若充入N2,则达到新平衡时,正、逆反应速率均增大
d.投料比:m1>m2>m3
(4)随着温度的升高,不同投料比下CO的平衡转化率趋于相近的原因为
您最近一年使用:0次
2023-07-02更新
|
557次组卷
|
5卷引用:吉林省长春外国语学校2023-2024学年高二下学期开学化学试题
吉林省长春外国语学校2023-2024学年高二下学期开学化学试题上海市育才中学2022-2023学年高二下学期(等级考)期末调研化学试题(已下线)专题04 可逆反应、化学平衡状态、化学平衡常数【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)重庆市第八中学校2023-2024学年高二上学期9月适应性考试化学试题(已下线)专题04 化学反应的速率与工业合成氨-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
名校
2 . 下列实验操作和现象能推出相应结论的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 相同条件下,将同等大小的钠分别加入无水乙醇和水中,钠与水反应更剧烈 | 乙醇中氢的活泼性比水中氢的活泼性弱 |
| B | 向淀粉溶液中加入适量稀硫酸,加热,冷却后加入过量NaOH溶液至碱性,再加少量碘水,溶液不变蓝 | 淀粉完全水解 |
| C | 向2mL0.01 KI溶液中加入4mL0.01 KI溶液中加入4mL0.01  溶液,充分反应后,再加入几滴0.01 溶液,充分反应后,再加入几滴0.01 KSCN溶液,溶液变红 KSCN溶液,溶液变红 | 该反应存在限度 |
| D | 在烧杯中将氢氧化钡晶体和氯化铵晶体混合搅拌,片刻后用手触摸烧杯底部感到冰凉,同时有刺激性气味的气体生成 | 该反应为放热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-27更新
|
175次组卷
|
2卷引用:吉林省长春市新解放学校2022-2023学年高一下学期7月期末考试化学试题
名校
解题方法
3 . 向绝热恒容密闭容器(绝热容器指该容器可阻止热量的传递,散失,对流)中通入 和
和 ,在一定条件下发生反应
,在一定条件下发生反应 ,正反应速率随时间变化的示意图如图所示,下列结论中正确的个数为
,正反应速率随时间变化的示意图如图所示,下列结论中正确的个数为
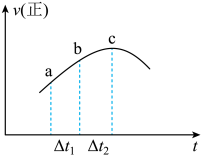
①反应在c点达到反应进行的限度
② 浓度:a点小于c点
浓度:a点小于c点
③逆反应速率图像在此时间段内和图中趋势相同
④ ,ab段
,ab段 的消耗量小于bc段
的消耗量小于bc段 的消耗量
的消耗量
⑤混合物颜色不再变化,说明反应达到平衡
⑥体系压强不再变化,说明反应达到平衡
 和
和 ,在一定条件下发生反应
,在一定条件下发生反应 ,正反应速率随时间变化的示意图如图所示,下列结论中正确的个数为
,正反应速率随时间变化的示意图如图所示,下列结论中正确的个数为
①反应在c点达到反应进行的限度
②
 浓度:a点小于c点
浓度:a点小于c点③逆反应速率图像在此时间段内和图中趋势相同
④
 ,ab段
,ab段 的消耗量小于bc段
的消耗量小于bc段 的消耗量
的消耗量⑤混合物颜色不再变化,说明反应达到平衡
⑥体系压强不再变化,说明反应达到平衡
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
2023-06-20更新
|
313次组卷
|
2卷引用:吉林省梅河口市第五中学2023-2024学年高二上学期开学考试化学试题
4 . 向一恒容密闭容器中加入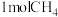 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比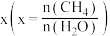 随温度的变化曲线如图所示。下列说法错误的是
随温度的变化曲线如图所示。下列说法错误的是
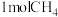 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比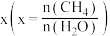 随温度的变化曲线如图所示。下列说法错误的是
随温度的变化曲线如图所示。下列说法错误的是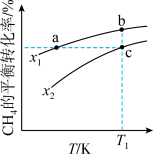
A.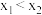 |
B.反应速率: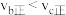 |
C.点a、b、c对应的平衡常数: |
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态 ,当容器内压强不变时,反应达到平衡状态 |
您最近一年使用:0次
2023-06-16更新
|
12882次组卷
|
35卷引用:吉林省长春市第五中学2022-2023学年高一下学期期末考试化学试题
吉林省长春市第五中学2022-2023学年高一下学期期末考试化学试题吉林省长春市东北师范大学附属中学2023-2024学年高二上学期10月期中化学试题2023年高考湖南卷化学真题(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)第13练 化学反应速率与化学平衡的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)2023年湖南卷高考真题变式题(选择题11-14)(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第26讲化学反应速率及影响因素(已下线)第27讲化学平衡和化学平衡常数浙江省宁波市北仑中学2023-2024学年高二上学期期初考试化学试题辽宁省大连市滨城高中联盟2023-2024学年高二上学期10月月考化学试题辽宁省东北育才中学少儿部2023-2024学年高二上学期第一次月考化学试题湖南省泸溪县第一中学等多校联考2023-2024学年高二上学期8月月考化学试题宁夏银川市唐徕中学2023-2024学年高二上学期9月月考化学试题(已下线)专题05 影响化学平衡的因素【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)辽宁省东北育才学校2023-2024学年高二上学期第一次月考化学试题(已下线)考点3 化学平衡常数及转化率的计算(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)重庆市第七中学校2023-2024学年高三上学期11月月考化学试卷北京市第二十中学2023-2024学年高三上学期10月月考化学试题北京市第二十中学2023-2024学年高三上学期12月月考化学试题安徽省当涂第一中学2023-2024学年高二上学期10月月考化学试题(已下线)题型04 化学反应速率与平衡图像分析-2024年高考化学答题技巧与模板构建2023—2024学年高二上学期化学期末考试模拟试题(一) (已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题03 化学平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)题型12 化学平衡图表分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)宁夏回族自治区石嘴山市第三中学2023-2024学年高二上学期1月期末化学试题(已下线)题型13 化学平衡常数的计算及应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)2024届山东省潍坊市昌乐二中高三模拟预测化学试题江苏省连云港市新海高级中学2023-2024学年高二下学期第一次月考化学试题浙江省四校联考2023-2024学年高二下学期3月月考化学试题
名校
解题方法
5 . 氢气是理想的能源,可由天然气和水反应制备,其主要反应为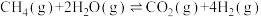 ,反应过程中能量变化如图所示:
,反应过程中能量变化如图所示:
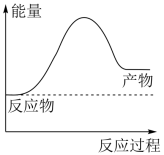
(1)该反应是_____ (填“吸热”或“放热”)反应。
(2)某温度下,在10L恒容密闭容器中充入2mol 和3mol
和3mol 制备氢气,反应中
制备氢气,反应中 的物质的量变化如图所示,5min时反应达到平衡状态。
的物质的量变化如图所示,5min时反应达到平衡状态。
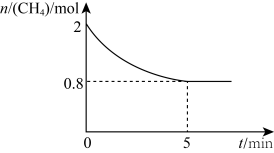
①5min前,该反应的正反应速率_____ (填“大于”、“小于”或“等于”)逆反应速率,逆反应速率不断_____ (填“增大”或“减小”)。
②下列能说明该反应已达到化学平衡状态的是_____ (填字母)。
a.容器内混合气体的密度不再发生变化
b.容器内气体原子总数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.单位时间内,4molC-H键断裂的同时有2molC=O键断裂
③0~5min内,以 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为_____ 
④若要加快化学反应速率,可采用的方法是_____ (填“升高”或“降低”)温度。
(3)某同学依据氧化还原反应: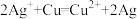 ,设计的原电池如图所示:
,设计的原电池如图所示:
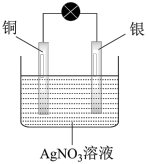
①负极的材料是_____ ,发生的电极反应式为_____ ;
②外电路中的电子是从_____ 电极流向_____ 电极。(写出电极材料的名称)
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是_____ 。(阿伏伽德罗常数为NA)
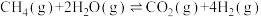 ,反应过程中能量变化如图所示:
,反应过程中能量变化如图所示:
(1)该反应是
(2)某温度下,在10L恒容密闭容器中充入2mol
 和3mol
和3mol 制备氢气,反应中
制备氢气,反应中 的物质的量变化如图所示,5min时反应达到平衡状态。
的物质的量变化如图所示,5min时反应达到平衡状态。
①5min前,该反应的正反应速率
②下列能说明该反应已达到化学平衡状态的是
a.容器内混合气体的密度不再发生变化
b.容器内气体原子总数不再发生变化
c.混合气体的平均相对分子质量不再发生变化
d.单位时间内,4molC-H键断裂的同时有2molC=O键断裂
③0~5min内,以
 的浓度变化表示该反应的平均速率为
的浓度变化表示该反应的平均速率为
④若要加快化学反应速率,可采用的方法是
(3)某同学依据氧化还原反应:
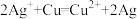 ,设计的原电池如图所示:
,设计的原电池如图所示: 
①负极的材料是
②外电路中的电子是从
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是
您最近一年使用:0次
名校
解题方法
6 . 二甲醚(CH3OCH3)是一种基本有机化工原料,可用作溶剂、气雾剂、制冷剂和麻醉剂等。利用二氧化碳氢化法合成二甲醚,可实现碳中和,对于保障经济高速、可持续发展具有重要的战略意义。其中涉及的反应有:
I.CO2(g)+ 3H2(g) CH3OH(g)+ H2O(g) ΔH1=- 49.1kJ·mol-1
CH3OH(g)+ H2O(g) ΔH1=- 49.1kJ·mol-1
II.2CH3OH(g) CH3OCH3(g)+ H2O(g) ΔH2= - 24.5 kJ·mol-1
CH3OCH3(g)+ H2O(g) ΔH2= - 24.5 kJ·mol-1
III.CO2(g)+ H2(g) CO(g)+ H2O(g) ΔH3=+41.2 kJ·mol-1
CO(g)+ H2O(g) ΔH3=+41.2 kJ·mol-1
已知:生成物A的选择性S=-
回答下列问题:
(1)写出CO2 (g) 与H2 (g)转化为CH3OCH3 (g)和H2O (g) (反应IV)的热化学方程式___________ 。
(2)在恒温恒压条件下,将一定量的CO2、H2通入密闭容器中(含催化剂)发生上述反应。下列不能够说明该反应体系已达化学平衡状态的是________ 。
A.反应I中v正(H2) = 3v逆(CH3OH)
B. n(CH3OH):n(CH3OCH3)=2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
E. CO2的转化率不变
(3)反应I、II、 III的吉布斯自由能随温度变化如下图1所示,下列说法正确的是___________。
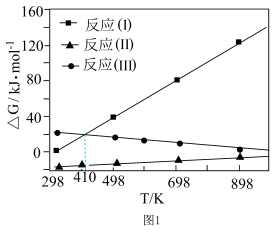
(4)在3.0MPa下,研究人员在恒压密闭容器中充入4molH2和lmolCO2发生反应,CO2的平衡转化率和生成物的选择性随温度变化如上图2所示(不考虑其他因素影响)。
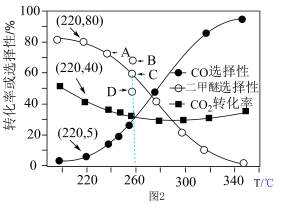
①在220°C条件下,平衡时n(H2O)=___________ ,计算反应2CH3OH(g) CH3OCH3(g)+ H2O(g)在220°C下的平衡常数为
CH3OCH3(g)+ H2O(g)在220°C下的平衡常数为___________ (结果保留三位有效数字)。
②温度高于280°C,CO2平衡转化率随温度升高而上升的原因是________ 。
③当其他条件不变,压强为4.0MPa、温度为260°C时,图中点________ (填“A”、“B”、“C”或“D”)可表示二甲醚的选择性。
I.CO2(g)+ 3H2(g)
 CH3OH(g)+ H2O(g) ΔH1=- 49.1kJ·mol-1
CH3OH(g)+ H2O(g) ΔH1=- 49.1kJ·mol-1II.2CH3OH(g)
 CH3OCH3(g)+ H2O(g) ΔH2= - 24.5 kJ·mol-1
CH3OCH3(g)+ H2O(g) ΔH2= - 24.5 kJ·mol-1III.CO2(g)+ H2(g)
 CO(g)+ H2O(g) ΔH3=+41.2 kJ·mol-1
CO(g)+ H2O(g) ΔH3=+41.2 kJ·mol-1已知:生成物A的选择性S=-

回答下列问题:
(1)写出CO2 (g) 与H2 (g)转化为CH3OCH3 (g)和H2O (g) (反应IV)的热化学方程式
(2)在恒温恒压条件下,将一定量的CO2、H2通入密闭容器中(含催化剂)发生上述反应。下列不能够说明该反应体系已达化学平衡状态的是
A.反应I中v正(H2) = 3v逆(CH3OH)
B. n(CH3OH):n(CH3OCH3)=2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
E. CO2的转化率不变
(3)反应I、II、 III的吉布斯自由能随温度变化如下图1所示,下列说法正确的是___________。

| A.常温下,反应I、II、III均能自发进行 |
| B.410K 时,反应II和反应III的热效应相同。 |
| C.温度升高,CH3OH 的选择性降低,CO 的选择性升高 |
| D.提高二甲醚产率的关键是寻找对甲醇具有高选择性的催化剂 |

①在220°C条件下,平衡时n(H2O)=
 CH3OCH3(g)+ H2O(g)在220°C下的平衡常数为
CH3OCH3(g)+ H2O(g)在220°C下的平衡常数为②温度高于280°C,CO2平衡转化率随温度升高而上升的原因是
③当其他条件不变,压强为4.0MPa、温度为260°C时,图中点
您最近一年使用:0次
2023-06-05更新
|
349次组卷
|
2卷引用:吉林省长春市东北师范大学附属中学2023届高三下学期模拟预测理综化学试题
名校
解题方法
7 . 化学反应进行的快慢和程度是研究化学反应的重要方向。请完成下列填空。
Ⅰ.在某一容积为4L的密闭容器中,A、B、C、D四种物质的物质的量随时间的变化曲线如图所示,完成下列问题:
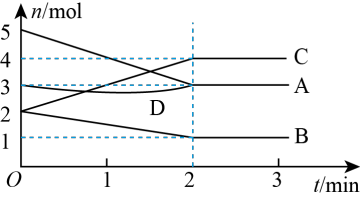
(1)该反应的化学方程式为___________ 。
(2)前 用A的浓度变化表示的化学反应速率为
用A的浓度变化表示的化学反应速率为___________ 。
Ⅱ. 是一种常用的还原剂。一定条件下,反应
是一种常用的还原剂。一定条件下,反应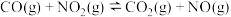 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关。与浓度无关)。某温度下,该反应在不同浓度下反应速率如下表所示:
(k为速率常数,只与温度、催化剂有关。与浓度无关)。某温度下,该反应在不同浓度下反应速率如下表所示:
(3)根据表中测定结果,推断出a=___________ 、b=___________ 。
(4)改变下列反应条件,反应速率增大的是___________(填字母)。
(5)可以判断反应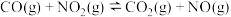 已经达到平衡状态的是
已经达到平衡状态的是___________ 。
A. 的物质的量分数保持不变
的物质的量分数保持不变
B.体系中气体颜色不变
C.等温等容,体系中气体密度保持不变
D.等温等压,体系压强不再发生变化
E.
 消耗的同时
消耗的同时
 生成
生成
F.若反应在绝热体系中进行,体系温度不再变化
Ⅰ.在某一容积为4L的密闭容器中,A、B、C、D四种物质的物质的量随时间的变化曲线如图所示,完成下列问题:

(1)该反应的化学方程式为
(2)前
 用A的浓度变化表示的化学反应速率为
用A的浓度变化表示的化学反应速率为Ⅱ.
 是一种常用的还原剂。一定条件下,反应
是一种常用的还原剂。一定条件下,反应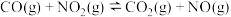 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关。与浓度无关)。某温度下,该反应在不同浓度下反应速率如下表所示:
(k为速率常数,只与温度、催化剂有关。与浓度无关)。某温度下,该反应在不同浓度下反应速率如下表所示: |  | 反应速率 | |
| ① | 0.10 | 0.10 |  |
| ② | 0.20 | 0.10 | 2 |
| ③ | 0.20 | 0.20 | 4 |
(4)改变下列反应条件,反应速率增大的是___________(填字母)。
| A.降温 | B.缩小体积 | C.加入催化剂 | D.减压 |
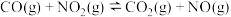 已经达到平衡状态的是
已经达到平衡状态的是A.
 的物质的量分数保持不变
的物质的量分数保持不变B.体系中气体颜色不变
C.等温等容,体系中气体密度保持不变
D.等温等压,体系压强不再发生变化
E.

 消耗的同时
消耗的同时
 生成
生成F.若反应在绝热体系中进行,体系温度不再变化
您最近一年使用:0次
名校
8 . 对可逆反应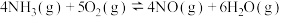 ,下列叙述错误的是
,下列叙述错误的是
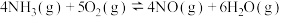 ,下列叙述错误的是
,下列叙述错误的是A. 时,反应达到平衡,反应停止 时,反应达到平衡,反应停止 |
B.达到化学平衡时, 的浓度不再变化 的浓度不再变化 |
| C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率也减小 |
D.若单位时间内生成 的同时生成 的同时生成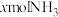 ,则反应达到平衡状态 ,则反应达到平衡状态 |
您最近一年使用:0次
2023-05-31更新
|
167次组卷
|
5卷引用:吉林省长春市公主岭一中,榆树实验,九台一中,农安2022-2023学年高一下学期7月期末化学试题
名校
9 . 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应生成另外两种气体,反应中各物质的物质的量变化如图所示,请回答下列问题:

(1)该反应的化学方程式为___________ 。
(2)反应开始至6s时,B的平均反应速率为___________ 。
(3)上图中1s时, v(正)___________ v(逆)(填“大于”“小于”或“等于”)。
(4)反应开始至6s时,C的转化率___________ 。
(5)下列能使该反应的化学反应速率增大的是___________。
(6)下列条件已达平衡状态的是___________ 。
A. 单位时间里生成n molA,同时生成n molB
B. 容器中的总压强不随时间而变化
C. A、B、C、D浓度不随时间而变化
D. B的物质的量保持不变
E. 容器内气体总物质的量不随时间而变化
F. 容器内混合气体的密度不再变化
G. 容器内混合气体的平均相对分子质量不再变化
H. A和D物质的物质的量的比值不再变化

(1)该反应的化学方程式为
(2)反应开始至6s时,B的平均反应速率为
(3)上图中1s时, v(正)
(4)反应开始至6s时,C的转化率
(5)下列能使该反应的化学反应速率增大的是___________。
| A.适当升高温度 | B.选择高效的催化剂 |
| C.充入氩气 | D.增大气体A的浓度 |
A. 单位时间里生成n molA,同时生成n molB
B. 容器中的总压强不随时间而变化
C. A、B、C、D浓度不随时间而变化
D. B的物质的量保持不变
E. 容器内气体总物质的量不随时间而变化
F. 容器内混合气体的密度不再变化
G. 容器内混合气体的平均相对分子质量不再变化
H. A和D物质的物质的量的比值不再变化
您最近一年使用:0次
名校
10 . 在一定温度下的定容密闭容器中,取一定量的A、B于反应容器中,当下列物理量不再改变时,表明反应:A(s)+2B(g)  C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
 C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是| A.混合气体的压强 | B.混合气体的密度 |
| C.A的浓度 | D.气体的总物质的量 |
您最近一年使用:0次



