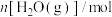名校
解题方法
1 . 化学是以头验为基础的学科。下列根据实验操作和现象能得到相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向 溶液KI中加入 溶液KI中加入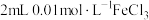 溶液( 溶液( ),溶液呈烹黄色,再滴加几滴KSCN溶液,溶液变为红色 ),溶液呈烹黄色,再滴加几滴KSCN溶液,溶液变为红色 |  和 和 的反应存在限度 的反应存在限度 |
| B | 常温下,将两块相同的未经打磨的铝片分别投入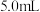 饱和的 饱和的 溶液和 溶液和 溶液中,前者无明显现象,后者迅速反应,现象明显 溶液中,前者无明显现象,后者迅速反应,现象明显 |  能加速破坏铝片表面的氧化膜 能加速破坏铝片表面的氧化膜 |
| C | 常温下,向 溶液中加入 溶液中加入 溶液,将带火星的木条放在试管口,木条复燃 溶液,将带火星的木条放在试管口,木条复燃 | 氧化性: |
| D | 向某无色溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的的气体 | 原溶液中一定含有 或 或 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-05更新
|
1481次组卷
|
6卷引用:吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷
吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷(已下线)题型04 氧化还原反应-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)山西省运城市盐湖区第五高级中学2023-2024学年高三上学期一轮复习检测卷(已下线)选择题6-10
名校
解题方法
2 . 下列实验能得出相关结论的是
| 实验操作 | 实验结论 | |
| A | 向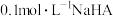 溶液中滴加酚酞溶液,溶液变为浅红色 溶液中滴加酚酞溶液,溶液变为浅红色 | 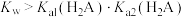 |
| B | 常温下将铝片投入浓硝酸中,无明显现象 | 铝与浓硝酸不反应 |
| C | 向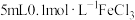 溶液中加入2滴 溶液中加入2滴 溶液,溶液显红色,再滴加2滴 溶液,溶液显红色,再滴加2滴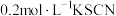 溶液,红色加深 溶液,红色加深 |  和 和 的反应是可逆反应 的反应是可逆反应 |
| D | 室温下,用pH计测定浓度均为 的 的 溶液和 溶液和 溶液的pH, 溶液的pH, 溶液pH大 溶液pH大 |  比 比 的酸性弱 的酸性弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-05更新
|
506次组卷
|
3卷引用:吉林省长春市2024届高三上学期质量监测(一)化学试题
3 . 甲醇是重要的化工原料。利用合成气(主要成分为CO、 和
和 )在催化剂的作用下合成甲醇,发生的主要反应如下:
)在催化剂的作用下合成甲醇,发生的主要反应如下:
Ⅰ.

Ⅱ.

在恒容密闭容器进行反应Ⅰ,测得其化学平衡常数K和温度t的关系如表:
(1)
_______ 0,其理由是_______ 。
(2)能判断该反应达到化学平衡状态的依据是_______。
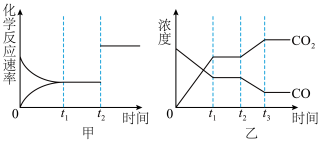
(3)图甲、图乙分别表示反应在 时刻达到平衡,在
时刻达到平衡,在 时刻因改变某个条件而发生变化的情况。图甲中
时刻因改变某个条件而发生变化的情况。图甲中 时刻发生改变的条件是
时刻发生改变的条件是_______ ,图乙中 时刻发生改变的条件是
时刻发生改变的条件是_______ 。
(4)若1200℃时,在某时刻平衡体系中 、
、 、
、 、
、 的浓度分别为
的浓度分别为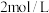 、
、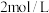 、
、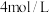 、
、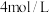 ,此时v(正)
,此时v(正)_______ v(逆)(填大于、小于或等于),其理由是_______ 。
 和
和 )在催化剂的作用下合成甲醇,发生的主要反应如下:
)在催化剂的作用下合成甲醇,发生的主要反应如下:Ⅰ.


Ⅱ.


在恒容密闭容器进行反应Ⅰ,测得其化学平衡常数K和温度t的关系如表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)

(2)能判断该反应达到化学平衡状态的依据是_______。
A. | B.容器内 的体积分数保持不变 的体积分数保持不变 |
| C.容器内气体密度保持不变 | D.容器中压强保持不变 |
(3)图甲、图乙分别表示反应在
 时刻达到平衡,在
时刻达到平衡,在 时刻因改变某个条件而发生变化的情况。图甲中
时刻因改变某个条件而发生变化的情况。图甲中 时刻发生改变的条件是
时刻发生改变的条件是 时刻发生改变的条件是
时刻发生改变的条件是
(4)若1200℃时,在某时刻平衡体系中
 、
、 、
、 、
、 的浓度分别为
的浓度分别为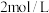 、
、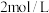 、
、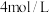 、
、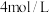 ,此时v(正)
,此时v(正)
您最近一年使用:0次
名校
解题方法
4 . 下列实验操作、现象及结论均正确是
| 选项 | 操作和现象 | 结论 |
| A | 常温下,用pH计分别测定等体积 溶液和 溶液和 溶液的pH,pH均为7 溶液的pH,pH均为7 | 两种 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| B | 向2mL 的KI溶液中滴加2mL 的KI溶液中滴加2mL 的 的 溶液,充分反应后加入2mL 溶液,充分反应后加入2mL ,取上层溶液滴加KSCN溶液,溶液变红色 ,取上层溶液滴加KSCN溶液,溶液变红色 |  与KI的反应存在限度 与KI的反应存在限度 |
| C | 向溶有 的 的 的溶液中通入气体X,出现白色沉淀 的溶液中通入气体X,出现白色沉淀 | X具有强氧化性 |
| D | 向2mL  溶液中滴入3滴 溶液中滴入3滴 NaOH溶液,再滴入4滴 NaOH溶液,再滴入4滴  溶液,先产生白色沉淀,后产生红褐色沉淀 溶液,先产生白色沉淀,后产生红褐色沉淀 | 同温度下的 : : |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-27更新
|
540次组卷
|
3卷引用:吉林省长春外国语学校2023-2024学年高二上学期12月月考化学试题
名校
解题方法
5 . 我国力争2030年前实现碳达峰,2060 年前实现碳中和。CO2 的综合利用是实现碳中和的措施之一。
Ⅰ.CO2和CH4在催化剂表面可以合成CH3COOH,该反应的历程和相对能量的变化情况如下图所示(*指微粒吸附在催化剂表面,H*指H吸附在催化剂载体上的氧原子上,TS表示过渡态):
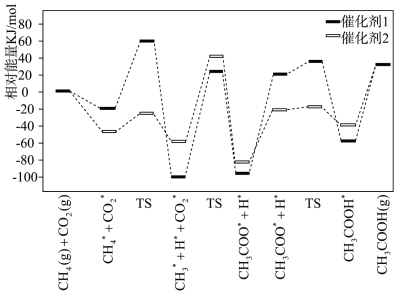
(1)决定该过程的总反应速率的基元反应方程式为_______ 。
(2)下列说法正确的有_______ 。
a.增大催化剂表面积可提高CO2在催化剂表面的吸附速率
b.CH3COOH*比CH3COOH(g)能量高
c.使用高活性催化剂可降低反应焓变,加快反应速率
d.催化效果更好的是催化剂2
Ⅱ.CO2和H2在一定条件下也可以合成甲醇,该过程存在副反应ii。
反应i:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-49.3kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.3kJ·mol-1
反应ii:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
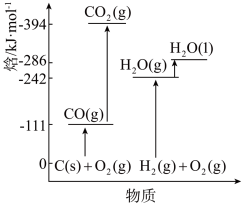
(3)有关物质能量变化如图所示,稳定单质的焓(H)为0,则ΔH2=_______ kJ·mol-1。
(4)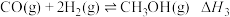 该反应的自发条件是
该反应的自发条件是_______ (填“高温自发”“低温自发”或“任何温度下都自发”)。
(5)恒温恒容条件下,仅发生反应ii,反应达到平衡的标志是_______ 。
a.CO的分压不再发生变化 b.气体平均相对分子质量不再发生变化
c.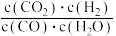 比值不再发生变化 d.气体密度不再发生变化
比值不再发生变化 d.气体密度不再发生变化
(6)在5.0MPa,将n(CO2):n(H2)=5:16的混合气体在催化剂作用下进行反应。体系中气体平衡组成比例(CO和CH3OH在含碳产物中物质的量百分数)及CO2的转化率随温度的变化如图所示。
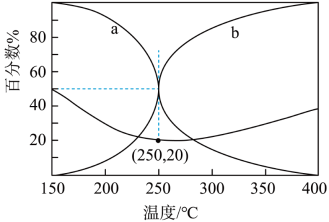
①表示平衡时CH3OH在含碳产物中物质的量百分数的曲线是_______ (填“a”或“b”)。
②CO2平衡转化率随温度的升高先减小后增大,增大的原因可能是_______ 。
③250℃时反应i:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)的Kp=_______ (MPa)-2(用最简分数表示)。
Ⅰ.CO2和CH4在催化剂表面可以合成CH3COOH,该反应的历程和相对能量的变化情况如下图所示(*指微粒吸附在催化剂表面,H*指H吸附在催化剂载体上的氧原子上,TS表示过渡态):

(1)决定该过程的总反应速率的基元反应方程式为
(2)下列说法正确的有
a.增大催化剂表面积可提高CO2在催化剂表面的吸附速率
b.CH3COOH*比CH3COOH(g)能量高
c.使用高活性催化剂可降低反应焓变,加快反应速率
d.催化效果更好的是催化剂2
Ⅱ.CO2和H2在一定条件下也可以合成甲醇,该过程存在副反应ii。
反应i:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-49.3kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.3kJ·mol-1反应ii:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2(3)有关物质能量变化如图所示,稳定单质的焓(H)为0,则ΔH2=

(4)
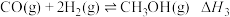 该反应的自发条件是
该反应的自发条件是(5)恒温恒容条件下,仅发生反应ii,反应达到平衡的标志是
a.CO的分压不再发生变化 b.气体平均相对分子质量不再发生变化
c.
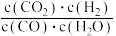 比值不再发生变化 d.气体密度不再发生变化
比值不再发生变化 d.气体密度不再发生变化(6)在5.0MPa,将n(CO2):n(H2)=5:16的混合气体在催化剂作用下进行反应。体系中气体平衡组成比例(CO和CH3OH在含碳产物中物质的量百分数)及CO2的转化率随温度的变化如图所示。

①表示平衡时CH3OH在含碳产物中物质的量百分数的曲线是
②CO2平衡转化率随温度的升高先减小后增大,增大的原因可能是
③250℃时反应i:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)的Kp=
您最近一年使用:0次
名校
6 . 已知: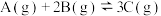
 向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应,
向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
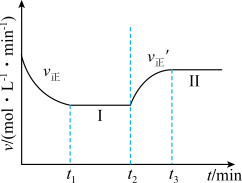
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
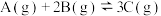
 向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应,
向一恒温恒容的密闭容器中充入1mol A和3mol B发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
A.平衡时A的体积分数 |
| B.容器内气体的平均相对分子质量不变,表明反应达到平衡 |
C. 时改变的条件:向容器中加入B 时改变的条件:向容器中加入B |
D.平衡常数 |
您最近一年使用:0次
2023-11-04更新
|
331次组卷
|
4卷引用:吉林省梅河口市第五中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
7 . 工业上在催化剂作用下可用 和
和 合成甲醇,其反应为
合成甲醇,其反应为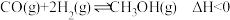 。一定条件下向一密闭容器中充入
。一定条件下向一密闭容器中充入 和
和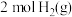 ,发生上述反应,
,发生上述反应, 的平衡转化率与温度、压强的关系如图所示,回答下列问题:
的平衡转化率与温度、压强的关系如图所示,回答下列问题:
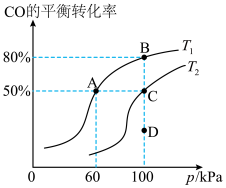
(1)该反应中反应物断键吸收的总能量___________ (填“>”“<”或“=”,下同)生成物成键放出的总能量;温度
___________  ;温度为
;温度为 时,D点反应速率:
时,D点反应速率:
___________  。
。
(2)下列说法可以表明该反应达到平衡状态的是___________ 。(填标号,下同)
a. 和
和 的物质的量之比不再改变
的物质的量之比不再改变
b. 的体积分数不再改变
的体积分数不再改变
c.断裂2个 键的同时有3个
键的同时有3个 键断裂
键断裂
d.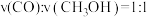
(3)在一恒容密闭容器中发生上述反应,其他条件不变,下列措施可以加快反应速率的是___________ (填序号,下同),能提高 平衡转化率的是
平衡转化率的是___________ 。
①升高温度 ②将 从体系中分离出来
从体系中分离出来
③充入 ,使体系总压强增大 ④再充入一定量的
,使体系总压强增大 ④再充入一定量的
(4)A、B、C三点中,正反应速率最大的是___________ (填“A”、“B”或“C”)点,该点对应的平衡常数
___________  (用最简分数表示;
(用最简分数表示; 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
 和
和 合成甲醇,其反应为
合成甲醇,其反应为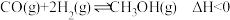 。一定条件下向一密闭容器中充入
。一定条件下向一密闭容器中充入 和
和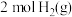 ,发生上述反应,
,发生上述反应, 的平衡转化率与温度、压强的关系如图所示,回答下列问题:
的平衡转化率与温度、压强的关系如图所示,回答下列问题:
(1)该反应中反应物断键吸收的总能量

 ;温度为
;温度为 时,D点反应速率:
时,D点反应速率:
 。
。(2)下列说法可以表明该反应达到平衡状态的是
a.
 和
和 的物质的量之比不再改变
的物质的量之比不再改变b.
 的体积分数不再改变
的体积分数不再改变c.断裂2个
 键的同时有3个
键的同时有3个 键断裂
键断裂d.
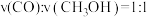
(3)在一恒容密闭容器中发生上述反应,其他条件不变,下列措施可以加快反应速率的是
 平衡转化率的是
平衡转化率的是①升高温度 ②将
 从体系中分离出来
从体系中分离出来③充入
 ,使体系总压强增大 ④再充入一定量的
,使体系总压强增大 ④再充入一定量的
(4)A、B、C三点中,正反应速率最大的是

 (用最简分数表示;
(用最简分数表示; 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
2023-11-04更新
|
192次组卷
|
3卷引用:吉林省松原市前郭县第五高级中学2023~2024学年高二上学期期中考试化学试题
8 . 科研、生产中常涉及碳的化合物。回答下列问题:
(1)700℃时,向容积为3L的恒容密闭容器中充入一定量的CO和 ,发生反应:
,发生反应: ,反应过程中测定的部分数据见下表:
,反应过程中测定的部分数据见下表:
①反应前2min内的平均反应速率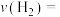
______ ;表中y的值为______ 。
②判定2min时达到平衡状态的理由是______ 。
(2)工业上可利用煤的气化产物(水煤气)合成二甲醚:
 。一定条件下的密闭容器中,该反应达到平衡,要提高
。一定条件下的密闭容器中,该反应达到平衡,要提高 的转化率,可以采取的措施是
的转化率,可以采取的措施是______ (填字母)。
a.升高温度 b.加入催化剂
c.减小 的浓度 d.增大压强(缩小容器体积)
的浓度 d.增大压强(缩小容器体积)
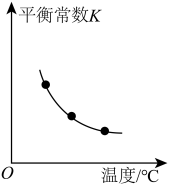
(3)高炉炼铁中发生的主要反应为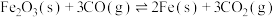 。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式为
。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式为
______ ,
______ 0(填“>”“<”或“=”)。
(4) 能与
能与 反应制得甲醇(
反应制得甲醇( ):
):
 。一定条件下,将2 mol
。一定条件下,将2 mol  和4 mol
和4 mol  充入密闭容器中,发生反应制取甲醇,
充入密闭容器中,发生反应制取甲醇, 的平衡转化率与温度、平衡总压强的关系如图所示。
的平衡转化率与温度、平衡总压强的关系如图所示。
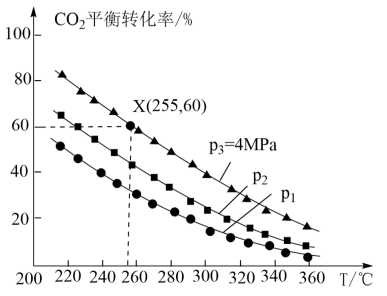
① 、
、 、
、 由大到小的顺序为
由大到小的顺序为______ 。
② 条件下255℃时,该反应的压强平衡常数
条件下255℃时,该反应的压强平衡常数
______  (
( 为以分压表示的平衡常数,分压=总压×物质的量分数;计算结果保留1位小数)。
为以分压表示的平衡常数,分压=总压×物质的量分数;计算结果保留1位小数)。
(1)700℃时,向容积为3L的恒容密闭容器中充入一定量的CO和
 ,发生反应:
,发生反应: ,反应过程中测定的部分数据见下表:
,反应过程中测定的部分数据见下表:反应时间/min |
|
|
0 | 1.8 | 0.9 |
2 | 1.2 | x |
4 | y | 0.3 |
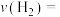
②判定2min时达到平衡状态的理由是
(2)工业上可利用煤的气化产物(水煤气)合成二甲醚:

 。一定条件下的密闭容器中,该反应达到平衡,要提高
。一定条件下的密闭容器中,该反应达到平衡,要提高 的转化率,可以采取的措施是
的转化率,可以采取的措施是a.升高温度 b.加入催化剂
c.减小
 的浓度 d.增大压强(缩小容器体积)
的浓度 d.增大压强(缩小容器体积)(3)高炉炼铁中发生的主要反应为
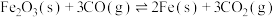 。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式为
。已知该反应平衡常数随温度变化如图所示,该反应平衡常数表达式为


(4)
 能与
能与 反应制得甲醇(
反应制得甲醇( ):
):
 。一定条件下,将2 mol
。一定条件下,将2 mol  和4 mol
和4 mol  充入密闭容器中,发生反应制取甲醇,
充入密闭容器中,发生反应制取甲醇, 的平衡转化率与温度、平衡总压强的关系如图所示。
的平衡转化率与温度、平衡总压强的关系如图所示。
①
 、
、 、
、 由大到小的顺序为
由大到小的顺序为②
 条件下255℃时,该反应的压强平衡常数
条件下255℃时,该反应的压强平衡常数
 (
( 为以分压表示的平衡常数,分压=总压×物质的量分数;计算结果保留1位小数)。
为以分压表示的平衡常数,分压=总压×物质的量分数;计算结果保留1位小数)。
您最近一年使用:0次
9 . 一定条件下密闭容器中发生反应: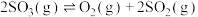 。该反应达到平衡状态的标志是
。该反应达到平衡状态的标志是
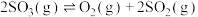 。该反应达到平衡状态的标志是
。该反应达到平衡状态的标志是A. 、 、 、 、 三种气体共存时 三种气体共存时 | B. 的消耗速率等于 的消耗速率等于 的消耗速率 的消耗速率 |
| C.容器中各组分的体积分数不随时间而变化 | D.容器混合气体的总质量不变 |
您最近一年使用:0次
名校
解题方法
10 . 丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。
已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l) △H=−2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=−566kJ/mol
(1)写出表示丙烷燃烧热的热化学方程式___________ 。
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+H2O CO2(g)+H2(g) △H>0
CO2(g)+H2(g) △H>0
①下列事实能说明该反应达到平衡的是___________ 。
a.体系中的压强不发生变化
b.v正(H2)=v逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO2的浓度不再发生变化
②在某温度下,反应物的起始浓度分别为:c(CO)=1mol•L﹣1,c(H2O)=2.4mol•L﹣1;达到平衡后,CO的转化率为60%,该温度下的化学平衡常数为___________ 。
已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l) △H=−2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=−566kJ/mol
(1)写出表示丙烷燃烧热的热化学方程式
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+H2O
 CO2(g)+H2(g) △H>0
CO2(g)+H2(g) △H>0①下列事实能说明该反应达到平衡的是
a.体系中的压强不发生变化
b.v正(H2)=v逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO2的浓度不再发生变化
②在某温度下,反应物的起始浓度分别为:c(CO)=1mol•L﹣1,c(H2O)=2.4mol•L﹣1;达到平衡后,CO的转化率为60%,该温度下的化学平衡常数为
您最近一年使用:0次