1 . 下列实验中,现象及结论都正确,且二者之间有因果关系的是()
选项 | 实验操作 | 现象 | 结论 |
A | 把水滴入盛有少量 的试管中,立即把带火星的木条放在试管口 的试管中,立即把带火星的木条放在试管口 | 木条复燃 | 反应生成了 |
B | 将稀硝酸加入过量铁粉中,充分反应后滴加 溶液 溶液 | 有气体生成,溶液呈棕黄色 | 稀硝酸将 氧化为 氧化为 |
C | 往密闭容器中通入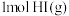 ,达到平衡后,压缩容器体积 ,达到平衡后,压缩容器体积 | 混合气体颜色加深 | 压缩体积,有利于反应往生成 的方向进行 的方向进行 |
D | 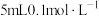 酸性 酸性 溶液与 溶液与 溶液充分混合 溶液充分混合 | 混合溶液呈粉红色 | 该反应是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 汽车尾气的污染不容忽视,对汽车尾气中污染气体 和
和 的转化是研究热点。回答下列问题:
的转化是研究热点。回答下列问题:
Ⅰ.利用铑催化处理汽车尾气中的 与
与 的化学反应方程式为
的化学反应方程式为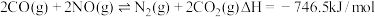 。
。
(1)已知该反应的逆反应活化能为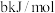 ,则其正反应活化能为
,则其正反应活化能为___________  。
。
(2)一定温度下,在 恒容密闭容器中充入
恒容密闭容器中充入 和
和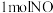 发生上述反应,部分物质的体积分数(φ)随时间(t)的变化如图所示。
发生上述反应,部分物质的体积分数(φ)随时间(t)的变化如图所示。
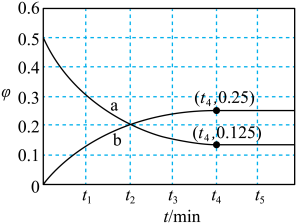
①用 的浓度变化表示
的浓度变化表示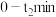 的平均反应速率为
的平均反应速率为___________ 。
②下列说法正确的是___________ (填选项字母)。
A.上述反应的正反应在低温下才能自发进行
B. 时,反应达到平衡状态
时,反应达到平衡状态
C.气体的平均相对分子质量: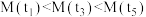
③ 还原
还原 的反应路径如图1所示,其中(s)指的是物质吸附在铑催化剂上,图2所示为随温度升高
的反应路径如图1所示,其中(s)指的是物质吸附在铑催化剂上,图2所示为随温度升高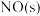 的解离速率,
的解离速率, 的生成速率,
的生成速率,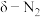 的生成速率以及
的生成速率以及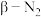 的生成速率变化曲线,根据图1可知生成
的生成速率变化曲线,根据图1可知生成 的基元反应有两个(
的基元反应有两个(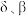 代表生成
代表生成 的两种不同路径),结合两图写出温度在
的两种不同路径),结合两图写出温度在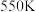 时生成
时生成 的主要基元反应方程式:
的主要基元反应方程式:___________ 。

Ⅱ.某研究小组探究催化剂对 转化率的影响。将
转化率的影响。将 和
和 按物质的量之比
按物质的量之比 以一定的流速通过两种不同的催化剂进行反应曲线Ⅰ和Ⅱ,相同时间内测量逸出气体中
以一定的流速通过两种不同的催化剂进行反应曲线Ⅰ和Ⅱ,相同时间内测量逸出气体中 含量,从而确定尾气脱氮率(即
含量,从而确定尾气脱氮率(即 的转化率),结果如图所示:
的转化率),结果如图所示:
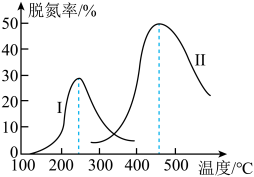
(3)温度低于 时,图中曲线Ⅰ脱氨率随温度升高变化不大的主要原因是
时,图中曲线Ⅰ脱氨率随温度升高变化不大的主要原因是___________ 。
(4) 时,平衡脱氨率为50%,压强恒为p,则
时,平衡脱氨率为50%,压强恒为p,则
___________ (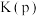 为以分压表示的平衡常数,用含p的代数式表示)。
为以分压表示的平衡常数,用含p的代数式表示)。
(5) 以后脱氮率下降的原因可能是
以后脱氮率下降的原因可能是___________ ,___________ 。
 和
和 的转化是研究热点。回答下列问题:
的转化是研究热点。回答下列问题:Ⅰ.利用铑催化处理汽车尾气中的
 与
与 的化学反应方程式为
的化学反应方程式为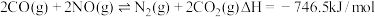 。
。(1)已知该反应的逆反应活化能为
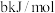 ,则其正反应活化能为
,则其正反应活化能为 。
。(2)一定温度下,在
 恒容密闭容器中充入
恒容密闭容器中充入 和
和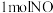 发生上述反应,部分物质的体积分数(φ)随时间(t)的变化如图所示。
发生上述反应,部分物质的体积分数(φ)随时间(t)的变化如图所示。
①用
 的浓度变化表示
的浓度变化表示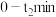 的平均反应速率为
的平均反应速率为②下列说法正确的是
A.上述反应的正反应在低温下才能自发进行
B.
 时,反应达到平衡状态
时,反应达到平衡状态C.气体的平均相对分子质量:
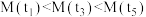
③
 还原
还原 的反应路径如图1所示,其中(s)指的是物质吸附在铑催化剂上,图2所示为随温度升高
的反应路径如图1所示,其中(s)指的是物质吸附在铑催化剂上,图2所示为随温度升高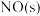 的解离速率,
的解离速率, 的生成速率,
的生成速率,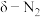 的生成速率以及
的生成速率以及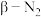 的生成速率变化曲线,根据图1可知生成
的生成速率变化曲线,根据图1可知生成 的基元反应有两个(
的基元反应有两个(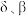 代表生成
代表生成 的两种不同路径),结合两图写出温度在
的两种不同路径),结合两图写出温度在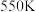 时生成
时生成 的主要基元反应方程式:
的主要基元反应方程式:
Ⅱ.某研究小组探究催化剂对
 转化率的影响。将
转化率的影响。将 和
和 按物质的量之比
按物质的量之比 以一定的流速通过两种不同的催化剂进行反应曲线Ⅰ和Ⅱ,相同时间内测量逸出气体中
以一定的流速通过两种不同的催化剂进行反应曲线Ⅰ和Ⅱ,相同时间内测量逸出气体中 含量,从而确定尾气脱氮率(即
含量,从而确定尾气脱氮率(即 的转化率),结果如图所示:
的转化率),结果如图所示:
(3)温度低于
 时,图中曲线Ⅰ脱氨率随温度升高变化不大的主要原因是
时,图中曲线Ⅰ脱氨率随温度升高变化不大的主要原因是(4)
 时,平衡脱氨率为50%,压强恒为p,则
时,平衡脱氨率为50%,压强恒为p,则
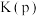 为以分压表示的平衡常数,用含p的代数式表示)。
为以分压表示的平衡常数,用含p的代数式表示)。(5)
 以后脱氮率下降的原因可能是
以后脱氮率下降的原因可能是
您最近一年使用:0次
名校
3 . 由γ-羟基丁酸生成γ-丁内酯的反应为HOCH2CH2CH2COOH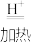
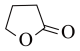 +H2O △H<0,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:
+H2O △H<0,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:

(1)该反应的平衡常数表达式为:___________ ,达到平衡后,升高温度,平衡___________ 移动(填“正向”“不”或“逆向)。
(2)在120min时,γ-羟基丁酸的转化率为___________ 。
(3)为提高平衡时γ-羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施___________ 。
(4)25℃时,该反应的平衡常数K=___________ (结果保留两位小数),在25℃时,当γ-丁内酯与γ-羟基丁酸的物质的量浓度之比保持不变时,反应___________ 达到平衡(填“一定”或“不一定”)。
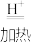
 +H2O △H<0,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:
+H2O △H<0,在298K下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:
(1)该反应的平衡常数表达式为:
(2)在120min时,γ-羟基丁酸的转化率为
(3)为提高平衡时γ-羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施
(4)25℃时,该反应的平衡常数K=
您最近一年使用:0次
名校
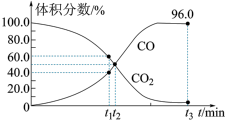
4 . 某固定容积的密闭容器中发生反应: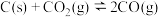 。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
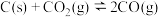 。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
A. 时,CO2的转化率为20.0% 时,CO2的转化率为20.0% |
B. 时,该反应体系处于平衡状态 时,该反应体系处于平衡状态 |
C. 时,向该容器中再充入CO2和CO各1.0 mol·L-1,平衡逆向移动 时,向该容器中再充入CO2和CO各1.0 mol·L-1,平衡逆向移动 |
D. 时,该反应的 时,该反应的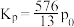 [气体分压(p分)=气体总压(p总)×体积分数] [气体分压(p分)=气体总压(p总)×体积分数] |
您最近一年使用:0次
名校
5 . 在一定温度下,加入A和B发生反应 ,下列叙述能说明反应达到平衡的标志的是
,下列叙述能说明反应达到平衡的标志的是
①D与C的浓度之比保持不变
②单位时间内生成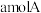 ,同时生成
,同时生成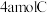
③A、B、C的质量分数不再变化
④恒容容器,混合气体的密度不再变化
⑤恒容容器,混合气体的总压强不再变化
⑥恒压容器,混合气体的平均摩尔质量不再变化
 ,下列叙述能说明反应达到平衡的标志的是
,下列叙述能说明反应达到平衡的标志的是①D与C的浓度之比保持不变
②单位时间内生成
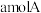 ,同时生成
,同时生成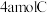
③A、B、C的质量分数不再变化
④恒容容器,混合气体的密度不再变化
⑤恒容容器,混合气体的总压强不再变化
⑥恒压容器,混合气体的平均摩尔质量不再变化
| A.①②③④⑤ | B.②③④⑥ | C.①③④⑤⑥ | D.③④⑤⑥ |
您最近一年使用:0次
名校
6 . 一定温度下,0.2molA(g)和0.2molB(s)在容积为2L的恒容密闭容器中发生反应: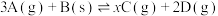 ,一段时间后反应达到平衡,此时C的浓度为
,一段时间后反应达到平衡,此时C的浓度为 ,同时生成0.08molD,下列叙述中错误的是
,同时生成0.08molD,下列叙述中错误的是
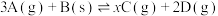 ,一段时间后反应达到平衡,此时C的浓度为
,一段时间后反应达到平衡,此时C的浓度为 ,同时生成0.08molD,下列叙述中错误的是
,同时生成0.08molD,下列叙述中错误的是| A.该温度下,反应达到平衡状态时,相同条件下容器内气体的压强与起始时的压强比为6:5 |
B.当 时,该反应达到化学平衡状态 时,该反应达到化学平衡状态 |
C.该温度下反应的平衡常数为 |
| D.该温度下,反应达到平衡状态时,A(g)的转化率为60% |
您最近一年使用:0次
2023-10-05更新
|
245次组卷
|
3卷引用:吉林省部分名校2023-2024学年高二上学期10月联考化学试题
名校
7 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 肼 肼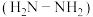 中含有的孤电子对数为 中含有的孤电子对数为 |
B. 含有的电子总数为 含有的电子总数为 |
C.足量 与含 与含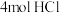 的浓盐酸充分反应,转移的电子数为 的浓盐酸充分反应,转移的电子数为 |
D. 和 和 于密闭容器中充分反应后, 于密闭容器中充分反应后, 分子总数为 分子总数为 |
您最近一年使用:0次
2023-09-28更新
|
42次组卷
|
3卷引用:吉林省四平市第一高级中学2023-2024学年高三上学期10月月考化学试题
8 .  是一种重要的化工原料,广泛应用于化工生产,根据所学回答下列问题:
是一种重要的化工原料,广泛应用于化工生产,根据所学回答下列问题:
(1)工业上制备甲醇的反应方程式为: ,某温度下,将1mol
,某温度下,将1mol  和3mol
和3mol  充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
①用 表示前2h的平均反应速率
表示前2h的平均反应速率
___________ 。
②该温度下, 的平衡转化率为
的平衡转化率为___________ 。
③在一定条件下,下列说法说明该可逆反应达到平衡状态的是___________ (填字母)。
A.容器中气体密度不变 B.容器中气体平均摩尔质量不变
C. D.形成2mol C=O同时断裂3mol H-H键
D.形成2mol C=O同时断裂3mol H-H键
④在温度为T,压强为P的条件下,将 和
和 按物质的量之比为1∶3通入一恒压密闭容器中发生上述反应,达到平衡时,测得
按物质的量之比为1∶3通入一恒压密闭容器中发生上述反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
________ (用含P的表达式表示,其中用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2) 制备与丙烯的反应为:
制备与丙烯的反应为: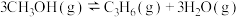 ,速率常数k与反应温度T的关系遵循Arrhenius方程,已知Arrhenius方程为:
,速率常数k与反应温度T的关系遵循Arrhenius方程,已知Arrhenius方程为: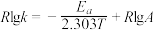 (其中k为速率常数,反应速率与其成正比;
(其中k为速率常数,反应速率与其成正比; 为活化能:
为活化能: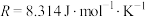 ,A为常数)。
,A为常数)。
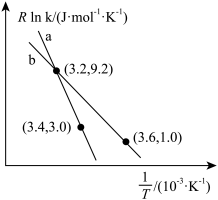
若实验时改变界条件,测得实验数据为如上图曲线b所示,则可能改变的外界条件是_______(填标号)
 是一种重要的化工原料,广泛应用于化工生产,根据所学回答下列问题:
是一种重要的化工原料,广泛应用于化工生产,根据所学回答下列问题:(1)工业上制备甲醇的反应方程式为:
 ,某温度下,将1mol
,某温度下,将1mol  和3mol
和3mol  充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:| 时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
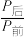 | 0.90 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
 表示前2h的平均反应速率
表示前2h的平均反应速率
②该温度下,
 的平衡转化率为
的平衡转化率为③在一定条件下,下列说法说明该可逆反应达到平衡状态的是
A.容器中气体密度不变 B.容器中气体平均摩尔质量不变
C.
 D.形成2mol C=O同时断裂3mol H-H键
D.形成2mol C=O同时断裂3mol H-H键④在温度为T,压强为P的条件下,将
 和
和 按物质的量之比为1∶3通入一恒压密闭容器中发生上述反应,达到平衡时,测得
按物质的量之比为1∶3通入一恒压密闭容器中发生上述反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
(2)
 制备与丙烯的反应为:
制备与丙烯的反应为: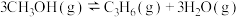 ,速率常数k与反应温度T的关系遵循Arrhenius方程,已知Arrhenius方程为:
,速率常数k与反应温度T的关系遵循Arrhenius方程,已知Arrhenius方程为: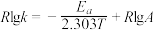 (其中k为速率常数,反应速率与其成正比;
(其中k为速率常数,反应速率与其成正比; 为活化能:
为活化能: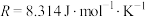 ,A为常数)。
,A为常数)。
若实验时改变界条件,测得实验数据为如上图曲线b所示,则可能改变的外界条件是_______(填标号)
| A.升高温度 | B.增大压强 | C.增大 | D.更换合适的催化剂 |
您最近一年使用:0次
名校
解题方法
9 . 在恒温恒容密闭容器中加入足量的Fe2O3(g)和CO(g),模拟炼铁高炉中的反应: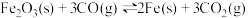 ,下列情况表明该可逆反应达到平衡状态的是
,下列情况表明该可逆反应达到平衡状态的是
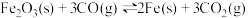 ,下列情况表明该可逆反应达到平衡状态的是
,下列情况表明该可逆反应达到平衡状态的是| A.容器中气体的压强不再改变 | B.容器中气体变化的密度不再改变 |
| C.Fe2O3的浓度比不再改变 | D.CO和CO2的正反应速率相等 |
您最近一年使用:0次
2023-09-11更新
|
241次组卷
|
3卷引用:吉林省普通高中友好学校联合体2023-2024学年高二上学期期中联考化学试题
2014·山东济南·一模
10 . 在容积一定的密闭容器中,置入一定量的NO(g)和足量C(s),发生反应C(s)+2NO(g) CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度与温度T的关系如图所示。则下列说法正确的是
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度与温度T的关系如图所示。则下列说法正确的是

 CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度与温度T的关系如图所示。则下列说法正确的是
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度与温度T的关系如图所示。则下列说法正确的是
| A.该反应的ΔH>0 |
| B.若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
| C.在T2时,若反应体系处于状态D,则此时一定有v(正)<v(逆) |
| D.在T3时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 |
您最近一年使用:0次
2023-08-27更新
|
2355次组卷
|
54卷引用:吉林省长春市第二实验中学2022-2023学年高二上学期期中考试化学试题
吉林省长春市第二实验中学2022-2023学年高二上学期期中考试化学试题(已下线)2013-2014山东省济南市高三5月针对性训练理综化学试卷2015-2016学年安徽省六安一中高二上第一阶段测化学试卷【全国百强校】福建省厦门外国语学校2018-2019学年高二下学期第一次月考化学试题黑龙江省牡丹江市第三高级中学2019-2020学年高二10月月考化学试题湖南省岳阳市岳阳县一中、汨罗市一中2019-2020学年高二10月联考化学试题黑龙江省绥化市青冈县第一中学2019-2020学年高二上学期(A)班月考化学试题山东省淄博市淄川中学2019-2020学年高二上学期期中考试化学试题贵州省遵义市南白中学2019-2020学年高二上学期期中考试化学试题福建省厦门双十中学2020届高三上学期期中考试化学试题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题安徽省枞阳县浮山中学2019-2020学年高二上学期期中考试化学试题湖南省张家界市2019-2020学年高二上学期期末考试化学试题陕西省渭南市瑞泉中学2019-2020学年高二上学期第一次月考化学试题(已下线)考点10 化学平衡常数及其图象分析-2020年高考化学命题预测与模拟试题分类精编江苏省苏州市相城区陆慕高级中学2019-2020高二下学期4月质量检测化学试题贵州省北京师范大学遵义附属学校2019-2020学年高二下学期第二次月考化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末考试化学试题湖南省长沙市南雅中学2020-2021学年度高二上学期入学考试化学试题河南省漯河市漯河实验高中2020-2021学年高二上学期期中考试化学试题河北省张家口宣化一中2020-2021学年高二上学期12月月考化学试题湖南省长沙宁乡市第十高级中学2020-2021学年高二上学期10月月考化学试题山东省2021-2022学年高二12月“山东学情”联考(鲁科版)化学试题(已下线)综合复习与测试(1)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)福建省莆田第二十五中学2021-2022学年高二上学期期末考试化学试题湖南省益阳市箴言中学2021-2022学年高二下学期入学考试化学检测题(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用) 陕西省咸阳市武功县2021--2022学年高二上学期质量调研化学试题山东省济北中学2021-2022学年高三上学期11月阶段性检测化学试题四川省成都市树德中学2022-2023学年高二上学期10月月考化学试题浙江省舟山市舟山中学2022-2023学年高二上学期阶段性质量监测化学试题陕西省安康市白河高中2021-2022学年高二上学期期末考试化学试题 广西钦州市2022-2023学年高二上学期第2次教学质量监测化学试卷浙江省杭师大附中2022-2023学年高二上学期期中考试 化学试题四川省广元中学2022-2023学年高二上学期期中考试化学试题重庆市荣昌永荣中学校2021-2022学年高二上学期期末考试化学试题四川省广安市第二中学校2022-2023学年高二下学期第一次月考化学试题陕西师范大学附属中学2022-2023学年高一下学期6月期末考试化学试题章末检测卷(二)化学反应的方向、限度与速率辽宁省铁岭市昌图县第一高级中学2022-2023学年高一下学期期末考试化学试题陕西省洛南中学2022-2023学年高二上学期10月月考化学试题重庆市长寿中学校2022-2023学年高二下学期4月期中考试化学试题新疆塔城地区第一高级中学2023-2024学年高二上学期9月月考化学试题(已下线)实验03 探究外界条件对化学平衡移动的影响-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)甘肃省天水市第一中学2023-2024学年高二上学期10月月考化学试题(已下线)专题05 影响化学平衡的因素【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)【精品卷】2.2.3 影响化学平衡的因素课堂例题-人教版2023-2024学年选择性必修1江西省宜春市上高二中2023-2024学年高二上学期第一次月考化学试题广西柳州高级中学2023-2024学年高三上学期10月月考化学试题河北定州中学2023-2024学年高二上学期12月月考化学试题内蒙古赤峰二中2023-2024学年高二上学期10月月考化学试题新疆石河子第一中学2023-2024学年高三上学期11月月考化学试题陕西省渭南市杜桥中学2023-2024学年高二上学期期中考试化学试卷 安徽省淮北市第一中学2023-2024学年高二上学期第三次月考化学试题



