1 . 化学是一门以实验为基础的学科。下列实验方法或操作能达到目的的是
选项 | 目的 | 实验操作 |
A | 探究温度对化学平衡的影响 | 加热 |
B | 探究浓度对化学反应速率的影响 | 取相同体积不同浓度的NaClO溶液,分别加入同体积同浓度的 |
C | 证明: | 向2mL0.01mol/L |
D | 获得纯净干燥的氯气 | 将混有氯化氢和水蒸气的氯气依次通过浓硫酸和饱和食盐水 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列实验装置,可以达到实验目的的是
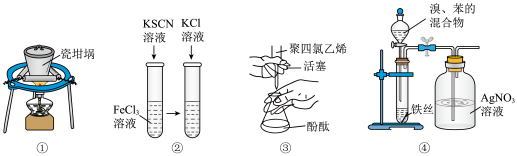

| A.①装置可用于熔融NaOH |
B.②可以探究KCl浓度是否对FeCl3+3KSCN Fe(SCN)3+3KCl的平衡移动有影响 Fe(SCN)3+3KCl的平衡移动有影响 |
| C.③可用于氢氧化钠标准溶液滴定未知浓度的盐酸 |
| D.④可以证明溴和苯发生的是取代反应而不是加成反应 |
您最近半年使用:0次
名校
3 . 根据措施或事实,下列有关解释错误的是
| 选项 | 措施或事实 | 相关解释 |
| A | Na着火不能用CO2灭火 | Na会与CO2反应生成O2 |
| B | 在实验室配制Na2S溶液时,常滴加几滴NaOH浓溶液 | 抑制 的水解 的水解 |
| C | 当面粉在相对密闭的空间内悬浮在空气中达到一定浓度时,遇火会发生爆炸 | 增大接触面积,可加快化学反应速率 |
| D | 工业盐酸因含 呈亮黄色,为证明这种配离子只有在高浓度 呈亮黄色,为证明这种配离子只有在高浓度 条件下才稳定,可向其中滴加AgNO3溶液观察现象 条件下才稳定,可向其中滴加AgNO3溶液观察现象 | 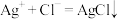 ,AgNO3可有效降低 ,AgNO3可有效降低 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究温度对化学平衡的影响 | 加热0.5 mol·L  溶液 溶液 |
| B | 证明干燥的氯气不具有漂白性 | 将干燥的氯气通入盛有红色鲜花的集气瓶中 |
| C | 证明溴与苯发生了取代反应 | 向溴水中加入苯,振荡后静置,水层颜色变浅 |
| D | 验证还原性: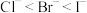 | 向NaCl、KI的混合溶液中加入少量溴水和 ,振荡,四氯化碳层为紫色 ,振荡,四氯化碳层为紫色 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . 室温下,1体积的水能溶解约2体积的Cl2.用试管收集Cl2后进行如图所示实验,下列对实验现象的分析或预测正确的是
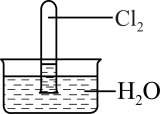
| A.试管内液面上升,证明Cl2与水发生了反应 |
| B.取出试管中的溶液,加入少量CaCO3粉末,溶液漂白能力减弱 |
C.取出试管中的溶液,光照一段时间后pH下降,与反应2HClO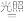 2HCl+O2↑有关 2HCl+O2↑有关 |
| D.取出试管中的溶液,滴加紫色石蕊溶液,溶液先变红后褪色,加热后颜色又变为红色 |
您最近半年使用:0次
6 . 下列实验操作、现象和解释或结论完全正确的是
| 选项 | 实验操作 | 解释或结论 |
| A | 将含有二氧化硫的气体通入酸性高锰酸钾中,然后加入足量氯化钡溶液。 | 通过测定白色沉淀的质量,可推算二氧化硫的物质的量 |
| B | 实验室用浓硫酸和乙醇制取乙烯,将产生的气体通入溴水中。 | 若溴水褪色,则证明混合气体中有乙烯 |
| C | 向盛有2 mL 0.1mol/L 溶液的试管中滴加2~4滴0.1mol/L NaOH溶液,产生白色沉淀,向上层清液中滴加4滴0.1mol/L 溶液的试管中滴加2~4滴0.1mol/L NaOH溶液,产生白色沉淀,向上层清液中滴加4滴0.1mol/L 溶液,生成红褐色沉淀。 溶液,生成红褐色沉淀。 | 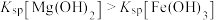 |
| D | 把 和 和 的混合气体通入两只连通的烧瓶,一只烧瓶浸泡在热水中,另一只浸泡在冰水中。浸泡在热水中的烧瓶内红棕色加深。 的混合气体通入两只连通的烧瓶,一只烧瓶浸泡在热水中,另一只浸泡在冰水中。浸泡在热水中的烧瓶内红棕色加深。 | 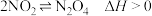 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7日内更新
|
102次组卷
|
2卷引用:东北三省四市教研联合体2024届高三下学期高考模拟(二)化学试题
名校
解题方法
7 . 下列实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 快速拉伸装有 的针筒活塞,气体颜色变浅 的针筒活塞,气体颜色变浅 | 证明压强改变对平衡的影响 |
| B | 常温下,测物质的量浓度相等的HA和HB溶液的 | 比较HA与HB的酸性强弱 |
| C | 用 稀硫酸与足量纯锌反应,产生气泡速率较慢,加入 稀硫酸与足量纯锌反应,产生气泡速率较慢,加入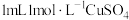 溶液后,迅速产生较多气泡 溶液后,迅速产生较多气泡 | 证明反应速率会随反应物浓度的增大而加快 |
| D | 向 硝酸银溶液中加入 硝酸银溶液中加入 溶液,出现白色沉淀,再加入几滴 溶液,出现白色沉淀,再加入几滴 的 的 溶液,有黑色沉淀生成 溶液,有黑色沉淀生成 | 证明在相同温度下的 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
8 . 近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下列事实中,能证明氢硫酸的酸性比亚硫酸的酸性弱的是___________(填标号)。
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为___________ 、___________ ,
制得等量H2所需能量较少的是___________ 。
(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①向反应器中再分别充入下列气体,能使H2S转化率增大的是___________ (填标号)。
A.H2S B.CO2 C.COS D.N2
②求610 K时,该反应的平衡常数K=___________ (写出详细的解答过程)。
(1)下列事实中,能证明氢硫酸的酸性比亚硫酸的酸性弱的是___________(填标号)。
| A.氢硫酸能还原亚硫酸生成硫单质和水 |
| B.0.10 mol·L−1的氢硫酸和亚硫酸的pH分别为4.5和2.1 |
| C.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以 |
| D.氢硫酸的导电能力低于亚硫酸 |

通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为
制得等量H2所需能量较少的是
(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g)
 COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。①向反应器中再分别充入下列气体,能使H2S转化率增大的是
A.H2S B.CO2 C.COS D.N2
②求610 K时,该反应的平衡常数K=
您最近半年使用:0次
解题方法
9 . 下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将盛有NO2气体的玻璃球放入热水浴中 | 探究2NO2(g) N2O4(g)的热效应 N2O4(g)的热效应 |
| B | 向各盛有5mLH2O2溶液的两支试管中分别滴入2滴0.1mol/L的FeCl3溶液和0.1mol/L的CuSO4溶液 | 比较Fe3+与Cu2+对H2O2分解的催化效果 |
| C | 向盛有淀粉溶液的试管中加入少量稀硫酸,加热,再滴加几滴银氨溶液,水浴加热 | 证明淀粉已发生水解 |
| D | 向5mL0.1mol/LAgNO3溶液中滴加几滴0.1mol/L NaCl溶液,再滴加几滴0.1mol/LKI溶液 | 验证Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 某校化学学习小组探究 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题:
(1)写出实验中制备 的化学方程式
的化学方程式________ 。
(2)配制100mL
 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和________ 。
【实验探究】
向3mL
 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
猜想1: 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;
猜想2: 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。
(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,________ ,证明猜想1不成立。
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。
已知:常温下,溶液中 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。________ (填写微粒符号),依据的实验证据是________ 。
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度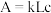 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验结果讨论:若 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若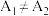 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。
(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如: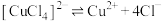 。
。
丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为: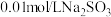 溶液,
溶液,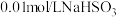 溶液,
溶液, 固体,
固体,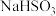 固体
固体
 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题: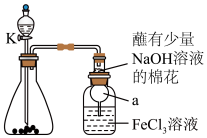
(1)写出实验中制备
 的化学方程式
的化学方程式(2)配制100mL

 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和【实验探究】
向3mL

 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:猜想1:
 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;猜想2:
 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是
 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。组别 | 溶液1(1mL) | 溶液2(2mL) | 现象 |
a |
|
| 溶液1和溶液2混合后,组别a、b、c所得溶液红棕色依次加深。 |
b |  的饱和溶液,用 的饱和溶液,用 固体调节. 固体调节. | ||
c |  的饱和溶液,用 的饱和溶液,用 固体调节 固体调节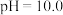 |
 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。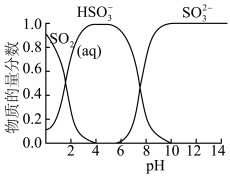
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度
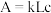 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验序号 | 操作 | 吸光度 |
1 | 把1mL 0.1mol/L 溶液与2mL 溶液与2mL 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 |
|
2 |
|
 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若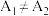 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如:
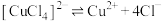 。
。丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为:
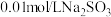 溶液,
溶液,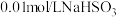 溶液,
溶液, 固体,
固体,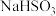 固体
固体实验序号 | 操作 | 吸光度 | 结论 |
3 | 向3mL 0.1mol/L 溶液中通入 溶液中通入 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 |
| |
4 |
  (填“大于”、“小于”或“等于”) (填“大于”、“小于”或“等于”) | 平衡向 |
您最近半年使用:0次

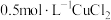 溶液
溶液
 溶液,有白色沉淀生成,再滴入0.01mol/L
溶液,有白色沉淀生成,再滴入0.01mol/L 溶液,有黑色沉淀生成
溶液,有黑色沉淀生成 溶液
溶液



