名校
1 . 某同学研究浓度对化学平衡的影响,下列说法不正确的是
已知: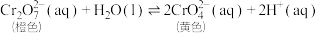 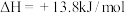 | |
| 实验步骤 | 实验现象 |
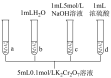 | ⅰ.待试管b中颜色不变后与试管a比较,试管b中橙色比试管a中的浅; ⅱ.待试管c中颜色不变后与试管b比较,试管c中的颜色比试管b中的浅; ⅲ.滴加浓硫酸,试管d温度略有升高,溶液颜色与试管b中的相比,变深 |
| A.试管b中的现象说明加水后平衡正向移动 |
| B.该实验能证明减小生成物浓度,平衡正向移动 |
| C.“待试管c中溶液颜色不变”的目的是使反应达到平衡状态 |
D.试管d中的现象能说明影响平衡的主要因素是 增大 增大 |
您最近半年使用:0次
名校
2 . 小组同学探究盐溶液对反应 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
ii. (黄色)
(黄色)
iii.已知 对实验无影响
对实验无影响
下列说法不正确的是
 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。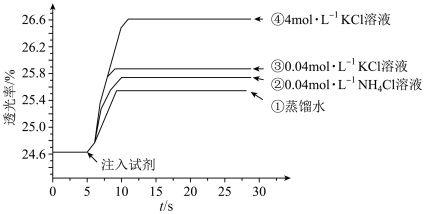
ii.
 (黄色)
(黄色)iii.已知
 对实验无影响
对实验无影响下列说法不正确的是
A.注入试剂①后溶液透光率增大,证明 逆向移动 逆向移动 |
B.透光率③比②高,可能是阳离子种类或溶液 不同导致的 不同导致的 |
C.透光率④比③高,可能发生了反应 |
D.若要证明试剂③中 对平衡体系有影响,还应使用 对平衡体系有影响,还应使用 的 的 溶液进行对照实验 溶液进行对照实验 |
您最近半年使用:0次
2023-11-21更新
|
337次组卷
|
7卷引用:北京市对外经济贸易大学附属中学2022-2023学年高二上学期期中考试化学试题
3 . 探究浓度对化学平衡的影响,某同学进行如图实验。下列说法不正确的是
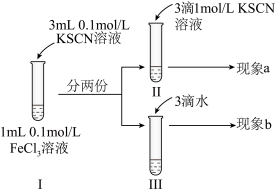

| A.该实验通过观察颜色变化来判断生成物浓度的变化 |
| B.实验Ⅱ中加3滴KSCN溶液后溶液颜色变深,说明平衡常数变大 |
| C.观察到现象a比现象b中红色更深,即可证明增加反应物浓度,平衡正向移动 |
| D.实验Ⅲ加3滴水的目的是保证体积与实验Ⅱ一致,是对比实验 |
您最近半年使用:0次
2023-11-18更新
|
159次组卷
|
2卷引用:福建省漳州市十校2023-2024学年高二上学期期中联考化学试题
4 . 关于如图所示实验的说法,正确的是
|
|
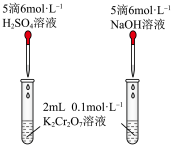
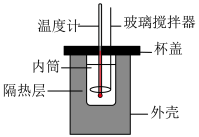
| i.推测CH3COOH的Ka和H2CO3的Ka1的大小 | ii.研究c(H+)对Cr2O 、CrO 、CrO 相互转化的影响 相互转化的影响 |
|
|
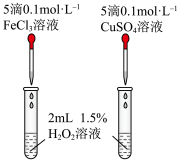
| iii.测定稀盐酸与NaOH溶液中和的反应热 | iv.比较Fe3+与Cu2+对H2O2分解反应的催化效果 |
A.图i反应的离子方程式为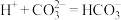 |
B.图ii证明增大 有利于增大 有利于增大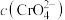 ,减小 ,减小 |
| C.图iii中去隔热层不保温,测得的反应热偏小 |
D.图iv中将 溶液换为 溶液换为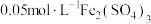 溶液更为合理 溶液更为合理 |
您最近半年使用:0次
名校
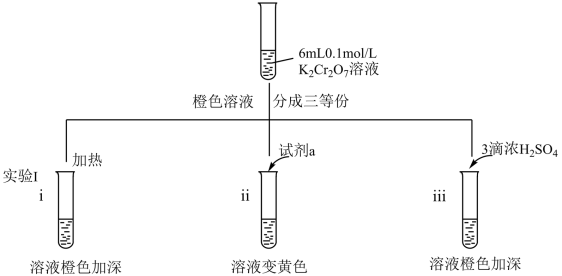
5 . 某兴趣小组以重铬酸钾⟨ )溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法不正确的是
)溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法不正确的是
已知:① 溶液存在平衡:
溶液存在平衡: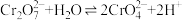 。
。
②含铬元素的离子在溶液中的颜色: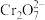 (橙色);
(橙色); (黄色);
(黄色); (绿色)。
(绿色)。
 )溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法不正确的是
)溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法不正确的是
已知:①
 溶液存在平衡:
溶液存在平衡: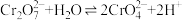 。
。②含铬元素的离子在溶液中的颜色:
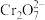 (橙色);
(橙色); (黄色);
(黄色); (绿色)。
(绿色)。A.ⅰ可证明反应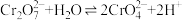 的正反应放热 的正反应放热 |
B.ⅱ是验证“只降低生成物的浓度,该平衡正向移动”,试剂 可以是 可以是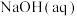 |
| C.向ⅲ所得橙色溶液中加入乙醇,溶液将由橙色变为绿色 |
| D.ⅲ平衡逆向移动可能原因不仅仅是增大了生成物的浓度 |
您最近半年使用:0次
名校
解题方法
6 . 25℃时,向40 mL 0.05 mol/L的 溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(体积变化忽略不计),发生反应
溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(体积变化忽略不计),发生反应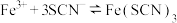 ,混合溶液中
,混合溶液中 与反应时间(t)的变化如图所示。下列说法不正确的是
与反应时间(t)的变化如图所示。下列说法不正确的是
 溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(体积变化忽略不计),发生反应
溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(体积变化忽略不计),发生反应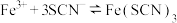 ,混合溶液中
,混合溶液中 与反应时间(t)的变化如图所示。下列说法不正确的是
与反应时间(t)的变化如图所示。下列说法不正确的是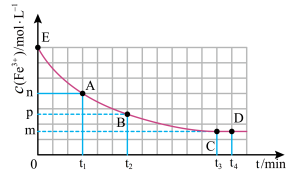
A. 时向溶液中加入50 mL 0.1 mol/L KCl溶液,平衡逆向移动。 时向溶液中加入50 mL 0.1 mol/L KCl溶液,平衡逆向移动。 |
| B.E点对应的坐标为(0,0.04) |
C.在25℃时该反应的平衡常数为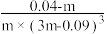 |
D. 分钟后加入少量KSCN固体,溶液红色加深,该现象可以证明 分钟后加入少量KSCN固体,溶液红色加深,该现象可以证明 与SCN-的反应是可逆反应 与SCN-的反应是可逆反应 |
您最近半年使用:0次
2023-12-12更新
|
223次组卷
|
3卷引用:北京市第十二中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
7 . 为探究浓度对化学平衡的影响,某同学进行如下实验:
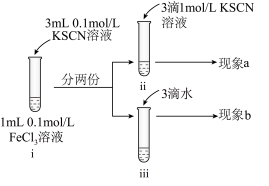
已知:i.中发生的化学反应为:
下列说法不正确 的是:

已知:i.中发生的化学反应为:

下列说法
| A.若i中加入KSCN溶液的体积改为2mL,不具有说服力,无法达到实验目的 |
| B.观察到现象a比现象b中红色更深,即可证明增加反应物浓度,平衡正向移动 |
| C.进行ii、iii对比实验的主要目的是防止由于溶液体积变化引起各离子浓度变化而干扰实验结论得出 |
| D.若将ii中加入试剂更换为3滴1mol/LKCl溶液,记为现象c,则平衡逆向移动,现象c比现象b红色更浅 |
您最近半年使用:0次
名校
8 . 甲烷水蒸气催化重整是制备高纯氢的方法之一、反应如下:
反应i.
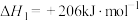 ;
;
反应ii.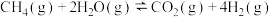
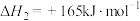 。
。
回答下列问题:
(1)反应iii. 的
的
________  ;若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高CO2转化率的措施有
;若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高CO2转化率的措施有________ ,下列说法可以证明该反应已达到平衡状态的是________ (填字母)。
a. b.容器内气体压强不再改变
b.容器内气体压强不再改变
c.H2的浓度不再改变 d.CO和H2O的浓度之比为1:1
(2)对于反应i,向体积为 的恒容密闭容器中,按
的恒容密闭容器中,按 投料。
投料。
①若在恒温条件下,反应达到平衡时CH4的转化率为50%,则平衡时容器内的压强与起始压强之比为___________ (最简单整数比)。
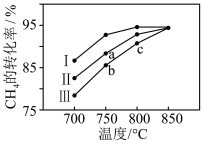
②其他条件相同时,在不同催化剂(I、Ⅱ、Ⅲ)作用下,反应相同时间,CH4的转化率随反应温度的变化如图所示。a点___________ (填“是”或“不是”)化学平衡状态。
(3)某科研小组研究了反应ii的动力学,获得其速率方程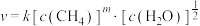 ,k为速率常数(只受温度影响),m为
,k为速率常数(只受温度影响),m为 的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
CH4的反应级数m=___________ ,当实验2进行到某时刻,测得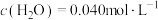 ,则此时的反应速率v=
,则此时的反应速率v=___________  (已知
(已知 )。
)。
(4)甲烷水蒸气催化重整制备高纯氢只发生反应i、反应ii.在恒温、恒压条件下,
 和
和
 反应达平衡时,
反应达平衡时, 的转化率为a,
的转化率为a, 的物质的量为
的物质的量为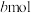 ,则反应i的平衡常数
,则反应i的平衡常数
___________ [写出含有a、b的计算式;对于反应 ,
,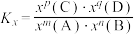 ,x为物质的量分数]。
,x为物质的量分数]。
反应i.

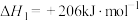 ;
;反应ii.
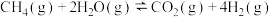
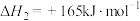 。
。回答下列问题:
(1)反应iii.
 的
的
 ;若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高CO2转化率的措施有
;若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高CO2转化率的措施有a.
 b.容器内气体压强不再改变
b.容器内气体压强不再改变c.H2的浓度不再改变 d.CO和H2O的浓度之比为1:1
(2)对于反应i,向体积为
 的恒容密闭容器中,按
的恒容密闭容器中,按 投料。
投料。①若在恒温条件下,反应达到平衡时CH4的转化率为50%,则平衡时容器内的压强与起始压强之比为
②其他条件相同时,在不同催化剂(I、Ⅱ、Ⅲ)作用下,反应相同时间,CH4的转化率随反应温度的变化如图所示。a点

(3)某科研小组研究了反应ii的动力学,获得其速率方程
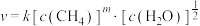 ,k为速率常数(只受温度影响),m为
,k为速率常数(只受温度影响),m为 的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:
的反应级数。在某温度下进行实验,测得各组分初浓度和反应初速率如下:| 实验序号 |  |  |  |
| 1 | 0.100 | 0.100 |  |
| 2 | 0.100 | 0.200 |  |
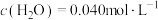 ,则此时的反应速率v=
,则此时的反应速率v= (已知
(已知 )。
)。(4)甲烷水蒸气催化重整制备高纯氢只发生反应i、反应ii.在恒温、恒压条件下,

 和
和
 反应达平衡时,
反应达平衡时, 的转化率为a,
的转化率为a, 的物质的量为
的物质的量为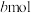 ,则反应i的平衡常数
,则反应i的平衡常数
 ,
,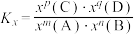 ,x为物质的量分数]。
,x为物质的量分数]。
您最近半年使用:0次
名校
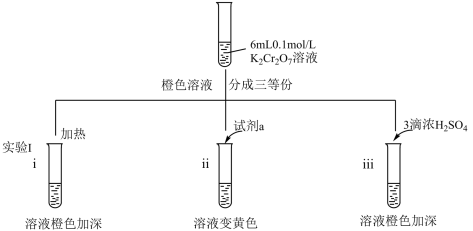
9 . 某兴趣小组以重铬酸钾(K2Cr2O7)溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法错误的是
已知:①K2Cr2O7溶液存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。
②含铬元素的离子在溶液中的颜色:Cr2O (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。
已知:①K2Cr2O7溶液存在平衡:Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。 ②含铬元素的离子在溶液中的颜色:Cr2O
 (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。 
A.i 可证明反应 Cr2O +H2O +H2O 2CrO 2CrO +2H+的正反应放热 +2H+的正反应放热 |
| B.ii 是验证“只降低生成物的浓度,该平衡正向移动”,试剂 a 可以是 NaOH |
| C.iii 平衡逆向移动仅仅是因为增大了生成物的浓度 |
| D.向 iii 所得橙色溶液中加入乙醇,溶液将由橙色变为绿色 |
您最近半年使用:0次
2023-08-26更新
|
402次组卷
|
4卷引用:山东省青岛第六十八中学2023-2024学年高二上学期期中考试化学试卷
名校
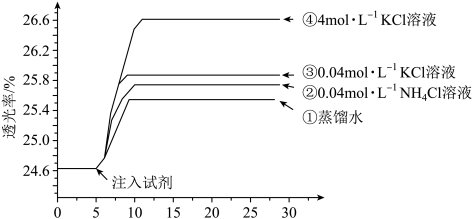
10 . 小组同学探究盐溶液对反应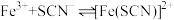 (血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
(血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
已知:ⅰ.溶液血红色越深,透光率越小,其它颜色对透光率的影响可忽略。
ⅱ. (黄色)
(黄色)
下列说法不正确的是
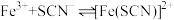 (血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
(血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。已知:ⅰ.溶液血红色越深,透光率越小,其它颜色对透光率的影响可忽略。
ⅱ.
 (黄色)
(黄色)
下列说法不正确的是
A.注入试剂①后溶液透光率增大,一定是由于 平衡逆向移动引起的 平衡逆向移动引起的 |
| B.透光率③比②高,可能是阳离子种类或溶液pH导致的 |
C.透光率④比③高,可能发生了反应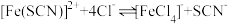 |
D.若要证明试剂③中Cl—对平衡体系有影响,还应使用与试剂③等体积的0.04mol/L的KNO3溶液进行对比实验(已知NO 对实验无影响) 对实验无影响) |
您最近半年使用:0次
2023-01-13更新
|
636次组卷
|
9卷引用:北京交通大学附属中学2022-2023学年高二上学期期中考试化学试题