名校
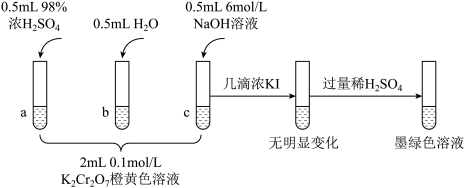
1 . 研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验:
已知:
资料1: (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+ △H=+13.8 kJ/mol;
(黄色)+2H+ △H=+13.8 kJ/mol;
资料2:+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
(1)试管c和b对比,推测试管c的现象是___________ 。
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?___________ (填“是”或“否”),理由是___________ 。
(3)对比试管a、b、c的实验现象,可知c(H+)增加时,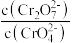
___________ (填“增大”,“减小”,“不变”)。
(4)试管c继续滴加KI溶液、过量稀H2SO4,写出此过程中氧化还原反应的离子方程式___________ 。

已知:
资料1:
 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+ △H=+13.8 kJ/mol;
(黄色)+2H+ △H=+13.8 kJ/mol;资料2:+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
(1)试管c和b对比,推测试管c的现象是
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?
(3)对比试管a、b、c的实验现象,可知c(H+)增加时,
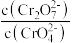
(4)试管c继续滴加KI溶液、过量稀H2SO4,写出此过程中氧化还原反应的离子方程式
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案不能达到相应目的的是
| A | B | C | D | |
| 目的 | 探究温度对化学平衡的影响 | 研究浓度对化学平衡的影响 | 实现铜棒镀银 | 证明化学反应存在一定的限度 |
| 实验方案 | 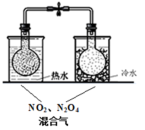 | 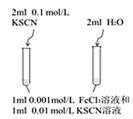 | 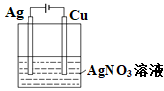 | 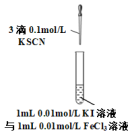 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-11-13更新
|
277次组卷
|
4卷引用:吉林省长春市希望高中2021-2022学年高二上学期期中考试化学试题
名校
3 . 环戊烯(C5H8)是一种重要的有机化工原料,可用环戊二烯(C5H6)制备。T℃时,将环戊二烯和HI按物质的量之比1:2充入容积为2L的恒容密闭容器中,仅发生反应: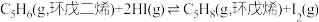 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是
已知:
反应Ⅰ: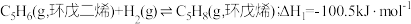
反应Ⅱ: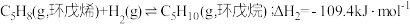
反应Ⅲ: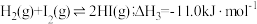
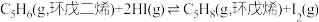 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是已知:
反应Ⅰ:
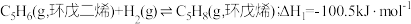
反应Ⅱ:
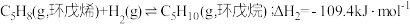
反应Ⅲ:
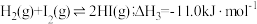
| A.该反应在高温下可自发进行 |
| B.升高温度,有利于提高环戊烯的平衡产率 |
| C.反应达到平衡时,环戊二烯和碘化氢的转化率相等 |
| D.降低温度,正反应速率改变程度大于逆反应速率改变程度 |
您最近一年使用:0次
名校
4 . 最新报道的“人工固氮”反应为: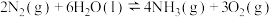 ,常压下测得该反应的部分数据如表所示。则关于该反应的说法中错误的是
,常压下测得该反应的部分数据如表所示。则关于该反应的说法中错误的是
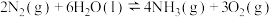 ,常压下测得该反应的部分数据如表所示。则关于该反应的说法中错误的是
,常压下测得该反应的部分数据如表所示。则关于该反应的说法中错误的是| T/℃ | 30 | 40 | 50 |
 的平衡浓度 的平衡浓度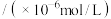 | 4.8 | 5.9 | 6.0 |
A.该反应的 |
B.常温下该反应的 |
C.反应在30℃、40℃时化学平衡常数分别为 、 、 ,则 ,则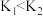 |
| D.在常温常压下,人工固氮比较容易进行 |
您最近一年使用:0次
2023-10-28更新
|
380次组卷
|
3卷引用:吉林省长春市东北师范大学附属中学2023-2024学年高二上学期10月期中化学试题
名校
解题方法
5 . 工业上在催化剂作用下可用 和
和 合成甲醇,其反应为
合成甲醇,其反应为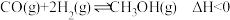 。一定条件下向一密闭容器中充入
。一定条件下向一密闭容器中充入 和
和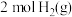 ,发生上述反应,
,发生上述反应, 的平衡转化率与温度、压强的关系如图所示,回答下列问题:
的平衡转化率与温度、压强的关系如图所示,回答下列问题:
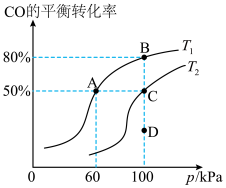
(1)该反应中反应物断键吸收的总能量___________ (填“>”“<”或“=”,下同)生成物成键放出的总能量;温度
___________  ;温度为
;温度为 时,D点反应速率:
时,D点反应速率:
___________  。
。
(2)下列说法可以表明该反应达到平衡状态的是___________ 。(填标号,下同)
a. 和
和 的物质的量之比不再改变
的物质的量之比不再改变
b. 的体积分数不再改变
的体积分数不再改变
c.断裂2个 键的同时有3个
键的同时有3个 键断裂
键断裂
d.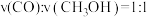
(3)在一恒容密闭容器中发生上述反应,其他条件不变,下列措施可以加快反应速率的是___________ (填序号,下同),能提高 平衡转化率的是
平衡转化率的是___________ 。
①升高温度 ②将 从体系中分离出来
从体系中分离出来
③充入 ,使体系总压强增大 ④再充入一定量的
,使体系总压强增大 ④再充入一定量的
(4)A、B、C三点中,正反应速率最大的是___________ (填“A”、“B”或“C”)点,该点对应的平衡常数
___________  (用最简分数表示;
(用最简分数表示; 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
 和
和 合成甲醇,其反应为
合成甲醇,其反应为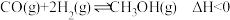 。一定条件下向一密闭容器中充入
。一定条件下向一密闭容器中充入 和
和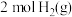 ,发生上述反应,
,发生上述反应, 的平衡转化率与温度、压强的关系如图所示,回答下列问题:
的平衡转化率与温度、压强的关系如图所示,回答下列问题:
(1)该反应中反应物断键吸收的总能量

 ;温度为
;温度为 时,D点反应速率:
时,D点反应速率:
 。
。(2)下列说法可以表明该反应达到平衡状态的是
a.
 和
和 的物质的量之比不再改变
的物质的量之比不再改变b.
 的体积分数不再改变
的体积分数不再改变c.断裂2个
 键的同时有3个
键的同时有3个 键断裂
键断裂d.
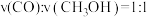
(3)在一恒容密闭容器中发生上述反应,其他条件不变,下列措施可以加快反应速率的是
 平衡转化率的是
平衡转化率的是①升高温度 ②将
 从体系中分离出来
从体系中分离出来③充入
 ,使体系总压强增大 ④再充入一定量的
,使体系总压强增大 ④再充入一定量的
(4)A、B、C三点中,正反应速率最大的是

 (用最简分数表示;
(用最简分数表示; 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
2023-11-04更新
|
192次组卷
|
3卷引用:吉林省松原市前郭县第五高级中学2023~2024学年高二上学期期中考试化学试题
11-12高二上·辽宁锦州·期末
6 . 在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
| A.反应达到平衡时,X的转化率为50% |
B.反应可表示为X+3Y 2Z,其平衡常数为1600 2Z,其平衡常数为1600 |
| C.增大压强使平衡向生成Z的方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
您最近一年使用:0次
2022-08-20更新
|
371次组卷
|
77卷引用:2011-2012学年吉林省扶余一中高二上学期期中考试化学试卷
(已下线)2011-2012学年吉林省扶余一中高二上学期期中考试化学试卷(已下线)2011-2012年湖南省醴陵二中、醴陵四中高二上学期期中考试化学试卷(已下线)2011-2012年广东东莞南城中学高二上学期期中考试化学试卷(已下线)2011-2012学年陕西省宝鸡中学高二下学期期中考试化学试题(已下线)2012-2013学年贵州省湄潭中学高二上学期期中考试化学试卷(已下线)2012-2013学年河南省河南大学附中高二上学期期中考试化学试卷(已下线)2013-2014学年江苏省常州市四校高二期中考试化学试卷(已下线)2013-2014吉林省白城市高二上学期期末考试化学(B卷)试卷(已下线)2014-2015学年山东安丘市实验中学期中考试高二化学模拟(B)卷(已下线)2014-2015学年山西省山大附中高二上学期期中化学试卷2014-2015学年河北省正定中学高一下学期期中化学试卷2015-2016学年黑龙江省红兴隆第一高级中学高二上期中理科化学试卷2015-2016学年河南省扶沟包屯高级中学高二上学期期中考试化学试卷2015-2016学年浙江省桐乡市高级中学高二上期中(普通班)化学试卷2016-2017学年黑龙江省鹤岗一中高二上学期期中化学试卷2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷河南省洛阳市2018届高三上学期期中考试化学试题山西省平遥中学2017-2018学年高二上学期期中考试化学试题【全国百强校】贵州省铜仁市第一中学2018-2019学年高二上学期期中考试化学试题浙江省宁波市咸祥中学2018-2019学年高二上学期期中考试化学试题广东省潮州市潮安区颜锡祺中学2019-2020学年高二上学期期中考试化学试题四川省自贡市田家炳中学2019-2020学年高二上学期期中考试化学试题山西省太原市第二十一中学2019-2020学年高二上学期期中考试化学试题吉林省长春市兴华中学2019-2020学年高二上学期期末考试化学试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期期中考试化学试题甘肃省民勤县第四中学2021-2022学年高二上学期期中考试(实验班)化学试题甘肃省民勤县第四中学2021-2022学年高二上学期期中考试化学试题新疆乌鲁木齐市第三十一中学2023-2024学年高二上学期期中考试化学试卷 (已下线)2010—2011学年辽宁省北镇高中高二上学期期末考试化学试卷(已下线)2010—2011学年安徽省合肥一中、6中、168中学高二下学期期末联考化学试卷(已下线)2012学年山东省潍坊市高二寒假作业化学试卷(四)(已下线)2011-2012学年江苏省南京三中高二下学期期末考试化学选修试卷(已下线)2011-2012学年安徽省无为县开城中学高二下学期期末考试化学试卷(已下线)2012-2013学年江西上饶中学高二第一次月考(潜能班)化学试卷(已下线)2013届山东省滨州市高三第一次(3月)模拟考试理综化学试卷(已下线)2014年高二化学人教版选修四 9化学平衡常数练习卷(已下线)2014高考名师推荐化学化学平衡常数(已下线)2015安徽望江中学同步课时练(人教选修4)2.3.3化学平衡常数试卷2014-2015陕西省西安市庆安高级中学高二上学期期末化学试卷2014—2015山东省泰安市高二上学期期末统考高二化学试卷2014-2015陕西省西安市七十中高二上学期期末考试化学试卷2015-2016学年河北大名县第一中学高二上学期第一次月考试化学试卷2015-2016学年山西省太原五中高二上12月月考化学试卷22015-2016学年河北省秦皇岛市卢龙县高二下学期期末化学试卷2016-2017学年河北省张家口万全中学高二上第一次月考化学试卷2016-2017学年广东省湛江一中高二上大考二化学卷2016-2017学年西藏拉萨中学高二上期末化学试卷2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷黑龙江省大庆市第十中学2016-2017学年高一下学期期末考试化学试题河南省襄城高中2017-2018学年高二9月月考化学试题安徽省定远重点中学2017-2018学年高一下学期第一次月考化学试题【全国市级联考】河南省洛阳市2017-2018学年高二下学期期末质量检测化学试题【全国校级联考】新疆伊宁生产建设兵团五校联考2017-2018学年高二下学期期末考试化学试题(已下线)2018年9月22日 《每日一题》人教选修4-周末培优山西省朔州市平鲁区李林中学2018-2019学年高二上学期第一次月考化学试题河南省安阳市第三十六中学2018-2019学年高二上学期第一次月考化学试题陕西省吴起高级中学2018-2019学年高一下学期第二次月考能力卷化学试题河北省张家口一中2019-2020学年高二(衔接班)上学期入学考试化学试题山西省应县第一中学校2019-2020学年高二上学期第一次月考化学试题新疆石河子第二中学2019-2020学年高二上学期第一次阶段考试化学试题河北省秦皇岛市第一中学2018-2019学年高二第一学期第一次月考化学试题湖南省怀化市第三中学2019-2020学年高二上学期9月月考化学试题河北省隆化县存瑞中学2019-2020学年高二上学期第二次质检化学试题安徽省滁州市定远县育才学校2019-2020学年高二(普通班)上学期第三次月考化学试题2020年安徽省全省教学质量检测统一考试(练习检测一)2020届高考二轮复习《化学反应速率与化学平衡》专题卷甘肃省武威市第十八中学2019-2020学年高二上学期期末考试化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末模拟考试化学试题(已下线)2.3.3+化学平衡常数-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 方法帮(已下线)2.3.3化学平衡常数(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)四川省什邡中学2019-2020学年高二上学期第二次月考化学试题河北省秦皇岛市卢龙县第二高级中学2021-2022学年高二上学期期末考试化学试题云南省富宁县第一中学校2021-2022学年高二下学期开学考试化学题重庆市九龙坡区2022-2023学年高二上学期第一次月考化学试题 重庆市渝高中学校2022-2023学年高二上学期第一次月考化学试题广西贺州市平桂管理区公会中学2021-2022学年上学期高二第二次月考化学(理)试题
7 . 当今,世界多国相继规划了碳达峰、碳中和的时间节点,我国提出争取2030年“碳达峰”,2060年“碳中和”。因此,研发二氧化碳利用技术、降低空气中二氧化碳含量成为热点。
(1)甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g) CH3OH(g) △H3=-90.77kJ·mol-1
CH3OH(g) △H3=-90.77kJ·mol-1
则:反应Ⅱ的ΔH2=___________ kJ·mol-1
(2)若反应II在一绝热恒容密闭容器中进行,下面能说明反应已达到平衡状态的是___________ ;
a、v(CO)=v(H2O) b、总压强不变
c、平衡常数不变 d、容器内n(CO2)/n(H2O)的值保持不变
(3)①对于反应Ⅰ,不同温度对CO2的转化率及催化剂的催化效率影响如图所示,下列有关说法正确的是___________ 。
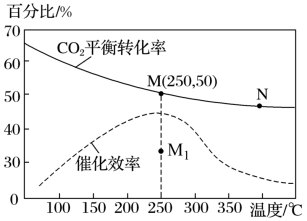
A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
B.温度低于250℃时,随温度升高甲醇的平衡产率增大
C.M点时平衡常数比N点时平衡常数大
D.若反应在较低的温度下进行,可以提高CO2的平衡转化率,符合勒沙特列原理
②若在2L密闭容器中充入3molH2和1molCO2只发生反应Ⅰ,250℃时反应的平衡常数K=___________ L2/mol2,若要进一步提高甲醇的体积分数,可采取的措施有___________ (写一条即可)。
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。回答下列问题:
①Li-CO2电池中,研究表明该电池反应产物为碳酸锂和单质碳,正极CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
I、2CO2+2e‑=C2O
II、C2O =CO2+CO
=CO2+CO
III、___________
IV、 +2Li+=Li2CO3
+2Li+=Li2CO3
②研究表明,在电解质水溶液中,CO2气体可被电化学还原。写出CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为___________ 。
(1)甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2反应Ⅲ:CO(g)+2H2(g)
 CH3OH(g) △H3=-90.77kJ·mol-1
CH3OH(g) △H3=-90.77kJ·mol-1则:反应Ⅱ的ΔH2=
(2)若反应II在一绝热恒容密闭容器中进行,下面能说明反应已达到平衡状态的是
a、v(CO)=v(H2O) b、总压强不变
c、平衡常数不变 d、容器内n(CO2)/n(H2O)的值保持不变
(3)①对于反应Ⅰ,不同温度对CO2的转化率及催化剂的催化效率影响如图所示,下列有关说法正确的是

A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
B.温度低于250℃时,随温度升高甲醇的平衡产率增大
C.M点时平衡常数比N点时平衡常数大
D.若反应在较低的温度下进行,可以提高CO2的平衡转化率,符合勒沙特列原理
②若在2L密闭容器中充入3molH2和1molCO2只发生反应Ⅰ,250℃时反应的平衡常数K=
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。回答下列问题:
①Li-CO2电池中,研究表明该电池反应产物为碳酸锂和单质碳,正极CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
I、2CO2+2e‑=C2O

II、C2O
 =CO2+CO
=CO2+CO
III、
IV、
 +2Li+=Li2CO3
+2Li+=Li2CO3②研究表明,在电解质水溶液中,CO2气体可被电化学还原。写出CO2在碱性介质中电还原为正丙醇(CH3CH2CH2OH)的电极反应方程式为
您最近一年使用:0次
名校
8 . 化学与社会、科学、技术、环境密切相关,下列说法错误的是
| A.铁表面镀锌可以增强铁的抗腐蚀性 |
| B.采用合适的催化剂可以提高合成氨工业中原料的转化率 |
| C.合理利用太阳能、风能和氢能等能源有利于实现“低碳经济” |
| D.钢铁在潮湿的空气中容易生锈,其主要原因是形成了原电池 |
您最近一年使用:0次
2022-01-01更新
|
291次组卷
|
4卷引用:吉林省长春市第二实验中学2022-2023学年高二上学期期中考试化学试题
名校
9 . 将装有 气体的圆底烧瓶(封口)置于冰水浴中,圆底烧瓶中气体颜色变浅。下列说法错误的是
气体的圆底烧瓶(封口)置于冰水浴中,圆底烧瓶中气体颜色变浅。下列说法错误的是
 气体的圆底烧瓶(封口)置于冰水浴中,圆底烧瓶中气体颜色变浅。下列说法错误的是
气体的圆底烧瓶(封口)置于冰水浴中,圆底烧瓶中气体颜色变浅。下列说法错误的是A.反应  |
| B.烧瓶内压强不再变化时,反应达到新的平衡 |
| C.气体颜色不再变化时,反应达到新的平衡 |
| D.混合气体的密度不再变化时,反应达到新的平衡 |
您最近一年使用:0次
2021-11-22更新
|
144次组卷
|
3卷引用:吉林油田高级中学2021-2022学年高二上学期期中考试化学试题
名校
10 . 羟胺(NH2OH)在水溶液中的电离方程式为NH2OH+ H2O NH3OH++OH-。常温下,向该溶液中加入NaOH固体,下列说法不正确的是
NH3OH++OH-。常温下,向该溶液中加入NaOH固体,下列说法不正确的是
 NH3OH++OH-。常温下,向该溶液中加入NaOH固体,下列说法不正确的是
NH3OH++OH-。常温下,向该溶液中加入NaOH固体,下列说法不正确的是| A.平衡常数K不变 | B.c(OH-)增大 |
| C.平衡向左移动 | D. 减小 减小 |
您最近一年使用:0次
2021-11-08更新
|
66次组卷
|
2卷引用:吉林省四平市普通高中2023-2024学年高二上学期期中教学质量检测化学试题



