名校
1 . NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业尾气中的 可通过催化氧化为
可通过催化氧化为 除去。将一定比例的
除去。将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性
的选择性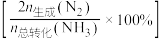 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是
 可通过催化氧化为
可通过催化氧化为 除去。将一定比例的
除去。将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性
的选择性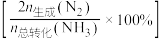 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是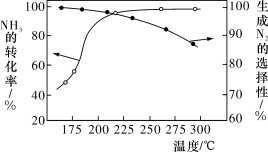
A.其他条件不变,升高温度, 的平衡转化率增大 的平衡转化率增大 |
B.其他条件不变,在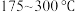 范围,随温度的升高,出口处 范围,随温度的升高,出口处 浓度不断增大 浓度不断增大 |
C.催化氧化除去尾气中的 应选择反应温度高于 应选择反应温度高于 |
D.高效除去尾气中的 ,需研发低温下 ,需研发低温下 转化率高和生成 转化率高和生成 选择性高的催化剂 选择性高的催化剂 |
您最近一年使用:0次
解题方法
2 . 含硫化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量SO2:Cu(s)+2H2SO4(l)=CuSO4(s)+SO2(g)+2H2O(l) ΔH=−11.9kJ·mol-1。判断该反应的自发性并说明理由___________ 。
(2)已知2SO2(g)+O2 2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
①反应开始到第10分钟,SO3反应速率为________ 。
②该温度下反应的平衡常数为________ 。
③平衡时SO2的转化率为________ 。
(3)工业上主要采用接触法用含硫矿石制备硫酸。其主要工艺是焙烧、炉气精制、用钒做催化剂将SO2氧化成SO3、吸收等。结合本大题的信息,完成下题。
①下列说法正确的是______ 。
a.须采用高温高压的反应条件使SO2氧化为SO3
b.通入过量的空气可以提高含硫矿石和SO2的转化率
c.进入接触室之前的气流无需净化处理
②在焙烧前要将硫铁矿粉碎,这样做的目的是______ 。
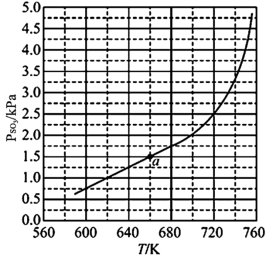
(4)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:2FeSO4(s) Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)_____ kPa,Kp(Ⅰ)随反应温度升高而_____ (填“增大”“减小”或“不变”)。
(1)实验室可用铜与浓硫酸反应制备少量SO2:Cu(s)+2H2SO4(l)=CuSO4(s)+SO2(g)+2H2O(l) ΔH=−11.9kJ·mol-1。判断该反应的自发性并说明理由
(2)已知2SO2(g)+O2
 2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。①反应开始到第10分钟,SO3反应速率为
②该温度下反应的平衡常数为
③平衡时SO2的转化率为
(3)工业上主要采用接触法用含硫矿石制备硫酸。其主要工艺是焙烧、炉气精制、用钒做催化剂将SO2氧化成SO3、吸收等。结合本大题的信息,完成下题。
①下列说法正确的是
a.须采用高温高压的反应条件使SO2氧化为SO3
b.通入过量的空气可以提高含硫矿石和SO2的转化率
c.进入接触室之前的气流无需净化处理
②在焙烧前要将硫铁矿粉碎,这样做的目的是
(4)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:2FeSO4(s)
 Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
您最近一年使用:0次
名校
解题方法
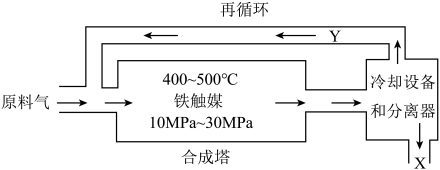
3 . 工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖。工业合成氨生产示意图如图所示。
(1)下列有关合成氨工业的说法正确的是___________
(2)循环利用的Y是氮气和氢气,目的是___________ 。
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有___________ (填编号)。
①使用催化剂 ②恒温恒容,增大原料气 和
和 充入量 ③及时分离产生的
充入量 ③及时分离产生的
④升高温度 ⑤恒温恒容,充入惰性气体 使压强增大
使压强增大
(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分 值。
值。
分析数据可知:
①在 下模拟工业固氮,某时刻
下模拟工业固氮,某时刻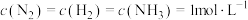 ,此时v正
,此时v正___________ v逆(填“>”“<”或“=”)。
②人类不适合大规模模拟大气固氮的原因是___________ 。
(5)哈伯1908年发表的文献中写到,在高温下,铁和铂都能作为使气态氨分解成为氢气、氮气的催化剂,下面是他做过的实验中的两组(条件都为901℃和3039.75 kPa)。
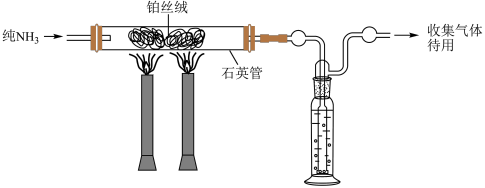
①使纯氨气通过白炽的铂丝,剩余的氨用浓硫酸洗涤除去。然后使气态混合物在相同条件下通过铁催化剂,出来的气体再缓缓通过20mL盐酸除去氨气。用气量计测得标准状况下剩余干燥气体的体积为2.02L。盐酸溶液用KOH溶液滴定,最终计算得到通入盐酸前氨气为1.86×10-4mol。
计算回答:在901℃下,N2 (g)+ 3H2 (g)
(g) 2NH3(g)的Kp=
2NH3(g)的Kp=___________ kPa-2。(保留一位有效数字)
②使纯氨气直接通过同一铁催化剂,出来的气体同样缓缓通入20mL盐酸,用气量计测得标准状况下剩余干燥气体的体积为1.82L。同理可以滴定后计算出通入盐酸前氨气的量,进而计算出Kp。在操作、计算误差合理的范围内,①、②得到的Kp基本相等。这对你有何启发?___________ 。

(1)下列有关合成氨工业的说法正确的是___________
| A.工业合成氨的反应是熵减小的放热反应,在低温时可自发进行 |
| B.合成氨反应中,反应物的总键能小于产物的总键能 |
C.合成氨厂一般采用的压强为 ,因为该压强下铁触媒的活性最高 ,因为该压强下铁触媒的活性最高 |
D. 的量越多, 的量越多, 的转化率越大,因此,充入的 的转化率越大,因此,充入的 越多越有利于 越多越有利于 的合成 的合成 |
(2)循环利用的Y是氮气和氢气,目的是
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有
①使用催化剂 ②恒温恒容,增大原料气
 和
和 充入量 ③及时分离产生的
充入量 ③及时分离产生的
④升高温度 ⑤恒温恒容,充入惰性气体
 使压强增大
使压强增大(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分
 值。
值。| 反应 | 大气固氮 | 工业固氮 | |||
温度 | 27 | 2000 | 25 | 400 | 450 |
 |  | 0.1 | 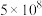 | 0.507 | 0.152 |
①在
 下模拟工业固氮,某时刻
下模拟工业固氮,某时刻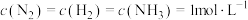 ,此时v正
,此时v正②人类不适合大规模模拟大气固氮的原因是
(5)哈伯1908年发表的文献中写到,在高温下,铁和铂都能作为使气态氨分解成为氢气、氮气的催化剂,下面是他做过的实验中的两组(条件都为901℃和3039.75 kPa)。

①使纯氨气通过白炽的铂丝,剩余的氨用浓硫酸洗涤除去。然后使气态混合物在相同条件下通过铁催化剂,出来的气体再缓缓通过20mL盐酸除去氨气。用气量计测得标准状况下剩余干燥气体的体积为2.02L。盐酸溶液用KOH溶液滴定,最终计算得到通入盐酸前氨气为1.86×10-4mol。
计算回答:在901℃下,N2 (g)+ 3H2
 (g)
(g) 2NH3(g)的Kp=
2NH3(g)的Kp=②使纯氨气直接通过同一铁催化剂,出来的气体同样缓缓通入20mL盐酸,用气量计测得标准状况下剩余干燥气体的体积为1.82L。同理可以滴定后计算出通入盐酸前氨气的量,进而计算出Kp。在操作、计算误差合理的范围内,①、②得到的Kp基本相等。这对你有何启发?
您最近一年使用:0次
2023-10-26更新
|
25次组卷
|
2卷引用:湖南省长沙市实验中学2023-2024学年高二上学期第一次月考化学试题
4 . 工业上可通过甲醇羰基化法制取甲酸甲酯(HCOOCH3):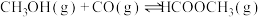 ,在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变化)。下列说法不合理的是
,在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变化)。下列说法不合理的是
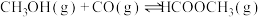 ,在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变化)。下列说法不合理的是
,在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图实线所示(图中虚线表示相同条件下CO的平衡转化率随温度的变化)。下列说法不合理的是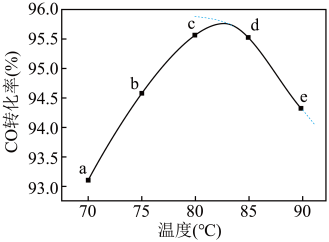
| A.适当增大压强可增大甲醇的平衡转化率 |
B.c点反应速率 |
C.反应速率 ,平衡常数 ,平衡常数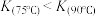 |
| D.生产时反应温度控制在80~85℃为宜 |
您最近一年使用:0次
2023-02-11更新
|
739次组卷
|
9卷引用:湖南省郴州市2021-2022学年高二上学期期末考试化学试题
湖南省郴州市2021-2022学年高二上学期期末考试化学试题山西省临汾市2022-2023学年高二下学期开学考试化学试题云南省部分名校2022-2023学年高二下学期6月联考化学试题云南省三校2024届高三上学期备考实用性联考(一)化学试题河南省陕州中学2023-2024学年高三上学期第三次月考化学试题天津市第四十五中学2023-2024学年高三12月月考化学试题(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河北省石家庄市河北正定中学2023-2024学年高三下学期4月模拟考试化学试题(已下线)江苏省南京外国语学校2024届高三下学期二模化学试题
名校
5 . 化学对提高人类生活质量和促进社会发展具有重要作用。下列人类活动中,运用了相应的化学原理的是
| 选项 | 人类活动 | 化学原理 |
| A | 实验室用锌与稀硫酸反应制氢气,同时有热量放出 | 该反应不遵循能量守恒定律 |
| B | 游轮底部定期更换锌块 | 利用电解原理可防止腐蚀 |
| C |  溶液除铁锈 溶液除铁锈 |  水解呈酸性 水解呈酸性 |
| D | 工业合成氨通常在高温条件下进行 | 高温促进合成氨平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-04更新
|
126次组卷
|
2卷引用:湖南省长沙市长郡中学2022--2023学年高二上学期第二次线上月考化学试题
6 . 下列有关合成氨工业的说法中正确的是
| A.铁触媒作催化剂可加快反应速率,且有利于化学平衡向合成氨的方向移动 |
| B.升高温度可以加快反应速率,且有利于化学平衡向合成氨的方向移动 |
| C.增大压强能缩短达到平衡状态所用的时间 |
| D.合成氨采用的压强是10~30MPa,因为该压强下铁触媒的活性最高 |
您最近一年使用:0次
2022-07-26更新
|
756次组卷
|
17卷引用:湖南省益阳市箴言中学2021-2022学年高二上学期10月月考化学试题
湖南省益阳市箴言中学2021-2022学年高二上学期10月月考化学试题湖南省怀化市第五中学2021-2022学年高二上学期期中考试化学试题湖南省隆回县第二中学2022-2023学年高二上学期线上课程摸底(期中)考试化学试题吉林省长春外国语学校2021-2022学年高二上学期第一次月考化学试题(已下线)必考点04 化学反应的方向和调控-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题(已下线)第12讲 化学反应的调控-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)2.4.1 合成氨生产适宜条件的选择-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)天津市第二十五中学2022 -2023学年高二上学期期中考试化学试题新疆昌吉州行知学校2022-2023学年高二上学期第一次线上月考化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期第二次月考化学试题重庆市为明学校2022-2023学年高二上学期期末检测化学试题第四节 化学反应的调控河南省周口市太康县2022-2023学年高二上学期11月期中考试化学试题第二章 第四节 化学反应的调控(已下线)专题06 化学反应的方向及调控【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)
7 . CO2资源化利用能有效减少碳排放,充分利用碳资源。
(1)CO2催化加氢合成二甲醚过程中主要发生下列反应:
反应Ⅰ:
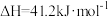
反应Ⅱ: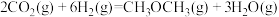
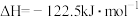
①反应Ⅰ中的CO2平衡转化率随温度升高而增大的原因是_______ 。
②在恒压、CO2和 的起始量一定的条件下,CO2平衡转化率和平衡时
的起始量一定的条件下,CO2平衡转化率和平衡时 的选择性(
的选择性( 的选择性
的选择性 ) 随温度的变化如图:
) 随温度的变化如图:

T℃时,起始投入 ,
, ,达到平衡时反应Ⅰ理论上消耗
,达到平衡时反应Ⅰ理论上消耗 的物质的量为
的物质的量为_______ 。该催化剂条件下合成二甲醚时较适宜的温度为260℃,其原因是_______ 。
(2)研究发现,(1)中的反应Ⅱ分两步完成,即发生反应Ⅲ和Ⅳ。
反应Ⅲ: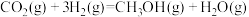
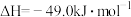
反应Ⅳ: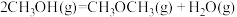
①反应Ⅳ的
_______ 
②其他条件相同时,若两容器中分别仅发生反应Ⅱ和反应Ⅲ,测得反应Ⅱ中CO2的平衡转化率更高,其原因可能是_______ 。
(1)CO2催化加氢合成二甲醚过程中主要发生下列反应:
反应Ⅰ:

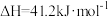
反应Ⅱ:
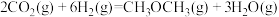
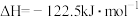
①反应Ⅰ中的CO2平衡转化率随温度升高而增大的原因是
②在恒压、CO2和
 的起始量一定的条件下,CO2平衡转化率和平衡时
的起始量一定的条件下,CO2平衡转化率和平衡时 的选择性(
的选择性( 的选择性
的选择性 ) 随温度的变化如图:
) 随温度的变化如图:
T℃时,起始投入
 ,
, ,达到平衡时反应Ⅰ理论上消耗
,达到平衡时反应Ⅰ理论上消耗 的物质的量为
的物质的量为(2)研究发现,(1)中的反应Ⅱ分两步完成,即发生反应Ⅲ和Ⅳ。
反应Ⅲ:
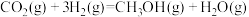
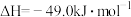
反应Ⅳ:
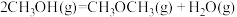
①反应Ⅳ的


②其他条件相同时,若两容器中分别仅发生反应Ⅱ和反应Ⅲ,测得反应Ⅱ中CO2的平衡转化率更高,其原因可能是
您最近一年使用:0次
2022-05-30更新
|
202次组卷
|
2卷引用:湖南省株洲市茶陵县2021-2022学年高二下学期期末考试化学试题
名校
解题方法
8 . 烟气脱硫脱硝技术是环境科学研究的热点。某小组模拟 氧化结合
氧化结合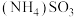 溶液吸收法同时脱除
溶液吸收法同时脱除 和NO的过程示意图如下。
和NO的过程示意图如下。
①已知: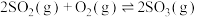
 ,则
,则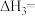
_______ 。
②其他条件不变时,高于150℃,在相同时间内 和NO的转化率均随温度升高而降低,原因是
和NO的转化率均随温度升高而降低,原因是_______ 。
③其他条件不变, 和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内, 和NO的转化率随
和NO的转化率随 的浓度的变化如图。结合数据分析NO的转化率高于
的浓度的变化如图。结合数据分析NO的转化率高于 的原因
的原因_______ 。 和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内, 与NO的物质的量之比对
与NO的物质的量之比对 和NO脱除率的影响如图。
和NO脱除率的影响如图。 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:_______ 。
② 的浓度很低时,
的浓度很低时, 的脱除率超过97%,原因是
的脱除率超过97%,原因是_______ 。
③在吸收器中, 与
与 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是_______ 。
④在吸收器中,随着吸收过程的进行,部分 被转化为
被转化为 ,反应中
,反应中 和
和 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是_______ 。
 氧化结合
氧化结合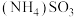 溶液吸收法同时脱除
溶液吸收法同时脱除 和NO的过程示意图如下。
和NO的过程示意图如下。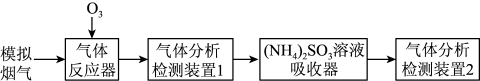
| 反应 | 平衡常数(25℃) | 活化能/(kJ/mol) |
反应a: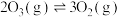 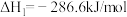 |  | 24.6 |
反应b: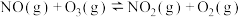 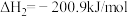 | 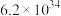 | 3.17 |
反应c:  | 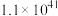 | 58.17 |
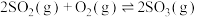
 ,则
,则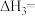
②其他条件不变时,高于150℃,在相同时间内
 和NO的转化率均随温度升高而降低,原因是
和NO的转化率均随温度升高而降低,原因是③其他条件不变,
 和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内, 和NO的转化率随
和NO的转化率随 的浓度的变化如图。结合数据分析NO的转化率高于
的浓度的变化如图。结合数据分析NO的转化率高于 的原因
的原因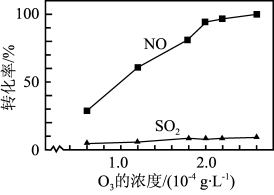
 和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内, 与NO的物质的量之比对
与NO的物质的量之比对 和NO脱除率的影响如图。
和NO脱除率的影响如图。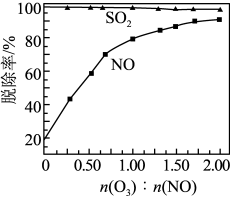
 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:②
 的浓度很低时,
的浓度很低时, 的脱除率超过97%,原因是
的脱除率超过97%,原因是③在吸收器中,
 与
与 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是④在吸收器中,随着吸收过程的进行,部分
 被转化为
被转化为 ,反应中
,反应中 和
和 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是
您最近一年使用:0次
2022-04-10更新
|
768次组卷
|
6卷引用:湖南省株洲市第四中学2022-2023学年高二上学期期中考试化学试题
解题方法
9 . 下列措施与化学反应速率无关的是
| A.炉膛内用煤粉代替煤块 | B.食物冷藏在冰箱 |
| C.工业合成氨时,及时将氨气液化分离 | D.在铁制品表面喷涂油漆 |
您最近一年使用:0次
2022-01-30更新
|
114次组卷
|
2卷引用:湖南省益阳市2021-2022学年高二上学期期末考试化学试题
10 . 化学在日常生活和生产中有着重要的应用,下列说法错误的是
| A.泡沫灭火器中的Al2(SO4)3溶液应贮存在玻璃筒内 |
| B.BaSO4在医学上用作钡餐所以Ba2+无毒对人体无害 |
| C.新能源汽车的推广与使用能减少氮氧化合物对环境的污染 |
| D.工业上通常采用铁触媒、400°C~500°C和10MPa~30MPa的条件来合成氨 |
您最近一年使用:0次



