名校
解题方法
1 . 硫酸工业生产中:
1.在接触室中进行的反应方程式为_______ 。
2.实际生产时采用了中间有热交换器的接触室(见图)
3.c处气体经热交换后再次催化氧化的目的是_______ 。
4.硫酸工业生产中 吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收
吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收 所用硫酸的适宜浓度为
所用硫酸的适宜浓度为_______ %左右,适宜温度为_______ ,而工业生产中一般采用60℃的可能原因是_______ 。
1.在接触室中进行的反应方程式为
2.实际生产时采用了中间有热交换器的接触室(见图)

A.a处进入的气体中 过量 过量 |
| B.a、b两处的混合气体成分含量相同,温度不同 |
| C.c、d两处的混合气体成分含量不同,温度相同 |
| D.热交换器的作用是预热待反应的气体,冷却反应后的气体 |
4.硫酸工业生产中
 吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收
吸收率与进入吸收塔的硫酸浓度和温度关系如图,由图可知吸收 所用硫酸的适宜浓度为
所用硫酸的适宜浓度为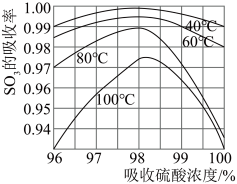
您最近一年使用:0次
解题方法
2 . 金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1) 转化为
转化为 有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:
有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:
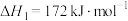 ,
,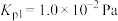
(ⅱ)碳氯化:
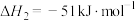 ,
,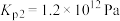
①反应 的
的 为
为________  。
。
②运用以上数据分析,你认为以上两种方法更优越的是__________ ,理由_________________ 。
(2)在压强为170kPa恒压作用下,将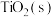 、
、 、
、 以物质的量之比为
以物质的量之比为 进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。 的平衡常数
的平衡常数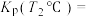
________  (分压
(分压 物质的量分数
物质的量分数 总压)。
总压)。
②图中显示,在T1℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是___________ 。
(1)
 转化为
转化为 有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:
有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:
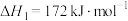 ,
,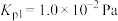
(ⅱ)碳氯化:

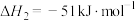 ,
,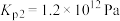
①反应
 的
的 为
为 。
。②运用以上数据分析,你认为以上两种方法更优越的是
(2)在压强为170kPa恒压作用下,将
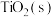 、
、 、
、 以物质的量之比为
以物质的量之比为 进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。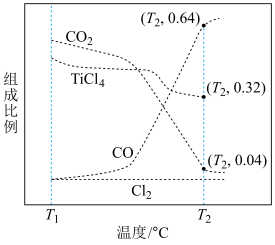
 的平衡常数
的平衡常数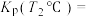
 (分压
(分压 物质的量分数
物质的量分数 总压)。
总压)。②图中显示,在T1℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是
您最近一年使用:0次
3 . 如图所示的是以黄铁矿( )为主要原料接触法制硫酸工业的流程示意图(A.沸腾炉 B.接触室 C.吸收塔)
)为主要原料接触法制硫酸工业的流程示意图(A.沸腾炉 B.接触室 C.吸收塔) 接触氧化的反应,下图中的甲、乙、丙分别表示在不同条件下,
接触氧化的反应,下图中的甲、乙、丙分别表示在不同条件下, 在反应混合物中的体积分数(Y)与时间(X)的关系,请按要求填写:
在反应混合物中的体积分数(Y)与时间(X)的关系,请按要求填写:______ 表示有催化剂的情况;
②若乙图两条曲线分别表示不同压强的情况,则______ 表示压强较大的情况;
③若丙图两条曲线分别表示600℃和400℃的情况,则______ 表示600℃的情况。
(2)在生产中常使用过量的空气是为了______ 。
(3)接触法制硫酸的沸腾炉处产生的炉气必须经过净化处理,目的是为了______ 。
(4)从⑤处排出的气体是______(填序号)
(5)在B设备中加热到400℃~500℃是由于①加快反应速率,②______ 。
(6)对从进口⑧喷进的液体的叙述最准确的是______ (填序号)。
A.水 B.98.3%的浓硫酸 C.稀硫酸
(7)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理得到较高浓度的 和铵盐,
和铵盐, 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的 ,请写出
,请写出 吸收
吸收 的离子方程式:
的离子方程式:______ 。
 )为主要原料接触法制硫酸工业的流程示意图(A.沸腾炉 B.接触室 C.吸收塔)
)为主要原料接触法制硫酸工业的流程示意图(A.沸腾炉 B.接触室 C.吸收塔)
 接触氧化的反应,下图中的甲、乙、丙分别表示在不同条件下,
接触氧化的反应,下图中的甲、乙、丙分别表示在不同条件下, 在反应混合物中的体积分数(Y)与时间(X)的关系,请按要求填写:
在反应混合物中的体积分数(Y)与时间(X)的关系,请按要求填写: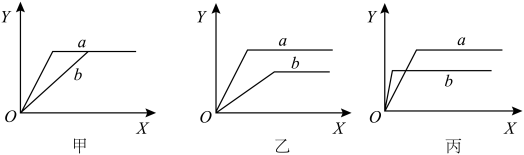
②若乙图两条曲线分别表示不同压强的情况,则
③若丙图两条曲线分别表示600℃和400℃的情况,则
(2)在生产中常使用过量的空气是为了
(3)接触法制硫酸的沸腾炉处产生的炉气必须经过净化处理,目的是为了
(4)从⑤处排出的气体是______(填序号)
A. 、 、 | B. 、 、 | C. 、 、 | D.水蒸气 |
(5)在B设备中加热到400℃~500℃是由于①加快反应速率,②
(6)对从进口⑧喷进的液体的叙述最准确的是
A.水 B.98.3%的浓硫酸 C.稀硫酸
(7)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理得到较高浓度的
 和铵盐,
和铵盐, 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的 ,请写出
,请写出 吸收
吸收 的离子方程式:
的离子方程式:
您最近一年使用:0次
4 . 利用向制取生物柴油的副产物甘油( )中通入一定量的水蒸气,可实现重整制氢。经一系列反应可获得
)中通入一定量的水蒸气,可实现重整制氢。经一系列反应可获得 、CO、
、CO、 、
、 等组成气体,通过调整反应的组成和条件可提高
等组成气体,通过调整反应的组成和条件可提高 产率。请回答:
产率。请回答:
(1)制氢的几个主要反应如下
反应1: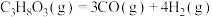
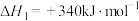
反应2:
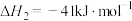
反应3:
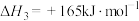
反应4: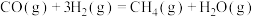

(1)计算
______ ,并判断该反应的自发性______ 。
(2)①温度控制不当,气相产物之间会发生积碳副反应从而影响氢气产率,反应如下:
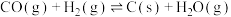
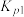 ,
,
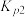 ;若仅考虑积碳副反应,一定温度下,测得在1.0MPa恒压反应体系中达到平衡时组分的分压(即组分的物质的量分数×总压),
;若仅考虑积碳副反应,一定温度下,测得在1.0MPa恒压反应体系中达到平衡时组分的分压(即组分的物质的量分数×总压), ,则平衡常数
,则平衡常数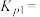
______ 。
②生产过程中,为减小积碳对氢气产率及催化剂的影响,下列措施合适的是______ (填序号)。
A.减小压强 B.通入过量的氧气 C.通入适量的水蒸气 D.选择合适的催化剂
③上述各反应达到平衡时,体系中各物质的物质的量分数受温度的影响如图,请结合图像解释,在图示温度范围内随着温度升高 的摩尔分数先迅速上升后缓慢下降的原因是
的摩尔分数先迅速上升后缓慢下降的原因是______ 。______ (表示在催化剂表面吸附态)(填序号)
A.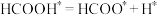
B.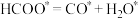
C.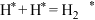
 )中通入一定量的水蒸气,可实现重整制氢。经一系列反应可获得
)中通入一定量的水蒸气,可实现重整制氢。经一系列反应可获得 、CO、
、CO、 、
、 等组成气体,通过调整反应的组成和条件可提高
等组成气体,通过调整反应的组成和条件可提高 产率。请回答:
产率。请回答:(1)制氢的几个主要反应如下
反应1:
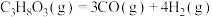
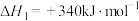
反应2:

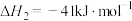
反应3:

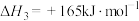
反应4:
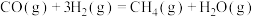

(1)计算

(2)①温度控制不当,气相产物之间会发生积碳副反应从而影响氢气产率,反应如下:
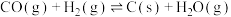
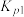 ,
,
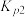 ;若仅考虑积碳副反应,一定温度下,测得在1.0MPa恒压反应体系中达到平衡时组分的分压(即组分的物质的量分数×总压),
;若仅考虑积碳副反应,一定温度下,测得在1.0MPa恒压反应体系中达到平衡时组分的分压(即组分的物质的量分数×总压), ,则平衡常数
,则平衡常数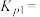
②生产过程中,为减小积碳对氢气产率及催化剂的影响,下列措施合适的是
A.减小压强 B.通入过量的氧气 C.通入适量的水蒸气 D.选择合适的催化剂
③上述各反应达到平衡时,体系中各物质的物质的量分数受温度的影响如图,请结合图像解释,在图示温度范围内随着温度升高
 的摩尔分数先迅速上升后缓慢下降的原因是
的摩尔分数先迅速上升后缓慢下降的原因是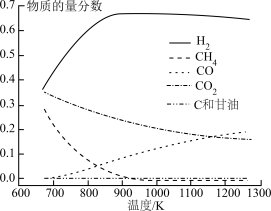
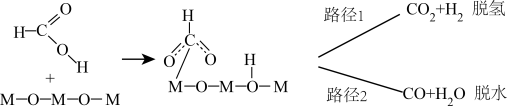
A.
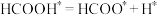
B.
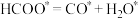
C.
您最近一年使用:0次
名校
解题方法
5 . 有效去除大气中的NOx和水体中的氮是环境保护的重要课题。
(1)已知:①2CO(g)+O2(g)=2CO2(g);ΔH1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g);ΔH2=+64kJ·mol-1
反应:2NO2(g)+4CO(g)=N2(g)+4CO2(g);ΔH3=________ 。
(2)近年研究发现,电催化CO2和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。________ 。
(3)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(NH 和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH
和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH ),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
①生成磷酸铵镁沉淀的离子反应方程式为________ 。
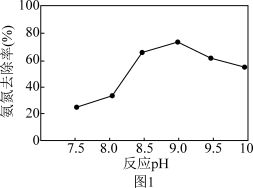
②测得反应pH对氨氮去除率的影响如下图1所示,当pH从7.5增至9.0的过程中,水中氨氮的去除率明显增加,原因是________ 。
①NZVI/BC和(CuPd)/BC复合材料还原硝酸盐的反应机理如下图2所示, 转化为N2或
转化为N2或 的过程可描述为
的过程可描述为________ 。 去除率的影响如上图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是
去除率的影响如上图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是________ 。
(1)已知:①2CO(g)+O2(g)=2CO2(g);ΔH1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g);ΔH2=+64kJ·mol-1
反应:2NO2(g)+4CO(g)=N2(g)+4CO2(g);ΔH3=
(2)近年研究发现,电催化CO2和含氮物质(
 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。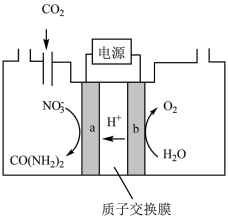
(3)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(NH
 和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH
和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH ),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。①生成磷酸铵镁沉淀的离子反应方程式为
②测得反应pH对氨氮去除率的影响如下图1所示,当pH从7.5增至9.0的过程中,水中氨氮的去除率明显增加,原因是
①NZVI/BC和(CuPd)/BC复合材料还原硝酸盐的反应机理如下图2所示,
 转化为N2或
转化为N2或 的过程可描述为
的过程可描述为 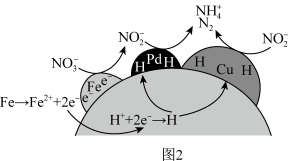
 去除率的影响如上图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是
去除率的影响如上图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是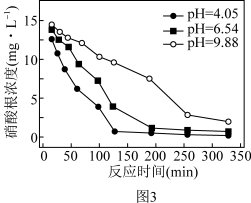
您最近一年使用:0次
名校
6 . 海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和制得一些重要的化工产品。海水提溴的工艺流程如图所示。
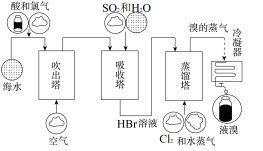
(1)工业上通过
 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是 ,利用了溴的
,利用了溴的A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(2)写出吸收塔中发生反应的离子方程式:
(3)某同学提出,证明HBr溶液中含有Br的实验方案是:取出少量溶液,先加入过量新制氯水,再加入淀粉—KI溶液,观察溶液是否变蓝。该方案是否合理并简述理由:
(4)蒸馏塔在蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因:
(5)从海水中获得淡水的主要方法有电渗析法、反渗透法和
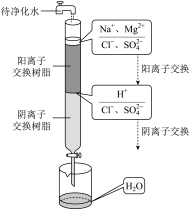
A.经过阳离子交换树脂后,水溶液中阳离子总数减少
B.通过阴离子交换树脂后,水溶液中只 被除去
被除去
C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:
您最近一年使用:0次
2024-03-28更新
|
165次组卷
|
2卷引用:河南省郑州市宇华实验学校2023-2024学年高二下学期开学考试化学试题
解题方法
7 . Ⅰ.习近平总书记十分重视生态环境保护,多次对生态文明建设作出重要指示,其中研究 、
、 、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
(1)处理含CO、 烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
①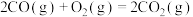
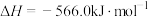
②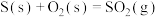

则CO与 反应生成S的热化学方程式是
反应生成S的热化学方程式是_______ 。
(2)在一绝热体系且容积固定的密闭容器中,用 催化还原
催化还原 也可以消除氮氧化物的污染,其中发生化学反应之一为:
也可以消除氮氧化物的污染,其中发生化学反应之一为: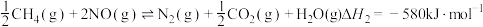 ,能说明上反应达到平衡状态的是
,能说明上反应达到平衡状态的是_______ 。
a.平均摩尔质量不变 b. 和
和 的体积比保持不变
的体积比保持不变
c.体系压强保持不变 d.每生成1mol 同时生成2molNO
同时生成2molNO
Ⅱ.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(3)生产氢气:将水蒸气通过红热的炭即产生水煤气;
 ,
,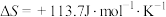 ,该反应在(填“高温”或“低温”或“任何温度”)
,该反应在(填“高温”或“低温”或“任何温度”)_______ 下,才能自发进行。
(4)合成氨工业中的主要反应是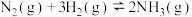
 ,从温度和压强的角度回答:要加快合成氨的反应速率应选择
,从温度和压强的角度回答:要加快合成氨的反应速率应选择_______ ;要提高氨的产率应选择_______ 。
 、
、 、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。(1)处理含CO、
 烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:①
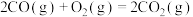
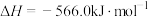
②
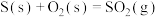

则CO与
 反应生成S的热化学方程式是
反应生成S的热化学方程式是(2)在一绝热体系且容积固定的密闭容器中,用
 催化还原
催化还原 也可以消除氮氧化物的污染,其中发生化学反应之一为:
也可以消除氮氧化物的污染,其中发生化学反应之一为: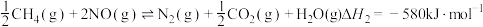 ,能说明上反应达到平衡状态的是
,能说明上反应达到平衡状态的是a.平均摩尔质量不变 b.
 和
和 的体积比保持不变
的体积比保持不变c.体系压强保持不变 d.每生成1mol
 同时生成2molNO
同时生成2molNOⅡ.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(3)生产氢气:将水蒸气通过红热的炭即产生水煤气;

 ,
,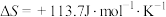 ,该反应在(填“高温”或“低温”或“任何温度”)
,该反应在(填“高温”或“低温”或“任何温度”)(4)合成氨工业中的主要反应是
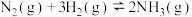
 ,从温度和压强的角度回答:要加快合成氨的反应速率应选择
,从温度和压强的角度回答:要加快合成氨的反应速率应选择
您最近一年使用:0次
名校
8 . 合成氨工业对国民经济和社会发展具有重要的意义。
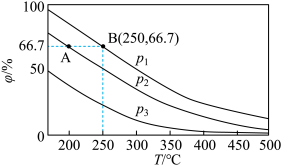
(1) 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
①其中,
___________  (填“>”或“<”),其原因是
(填“>”或“<”),其原因是___________ 。
②A、B两点的反应速率: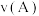
___________ 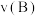 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③若在250℃、 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
___________  (保留一位小数)。
(保留一位小数)。
(2)工业合成氨生产流程示意图如下:
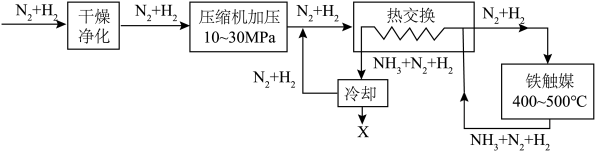
①X为___________ 。
②上述流程中,有利于提高原料利用率的措施是___________ (填标号)。
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:
 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议___________ 。
(1)
 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
①其中,

 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是②A、B两点的反应速率:
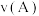
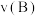 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③若在250℃、
 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
 (保留一位小数)。
(保留一位小数)。(2)工业合成氨生产流程示意图如下:

①X为
②上述流程中,有利于提高原料利用率的措施是
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:

 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议
您最近一年使用:0次
名校
解题方法
9 . 近年来我国大力加强温室气体 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题。
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题。
(1)已知:

写出 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式:________________________________ ;形成甲醇中的 键需要
键需要________ (填“吸收”或“释放”)能量。
(2)为提高 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是________ (填字母)。
a.高温、高压 b.低温、低压 c.高温、低压 d.低温、高压
(3)在 时,在某恒容密闭容器中进行由
时,在某恒容密闭容器中进行由 催化氢化合成
催化氢化合成 的反应。如图为不同投料比
的反应。如图为不同投料比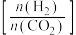 时某反应物
时某反应物 的平衡转化率的变化曲线,则反应物
的平衡转化率的变化曲线,则反应物 是
是________ (填“ ”或“
”或“ ”)。
”)。

(4)在 时,在
时,在 的恒容密闭容器中加入
的恒容密闭容器中加入 、
、 及催化剂,
及催化剂, 时反应达到平衡,测得
时反应达到平衡,测得 。
。
①前 内
内 的平均反应速率
的平均反应速率
________  。
。
②化学平衡常数
________________________ 。
③下列描述中能说明上述反应已达平衡的是________ (填字母)。
a.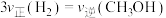
b.单位时间内生成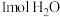 的同时生成
的同时生成
c.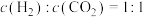
d.容器中气体的平均相对分子质量不随时间而变化
④催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下表四组实验数据。
根据上表所给数据,用 生产甲醇的最优条件为
生产甲醇的最优条件为________ (填实验编号)。
 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题。
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题。(1)已知:


写出
 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式: 键需要
键需要(2)为提高
 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是a.高温、高压 b.低温、低压 c.高温、低压 d.低温、高压
(3)在
 时,在某恒容密闭容器中进行由
时,在某恒容密闭容器中进行由 催化氢化合成
催化氢化合成 的反应。如图为不同投料比
的反应。如图为不同投料比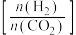 时某反应物
时某反应物 的平衡转化率的变化曲线,则反应物
的平衡转化率的变化曲线,则反应物 是
是 ”或“
”或“ ”)。
”)。
(4)在
 时,在
时,在 的恒容密闭容器中加入
的恒容密闭容器中加入 、
、 及催化剂,
及催化剂, 时反应达到平衡,测得
时反应达到平衡,测得 。
。①前
 内
内 的平均反应速率
的平均反应速率
 。
。②化学平衡常数

③下列描述中能说明上述反应已达平衡的是
a.
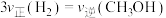
b.单位时间内生成
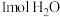 的同时生成
的同时生成
c.
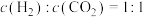
d.容器中气体的平均相对分子质量不随时间而变化
④催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下表四组实验数据。
实验编号 | 温度 | 催化剂 |
| 甲醇的选择性 |
| 543 |
| 12.3 | 42.3 |
| 543 |
| 11.9 | 72.7 |
| 553 |
| 15.3 | 39.1 |
| 553 |
| 12.0 | 70.6 |
 生产甲醇的最优条件为
生产甲醇的最优条件为
您最近一年使用:0次
2024-02-23更新
|
43次组卷
|
2卷引用:河北省百师联盟2023-2024学年高二上学期1月期末大联考化学试题
名校
解题方法
10 . 尿素是一种很好用的保湿成分,它存在于肌肤的角质层当中,属于肌肤天然保湿因子NMF的主要成分。工业上以氨气和二氧化碳为原料合成尿素,反应分为如下两步:
反应①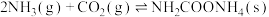
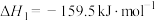
反应②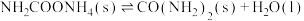

(1)下列反应与反应②的热效应相同的是___________。
(2)下图能表示上述两步反应能量变化的是___________。
(3)恒温恒容时,将2mol 和1mol
和1mol  充入2L反应器中合成尿素,经10min测得反应器内气体压强变为起始的80%(已知此时尿素为固态。水为液态),则从反应开始至10min时,
充入2L反应器中合成尿素,经10min测得反应器内气体压强变为起始的80%(已知此时尿素为固态。水为液态),则从反应开始至10min时, 的平均反应速率
的平均反应速率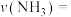
___________ (写出计算过程)。
(4)若将2mol 和1mol
和1mol  充入一容积可变的容器中进行,初始体积固定为V,10min后达到平衡时,
充入一容积可变的容器中进行,初始体积固定为V,10min后达到平衡时, 随时间变化如图所示:
随时间变化如图所示:
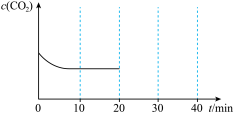
20min时压缩容器,使体积变为0.5V并保持不变,30min时达到新平衡,请在图中大致画出20min~40min内 随时间t变化的曲线
随时间t变化的曲线___________ 。
(5)实际生产中,为节约成本并提高反应②的生产效率,尿素合成工厂通常将反应②的发生场所设置在反应①的发生场所附近,请说明理由:___________ 。
反应①
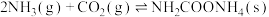
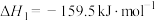
反应②
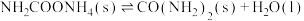

(1)下列反应与反应②的热效应相同的是___________。
| A.木炭与高温水蒸气反应 | B.镁条与稀盐酸反应 |
| C.小苏打与柠檬酸钠反应 | D.氢气与氯气反应 |
(2)下图能表示上述两步反应能量变化的是___________。
A.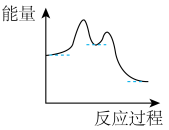 | B.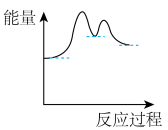 | C. | D.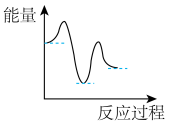 |
(3)恒温恒容时,将2mol
 和1mol
和1mol  充入2L反应器中合成尿素,经10min测得反应器内气体压强变为起始的80%(已知此时尿素为固态。水为液态),则从反应开始至10min时,
充入2L反应器中合成尿素,经10min测得反应器内气体压强变为起始的80%(已知此时尿素为固态。水为液态),则从反应开始至10min时, 的平均反应速率
的平均反应速率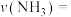
(4)若将2mol
 和1mol
和1mol  充入一容积可变的容器中进行,初始体积固定为V,10min后达到平衡时,
充入一容积可变的容器中进行,初始体积固定为V,10min后达到平衡时, 随时间变化如图所示:
随时间变化如图所示:
20min时压缩容器,使体积变为0.5V并保持不变,30min时达到新平衡,请在图中大致画出20min~40min内
 随时间t变化的曲线
随时间t变化的曲线(5)实际生产中,为节约成本并提高反应②的生产效率,尿素合成工厂通常将反应②的发生场所设置在反应①的发生场所附近,请说明理由:
您最近一年使用:0次



 纳米棒
纳米棒




