名校
1 . 合成氨反应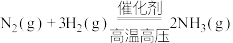 是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
(1)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:
①写出N2参与化学吸附的反应方程式:_____________ 。
②以上历程须克服的最大能垒为______ eV。
(2)t℃、0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:
______  ,该反应的
,该反应的
______ (用数字表达式表示,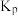 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
②下列叙述能说明该条件下反应达到平衡状态的是______ (填标号)。
a.氨气的体积分数保持不变
b.容器中氢氮比保持不变
c.N2和NH3的平均反应速率之比为1∶2
d.气体密度保持不变
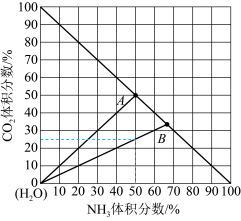
(3)如图是20℃时,NH3-CO2-H2O三元体系相图。纵坐标代表CO2的体积分数,横坐标代表NH3的体积分数,坐标原点代表液态纯水。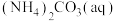 与
与 ,也可选择无水体系反应得到
,也可选择无水体系反应得到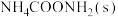 。
。
①20℃时,利用NH3(g)、CO2(g)和H2O(l)制备NH4HCO3(aq)的最佳曲线是______ (填“A-H2O”或“B-H2O”)。
②B点可得到的产品是______ (填化学式)。
(4)钌系催化剂是目前合成氨最先进的催化剂。一种钌的化合物晶胞结构如图。该晶胞中与 等距最近的
等距最近的 有
有______ 个,若该晶胞边长为a pm,该晶体的密度为______  (
(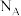 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
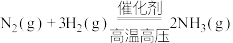 是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:(1)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:

①写出N2参与化学吸附的反应方程式:
②以上历程须克服的最大能垒为
(2)t℃、0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:


 ,该反应的
,该反应的
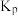 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。②下列叙述能说明该条件下反应达到平衡状态的是
a.氨气的体积分数保持不变
b.容器中氢氮比保持不变
c.N2和NH3的平均反应速率之比为1∶2
d.气体密度保持不变
(3)如图是20℃时,NH3-CO2-H2O三元体系相图。纵坐标代表CO2的体积分数,横坐标代表NH3的体积分数,坐标原点代表液态纯水。
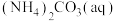 与
与 ,也可选择无水体系反应得到
,也可选择无水体系反应得到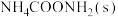 。
。①20℃时,利用NH3(g)、CO2(g)和H2O(l)制备NH4HCO3(aq)的最佳曲线是
②B点可得到的产品是
(4)钌系催化剂是目前合成氨最先进的催化剂。一种钌的化合物晶胞结构如图。该晶胞中与
 等距最近的
等距最近的 有
有 (
(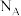 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2 . 丙烷的价格低廉且产量大,丙烷脱氢制丙烯是获取丙烯及其衍生物的重要途径。
反应ⅰ(直接脱氢):

反应ⅱ:

(1)已知下列键能数据,结合反应ⅰ数据,计算 的键能是
的键能是________  。
。
(2)计算反应ⅲ( 氧化丙烷脱氢):
氧化丙烷脱氢): 的
的
________  。
。
(3) 催化丙烷直接脱氢的主要副反应为
催化丙烷直接脱氢的主要副反应为 。
。
①一定温度下,向恒容容器中充入一定量丙烷,在 催化作用下脱氢制丙烯,下列情况表明反应达到平衡状态的是
催化作用下脱氢制丙烯,下列情况表明反应达到平衡状态的是________________ (填标号)。
A.气体密度不再改变
B.气体平均摩尔质量不再改变
C.体系压强不再改变
D.单位时间内消耗 的物质的量与生成
的物质的量与生成 的物质的量相等
的物质的量相等
② 下,在
下,在 容器中充入
容器中充入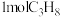 ,
,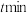 后达到平衡状态时,
后达到平衡状态时, 转化率为
转化率为 ,
, 选择性为
选择性为 ,则
,则 的消耗速率
的消耗速率
________  ,丙烷脱氢反应的平衡常数
,丙烷脱氢反应的平衡常数
________ 。(已知 选择性
选择性 )
)
(4)以 作催化剂,对反应ⅲ的机理展开研究.以
作催化剂,对反应ⅲ的机理展开研究.以 和
和 为原料,初期产物中没有检测到
为原料,初期产物中没有检测到 ;以含有
;以含有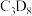 的
的 和
和 为原料,反应过程中没有检测到
为原料,反应过程中没有检测到 。下列推断合理的是
。下列推断合理的是________ (填标号)
A. 先吸附氧气,吸附的氧气直接与吸附的丙烷反应
先吸附氧气,吸附的氧气直接与吸附的丙烷反应
B. 直接氧化吸附的丙烷,吸附的氧气补充
直接氧化吸附的丙烷,吸附的氧气补充 中反应掉的氧
中反应掉的氧
C. 催化丙烷脱氢过程中,碳氢键的断裂是可逆的
催化丙烷脱氢过程中,碳氢键的断裂是可逆的
(5)用 替换
替换 ,进行氧化丙烷脱氢,可避免丙烷深度氧化、
,进行氧化丙烷脱氢,可避免丙烷深度氧化、 资源化利用等优势。
资源化利用等优势。
①结合键能数据分析 氧化丙烷脱氢反应的挑战和难点
氧化丙烷脱氢反应的挑战和难点________________ 。
② 也可以进行氧化乙苯脱氢制取苯乙烯,
也可以进行氧化乙苯脱氢制取苯乙烯, 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( ,
, 表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。
位点带部分负电荷)。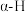 带部分正电荷,被带部分负电荷的
带部分正电荷,被带部分负电荷的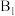 位点吸引,随后解离出
位点吸引,随后解离出 并吸附在
并吸附在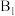 位点上;步骤Ⅱ可描述为:
位点上;步骤Ⅱ可描述为:________________ 。
反应ⅰ(直接脱氢):


反应ⅱ:


(1)已知下列键能数据,结合反应ⅰ数据,计算
 的键能是
的键能是 。
。化学键 |
|
|
|
|
键能( | 347.7 | 413.4 | 436.0 | 745 |
(2)计算反应ⅲ(
 氧化丙烷脱氢):
氧化丙烷脱氢): 的
的
 。
。(3)
 催化丙烷直接脱氢的主要副反应为
催化丙烷直接脱氢的主要副反应为 。
。①一定温度下,向恒容容器中充入一定量丙烷,在
 催化作用下脱氢制丙烯,下列情况表明反应达到平衡状态的是
催化作用下脱氢制丙烯,下列情况表明反应达到平衡状态的是A.气体密度不再改变
B.气体平均摩尔质量不再改变
C.体系压强不再改变
D.单位时间内消耗
 的物质的量与生成
的物质的量与生成 的物质的量相等
的物质的量相等②
 下,在
下,在 容器中充入
容器中充入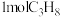 ,
,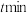 后达到平衡状态时,
后达到平衡状态时, 转化率为
转化率为 ,
, 选择性为
选择性为 ,则
,则 的消耗速率
的消耗速率
 ,丙烷脱氢反应的平衡常数
,丙烷脱氢反应的平衡常数
 选择性
选择性 )
)(4)以
 作催化剂,对反应ⅲ的机理展开研究.以
作催化剂,对反应ⅲ的机理展开研究.以 和
和 为原料,初期产物中没有检测到
为原料,初期产物中没有检测到 ;以含有
;以含有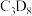 的
的 和
和 为原料,反应过程中没有检测到
为原料,反应过程中没有检测到 。下列推断合理的是
。下列推断合理的是A.
 先吸附氧气,吸附的氧气直接与吸附的丙烷反应
先吸附氧气,吸附的氧气直接与吸附的丙烷反应B.
 直接氧化吸附的丙烷,吸附的氧气补充
直接氧化吸附的丙烷,吸附的氧气补充 中反应掉的氧
中反应掉的氧C.
 催化丙烷脱氢过程中,碳氢键的断裂是可逆的
催化丙烷脱氢过程中,碳氢键的断裂是可逆的(5)用
 替换
替换 ,进行氧化丙烷脱氢,可避免丙烷深度氧化、
,进行氧化丙烷脱氢,可避免丙烷深度氧化、 资源化利用等优势。
资源化利用等优势。①结合键能数据分析
 氧化丙烷脱氢反应的挑战和难点
氧化丙烷脱氢反应的挑战和难点②
 也可以进行氧化乙苯脱氢制取苯乙烯,
也可以进行氧化乙苯脱氢制取苯乙烯, 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( ,
, 表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。
位点带部分负电荷)。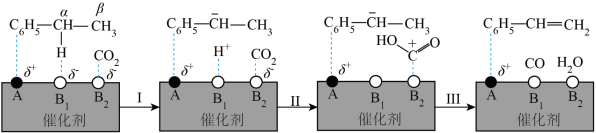
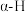 带部分正电荷,被带部分负电荷的
带部分正电荷,被带部分负电荷的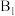 位点吸引,随后解离出
位点吸引,随后解离出 并吸附在
并吸附在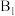 位点上;步骤Ⅱ可描述为:
位点上;步骤Ⅱ可描述为:
您最近一年使用:0次
名校
解题方法
3 . T℃时,在容积为1.5L的恒容密闭容器内充入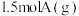 发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,回答下列问题:
发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,回答下列问题:___________ 。
(2)达到平衡时,B的物质的量浓度为___________  ,A的转化率为
,A的转化率为___________ %,0~2min内A的平均反应速率为___________  。
。
(3)若将反应容器的容积压缩为1L,达到平衡所需的时间将___________ (填“延长”“缩短”或“不变”)。
(4)判断该反应达到平衡状态的标志是___________ (填标号)。
a.A和B的浓度相等 b.B的生成速率与C的消耗速率相等
c.容器中混合气体的密度保持不变 d.容器中气体的平均摩尔质量不变
(5)T℃下,若将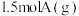 充入如图所示的可变容器中(起始时容器体积为1.5L),平衡时活塞所处位置如图。
充入如图所示的可变容器中(起始时容器体积为1.5L),平衡时活塞所处位置如图。___________ %。
②该温度下,体积可变容器中进行该反应时A的平衡转化率比恒容容器中进行该反应时A的平衡转化率___________ (填“高”或“低”)。
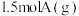 发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,回答下列问题:
发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,回答下列问题:
(2)达到平衡时,B的物质的量浓度为
 ,A的转化率为
,A的转化率为 。
。(3)若将反应容器的容积压缩为1L,达到平衡所需的时间将
(4)判断该反应达到平衡状态的标志是
a.A和B的浓度相等 b.B的生成速率与C的消耗速率相等
c.容器中混合气体的密度保持不变 d.容器中气体的平均摩尔质量不变
(5)T℃下,若将
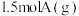 充入如图所示的可变容器中(起始时容器体积为1.5L),平衡时活塞所处位置如图。
充入如图所示的可变容器中(起始时容器体积为1.5L),平衡时活塞所处位置如图。
②该温度下,体积可变容器中进行该反应时A的平衡转化率比恒容容器中进行该反应时A的平衡转化率
您最近一年使用:0次
2024-06-02更新
|
98次组卷
|
2卷引用:福建省龙岩市2023-2024学年高一下学期期中考试化学试题
4 . 苯乙烯是生产塑料、橡胶的重要原料,工业上以铁钴催化剂催化乙苯催化脱氢可获得苯乙烯。主要发生的反应为:_______ 。
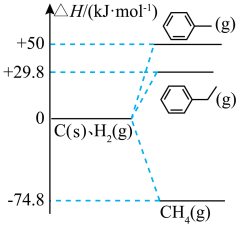
(2)已知,在298K、101kPa条件下,某些物质的相对能量(△H)变化关系如图所示,则△H2=_______ kJ•mol-1。_______ 。
(4)往刚性密闭容器中同时通入乙苯和一定比例水蒸气,控制反应温度为600℃、体系起始总压强为100kPa的条件下进行反应。
①通入水蒸气的作用有_______ 。
②假设容器中只发生反应I,测得体系总压和乙苯转化率随时间变化结果如图所示。_______ kPa,平衡常数Kp=_______ kPa(Kp为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
③反应速率v正=k正×p(乙苯),v逆=k逆×p(苯乙烯)×p(氢气),k正、k逆分别为正、逆反应速率常数,则a点时 =
=_______ 。
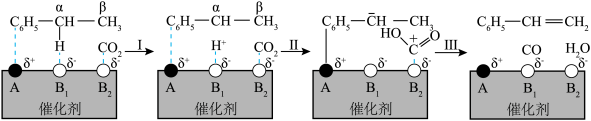
(5)工业上也可以利用CO2弱氧化性在催化剂条件下制备苯乙烯,其反应的机理如图所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,B1、B2位点带部分负电荷)。αC—H的极性_______ (选填“>”或“<”)βC—H,步骤Ⅲ形成苯乙烯后更容易脱附的原因为_______ 。
反应I: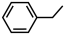 (g)
(g)
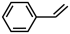 (g)+H2(g) △H1=+117.6kJ•mol-1
(g)+H2(g) △H1=+117.6kJ•mol-1
反应Ⅱ: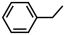 (g)+H2(g)
(g)+H2(g)
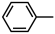 (g)+CH4(g) △H2
(g)+CH4(g) △H2
反应Ⅲ: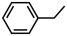 (g)
(g) 8C(s)+H2(g) △H3=-1.67kJ•mol-1
8C(s)+H2(g) △H3=-1.67kJ•mol-1
(2)已知,在298K、101kPa条件下,某些物质的相对能量(△H)变化关系如图所示,则△H2=
| A.v正(C6H5C2H5)=v正(C6H5C2H3) | B.容器内气体密度不再变化 |
| C.苯乙烯、H2的分子数之比不再变化 | D.气体的平均相对分子质量不再变化 |
(4)往刚性密闭容器中同时通入乙苯和一定比例水蒸气,控制反应温度为600℃、体系起始总压强为100kPa的条件下进行反应。
①通入水蒸气的作用有
②假设容器中只发生反应I,测得体系总压和乙苯转化率随时间变化结果如图所示。
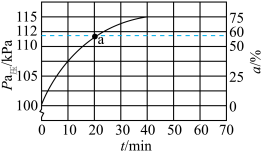
③反应速率v正=k正×p(乙苯),v逆=k逆×p(苯乙烯)×p(氢气),k正、k逆分别为正、逆反应速率常数,则a点时
 =
=(5)工业上也可以利用CO2弱氧化性在催化剂条件下制备苯乙烯,其反应的机理如图所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,B1、B2位点带部分负电荷)。αC—H的极性
您最近一年使用:0次
5 . 一定条件下的密闭容器中,可逆反应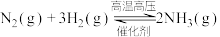 达到平衡时,下列说法正确的是
达到平衡时,下列说法正确的是
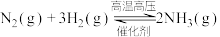 达到平衡时,下列说法正确的是
达到平衡时,下列说法正确的是| A.正反应速率为0 |
B. 、 、 、 、 的百分含量相等 的百分含量相等 |
C. 的浓度不再随时间的变化而变化 的浓度不再随时间的变化而变化 |
D. 、 、 、 、 的物质的量之比为1∶3∶2 的物质的量之比为1∶3∶2 |
您最近一年使用:0次
解题方法
6 . 在一定条件下,对于密闭容器中进行的反应: ,下列说法能充分说明该反应已达到化学平衡状态的是
,下列说法能充分说明该反应已达到化学平衡状态的是
 ,下列说法能充分说明该反应已达到化学平衡状态的是
,下列说法能充分说明该反应已达到化学平衡状态的是A. 、 、 完全转化为 完全转化为 | B. 、 、 、 、 的浓度一定相等 的浓度一定相等 |
| C.正、逆反应速率相等且等于零 | D. 、 、 、 、 的浓度不再改变 的浓度不再改变 |
您最近一年使用:0次
名校
解题方法
7 . 道路千万条,安全第一条。当汽车在高速行驶中受到猛烈撞击时,会产生大量气体充满气囊,从而保护驾驶员和乘客的安全。
Ⅰ.安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示:______ (填“吸热”或“放热”)反应。
(2)若爆炸过程中有24mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应吸收(或释放)的能量为______ kJ(用含a、b的代数式表示)。
Ⅱ.汽车尾气中的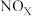 是常见的一种大气污染物,在2L密闭容器内,800℃时反应
是常见的一种大气污染物,在2L密闭容器内,800℃时反应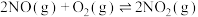 体系中,
体系中, 随时间的变化如表:
随时间的变化如表:
(3)下图表示 的变化的曲线是
的变化的曲线是______ ______ (选填序号,下同)。
a.容器内气体的颜色不再变化 b.
c. d.消耗
d.消耗 的同时生成
的同时生成
(5)为使该反应的反应速率增大,下列措施正确的是______ 。
a.增大 的浓度 b.适当升高温度 c.及时分离出
的浓度 b.适当升高温度 c.及时分离出 气体
气体
Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应 为原理设计成利用率高的燃料电池,装置如图所示:
为原理设计成利用率高的燃料电池,装置如图所示:______ 极(填写“正”或“负”),M处电极反应式是______ ;
(7)该电池产生11.2L(标况下) ,则外电路中转移的电子数目为
,则外电路中转移的电子数目为______ 。
Ⅰ.安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示:
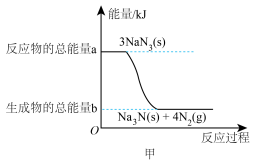
(2)若爆炸过程中有24mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应吸收(或释放)的能量为
Ⅱ.汽车尾气中的
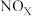 是常见的一种大气污染物,在2L密闭容器内,800℃时反应
是常见的一种大气污染物,在2L密闭容器内,800℃时反应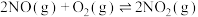 体系中,
体系中, 随时间的变化如表:
随时间的变化如表:时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(3)下图表示
 的变化的曲线是
的变化的曲线是 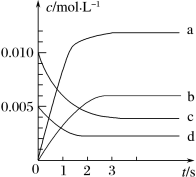
a.容器内气体的颜色不再变化 b.

c.
 d.消耗
d.消耗 的同时生成
的同时生成
(5)为使该反应的反应速率增大,下列措施正确的是
a.增大
 的浓度 b.适当升高温度 c.及时分离出
的浓度 b.适当升高温度 c.及时分离出 气体
气体Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应
 为原理设计成利用率高的燃料电池,装置如图所示:
为原理设计成利用率高的燃料电池,装置如图所示: 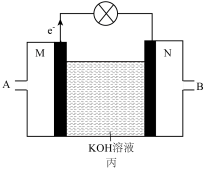
(7)该电池产生11.2L(标况下)
 ,则外电路中转移的电子数目为
,则外电路中转移的电子数目为
您最近一年使用:0次
8 .  和
和 催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。 的量不变,向体积相同的恒容密闭容器中分别通入
的量不变,向体积相同的恒容密闭容器中分别通入 为0:1、1:1、2:1、3:1的
为0:1、1:1、2:1、3:1的 的混合气,测得
的混合气,测得 的平衡转化率随温度的变化曲线如图2。
的平衡转化率随温度的变化曲线如图2。
Ⅰ.
Ⅱ.
Ⅲ.
(1) =
=___________ 。
(2)① =1:1对应图中曲线
=1:1对应图中曲线___________ (填序号)。
②900K下,曲线b、c、d的平衡转化率显著大于a的原理为___________ 。
(3)900K,将 =3:1的混合气通入恒容密闭容器中进行反应。
=3:1的混合气通入恒容密闭容器中进行反应。
①下列说法正确的是___________ (填序号)。
A.通入氩气可提高 的平衡转化率
的平衡转化率
B.体系达到平衡时,若缩小容器容积,反应Ⅱ平衡不移动
C.当 和
和 的比值不变时,体系达到平衡
的比值不变时,体系达到平衡
D.改善催化剂的性能可提高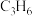 生产效率
生产效率
②若初始压强为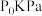 ,t min时达到平衡,此时
,t min时达到平衡,此时 分压是CO的5倍,0~t min内
分压是CO的5倍,0~t min内 =
=___________  ;反应Ⅰ的压强平衡常数
;反应Ⅰ的压强平衡常数 =
=___________ 。
(4)利用反应 可制备高纯Ni。
可制备高纯Ni。
① 晶体中不存在的作用力有
晶体中不存在的作用力有___________ 。
A.离子键 B.π键 C.范德华力 D.极性键 E.金属键
② 中Ni为
中Ni为 杂化,配位原子是
杂化,配位原子是___________ ,判断依据是___________ 。
 和
和 催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
 的量不变,向体积相同的恒容密闭容器中分别通入
的量不变,向体积相同的恒容密闭容器中分别通入 为0:1、1:1、2:1、3:1的
为0:1、1:1、2:1、3:1的 的混合气,测得
的混合气,测得 的平衡转化率随温度的变化曲线如图2。
的平衡转化率随温度的变化曲线如图2。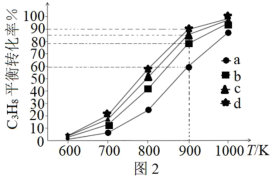
Ⅰ.

Ⅱ.

Ⅲ.

(1)
 =
=(2)①
 =1:1对应图中曲线
=1:1对应图中曲线②900K下,曲线b、c、d的平衡转化率显著大于a的原理为
(3)900K,将
 =3:1的混合气通入恒容密闭容器中进行反应。
=3:1的混合气通入恒容密闭容器中进行反应。①下列说法正确的是
A.通入氩气可提高
 的平衡转化率
的平衡转化率B.体系达到平衡时,若缩小容器容积,反应Ⅱ平衡不移动
C.当
 和
和 的比值不变时,体系达到平衡
的比值不变时,体系达到平衡D.改善催化剂的性能可提高
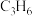 生产效率
生产效率②若初始压强为
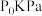 ,t min时达到平衡,此时
,t min时达到平衡,此时 分压是CO的5倍,0~t min内
分压是CO的5倍,0~t min内 =
= ;反应Ⅰ的压强平衡常数
;反应Ⅰ的压强平衡常数 =
=(4)利用反应
 可制备高纯Ni。
可制备高纯Ni。①
 晶体中不存在的作用力有
晶体中不存在的作用力有A.离子键 B.π键 C.范德华力 D.极性键 E.金属键
②
 中Ni为
中Ni为 杂化,配位原子是
杂化,配位原子是
您最近一年使用:0次
9 . 甲硫醇(CH3SH)是重要的有机化工中间体,可用于合成维生素。通过CH3OH和H2S合成CH3SH的主要反应为:
Ⅰ.
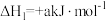
Ⅱ.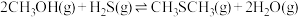
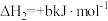
回答下列问题:
(1)计算反应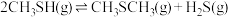 的△H=
的△H=________ kJ/mol。
(2)T1℃时,向恒容密闭容器中充入一定量CH3OH(g)和H2S(g)发生反应,下列事实能说明反应达到平衡状态的是________ (填选项字母);若按相同比例再充入一定量CH3OH(g)和H2S(g),CH3OH(g)的平衡转化率将________ (填“变大”“变小”或“不变”)。
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C.H2S(g)的体积分数不再发生变化 D.CH3SCH3(g)和H2O(g)的物质的量之比不再变化
(3)T2℃时,向压强为P0的恒压密闭容器中按物质的量之比为1:2充入CH3OH(g)和H2S(g)发生反应,达到平衡时,CH3OH(g)的转化率为80%,CH3SCH3(g)的体积分数为5%。
①计算H2S(g)的选择性为________ (CH3SH的选择性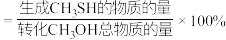 )。
)。
②反应Ⅰ的平衡常数Kp=________ (Kp是用分压表示的平衡常数,结果保留两位小数)。
(4)在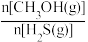 =1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。
=1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。________ Mpa/min(结果保留两位有效数字)。
②当温度高于370℃时,CH3OH(g)转化率随温度升高而降低的原因可能为________ 。
③从电负性的角度描述ⅲ→ⅰ中脱水的过程:________ 。
Ⅰ.

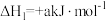
Ⅱ.
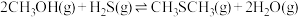
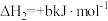
回答下列问题:
(1)计算反应
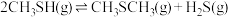 的△H=
的△H=(2)T1℃时,向恒容密闭容器中充入一定量CH3OH(g)和H2S(g)发生反应,下列事实能说明反应达到平衡状态的是
A.容器内气体密度不再发生变化 B.混合气体的平均相对分子质量不再发生变化
C.H2S(g)的体积分数不再发生变化 D.CH3SCH3(g)和H2O(g)的物质的量之比不再变化
(3)T2℃时,向压强为P0的恒压密闭容器中按物质的量之比为1:2充入CH3OH(g)和H2S(g)发生反应,达到平衡时,CH3OH(g)的转化率为80%,CH3SCH3(g)的体积分数为5%。
①计算H2S(g)的选择性为
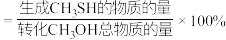 )。
)。②反应Ⅰ的平衡常数Kp=
(4)在
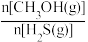 =1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。
=1:2、反应压力为0.7Mpa条件下,气体按90 mL/min的速率通过催化剂表面发生反应,每分钟反应体系中CH3OH(g)转化率、CH3SH(g)选择性随温度的变化如图甲所示,催化机理如图乙所示。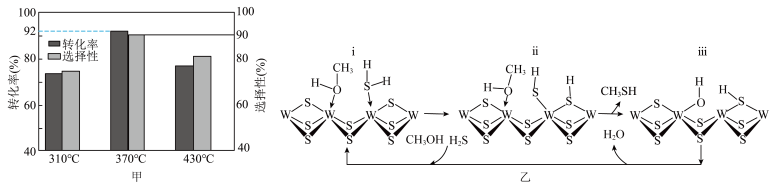
②当温度高于370℃时,CH3OH(g)转化率随温度升高而降低的原因可能为
③从电负性的角度描述ⅲ→ⅰ中脱水的过程:
您最近一年使用:0次
名校
10 . 化学反应过程既有物质变化也有能量变化。
Ⅰ.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436 、391
、391 、946
、946 。请根据键能的数据判断下列问题。
。请根据键能的数据判断下列问题。
(1)由 和
和 合成氨时,需要
合成氨时,需要_____________ (填“吸收”或“放出”)能量,写出该反应的热化学方程式_________________ 。
Ⅱ.原电池是化学能转化为电能的装置。
(2)肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图。_______ (填“氧化反应”或“还原反应”),电池工作过程中, 向极移动
向极移动_________ (填“A”或“B”);
②该燃料电池的总反应方程式可表示为__________ 。在标准状况下,若A极区产生11.2L  ,则外电路中理论上通过的电子的物质的量是
,则外电路中理论上通过的电子的物质的量是__________ mol。
Ⅲ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:_____________ 。
(4)反应开始至2min,以气体X表示的平均反应速率为___________ 。
(5)下列措施能增大反应速率的是_________ 。
A.升高温度 B.加入高效催化剂
C.持容器压强不变,充入一定量氦气 D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
(6)能说明上述反应达到平衡状态的是 。(填字母)
Ⅰ.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436
 、391
、391 、946
、946 。请根据键能的数据判断下列问题。
。请根据键能的数据判断下列问题。(1)由
 和
和 合成氨时,需要
合成氨时,需要Ⅱ.原电池是化学能转化为电能的装置。
(2)肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图。
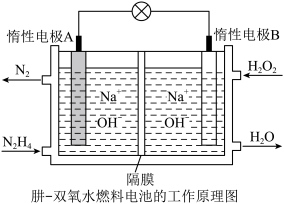
 向极移动
向极移动②该燃料电池的总反应方程式可表示为
 ,则外电路中理论上通过的电子的物质的量是
,则外电路中理论上通过的电子的物质的量是Ⅲ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
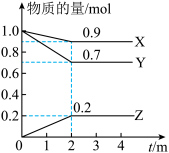
(4)反应开始至2min,以气体X表示的平均反应速率为
(5)下列措施能增大反应速率的是
A.升高温度 B.加入高效催化剂
C.持容器压强不变,充入一定量氦气 D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
(6)能说明上述反应达到平衡状态的是 。(填字母)
| A.混合气体的压强不随时间的变化而变化 | B. |
| C.X体积分数保持不变 | D.混合气体的密度不随时间的变化而变化 |
您最近一年使用:0次





 )
)