名校
解题方法
1 . 利用化学反应原理分析指导工业生产具有重要的现实意义,回答下列问题。___________ 。
(2)合成氨的反应,T1℃时在容积为2L的恒容密闭容器中通入2molN2和5molH2发生反应。5min时反应达到平衡状态,达平衡时N2(g)的转化率为50%,求:
①0~5min内该反应的平均速率v(H2)=___________ mol/(L•min);平衡常数K=___________ 。___________ (填序号)。
a.升高温度 b.将平衡体系中的NH3(g)分离出来
c.减小容器的体积增大体系压强 d.加入合适的催化剂
(3)泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式___________ 。
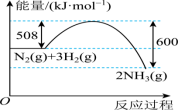
(2)合成氨的反应,T1℃时在容积为2L的恒容密闭容器中通入2molN2和5molH2发生反应。5min时反应达到平衡状态,达平衡时N2(g)的转化率为50%,求:
①0~5min内该反应的平均速率v(H2)=
②相同条件下,改变反应物的起始通入量,某时刻测得N2、H2、NH3的物质的量分别为2mol、4mol、2mol,则此时反应达到平衡状态 ),v正
),v正
a.升高温度 b.将平衡体系中的NH3(g)分离出来
c.减小容器的体积增大体系压强 d.加入合适的催化剂
(3)泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式
您最近一年使用:0次
2 . 在恒温恒容密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应:
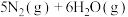 。下列不能说明该反应已达到平衡状态的是
。下列不能说明该反应已达到平衡状态的是
 ,在一定条件下发生反应:
,在一定条件下发生反应:
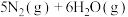 。下列不能说明该反应已达到平衡状态的是
。下列不能说明该反应已达到平衡状态的是A.反应速率 |
| B.容器内压强不再随时间变化而发生变化 |
| C.容器内气体的平均相对分子质量不再改变 |
D.容器内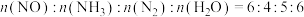 |
您最近一年使用:0次
3 . 某温度下,在1 L恒容密闭容器中3.0 mol A发生反应 ,有关数据如下:
,有关数据如下:
下列说法错误的是
 ,有关数据如下:
,有关数据如下:| 时间段/min | 产物C的平均生成速率/mol·L-1·min-1 |
| 0~2 | 0.20 |
| 0~4 | 0.15 |
| 0~6 | 0.10 |
| A.当容器内压强不再变化时,反应达到平衡状态 |
| B.2 min时,加入0.2 mol C,此时平衡逆向移动 |
| C.该温度下的平衡常数K=0.108 |
| D.5 min时,A的物质的量为2.1 mol |
您最近一年使用:0次
4 . 由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一
反应②: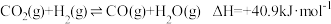
反应③: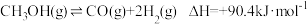
(1)反应①: 的
的
_______ 。
(2) 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。_______ 逆反应速率(填“>或<或=”)。
②下列叙述能说明上述反应能达到化学平衡状态的是_______ 。(填字母)。
a.3v(CO2)=v(H2) b. 的体积分数不再改变
的体积分数不再改变
c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后 2的平衡转化率降低的原因
2的平衡转化率降低的原因_______
(3)往一容积为 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与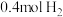 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是_______ ,则c点时 的体积分数是
的体积分数是_______ ;平衡后再加入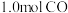 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率_______ (填“增大”或“不变”或“减小”)。
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一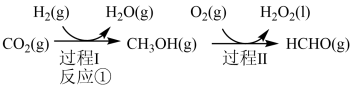
反应②:
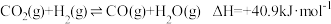
反应③:
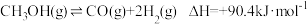
(1)反应①:
 的
的
(2)
 2的转化率与温度的关系如图所示。
2的转化率与温度的关系如图所示。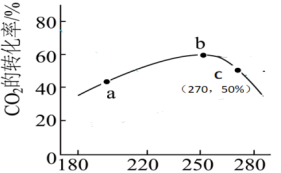
②下列叙述能说明上述反应能达到化学平衡状态的是
a.3v(CO2)=v(H2) b.
 的体积分数不再改变
的体积分数不再改变c.消耗1mol CO2的同时消耗3mol H2 d.混合气体的平均相对分子质量不再改变
③250℃后
 2的平衡转化率降低的原因
2的平衡转化率降低的原因(3)往一容积为
 的密闭容器内,充入0.2mol CO2与
的密闭容器内,充入0.2mol CO2与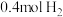 发生反应,反应达到c点时,从上图像可知在平衡时
发生反应,反应达到c点时,从上图像可知在平衡时 2的转化率是
2的转化率是 的体积分数是
的体积分数是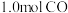 2后重新到达平衡,则H2的转化率
2后重新到达平衡,则H2的转化率
您最近一年使用:0次
解题方法
5 . 中国科学家首次实现了二氧化碳到淀粉的全合成,相关成果于北京时间 9 月 24 日由国际知名学术期刊《科学》在线发表。CO2的捕集、利用与封存是科学家研究的重要课题,利用 CH4与 CO2制备“合成气”(CO、H2),合成气可直接制备甲醇,反应原理为:

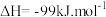 。
。
(1)已知:
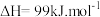 ,部分键能数据如下:(CO 的结构式为 C≡O)
,部分键能数据如下:(CO 的结构式为 C≡O)
计算 C—H 的键能 x= ______________ kJ/mol,(保留一位小数)。
(2)若要该反应自发进行,_______ (填“高温”或“低温”)更有利,该反应必须在高温下才能启动,原因是_______ 。
(3)已知:H2 (g)的燃烧热ΔH=-285.8kJ.mol-1,写出H2 (g)燃烧热的热化学反应方程式____________ 。
(4)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是_______(填字母序号)。
(5)T1℃下,在 2L 恒容密闭容器中充入 2molCO 和 6molH2合成 CH3OH(g),测得 CO 的物质的量浓度随反应时间的变化如图所示:_______ 。
②T1℃时,该反应的化学平衡常数 K=_______ 。
③10min 时,改变的外界条件可能是_______ 。
(6)T1℃下,在 1L 恒容密闭容器中充入 2molCO、2molH2和 3molCH3OH(g),此时反应将_______ (填“向左进行”“向右进行”“达到平衡”或“无法判断”)。

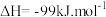 。
。(1)已知:

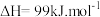 ,部分键能数据如下:(CO 的结构式为 C≡O)
,部分键能数据如下:(CO 的结构式为 C≡O)| 共价键 | C≡O | C—O | C—H | O—H | H—H |
| 键能/(kJ/mol) | 1072 | 326 | 464 | 436 |
(2)若要该反应自发进行,
(3)已知:H2 (g)的燃烧热ΔH=-285.8kJ.mol-1,写出H2 (g)燃烧热的热化学反应方程式
(4)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是_______(填字母序号)。
| A.混合气体的平均相对分子质量不再变化 |
| B.混合气体的密度不再变化 |
| C.CO 的百分含量不再变化 |
| D.CO、H2、CH3OH 的物质的量之比为 1∶2∶1 |
(5)T1℃下,在 2L 恒容密闭容器中充入 2molCO 和 6molH2合成 CH3OH(g),测得 CO 的物质的量浓度随反应时间的变化如图所示:
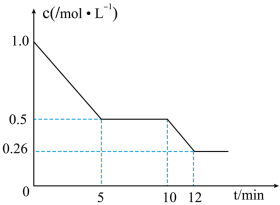
②T1℃时,该反应的化学平衡常数 K=
③10min 时,改变的外界条件可能是
(6)T1℃下,在 1L 恒容密闭容器中充入 2molCO、2molH2和 3molCH3OH(g),此时反应将
您最近一年使用:0次
6 . 含氮化合物是化工、能源、环保等领域的研究热点。
(1)工业上常用NH3和CO2合成尿素[CO(NH2)2],利用该反应可以在一定程度上减缓温室效应。该反应可分两步进行,其能量变化和反应历程如图所示___________ ;
②合成尿素总反应自发进行的条件是___________ (填“高温”或“低温”)。
(2)一定温度下,将NH3和CO2按2:1的物质的量之比充入一容积恒为10L的密闭容器中发生总反应。15min时达到平衡,各物质的浓度变化曲线如图所示。___________ g min﹣1。
min﹣1。
②下列叙述中能说明该反应达到平衡状态的是___________ (填选项字母)。
A.体系压强不再变化
B.NH3和CO2的浓度之比为2:1
C.气体平均摩尔质量不再变化
D.NH3的消耗速率和CO2的消耗速率之比为2:1
③25min时再向容器中充入2mol的NH3、1molCO2和2molH2O,则此时平衡___________ (填“正向移动”或“逆向移动”),再次平衡时总反应的平衡常数为 ___________ 。
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量NO。中国科学家在以H2为还原剂清除NO的研究方面取得了显著成果,其化学方程式为2NO(g)+2H2(g)⇌N2(g)+2H2O(g) ΔH<0。当固定比例的NO(g)和H2(g)的混合气体,以相同流速分别通过填充有两种催化剂的反应器,测得NO的转化率与温度的关系如图所示。___________ 。
②M、N、P、Q四点中一定未达到平衡状态的是___________ (填字母)。
(1)工业上常用NH3和CO2合成尿素[CO(NH2)2],利用该反应可以在一定程度上减缓温室效应。该反应可分两步进行,其能量变化和反应历程如图所示

②合成尿素总反应自发进行的条件是
(2)一定温度下,将NH3和CO2按2:1的物质的量之比充入一容积恒为10L的密闭容器中发生总反应。15min时达到平衡,各物质的浓度变化曲线如图所示。

 min﹣1。
min﹣1。②下列叙述中能说明该反应达到平衡状态的是
A.体系压强不再变化
B.NH3和CO2的浓度之比为2:1
C.气体平均摩尔质量不再变化
D.NH3的消耗速率和CO2的消耗速率之比为2:1
③25min时再向容器中充入2mol的NH3、1molCO2和2molH2O,则此时平衡
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量NO。中国科学家在以H2为还原剂清除NO的研究方面取得了显著成果,其化学方程式为2NO(g)+2H2(g)⇌N2(g)+2H2O(g) ΔH<0。当固定比例的NO(g)和H2(g)的混合气体,以相同流速分别通过填充有两种催化剂的反应器,测得NO的转化率与温度的关系如图所示。
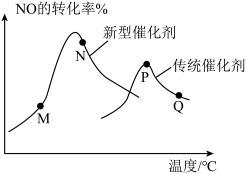
②M、N、P、Q四点中一定未达到平衡状态的是
您最近一年使用:0次
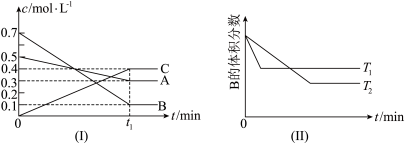
7 . I.T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如(Ⅱ)所示:
(1)反应的化学方程式为___________ 。
(2)当反应达到平衡后升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量___________ (填“变大”、“变小”或“不变”)。
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(3)一般说化学平衡常数数值K___________ ,通常认为该反应进行较完全。
(4)该反应为___________ 反应(填“吸热”或“放热”)。
(5)能判断该反应是否达到化学平衡状态的依据是___________。
(6)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为___________ 。
(1)反应的化学方程式为
(2)当反应达到平衡后升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)一般说化学平衡常数数值K
(4)该反应为
(5)能判断该反应是否达到化学平衡状态的依据是___________。
| A.v正(H2) = v逆(H2O) | B.反应停止,正、逆反应速率都等于零 |
| C.容器中压强不再发生变化 | D.混合气体中c(CO2)不变 |
(6)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为
您最近一年使用:0次
解题方法
8 . 已知橙红色的配离子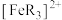 可被
可被 氧化成淡蓝色的配离子
氧化成淡蓝色的配离子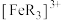 (
( 的还原产物是
的还原产物是 ),现用浓度分别为
),现用浓度分别为 、
、 、
、 的
的 溶液进行实验,
溶液进行实验,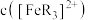 随时间
随时间 的变化曲线如图所示。下列有关说法错误的是
的变化曲线如图所示。下列有关说法错误的是
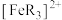 可被
可被 氧化成淡蓝色的配离子
氧化成淡蓝色的配离子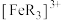 (
( 的还原产物是
的还原产物是 ),现用浓度分别为
),现用浓度分别为 、
、 、
、 的
的 溶液进行实验,
溶液进行实验,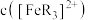 随时间
随时间 的变化曲线如图所示。下列有关说法错误的是
的变化曲线如图所示。下列有关说法错误的是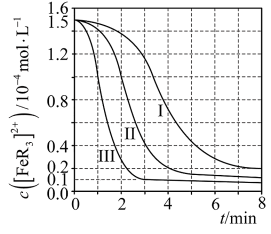
A.实验中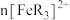 、 、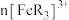 之和不变时,反应达到平衡状态 之和不变时,反应达到平衡状态 |
| B.三组实验中,反应速率都是前期速率增加,后期速率减小 |
C. 的硝酸进行实验,平衡时 的硝酸进行实验,平衡时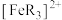 的平均消耗速率为 的平均消耗速率为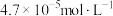 |
D.平衡后加水稀释, 增大 增大 |
您最近一年使用:0次
9 . 工业合成氨是人类科学技术的一项重大突破,对人类生存和发展有着重要意义。
(1)一定温度下,在2L恒容密闭容器中充入0.2mol的N2和0.6mol的H2发生反应:N2+3H2 2NH3
2NH3  H<0,若在5min时测得NH3的物质的量为0.2mol,则前5min中平均反应速率v(N2)=
H<0,若在5min时测得NH3的物质的量为0.2mol,则前5min中平均反应速率v(N2)= ___________ mol/(L·min)。此时能说明反应一定达到化学平衡状态的是___________ 。
A.NH3的体积分数不再改变 B.容器内气体的质量不再改变
C.容器内的压强不再改变 D.v正(N2)=2v逆(NH3)
(2)合成氨生产流程示意图如下。___________ ,提高原料利用率。流程中其他有利于提高原料利用率的措施是___________ ;有利于提高单位时间内氨的产率的措施有___________ 。(至少写出两点)
②根据下表各物质的沸点判断,要将产物NH3与N2、H2分离开来,最适宜的温度应该控制在___________ 。
A.-195.8℃<t<-33.35℃ B. -252℃<t<-195.8℃ C.-252℃<t<-33.35℃
(3)对于合成氨的反应,下列图像一定正确的是___________。
(1)一定温度下,在2L恒容密闭容器中充入0.2mol的N2和0.6mol的H2发生反应:N2+3H2
 2NH3
2NH3  H<0,若在5min时测得NH3的物质的量为0.2mol,则前5min中平均反应速率v(N2)=
H<0,若在5min时测得NH3的物质的量为0.2mol,则前5min中平均反应速率v(N2)= A.NH3的体积分数不再改变 B.容器内气体的质量不再改变
C.容器内的压强不再改变 D.v正(N2)=2v逆(NH3)
(2)合成氨生产流程示意图如下。

②根据下表各物质的沸点判断,要将产物NH3与N2、H2分离开来,最适宜的温度应该控制在
| 物质 | H2 | N2 | NH3 |
| 沸点 | -252℃ | -195.8℃ | -33.35℃ |
(3)对于合成氨的反应,下列图像一定正确的是___________。
A.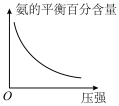 | B.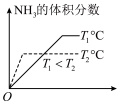 | C.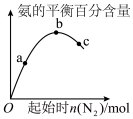 | D. |
您最近一年使用:0次
解题方法
10 . 工业上采用高温活性炭催化CO与C12合成光气(COCl2)。T℃时,向2L刚性密闭容器中充入2molCO气体、2molCl2气体和适量的活性炭,发生反应:CO(g)+Cl2(g) COCl2(g)
COCl2(g)  H<0,测得混合气中COCl2的体积分数
H<0,测得混合气中COCl2的体积分数 (COCl2)随时间t的关系如图曲线I所示。下列说法正确的是
(COCl2)随时间t的关系如图曲线I所示。下列说法正确的是
 COCl2(g)
COCl2(g)  H<0,测得混合气中COCl2的体积分数
H<0,测得混合气中COCl2的体积分数 (COCl2)随时间t的关系如图曲线I所示。下列说法正确的是
(COCl2)随时间t的关系如图曲线I所示。下列说法正确的是
A.当体系中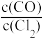 保持不变,则该反应达到化学平衡状态 保持不变,则该反应达到化学平衡状态 |
| B.曲线Ⅱ相对曲线I改变的条件可能升高温度 |
| C.A点时,向容器中加入等物质的量CO和Cl2,反应速率减小 |
| D.A点CO的转化率为60% |
您最近一年使用:0次



