解题方法
1 . 丙烯是一种重要的化工原料,工业上丙烷制丙烯的相关反应如下:
ⅰ.
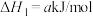
ⅱ.

ⅲ.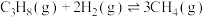
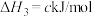
回答下列问题:
Ⅰ.单独投料(副反应抑制法)。
(1)反应: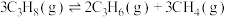

_________  。
。
(2) 时,单独加入
时,单独加入 至
至 后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数
后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数 见下表。
见下表。
①若只考虑体系中反应ⅱ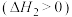 ,以下操作有利于减小
,以下操作有利于减小 平衡转化率的是
平衡转化率的是___________ (填字母)。
A.通入少量 B.使用高选择性催化剂 C.降温 D.减压
B.使用高选择性催化剂 C.降温 D.减压
② 内
内 消耗的平均速率:反应ⅰ
消耗的平均速率:反应ⅰ_________ 反应ⅱ(填“<”、“>”或“=”)。
(3)一定温度下,向 恒容密闭容器中通入
恒容密闭容器中通入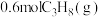 ,压强为
,压强为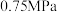 ,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数
,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数 总压)为
总压)为 、
、 ,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
___________ 。
Ⅱ.共进料投料(耦合反应法)。
工业上也常采用 与
与 共进料投料,通过发生耦合反应制丙烯,反应如下:
共进料投料,通过发生耦合反应制丙烯,反应如下:
(4) 为用压强表示的反应平衡常数,一定温度下:
为用压强表示的反应平衡常数,一定温度下:
ⅰ.

ⅳ.
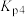
则体系中反应

___________ (用含 、
、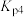 的式子表示)。
的式子表示)。
(5)实际工艺生产中按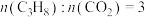 进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:
进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:________ (填“吸热”或“放热”)反应,在________ (填“高温”或“低温”)下进行自发反应。
②生产中温度须不低于 ,原因是
,原因是___________ 。
ⅰ.

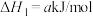
ⅱ.


ⅲ.
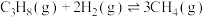
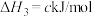
回答下列问题:
Ⅰ.单独投料(副反应抑制法)。
(1)反应:
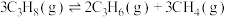

 。
。(2)
 时,单独加入
时,单独加入 至
至 后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数
后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数 见下表。
见下表。| 物质 |  |  |  |  |
体积分数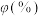 | 18 | 20 | 47 | 0 |
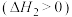 ,以下操作有利于减小
,以下操作有利于减小 平衡转化率的是
平衡转化率的是A.通入少量
 B.使用高选择性催化剂 C.降温 D.减压
B.使用高选择性催化剂 C.降温 D.减压②
 内
内 消耗的平均速率:反应ⅰ
消耗的平均速率:反应ⅰ(3)一定温度下,向
 恒容密闭容器中通入
恒容密闭容器中通入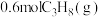 ,压强为
,压强为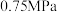 ,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数
,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数 总压)为
总压)为 、
、 ,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
Ⅱ.共进料投料(耦合反应法)。
工业上也常采用
 与
与 共进料投料,通过发生耦合反应制丙烯,反应如下:
共进料投料,通过发生耦合反应制丙烯,反应如下:
(4)
 为用压强表示的反应平衡常数,一定温度下:
为用压强表示的反应平衡常数,一定温度下:ⅰ.


ⅳ.

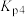
则体系中反应


 、
、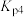 的式子表示)。
的式子表示)。(5)实际工艺生产中按
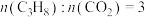 进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:
进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析: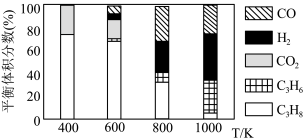
②生产中温度须不低于
 ,原因是
,原因是
您最近一年使用:0次
解题方法
2 . 已知 溶液中存在平衡:
溶液中存在平衡:
 。
。 溶液为橙色,
溶液为橙色, 溶液为黄色。为探究浓度对化学平衡的影响,某兴趣小组设计了如下实验方案。
溶液为黄色。为探究浓度对化学平衡的影响,某兴趣小组设计了如下实验方案。
Ⅰ.方案讨论
(1)ⅰ~ⅳ中依据减少生成物浓度可导致平衡移动的原理设计的是___________ (填序号)。
(2)已知 为黄色沉淀。某同学认为试剂X还可设计为
为黄色沉淀。某同学认为试剂X还可设计为 溶液,加入该试剂后,平衡向着
溶液,加入该试剂后,平衡向着___________ (填“正反应”或“逆反应”)方向移动,溶液颜色将___________ (填“变深”、“变浅”或“不变”)。
Ⅱ.实验分析
(3)实验ⅰ没有观察到预期现象的原因是___________ ,实验ⅱ的原因与其相似。
(4)通过实验ⅲ和ⅳ得出的结论为___________ 。
(5)某同学认为将ⅲ中浓盐酸替换为浓硫酸也可得出相应的实验结论。用浓硫酸替换浓盐酸___________ (填“能”或“不能”)达到预期目的,理由是___________ 。
(6)某同学查阅资料发现: 溶液与浓盐酸可发生氧化还原反应,但实验i中没有观察到明显现象,小组同学设计了两个实验,验证了该反应的发生。
溶液与浓盐酸可发生氧化还原反应,但实验i中没有观察到明显现象,小组同学设计了两个实验,验证了该反应的发生。
①方案一:取5mL浓盐酸,向其中加入15滴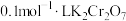 溶液,一段时间后,溶液变为绿色(
溶液,一段时间后,溶液变为绿色( 水溶液呈绿色),有黄绿色气体生成。写出发生反应的化学方程式
水溶液呈绿色),有黄绿色气体生成。写出发生反应的化学方程式___________ 。
②请你设计方案二:___________ 。
 溶液中存在平衡:
溶液中存在平衡:
 。
。 溶液为橙色,
溶液为橙色, 溶液为黄色。为探究浓度对化学平衡的影响,某兴趣小组设计了如下实验方案。
溶液为黄色。为探究浓度对化学平衡的影响,某兴趣小组设计了如下实验方案。 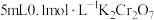 溶液 溶液 | 序号 | 试剂X |
| ⅰ | 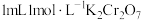 溶液 溶液 | |
| ⅱ | 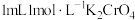 溶液 溶液 | |
| ⅲ | 5~15滴浓盐酸 | |
| ⅳ | 5~15滴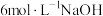 溶液 溶液 |
(1)ⅰ~ⅳ中依据减少生成物浓度可导致平衡移动的原理设计的是
(2)已知
 为黄色沉淀。某同学认为试剂X还可设计为
为黄色沉淀。某同学认为试剂X还可设计为 溶液,加入该试剂后,平衡向着
溶液,加入该试剂后,平衡向着Ⅱ.实验分析
| 序号 | 试剂X | 预期现象 | 实际现象 |
| ⅰ | 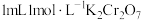 溶液 溶液 | 溶液变黄 | 溶液橙色加深 |
| ⅱ | 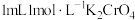 溶液 溶液 | 溶液橙色加深 | 溶液颜色变浅 |
| ⅲ | 5~15滴浓盐酸 | 溶液橙色加深 | 溶液橙色加深 |
| ⅳ | 5~15滴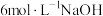 溶液 溶液 | 溶液变黄 | 溶液变黄 |
(3)实验ⅰ没有观察到预期现象的原因是
(4)通过实验ⅲ和ⅳ得出的结论为
(5)某同学认为将ⅲ中浓盐酸替换为浓硫酸也可得出相应的实验结论。用浓硫酸替换浓盐酸
(6)某同学查阅资料发现:
 溶液与浓盐酸可发生氧化还原反应,但实验i中没有观察到明显现象,小组同学设计了两个实验,验证了该反应的发生。
溶液与浓盐酸可发生氧化还原反应,但实验i中没有观察到明显现象,小组同学设计了两个实验,验证了该反应的发生。①方案一:取5mL浓盐酸,向其中加入15滴
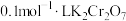 溶液,一段时间后,溶液变为绿色(
溶液,一段时间后,溶液变为绿色( 水溶液呈绿色),有黄绿色气体生成。写出发生反应的化学方程式
水溶液呈绿色),有黄绿色气体生成。写出发生反应的化学方程式②请你设计方案二:
您最近一年使用:0次
名校
解题方法
3 . 某研究小组查阅资料发现 与
与 的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在
的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在 ,并据此设计实验1(如图所示),发现溶液未变红。该小组对溶液未变红的原因进行了如下探究。
,并据此设计实验1(如图所示),发现溶液未变红。该小组对溶液未变红的原因进行了如下探究。

I、初步探究
实验2:用煮沸后的蒸馏水重新配制两种饱和溶液,并在注射器中进行实验,记录如下表。
(1)研究小组同学根据查阅资料写出的 与
与 反应的离子方程式为
反应的离子方程式为_____ 。
(2)小组同学做出推断:反应速率不是导致实验1中溶液未变红的主要原因,他们的理由是_____ 。
Ⅱ、查阅资料,继续探究。
资料: 为不溶于水的白色固体。
为不溶于水的白色固体。
实验3:

(3)试管a的实验现象说明滤液1中含有_____ 。
(4)试管b中,加入 溶液后所产生实验现象的原因是
溶液后所产生实验现象的原因是_____ 。
(5)甲同学对实验3提出了质疑,认为其实验现象并不能证明 氧化了
氧化了 。他提出如下假设:
。他提出如下假设:
i、可能是 氧化了
氧化了 ;
;
ii、可能是空气中的 氧化了
氧化了 。
。
他设计实施了实验4,实验记录如下表。
①试剂a是_____ 。
②依据实验4,甲同学做出判断:假设_____ 不成立。
(6)根据实验1~4可得实验1溶液未变红的原因是_____ 。
 与
与 的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在
的反应具有可逆性,推测亚铁盐与饱和碘水的混合液中会存在 ,并据此设计实验1(如图所示),发现溶液未变红。该小组对溶液未变红的原因进行了如下探究。
,并据此设计实验1(如图所示),发现溶液未变红。该小组对溶液未变红的原因进行了如下探究。
I、初步探究
实验2:用煮沸后的蒸馏水重新配制两种饱和溶液,并在注射器中进行实验,记录如下表。
| 编号 | 饱和 溶液 溶液 | 饱和碘水 | 操作 |  溶液 溶液 | 现象 |
| 2-1 | 1滴 |  | 不加热 | 1滴 | 无明显现象 |
| 2-2 | 1滴 |  | 加热一段时间后冷却 | 1滴 | 无明显现象 |
(1)研究小组同学根据查阅资料写出的
 与
与 反应的离子方程式为
反应的离子方程式为(2)小组同学做出推断:反应速率不是导致实验1中溶液未变红的主要原因,他们的理由是
Ⅱ、查阅资料,继续探究。
资料:
 为不溶于水的白色固体。
为不溶于水的白色固体。实验3:

(3)试管a的实验现象说明滤液1中含有
(4)试管b中,加入
 溶液后所产生实验现象的原因是
溶液后所产生实验现象的原因是(5)甲同学对实验3提出了质疑,认为其实验现象并不能证明
 氧化了
氧化了 。他提出如下假设:
。他提出如下假设:i、可能是
 氧化了
氧化了 ;
;ii、可能是空气中的
 氧化了
氧化了 。
。他设计实施了实验4,实验记录如下表。
| 编号 | 实验操作 | 实验现象 |
| 4 | 在试管中加入1滴 溶液, 溶液, 蒸馏水,1滴试剂a,一段时间后加入1滴 蒸馏水,1滴试剂a,一段时间后加入1滴 溶液 溶液 | 溶液不变红 |
②依据实验4,甲同学做出判断:假设
(6)根据实验1~4可得实验1溶液未变红的原因是
您最近一年使用:0次
4 . 一定温度下,在三个体积均为 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应:
下列说法正确的是
 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应:
| 容器编号 | 温度(℃) | 起始物质的量 | 平衡物质的量 | |||
 | 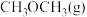 |  | 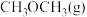 |  | ||
| ① | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
| ② | 387 | 0.40 | 0 | 0 | a | A |
| ③ | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
| A.该反应的正反应为吸热反应 |
B.容器②反应达到平衡时, |
| C.若容器①中反应达到平衡时增大压强,则各物质浓度保持不变 |
D.若起始向容器①中充入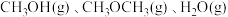 各 各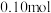 ,则反应将向正反应方向进行 ,则反应将向正反应方向进行 |
您最近一年使用:0次
5 . Ⅰ.以下是关于合成氨的有关问题,请回答:
(1)若在容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2+3H2 2NH3 △H<0,若5min反应达到平衡,此时测得NH3的物质的量为0.2mol。则0-5min内,用H2表示的化学反应速率为
2NH3 △H<0,若5min反应达到平衡,此时测得NH3的物质的量为0.2mol。则0-5min内,用H2表示的化学反应速率为___________ 。
(2)平衡后,若提高H2的转化率,可以采取的措施有___________。
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,其化学平衡常数K与温度t的关系如表所示:
2NH3(g) △H<0,其化学平衡常数K与温度t的关系如表所示:
请完成下列问题:
①试比较K1、K2的大小,K1___________ K2(填">”、“<”或“=”);
②400℃时,反应2NH3(g) N2(g)+ 3H2(g)的化学平衡常数为
N2(g)+ 3H2(g)的化学平衡常数为___________ 。当测得NH3、N2和H2物质的量分别为3mol、2mol和2mol时,则该反应的v(N2)正___________ v(N2)逆(填“>” “<”或“=”)。
Ⅱ.肼(N2H4)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
(4)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-544kJ/mol,键能数据如下表:
则氮氮三键的键能为___________ kJ/mol。
(5)已知:N2(g)+2O2(g)=2NO2(g) △H= + 68kJ/mol,则肼和二氧化氮反应生成氮气和水蒸气的热化学方程式为___________ 。
(1)若在容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2+3H2
 2NH3 △H<0,若5min反应达到平衡,此时测得NH3的物质的量为0.2mol。则0-5min内,用H2表示的化学反应速率为
2NH3 △H<0,若5min反应达到平衡,此时测得NH3的物质的量为0.2mol。则0-5min内,用H2表示的化学反应速率为(2)平衡后,若提高H2的转化率,可以采取的措施有___________。
| A.加催化剂 | B.增大容器体积 |
| C.降低反应体系的温度 | D.加入一定量N2 |
 2NH3(g) △H<0,其化学平衡常数K与温度t的关系如表所示:
2NH3(g) △H<0,其化学平衡常数K与温度t的关系如表所示:| t℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②400℃时,反应2NH3(g)
 N2(g)+ 3H2(g)的化学平衡常数为
N2(g)+ 3H2(g)的化学平衡常数为Ⅱ.肼(N2H4)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
(4)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-544kJ/mol,键能数据如下表:
| 化学键 | N-N | N-H | O=O | O-H |
| 键能/(kJ/mol) | 193 | 391 | 497 | 463 |
(5)已知:N2(g)+2O2(g)=2NO2(g) △H= + 68kJ/mol,则肼和二氧化氮反应生成氮气和水蒸气的热化学方程式为
您最近一年使用:0次
2023-11-14更新
|
139次组卷
|
2卷引用:陕西省西安中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
6 . 低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。结合下列有关图示和所学知识回答:

(1)用 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: 。若该反应体系的能量随反应过程变化关系如上图所示,则该反应属于
。若该反应体系的能量随反应过程变化关系如上图所示,则该反应属于_______ 反应(填“吸热”或“放热”),该反应的
______ (用含a、b的式子表示)。又知:相关化学键的键能如下表所示,实验测得上述反应的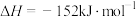 ,则表中的
,则表中的
______ 。
注:乙烯结构如图:
(2)在 完全燃烧生成
完全燃烧生成 和液态水的反应中,每有5mol电子转移时,放出650kJ的热量,其燃烧热的热化学方程式为
和液态水的反应中,每有5mol电子转移时,放出650kJ的热量,其燃烧热的热化学方程式为_________________________________ 。
(3)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:

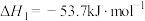 ,
,

 ,
,
则

______  。为提高该反应中
。为提高该反应中 的转化率,可采用的方式有
的转化率,可采用的方式有_______ 。
A加入合适的催化剂 B.升高温度 C.增大 浓度 D.减小压强
浓度 D.减小压强

(1)用
 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: 。若该反应体系的能量随反应过程变化关系如上图所示,则该反应属于
。若该反应体系的能量随反应过程变化关系如上图所示,则该反应属于
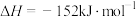 ,则表中的
,则表中的
化学键 |
| H-H |
| C-H | H-O |
健能 | 803 | 436 | x | 414 | 464 |

(2)在
 完全燃烧生成
完全燃烧生成 和液态水的反应中,每有5mol电子转移时,放出650kJ的热量,其燃烧热的热化学方程式为
和液态水的反应中,每有5mol电子转移时,放出650kJ的热量,其燃烧热的热化学方程式为(3)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
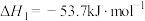 ,
,
 ,
,则


 。为提高该反应中
。为提高该反应中 的转化率,可采用的方式有
的转化率,可采用的方式有A加入合适的催化剂 B.升高温度 C.增大
 浓度 D.减小压强
浓度 D.减小压强
您最近一年使用:0次
7 . 下列不能用勒夏特列原理解释的是
| A.摇晃后的可乐开启后有大量气泡 |
| B.火电厂燃烧煤粉以提高燃煤效率 |
C.新制氯水中存在平衡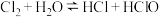 ,当加入 ,当加入 溶液后溶液颜色变浅 溶液后溶液颜色变浅 |
| D.生产硫酸的过程中用过量的空气和二氧化硫反应 |
您最近一年使用:0次
8 . 氯化亚铜( )广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产
)广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产 的工艺如下:
的工艺如下: 难溶于醇和水,溶于
难溶于醇和水,溶于 较大的体系
较大的体系 ,潮湿空气中易水解氧化。
,潮湿空气中易水解氧化。
(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是___________ 。
(2)步骤2是溶解过程,溶解时反应的离子方程式___________ 。
(3)步骤3为主反应, 的沉淀率与加入的
的沉淀率与加入的 的量关系如图所示。
的量关系如图所示。___________ ;
②比较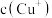 相对大小:A点
相对大小:A点___________ C点(填“>”、“<”或“=”);
③提高C点状态混合物中 沉淀率的措施是
沉淀率的措施是___________ ;
(4)步骤4进行的实验操作是___________ ;
(5)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是___________ 。用乙醇洗涤的目的是___________ 。
(6)产品纯度测定:称取 产品a g于锥形瓶中,加入足量的酸性
产品a g于锥形瓶中,加入足量的酸性 溶液使其充分溶解,然后用
溶液使其充分溶解,然后用
 标准溶液滴定
标准溶液滴定 ,消耗
,消耗 溶液b mL。(本实验中
溶液b mL。(本实验中 的被还原为
的被还原为 ,不与产品中杂质和
,不与产品中杂质和 反应)。
反应)。
① 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是___________ 。
②产品中 (摩尔质量为99g/mol)的质量分数为
(摩尔质量为99g/mol)的质量分数为___________ 。
 )广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产
)广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产 的工艺如下:
的工艺如下:
 难溶于醇和水,溶于
难溶于醇和水,溶于 较大的体系
较大的体系 ,潮湿空气中易水解氧化。
,潮湿空气中易水解氧化。(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是
(2)步骤2是溶解过程,溶解时反应的离子方程式
(3)步骤3为主反应,
 的沉淀率与加入的
的沉淀率与加入的 的量关系如图所示。
的量关系如图所示。
②比较
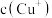 相对大小:A点
相对大小:A点③提高C点状态混合物中
 沉淀率的措施是
沉淀率的措施是(4)步骤4进行的实验操作是
(5)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是
(6)产品纯度测定:称取
 产品a g于锥形瓶中,加入足量的酸性
产品a g于锥形瓶中,加入足量的酸性 溶液使其充分溶解,然后用
溶液使其充分溶解,然后用
 标准溶液滴定
标准溶液滴定 ,消耗
,消耗 溶液b mL。(本实验中
溶液b mL。(本实验中 的被还原为
的被还原为 ,不与产品中杂质和
,不与产品中杂质和 反应)。
反应)。①
 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是②产品中
 (摩尔质量为99g/mol)的质量分数为
(摩尔质量为99g/mol)的质量分数为
您最近一年使用:0次
2023-05-31更新
|
709次组卷
|
7卷引用:陕西省西安工业大学附属中学2023-2024学年高三下学期第七次适应性考试理综试题-高中化学
9 . 下列不能用勒夏特列原理解释的是
A.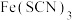 溶液中加入固体KSCN后颜色变深 溶液中加入固体KSCN后颜色变深 |
| B.用热的纯碱溶液洗油污时,去污效果好 |
C.用饱和食盐水除去 中的HCl,可以减少 中的HCl,可以减少 的损失 的损失 |
D.在密闭容器中进行反应 ,增大压强,混合气体颜色加深 ,增大压强,混合气体颜色加深 |
您最近一年使用:0次
2023-02-12更新
|
73次组卷
|
2卷引用:陕西省榆林市2022-2023学年高二上学期教学质量过程性评价化学试题
名校
10 . 下列事实不能用勒夏特列原理解释的是
| A.工业合成氨中,将氨气液化分离以提高氨气产率 |
| B.实验室可用排饱和食盐水的方法收集氯气 |
| C.由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深 |
| D.工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
您最近一年使用:0次






