名校
1 . 一定温度下,在2个容积均为1L的恒容密闭容器中,加入一定量的反应物,发生反应: △H<0,相关数据见下表。
△H<0,相关数据见下表。
下列说法不正确 的是
 △H<0,相关数据见下表。
△H<0,相关数据见下表。容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
|
|
| ||
Ⅰ |
| 0.2 | 0.2 | 0.1 |
Ⅱ |
| 0.2 | 0.2 | 0.12 |
| A.T1>T2 |
| B.达到平衡所需要的时间:Ⅰ<Ⅱ |
| C.Ⅱ中反应达到平衡时,NO的转化率为60% |
| D.对于Ⅰ,平衡后向容器中再充入0.2mol CO和0.2mol CO2,平衡正向移动 |
您最近一年使用:0次
名校
解题方法
2 . 下列实验操作及现象对应的解释正确的是
| 选项 | 实验操作 | 现象 | 解释 |
| A | 向碘水中加入1mLCCl4,振荡,溶液分层,下层CCl4层显紫色,再向试管中加入1mL浓KI溶液,振荡 | CCl4层紫色变浅 | 在水溶液中发生:I2+I-⇌ |
| B | 向酸性KMnO4溶液中通入乙烯气体 | 溶液紫色褪去 | 乙烯发生加成反应 |
| C | 向5mL0.1mol•L-1的CuSO4溶液逐滴加入1mol•L-1的氨水,至出现的蓝色沉淀消失,再加入8mL95%的乙醇溶液,用玻璃棒摩擦试管壁 | 加入乙醇后析出深蓝色晶体 | 乙醇是极性较大的溶剂,导致硫酸四氨合铜晶体析出 |
| D | 点燃某无色气体,将产物通入装有无水CuSO4的U型管中 | 固体变蓝 | 该气体为H2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 二水合重铬酸钠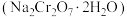 是重要的工业氧化剂,工业上可由铬铁矿(主要成分为
是重要的工业氧化剂,工业上可由铬铁矿(主要成分为 ,含铝、硅的氧化物等杂质)制备。工艺流程如图所示。下列说法错误的是
,含铝、硅的氧化物等杂质)制备。工艺流程如图所示。下列说法错误的是
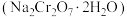 是重要的工业氧化剂,工业上可由铬铁矿(主要成分为
是重要的工业氧化剂,工业上可由铬铁矿(主要成分为 ,含铝、硅的氧化物等杂质)制备。工艺流程如图所示。下列说法错误的是
,含铝、硅的氧化物等杂质)制备。工艺流程如图所示。下列说法错误的是
| A.“焙烧”时,纯碱的作用是将铝、硅、铬元素转化为可溶性钠盐 |
B.滤渣1的主要成分是 、 、 |
C.“调 ”的目的是除去含铝、硅元素的杂质 ”的目的是除去含铝、硅元素的杂质 |
D.“转化”的目的是将 转化为 转化为 |
您最近一年使用:0次
4 . 下列事实不能 用平衡移动原理解释的是
A.FeS可用于除去废水中的 |
| B.25℃~100℃,随温度升高,纯水的pH减小 |
C.加热 溶液,液体由黄色变为红褐色 溶液,液体由黄色变为红褐色 |
D.  ,采用高温提高单位时间内 ,采用高温提高单位时间内 的产率 的产率 |
您最近一年使用:0次
解题方法
5 . 在一定条件下的密闭容器中发生反应: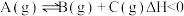 下列措施中,不能提高A的平衡转化率的是
下列措施中,不能提高A的平衡转化率的是
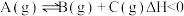 下列措施中,不能提高A的平衡转化率的是
下列措施中,不能提高A的平衡转化率的是| A.恒容条件下通入稀有气体 | B.及时分离出C |
| C.降低反应温度 | D.增大容器的体积 |
您最近一年使用:0次
6 . 丙烯腈(C3H3N)是制备腈纶的单体。一种制备丙烯腈反应的热化学方程式为C3H6(g)+NH3(g)+ O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是
 O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是| A.该反应只有在低温下才能自发进行 |
B.该反应的平衡常数K= |
| C.该反应每消耗1molC3H6,转移电子的物质的量为6mol |
| D.其他条件相同,减压和升温均有利于提高丙烯腊的平衡产率 |
您最近一年使用:0次
7 . 向密闭容器中充入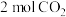 和
和 ,发生反应
,发生反应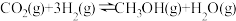
 ,测得反应在不同压强、不同温度下,平衡混合物中
,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图I所示,测得反应时逆反应速率与容器中
体积分数如图I所示,测得反应时逆反应速率与容器中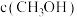 关系如图Ⅱ所示。下列说法错误的是
关系如图Ⅱ所示。下列说法错误的是
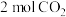 和
和 ,发生反应
,发生反应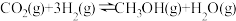
 ,测得反应在不同压强、不同温度下,平衡混合物中
,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图I所示,测得反应时逆反应速率与容器中
体积分数如图I所示,测得反应时逆反应速率与容器中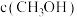 关系如图Ⅱ所示。下列说法错误的是
关系如图Ⅱ所示。下列说法错误的是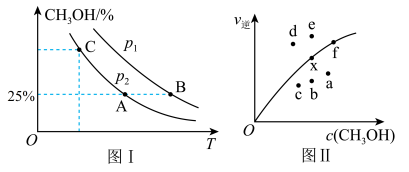
A.压强: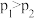 ,平衡常数: ,平衡常数: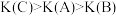 |
B.图1中 条件下,A和C两点反应速率: 条件下,A和C两点反应速率: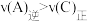 |
C.恒温恒压时,若反应从开始到A点达平衡,则 的平衡转化率约为 的平衡转化率约为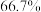 |
| D.图Ⅱ中当x点平衡体系降温至某一温度时,反应可重新达平衡状态,新平衡点可能是c |
您最近一年使用:0次
2024-04-29更新
|
120次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
名校
解题方法
8 . 下列不能用勒夏特列原理解释的事实是
| A.红棕色的NO2加压后颜色先变深后变浅 |
| B.黄绿色的氯水光照后颜色变浅 |
| C.盐碱地(含较多NaCl、Na2CO3)通过施加适量的石膏(CaSO4•H2O),可以降低土壤碱性 |
| D.500 ℃左右比室温更有利于合成氨反应 |
您最近一年使用:0次
9 . 一种芳香族化合物 结构如图。
结构如图。 萃取稀土离子
萃取稀土离子 的原理为
的原理为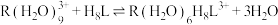 。分配比
。分配比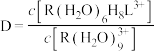 ,水相初始浓度
,水相初始浓度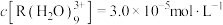 ,萃取平衡时
,萃取平衡时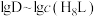 关系如图。下列说法正确的是
关系如图。下列说法正确的是

 结构如图。
结构如图。 萃取稀土离子
萃取稀土离子 的原理为
的原理为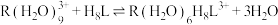 。分配比
。分配比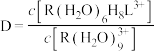 ,水相初始浓度
,水相初始浓度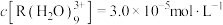 ,萃取平衡时
,萃取平衡时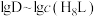 关系如图。下列说法正确的是
关系如图。下列说法正确的是
A.该条件下, 对图中三种阳离子的萃取平衡常数数量级相同 对图中三种阳离子的萃取平衡常数数量级相同 |
B.达平衡时水相中 |
C. 对 对 的萃取效果最好 的萃取效果最好 |
D.萃取平衡时,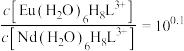 |
您最近一年使用:0次
解题方法
10 . 工业上常利用乙苯催化脱氢制备苯乙烯,发生的主反应是:
Ⅰ.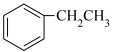 (g)
(g)
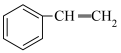 (g)+H2(g) ∆H=+117.6kJ/mol
(g)+H2(g) ∆H=+117.6kJ/mol
同时有副反应发生:
Ⅱ. (g)+H2(g)
(g)+H2(g)
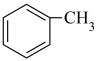 (g)+CH4(g) ∆H=-64.5kJ/mol
(g)+CH4(g) ∆H=-64.5kJ/mol
Ⅲ. (g)
(g) 8C(s)+5H2(g) ∆H=-1.67kJ/mol
8C(s)+5H2(g) ∆H=-1.67kJ/mol
某实验将乙苯和水蒸气混合,以恒定流速通入反应器,经过相同时间,测得乙苯的转化率,苯乙烯的选择性随温度、水蒸气与乙苯质量比的变化关系分别如图1、图2。

资料:苯乙烯的选择性是指生成苯乙烯的物质的量与消耗的乙苯的物质的量的比值。
下列说法不正确 的是
Ⅰ.
 (g)
(g)
 (g)+H2(g) ∆H=+117.6kJ/mol
(g)+H2(g) ∆H=+117.6kJ/mol同时有副反应发生:
Ⅱ.
 (g)+H2(g)
(g)+H2(g)
 (g)+CH4(g) ∆H=-64.5kJ/mol
(g)+CH4(g) ∆H=-64.5kJ/molⅢ.
 (g)
(g) 8C(s)+5H2(g) ∆H=-1.67kJ/mol
8C(s)+5H2(g) ∆H=-1.67kJ/mol某实验将乙苯和水蒸气混合,以恒定流速通入反应器,经过相同时间,测得乙苯的转化率,苯乙烯的选择性随温度、水蒸气与乙苯质量比的变化关系分别如图1、图2。

资料:苯乙烯的选择性是指生成苯乙烯的物质的量与消耗的乙苯的物质的量的比值。
下列说法
| A.从平衡角度分析,高温和低压有利于苯乙烯的制备 |
| B.随温度升高,副反应速率增大的程度比主反应的小 |
| C.乙苯中加入水蒸气,有利于催化剂表面积碳的消除 |
| D.本实验选择水蒸气与乙苯质量比为2:1、反应温度为620℃,是综合考虑乙苯转化率、苯乙烯选择性及能耗等工业实际 |
您最近一年使用:0次








