名校
解题方法
1 . 探究溶液中Ag+与单质S的反应。
资料:Ag2S不溶于6mol/L盐酸,Ag2SO3和Ag2SO4在6mol/L盐酸中均发生沉淀的转化
实验Ⅰ.在注射器中将10mL0.04mol/LAgNO3溶液(pH≈6)与0.01g S粉混合,水浴加热,充分反应后,过滤,得到无色溶液a(pH≈1),沉淀除S、洗涤后得到黑色固体b。
(1)研究黑色固体b的组成
①根据S具有__________ 性,推测b中可能含有Ag2S、Ag、Ag2SO3或Ag2SO4。
②检验黑色固体b的成分______ 。
ⅱ.用滤液c继续实验证明了黑色固体b中不含Ag2SO3,可选择的试剂是______ (填序号)。
a.酸性KMnO4溶液 b.H2O2和BaCl2的混合溶液 c.溴水
ⅲ.进一步实验证实了黑色固体b中不含Ag。根据沉淀e含有Ag、气体含有H2S,写出同时生成Ag和H2S的离子方程式:_________________ 。
(2)研究无色溶液a的组成
结合上述实验结果,分析溶液a中可能存在 或H2SO3,依据是
或H2SO3,依据是_______________ 。___________________ 。
②加入足量稀盐酸的作用是_________________ 。
(3)在注射器中进行实验Ⅳ,探究Ag2SO4溶液与S的反应,所得产物与实验Ⅰ相同。向注射器中加入的物质是__________________ 。
(4)用酸化的NaNO3溶液(pH≈6)与S进行实验Ⅴ,发现二者不反应。综合以上实验,写出溶液中Ag+与S反应的离子方程式并简要说明Ag+的作用:_______________ 。
资料:Ag2S不溶于6mol/L盐酸,Ag2SO3和Ag2SO4在6mol/L盐酸中均发生沉淀的转化
实验Ⅰ.在注射器中将10mL0.04mol/LAgNO3溶液(pH≈6)与0.01g S粉混合,水浴加热,充分反应后,过滤,得到无色溶液a(pH≈1),沉淀除S、洗涤后得到黑色固体b。
(1)研究黑色固体b的组成
①根据S具有
②检验黑色固体b的成分
实验Ⅱ.
ⅱ.用滤液c继续实验证明了黑色固体b中不含Ag2SO3,可选择的试剂是
a.酸性KMnO4溶液 b.H2O2和BaCl2的混合溶液 c.溴水
ⅲ.进一步实验证实了黑色固体b中不含Ag。根据沉淀e含有Ag、气体含有H2S,写出同时生成Ag和H2S的离子方程式:
(2)研究无色溶液a的组成
结合上述实验结果,分析溶液a中可能存在
 或H2SO3,依据是
或H2SO3,依据是实验Ⅲ.
②加入足量稀盐酸的作用是
(3)在注射器中进行实验Ⅳ,探究Ag2SO4溶液与S的反应,所得产物与实验Ⅰ相同。向注射器中加入的物质是
(4)用酸化的NaNO3溶液(pH≈6)与S进行实验Ⅴ,发现二者不反应。综合以上实验,写出溶液中Ag+与S反应的离子方程式并简要说明Ag+的作用:
您最近一年使用:0次
名校
2 . 化学小组探究 与
与 是否存在反应,实验过程如下图所示。
是否存在反应,实验过程如下图所示。
 与
与 是否存在反应,实验过程如下图所示。
是否存在反应,实验过程如下图所示。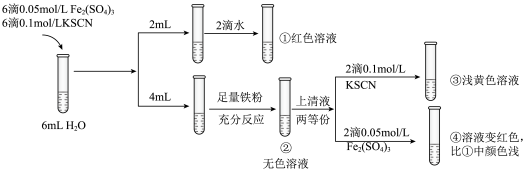
A.②中溶液无色是因为 ,导致平衡 ,导致平衡 逆向移动 逆向移动 |
B.③中溶液略显黄色,可能是因为②→③过程中 被空气氧化 被空气氧化 |
C.④中溶液颜色比①浅,说明 与 与 反应导致 反应导致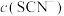 减小 减小 |
D.将向①中加入的2滴水改为2滴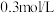  溶液,两次实验后的溶液颜色相同 溶液,两次实验后的溶液颜色相同 |
您最近一年使用:0次
名校
3 . 下列事实不能用平衡移动原理解释的是
A.镁条在水中产生少量气泡后反应停止,在1mol/L 溶液中持续产生气泡 溶液中持续产生气泡 |
| B.二氧化锰与稀盐酸共热不产生氯气,与浓盐酸共热产生氯气 |
| C.在硫酸铜溶液中加入氯化钠固体,充分溶解后溶液变为蓝绿色 |
| D.在氯水中加入少量碳酸钙,可以增强氯水的氧化性 |
您最近一年使用:0次
名校
4 . 某小组对 的性质进行探究,实验操作及现象如下,下列说法不正确的是
的性质进行探究,实验操作及现象如下,下列说法不正确的是
资料:
 的性质进行探究,实验操作及现象如下,下列说法不正确的是
的性质进行探究,实验操作及现象如下,下列说法不正确的是资料:
| 物质 |  |  |  |
| 溶液中的颜色 | 粉红色 | 蓝色 | 无色 |
| 操作 |
| 将a中得到的蓝色溶液均分为3份,分别倒入试管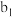 、 、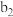 、 、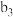 中 中 | ||
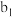 |
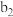 |
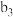 | ||
| 现象 | a中现象:加入浓盐酸后,溶液由粉红色变为蓝色 | 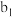 中现象:溶液变为粉红色 中现象:溶液变为粉红色 | 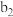 中现象 中现象 | 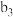 中现象 中现象 |
A.试管a中存在平衡: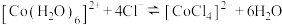 |
B.由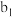 中现象可推测稳定性: 中现象可推测稳定性: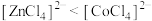 |
C.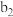 中现象可能为产生白色沉淀 中现象可能为产生白色沉淀 |
D.推测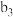 中现象为溶液变为粉红色,因为加入水使各组分离子浓度变化,平衡移动 中现象为溶液变为粉红色,因为加入水使各组分离子浓度变化,平衡移动 |
您最近一年使用:0次
2024-05-31更新
|
174次组卷
|
2卷引用:北京市昌平区2023-2024学年高三下学期二模化学试题
5 . 以 溶液、浓盐酸为腐蚀液,能将覆铜板上不需要的铜腐蚀。某小组对此反应过程进行探究。
溶液、浓盐酸为腐蚀液,能将覆铜板上不需要的铜腐蚀。某小组对此反应过程进行探究。
资料:i.水溶液中: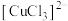 呈无色;
呈无色;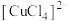 呈黄色;
呈黄色; 呈棕色。
呈棕色。
ii. ;CuCl为白色固体,难溶于水。
;CuCl为白色固体,难溶于水。
将等体积的溶液a分别加到等量铜粉中,实验记录如下:
(1)Ⅰ中产生白色沉淀的离子方程式是____________ 。
(2)对于实验Ⅱ的现象进行分析。
①经检验Ⅱ中气体为 。分析气体产生的原因,进行实验:将
。分析气体产生的原因,进行实验:将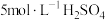 溶液加到铜粉中,溶液慢慢变蓝,未检测到
溶液加到铜粉中,溶液慢慢变蓝,未检测到 。
。
依据电极反应式,分析产生 的原因
的原因____________ 。
②Ⅱ中溶液变为黄色,用离子方程式解释可能原因____________ 。
(3)对比实验Ⅰ、Ⅲ,分析实验Ⅲ中将溶液a加到铜粉中未产生白色沉淀的原因。
①假设1: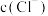 增大,白色沉淀不能稳定存在。
增大,白色沉淀不能稳定存在。
实验验证:取Ⅰ中洗涤后的沉淀,加入饱和NaCl溶液,白色沉淀溶解。结合平衡移动原理解释沉淀溶解的原因____________ 。
②假设2: 增大,白色沉淀不能稳定存在。
增大,白色沉淀不能稳定存在。
实验验证:______ (填操作和现象),证实假设2不合理。
(4)实验Ⅱ、Ⅲ对比,实验Ⅱ中产生气泡,实验Ⅲ中无气泡。分析可能原因______ 。
(5)结合现象和化学反应原理解释选择 与浓盐酸的混合液而不单独选择
与浓盐酸的混合液而不单独选择 溶液或浓盐酸做腐蚀液的原因
溶液或浓盐酸做腐蚀液的原因____________ 。
 溶液、浓盐酸为腐蚀液,能将覆铜板上不需要的铜腐蚀。某小组对此反应过程进行探究。
溶液、浓盐酸为腐蚀液,能将覆铜板上不需要的铜腐蚀。某小组对此反应过程进行探究。资料:i.水溶液中:
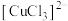 呈无色;
呈无色;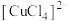 呈黄色;
呈黄色; 呈棕色。
呈棕色。ii.
 ;CuCl为白色固体,难溶于水。
;CuCl为白色固体,难溶于水。将等体积的溶液a分别加到等量铜粉中,实验记录如下:
实验 | 溶液a | 现象 |
Ⅰ |  溶液( 溶液( ) ) | 产生白色沉淀,溶液蓝色变浅,5h时铜粉剩余 |
Ⅱ | 浓盐酸( ) ) | 产生无色气泡,溶液无色;继而溶液变为黄色;较长时间后溶液变为棕色,5h时铜粉剩余 |
Ⅲ |  溶液( 溶液( )和浓盐酸( )和浓盐酸( ) ) | 溶液由黄绿色变为棕色,无气泡;随着反应进行,溶液颜色变浅,后接近于无色,5h时铜粉几乎无剩余 |
(1)Ⅰ中产生白色沉淀的离子方程式是
(2)对于实验Ⅱ的现象进行分析。
①经检验Ⅱ中气体为
 。分析气体产生的原因,进行实验:将
。分析气体产生的原因,进行实验:将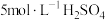 溶液加到铜粉中,溶液慢慢变蓝,未检测到
溶液加到铜粉中,溶液慢慢变蓝,未检测到 。
。依据电极反应式,分析产生
 的原因
的原因②Ⅱ中溶液变为黄色,用离子方程式解释可能原因
(3)对比实验Ⅰ、Ⅲ,分析实验Ⅲ中将溶液a加到铜粉中未产生白色沉淀的原因。
①假设1:
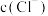 增大,白色沉淀不能稳定存在。
增大,白色沉淀不能稳定存在。实验验证:取Ⅰ中洗涤后的沉淀,加入饱和NaCl溶液,白色沉淀溶解。结合平衡移动原理解释沉淀溶解的原因
②假设2:
 增大,白色沉淀不能稳定存在。
增大,白色沉淀不能稳定存在。实验验证:
(4)实验Ⅱ、Ⅲ对比,实验Ⅱ中产生气泡,实验Ⅲ中无气泡。分析可能原因
(5)结合现象和化学反应原理解释选择
 与浓盐酸的混合液而不单独选择
与浓盐酸的混合液而不单独选择 溶液或浓盐酸做腐蚀液的原因
溶液或浓盐酸做腐蚀液的原因
您最近一年使用:0次
解题方法
6 . 废电池中含磷酸铁锂,提锂后的废渣主要含 、
、 和金属铝等,以废渣为原料制备电池级
和金属铝等,以废渣为原料制备电池级 的一种工艺流程如下。
的一种工艺流程如下。 、
、 均难溶于水。
均难溶于水。
ii.将 转化为
转化为 有利于更彻底除去
有利于更彻底除去 。
。
(1)酸浸前,将废渣粉碎的目的是________ 。
(2)从平衡移动的角度解释加入硝酸溶解 的原因:
的原因:________ 。
(3)在酸浸液中加入 进行电解,电解原理的示意图如下图所示,电解过程中
进行电解,电解原理的示意图如下图所示,电解过程中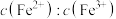 不断增大。结合电极反应说明
不断增大。结合电极反应说明 在电解中的作用:
在电解中的作用:________ 。 。向“氧化”后的溶液中加入HCHO,加热,产生NO和
。向“氧化”后的溶液中加入HCHO,加热,产生NO和 ,当液面上方不再产生红棕色气体时,静置一段时间,产生
,当液面上方不再产生红棕色气体时,静置一段时间,产生 沉淀。阐述此过程中HCHO的作用:
沉淀。阐述此过程中HCHO的作用:________ 。
(5)过滤得到电池级 后,滤液中主要的金属阳离子有
后,滤液中主要的金属阳离子有________ 。
(6)磷酸铁锂-石墨电池的总反应: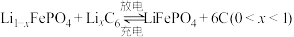 。
。
①高温条件下, 、葡萄糖(
、葡萄糖( )和
)和 可制备电极材料
可制备电极材料 ,同时生成CO和
,同时生成CO和 ,反应的化学方程式是
,反应的化学方程式是________ 。
②放电时负极的电极反应式是________ 。
 、
、 和金属铝等,以废渣为原料制备电池级
和金属铝等,以废渣为原料制备电池级 的一种工艺流程如下。
的一种工艺流程如下。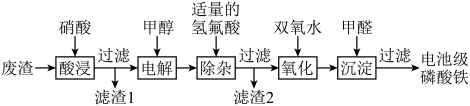
 、
、 均难溶于水。
均难溶于水。ii.将
 转化为
转化为 有利于更彻底除去
有利于更彻底除去 。
。(1)酸浸前,将废渣粉碎的目的是
(2)从平衡移动的角度解释加入硝酸溶解
 的原因:
的原因:(3)在酸浸液中加入
 进行电解,电解原理的示意图如下图所示,电解过程中
进行电解,电解原理的示意图如下图所示,电解过程中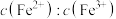 不断增大。结合电极反应说明
不断增大。结合电极反应说明 在电解中的作用:
在电解中的作用: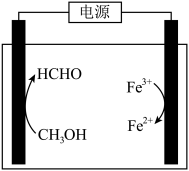
 。向“氧化”后的溶液中加入HCHO,加热,产生NO和
。向“氧化”后的溶液中加入HCHO,加热,产生NO和 ,当液面上方不再产生红棕色气体时,静置一段时间,产生
,当液面上方不再产生红棕色气体时,静置一段时间,产生 沉淀。阐述此过程中HCHO的作用:
沉淀。阐述此过程中HCHO的作用:(5)过滤得到电池级
 后,滤液中主要的金属阳离子有
后,滤液中主要的金属阳离子有(6)磷酸铁锂-石墨电池的总反应:
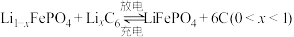 。
。①高温条件下,
 、葡萄糖(
、葡萄糖( )和
)和 可制备电极材料
可制备电极材料 ,同时生成CO和
,同时生成CO和 ,反应的化学方程式是
,反应的化学方程式是②放电时负极的电极反应式是
您最近一年使用:0次
7 . 向锌氨溶液(由 液、氨水-硫酸铵混合溶液配制而成)中加入萃取剂
液、氨水-硫酸铵混合溶液配制而成)中加入萃取剂 。不同
。不同 下(其它条件不变)达到平衡后
下(其它条件不变)达到平衡后 和
和 的萃取效果如图所示。
的萃取效果如图所示。
反应ⅱ:
反应ⅲ:
②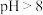 的锌氨溶液中,
的锌氨溶液中,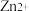 主要以
主要以 形式存在
形式存在
下列说法不正确 的是
 液、氨水-硫酸铵混合溶液配制而成)中加入萃取剂
液、氨水-硫酸铵混合溶液配制而成)中加入萃取剂 。不同
。不同 下(其它条件不变)达到平衡后
下(其它条件不变)达到平衡后 和
和 的萃取效果如图所示。
的萃取效果如图所示。

反应ⅱ:

反应ⅲ:

②
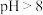 的锌氨溶液中,
的锌氨溶液中,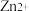 主要以
主要以 形式存在
形式存在下列说法
A.锌氨溶液中存在 的电离平衡和 的电离平衡和 的水解平衡 的水解平衡 |
B. 时,加入萃取剂 时,加入萃取剂 达到平衡后, 达到平衡后,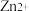 主要以 主要以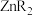 的形式存在 的形式存在 |
C. 由8到10,萃取剂中氨的含量增大的原因是反应ⅲ的平衡向正反应方向移动 由8到10,萃取剂中氨的含量增大的原因是反应ⅲ的平衡向正反应方向移动 |
D. 由8到6, 由8到6, 和 和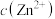 均增大,前者对反应ⅱ的影响小于后者 均增大,前者对反应ⅱ的影响小于后者 |
您最近一年使用:0次
8 . 乙烯合成的发展体现了化学科学与技术的不断进步。
(1)用烃类热裂解法制乙烯是乙烯工业化生产的开端。
①乙烷高温裂解制备乙烯(反应Ⅰ)的化学方程式是______ 。
②在裂解过程中伴随反应Ⅱ: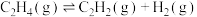 ,在高温下缩短
,在高温下缩短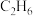 在反应器中的停留时间可提高乙烯的获取率,由此判断反应速率:反应Ⅰ
在反应器中的停留时间可提高乙烯的获取率,由此判断反应速率:反应Ⅰ______ 反应Ⅱ。(填“>”“<”或“=”)
(2)乙炔选择性加氢制乙烯是石油化工领域重要的发展阶段。
以钯(Pd)为催化剂可有效提高乙烯产率,在催化剂表面的反应机理如下图所示(吸附在催化剂表面的粒子用*标注)。______ 。
a.NP-Pd催化反应过程中步骤Ⅰ为放热反应
b.ISA-Pd催化反应过程中步骤Ⅱ为决速步骤
c.两种催化剂均能降低总反应的反应热
②吸附态乙烯( )脱离催化剂表面,可得到
)脱离催化剂表面,可得到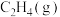 ,如未及时脱附,易在催化剂表面继续氢化经过渡态Ⅲ后而形成乙烷。制
,如未及时脱附,易在催化剂表面继续氢化经过渡态Ⅲ后而形成乙烷。制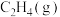 选择性较好的催化剂是
选择性较好的催化剂是______ 。
(3)以 为原料用不同的方法制乙烯有助于实现碳中和。
为原料用不同的方法制乙烯有助于实现碳中和。
I.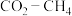 干气重整制乙烯。下图是2种投料比[
干气重整制乙烯。下图是2种投料比[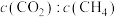 ,分别为1:1、2:1]下,反应温度对
,分别为1:1、2:1]下,反应温度对 平衡转化率影响的曲线。
平衡转化率影响的曲线。______ 。
②当曲线a、b对应的投料比达到相同的 平衡转化率时,对应的反应温度与投料比的关系是
平衡转化率时,对应的反应温度与投料比的关系是______ 。
Ⅱ.双金属串联催化剂电催化 制乙烯,装置示意图如图所示。
制乙烯,装置示意图如图所示。
已知:法拉第效率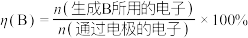
______ 。
④该环境下,测得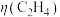 可达50%,若电路中通过1.2mol电子时,则产生乙烯的物质的量是
可达50%,若电路中通过1.2mol电子时,则产生乙烯的物质的量是______ mol。
(1)用烃类热裂解法制乙烯是乙烯工业化生产的开端。
①乙烷高温裂解制备乙烯(反应Ⅰ)的化学方程式是
②在裂解过程中伴随反应Ⅱ:
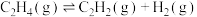 ,在高温下缩短
,在高温下缩短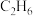 在反应器中的停留时间可提高乙烯的获取率,由此判断反应速率:反应Ⅰ
在反应器中的停留时间可提高乙烯的获取率,由此判断反应速率:反应Ⅰ(2)乙炔选择性加氢制乙烯是石油化工领域重要的发展阶段。
以钯(Pd)为催化剂可有效提高乙烯产率,在催化剂表面的反应机理如下图所示(吸附在催化剂表面的粒子用*标注)。
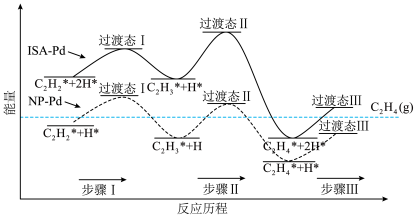
a.NP-Pd催化反应过程中步骤Ⅰ为放热反应
b.ISA-Pd催化反应过程中步骤Ⅱ为决速步骤
c.两种催化剂均能降低总反应的反应热
②吸附态乙烯(
 )脱离催化剂表面,可得到
)脱离催化剂表面,可得到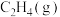 ,如未及时脱附,易在催化剂表面继续氢化经过渡态Ⅲ后而形成乙烷。制
,如未及时脱附,易在催化剂表面继续氢化经过渡态Ⅲ后而形成乙烷。制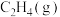 选择性较好的催化剂是
选择性较好的催化剂是(3)以
 为原料用不同的方法制乙烯有助于实现碳中和。
为原料用不同的方法制乙烯有助于实现碳中和。I.
 干气重整制乙烯。下图是2种投料比[
干气重整制乙烯。下图是2种投料比[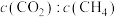 ,分别为1:1、2:1]下,反应温度对
,分别为1:1、2:1]下,反应温度对 平衡转化率影响的曲线。
平衡转化率影响的曲线。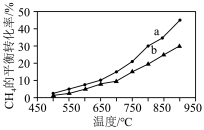
②当曲线a、b对应的投料比达到相同的
 平衡转化率时,对应的反应温度与投料比的关系是
平衡转化率时,对应的反应温度与投料比的关系是Ⅱ.双金属串联催化剂电催化
 制乙烯,装置示意图如图所示。
制乙烯,装置示意图如图所示。已知:法拉第效率
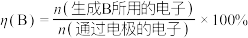
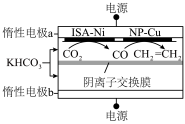
④该环境下,测得
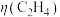 可达50%,若电路中通过1.2mol电子时,则产生乙烯的物质的量是
可达50%,若电路中通过1.2mol电子时,则产生乙烯的物质的量是
您最近一年使用:0次
9 . 下列事实能用平衡移动原理解释的是
| A.合成氨工业中使用铁触媒作催化剂 |
B.铁钉放入浓 中不再变化后,加热能产生大量红棕色气体 中不再变化后,加热能产生大量红棕色气体 |
C.氯碱工业中阳极区的溶液用盐酸调pH为2~3,促进 的产生 的产生 |
D.锌片与稀 反应过程中,加入少量 反应过程中,加入少量 固体,促进 固体,促进 的产生 的产生 |
您最近一年使用:0次
名校
10 . 下列实验方案能达实验目的的是
| A | B | |
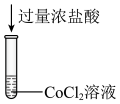
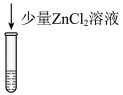
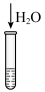
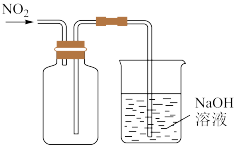
| 目的 | 收集并吸收NO2 | 比较Mg、Al金属性的强弱 |
| 实验方案 |
|
|
| C | D | |
| 目的 | 比较Na2CO3、NaHCO3与酸反应快慢 | 研究浓度对化学平衡的影响 |
| 实验方案 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次