1 . 下列实验操作可以达到实验目的的是
| 选项 | 实验目的 | 实验操作及现象 |
| A | 比较CH3COOH和H2CO3的酸性 | 用pH计分别测定0.1000mol/LCH3COONH4溶液和Na2CO3溶液的pH后者大于前者 |
| B | 检验铁锈中含有二价铁 | 将铁锈溶于浓盐酸,滴入KMnO4溶液,紫色褪去 |
| C | 探究氢离子浓度对 相互转化的影响 相互转化的影响 | 向K2CrO4溶液中缓慢滴加硫酸,观察到溶液由黄色变为橙红色 |
| D | 证明Cl2、Br2、I2的氧化性 | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液,溶液先变橙色,后变蓝色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022·河北石家庄·一模
解题方法
2 . 镁条投入盐酸时,快速溶解并产生大量气泡;投入热水时,其表面会附着微量气泡。受此启发,某兴趣小组对Mg与NaHCO3溶液的反应进行了如下探究:
I.探究反应产生的气体成分。
(1)经检验反应产生的气体有H2,实验室检验H2的方法为_______ 。
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
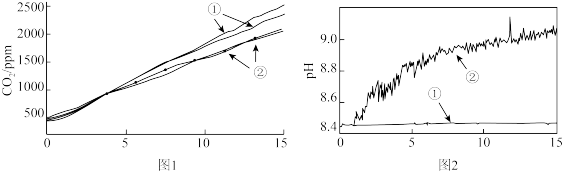
图1中曲线②对应的CO2含量逐渐增大的原因为_______ (用化学方程式表示);结合实验3解释,随着时间推移,图1中曲线②的数值低于曲线①的原因为_______ 。
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:
(3)结合实验1和4,可知溶液中的HCO 加快了反应的发生。
加快了反应的发生。
①实验4中横线处内容为_______ 。
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO 能加快该反应的原因为
能加快该反应的原因为_______ 。
III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
(4)甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为_______ (填字母编号)。

(5)乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=_______ 。
| 实验序号 | 实验操作 | 实验现象 |
| 1 | 向7.5 mL1mol·L-1NaHCO3溶液中加入长3cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
(1)经检验反应产生的气体有H2,实验室检验H2的方法为
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
| 实验序号 | 实验操作 |
| 2 | 分别称取两份6.0 mL 1 mol·L-1NaHCO3溶液于两个相同塑料瓶中(其中一个加入0.1g镁条),塞紧CO2气体传感器,采集数据,各重复实验1次,得到图1所示曲线 |
| 3 | 分别称取两份30.0 mL 1 mol·L-1NaHCO3溶液于两个相同烧杯中(其中一个加入1.1g镁条),插入pH传感器,搅拌并采集数据,得到图2所示曲线 |

图1中曲线②对应的CO2含量逐渐增大的原因为
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO
 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:| 实验序号 | 实验操作 | 实验现象 |
| 4 | 向_______溶液中加入长3 cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
 加快了反应的发生。
加快了反应的发生。①实验4中横线处内容为
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO
 能加快该反应的原因为
能加快该反应的原因为III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
(4)甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为

(5)乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=
您最近一年使用:0次
2022-04-09更新
|
1136次组卷
|
7卷引用:押江苏卷第17题 化学实验综合题 -备战2022年高考化学临考题号押题(江苏卷)
(已下线)押江苏卷第17题 化学实验综合题 -备战2022年高考化学临考题号押题(江苏卷)河北省石家庄市2022届高三毕业班教学质量检测二(一模)化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)秘籍21 性质探究实验-备战2022年高考化学抢分秘籍(全国通用)(已下线)化学-2022年高考押题预测卷01(福建卷)(已下线)化学-2022年高考押题预测卷03(山东卷)(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(实验探究题)
3 . 为探讨化学平衡移动原理与氧化还原反应规律的联系,小睿同学通过改变浓度研究:“ ”反应中Fe3+和Fe2+的相互转化。实验如下:
”反应中Fe3+和Fe2+的相互转化。实验如下:
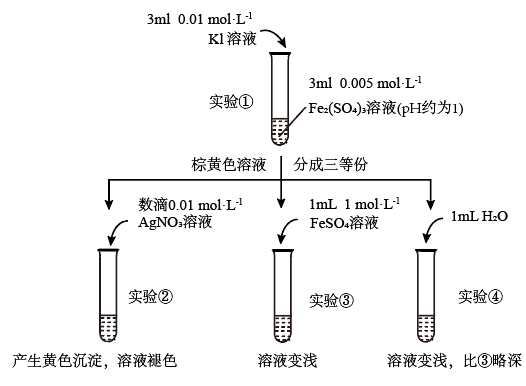
(1)待实验①溶液颜色不再改变时,再进行实验②③④,目的是使实验①的反应达到_______ 。
(2)实验④是实验③的_______ 试验,目的是_______ 。
(3)实验②的颜色变化表明平衡逆向移动,Fe2+向Fe3+转化。根据氧化还原反应的规律,该同学推测实验②中Fe2+向Fe3+转化的原因:外加Ag+使c(I-)降低,导致 的还原性弱于Fe2+,用如图装置(a、b均为石墨电极)进行实验验证。
的还原性弱于Fe2+,用如图装置(a、b均为石墨电极)进行实验验证。
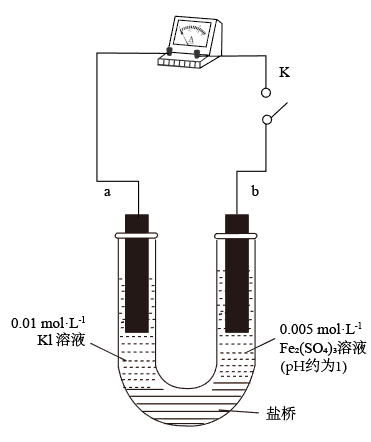
①K闭合时,指针向右偏转,b作_______ 极。
②当指针归零(反应达到平衡)后,向U形管左管滴加0.01 mol/LAgNO3溶液,产生的现象证实了其推测,该现象是_______ 。
(4)按照(3)的原理,该同学用上图装置再进行实验,证实了实验③中Fe2+向Fe3+转化的原因。
①转化原因是_______ 。
②与(3)实验对比,不同的操作是_______ 。
(5)实验①中,还原性:I->Fe2+,而实验②③中,还原性:Fe2+>I-,将(3)和(4)作对比,得出的结论是_______ 。
 ”反应中Fe3+和Fe2+的相互转化。实验如下:
”反应中Fe3+和Fe2+的相互转化。实验如下:
(1)待实验①溶液颜色不再改变时,再进行实验②③④,目的是使实验①的反应达到
(2)实验④是实验③的
(3)实验②的颜色变化表明平衡逆向移动,Fe2+向Fe3+转化。根据氧化还原反应的规律,该同学推测实验②中Fe2+向Fe3+转化的原因:外加Ag+使c(I-)降低,导致
 的还原性弱于Fe2+,用如图装置(a、b均为石墨电极)进行实验验证。
的还原性弱于Fe2+,用如图装置(a、b均为石墨电极)进行实验验证。
①K闭合时,指针向右偏转,b作
②当指针归零(反应达到平衡)后,向U形管左管滴加0.01 mol/LAgNO3溶液,产生的现象证实了其推测,该现象是
(4)按照(3)的原理,该同学用上图装置再进行实验,证实了实验③中Fe2+向Fe3+转化的原因。
①转化原因是
②与(3)实验对比,不同的操作是
(5)实验①中,还原性:I->Fe2+,而实验②③中,还原性:Fe2+>I-,将(3)和(4)作对比,得出的结论是
您最近一年使用:0次
2021-04-26更新
|
285次组卷
|
3卷引用:江苏省昆山市2020-2021学年高二下学期期中教学质量调研化学试题
江苏省昆山市2020-2021学年高二下学期期中教学质量调研化学试题(已下线)2.3.2 影响化学平衡状态的因素-2021-2022学年高二化学课后培优练(人教版选修4)江西省吉安市(吉安县三中、泰和二中、安福二中、井大附中 )2021-2022学年高二上学期9月联考化学试题
解题方法
4 . 铼(Re)广泛应用于喷气式发动机和火箭发动机,是重要的战略贵金属,可以通过还原剂在高温条件下还原其氧化物制取。
Ⅰ.实验室以富铼渣(主要成份 )为原料制备高纯高铼酸铵(
)为原料制备高纯高铼酸铵( ),其部分实验过程如下:
),其部分实验过程如下:
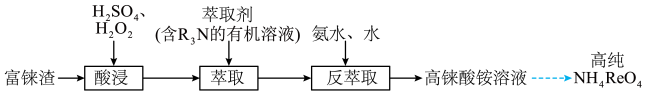
(萃取原理可表示为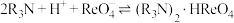 )
)
(1)酸浸时 转化为两种强酸,该反应的离子方程式为
转化为两种强酸,该反应的离子方程式为_______ 。
(2)通过萃取与反萃取可实现铼元素的富集。
①萃取剂应具有的性质_______ (填序号)。
A.密度大于水
B. 在萃取剂中的溶解度大于水中的
在萃取剂中的溶解度大于水中的
C.不溶于水
②在反萃取时,加入氨水、水的目的是_______ 。
Ⅱ.以ReS2为原料制备NH4ReO4的装置如图所示:
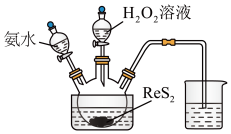
(3)反应开始前,先向三颈瓶中加入一定量的 和水,60℃下,通过分液漏斗依次滴入两种溶液。充分反应后可得
和水,60℃下,通过分液漏斗依次滴入两种溶液。充分反应后可得 和
和 的混合溶液。
的混合溶液。
①滴入两种溶液时候,向三颈瓶中先滴加的是_______ 。(填序号)
A.氨水 B. 溶液
溶液
②不考虑原料损失,实验中加入的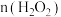 与
与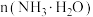 的最佳比为
的最佳比为_______ 。
(4)请设计以三颈瓶中反应后的溶液为原料,制备金属铼粉的实验方案_______ 。(实验须使用的试剂:Zn粒,稀硫酸,浓硫酸、 )
)
已知①:有关物质溶解度如下表
②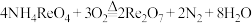
Ⅰ.实验室以富铼渣(主要成份
 )为原料制备高纯高铼酸铵(
)为原料制备高纯高铼酸铵( ),其部分实验过程如下:
),其部分实验过程如下:
(萃取原理可表示为
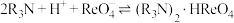 )
)(1)酸浸时
 转化为两种强酸,该反应的离子方程式为
转化为两种强酸,该反应的离子方程式为(2)通过萃取与反萃取可实现铼元素的富集。
①萃取剂应具有的性质
A.密度大于水
B.
 在萃取剂中的溶解度大于水中的
在萃取剂中的溶解度大于水中的C.不溶于水
②在反萃取时,加入氨水、水的目的是
Ⅱ.以ReS2为原料制备NH4ReO4的装置如图所示:

(3)反应开始前,先向三颈瓶中加入一定量的
 和水,60℃下,通过分液漏斗依次滴入两种溶液。充分反应后可得
和水,60℃下,通过分液漏斗依次滴入两种溶液。充分反应后可得 和
和 的混合溶液。
的混合溶液。①滴入两种溶液时候,向三颈瓶中先滴加的是
A.氨水 B.
 溶液
溶液②不考虑原料损失,实验中加入的
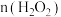 与
与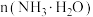 的最佳比为
的最佳比为(4)请设计以三颈瓶中反应后的溶液为原料,制备金属铼粉的实验方案
 )
)已知①:有关物质溶解度如下表
| 温度/℃ | 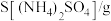 |  |
| 20 | 75.4 | 6.1 |
| 30 | 78.0 | 32.3 |
您最近一年使用:0次
5 . 脱除烟气中的氮氧化物(主要是指NO和 )可净化空气、改善环境,是环境保护的主要课题。
)可净化空气、改善环境,是环境保护的主要课题。
(1) 的消除。可以用碳酸钠溶液来进行吸收,在产生
的消除。可以用碳酸钠溶液来进行吸收,在产生 的同时,会生成
的同时,会生成 等物质,
等物质, 是工业盐的主要成分,在漂白、电镀等方面应用广泛。写出碳酸钠溶液消除
是工业盐的主要成分,在漂白、电镀等方面应用广泛。写出碳酸钠溶液消除 的化学方程式:
的化学方程式:_______ 。
(2)NO的消除。
① 可有效脱除NO,但
可有效脱除NO,但 不稳定,实际应用中常用其盐。
不稳定,实际应用中常用其盐。 和
和 制取漂白粉的化学方程式是
制取漂白粉的化学方程式是_______ 。
次氯酸盐溶液脱除NO的主要过程如下:
a.
b.
c.
②下列分析正确的是_______ 。
A.烟气中含有少量 能提高NO的脱除率
能提高NO的脱除率
B. 单独存在时不能被脱除
单独存在时不能被脱除
C.脱除过程中,次氯酸盐溶液的 下降
下降
③研究不同温度下 溶液对NO脱除率的影响,结果如图所示。脱除过程中往往有
溶液对NO脱除率的影响,结果如图所示。脱除过程中往往有 产生,原因是
产生,原因是_______ 。(用离子方程式表示);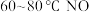 脱除率下降的原因是
脱除率下降的原因是_______ 。
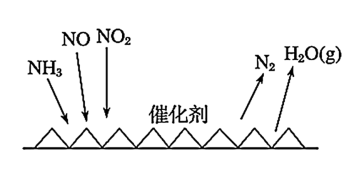
(3) 催化还原氮氧化物(
催化还原氮氧化物( )技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当
)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当 与NO的物质的量之比为
与NO的物质的量之比为 时,与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为
时,与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为_______ 。
(4)利用电化学装置可消除氮氧化物污染,变废为宝。如图为电解NO制备 的装置,该装置中阳极的电极反应式为
的装置,该装置中阳极的电极反应式为_______ 。

 )可净化空气、改善环境,是环境保护的主要课题。
)可净化空气、改善环境,是环境保护的主要课题。(1)
 的消除。可以用碳酸钠溶液来进行吸收,在产生
的消除。可以用碳酸钠溶液来进行吸收,在产生 的同时,会生成
的同时,会生成 等物质,
等物质, 是工业盐的主要成分,在漂白、电镀等方面应用广泛。写出碳酸钠溶液消除
是工业盐的主要成分,在漂白、电镀等方面应用广泛。写出碳酸钠溶液消除 的化学方程式:
的化学方程式:(2)NO的消除。
①
 可有效脱除NO,但
可有效脱除NO,但 不稳定,实际应用中常用其盐。
不稳定,实际应用中常用其盐。 和
和 制取漂白粉的化学方程式是
制取漂白粉的化学方程式是次氯酸盐溶液脱除NO的主要过程如下:
a.

b.

c.

②下列分析正确的是
A.烟气中含有少量
 能提高NO的脱除率
能提高NO的脱除率B.
 单独存在时不能被脱除
单独存在时不能被脱除C.脱除过程中,次氯酸盐溶液的
 下降
下降③研究不同温度下
 溶液对NO脱除率的影响,结果如图所示。脱除过程中往往有
溶液对NO脱除率的影响,结果如图所示。脱除过程中往往有 产生,原因是
产生,原因是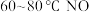 脱除率下降的原因是
脱除率下降的原因是
(3)
 催化还原氮氧化物(
催化还原氮氧化物( )技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当
)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示。当 与NO的物质的量之比为
与NO的物质的量之比为 时,与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为
时,与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为
(4)利用电化学装置可消除氮氧化物污染,变废为宝。如图为电解NO制备
 的装置,该装置中阳极的电极反应式为
的装置,该装置中阳极的电极反应式为
您最近一年使用:0次
名校
6 . 某硫酸厂产生的烧渣(主要含 、
、 及少量
及少量 )可用于制备
)可用于制备 和还原铁粉,其流程如图:
和还原铁粉,其流程如图:
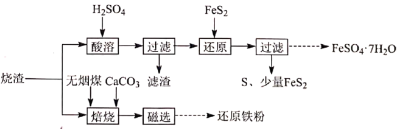
(1)“酸溶”前需粉碎烧渣,其目的是_________ 、________ 。
(2)“滤渣”的主要成分是_________ (填化学式)。
(3)“还原”时, 被氧化为
被氧化为 的离子方程式是
的离子方程式是_________ 。
(4)“焙烧”时,烧渣、无烟煤、 的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
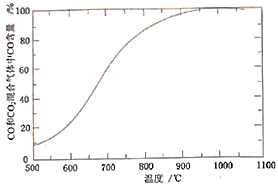
添加 的目的是:①脱除
的目的是:①脱除 等;②
等;②_________ 。
(5)“焙烧”在半封闭装置中进行,投料层表面盖有适当厚度的煤层,“焙烧”时间控制在4~4.5小时(焙烧时间对还原铁粉产率的影响如图所示),超过5小时后还原铁粉产率降低的原因是_______ 。

 、
、 及少量
及少量 )可用于制备
)可用于制备 和还原铁粉,其流程如图:
和还原铁粉,其流程如图:
(1)“酸溶”前需粉碎烧渣,其目的是
(2)“滤渣”的主要成分是
(3)“还原”时,
 被氧化为
被氧化为 的离子方程式是
的离子方程式是(4)“焙烧”时,烧渣、无烟煤、
 的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
添加
 的目的是:①脱除
的目的是:①脱除 等;②
等;②(5)“焙烧”在半封闭装置中进行,投料层表面盖有适当厚度的煤层,“焙烧”时间控制在4~4.5小时(焙烧时间对还原铁粉产率的影响如图所示),超过5小时后还原铁粉产率降低的原因是

您最近一年使用:0次
2020-03-14更新
|
269次组卷
|
2卷引用:江苏省扬州市2020届高三上学期期末检测化学试题
名校
解题方法
7 . 氯化铬晶体(CrCl3·6H2O)是一种重要的工业原料,工业上常用铬酸钠(Na2CrO4)来制备。实验室中以红矾钠(Na2Cr2O7)为原料制备CrCl3·6H2O的流程如下:
已知:①Cr2O72-+H2O 2CrO42-+2H+;②CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
2CrO42-+2H+;②CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
(1)碱溶的目的是__________ ,所加40%NaOH不宜过量太多的原因是______________________ 。
(2)还原时先加入过量CH3OH再加入10%HCl,生成CO2,写出该反应的离子方程式_____________ 。
(3)使用下列用品来测定溶液的pH,合理的是_____ (填字母)。
A.pH计 B.pH试纸 C.酚酞溶液
(4)使用下图装置从滤液中分离出CH3OH。
①图中仪器A的名称为_______ 。
②在仪器A中加入沸石,再加入滤液,蒸馏,收集蒸馏出的CH3OH循环使用。有的同学认为,该过程中需要加入CaO,防止水随CH3OH一起蒸出,你认为是否有必要并说明理由:___________ 。
(5)请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得固体_____ ,____ ,冷却结晶,过滤,____ ,低温干燥,得到CrCl3·6H2O。(实验中可供选择的试剂:盐酸、硫酸、蒸馏水、乙醇、乙醚)

已知:①Cr2O72-+H2O
 2CrO42-+2H+;②CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
2CrO42-+2H+;②CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。(1)碱溶的目的是
(2)还原时先加入过量CH3OH再加入10%HCl,生成CO2,写出该反应的离子方程式
(3)使用下列用品来测定溶液的pH,合理的是
A.pH计 B.pH试纸 C.酚酞溶液
(4)使用下图装置从滤液中分离出CH3OH。
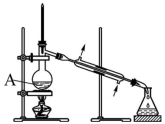
①图中仪器A的名称为
②在仪器A中加入沸石,再加入滤液,蒸馏,收集蒸馏出的CH3OH循环使用。有的同学认为,该过程中需要加入CaO,防止水随CH3OH一起蒸出,你认为是否有必要并说明理由:
(5)请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得固体
您最近一年使用:0次



