1 . 向一恒容密闭容器中加入 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
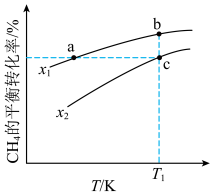
的平衡转化率按不同投料比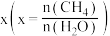 温度的变化曲线如图所示。下列说法不正确的是
温度的变化曲线如图所示。下列说法不正确的是
 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比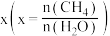 温度的变化曲线如图所示。下列说法不正确的是
温度的变化曲线如图所示。下列说法不正确的是
A.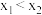 |
B. 两点的正反应速率: 两点的正反应速率: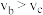 |
| C.此反应在任意温度下都可自发进行 |
| D.当容器内气体的平均相对分子质量不变时,反应达平衡状态 |
您最近一年使用:0次
解题方法
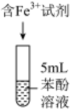
2 . 某小组同学探究铁离子与苯酚的反应。
已知: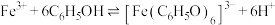 ;
;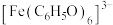 为紫色配合物。
为紫色配合物。
(1)配制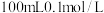 苯酚溶液,需要用到的玻璃仪器有:烧杯、胶头滴管、玻璃棒、
苯酚溶液,需要用到的玻璃仪器有:烧杯、胶头滴管、玻璃棒、__________ 。
(2)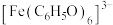 中,提供空轨道用以形成配位键的微粒是
中,提供空轨道用以形成配位键的微粒是__________ ,配位数为__________ 。
(3)探究铁盐种类和pH对苯酚与 显色反应的影响。
显色反应的影响。
查阅资料:
ⅰ. 对苯酚与
对苯酚与 的显色反应无影响;
的显色反应无影响;
ⅱ.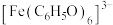 对特定波长光的吸收程度(用吸光度A表示)与
对特定波长光的吸收程度(用吸光度A表示)与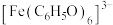 浓度在一定范围内成正比。
浓度在一定范围内成正比。
提出猜想:猜想1: 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响
猜想2: 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响
猜想3: 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响
进行实验:
常温下,用盐酸调节pH,配制得到pH分别为a和b的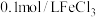 溶液(
溶液( );用硫酸调节pH,配制得到pH分别为a和b的
);用硫酸调节pH,配制得到pH分别为a和b的 溶液。取4支试管各加入
溶液。取4支试管各加入 苯酚溶液,按实验1~4分别再加入0.1mL含
苯酚溶液,按实验1~4分别再加入0.1mL含 的试剂,显色10min后用紫外一可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对
的试剂,显色10min后用紫外一可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对 水解程度的影响可忽略)。
水解程度的影响可忽略)。
结果讨论:实验结果为
①根据实验结果,小组同学认为此结果不足以证明猜想3成立的理由是__________________ 。
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中试剂M为__________________ 。(限选试剂:NaCl溶液、 溶液、NaCl固体、
溶液、NaCl固体、 固体)。
固体)。
③根据实验1~6的结果,小组同学得出猜想1不成立,猜想2成立,且 对苯酚与
对苯酚与 的显色反应起抑制作用,得出此结论的依据是:
的显色反应起抑制作用,得出此结论的依据是: 、A1
、A1__________ A6(填“>”“<”或者“=”)。
④根据实验1~6的结果,小组同学得出猜想3成立,且 对
对 与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是
与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是______________________________ 。
(4)通过以上实验结论分析:与苯酚相比,对羟基苯甲酸(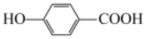 )与
)与 溶液发生显色反应
溶液发生显色反应__________ (填“容易”或“更难”)。
(5)实验室中常用某些配合物的性质进行物质的检验,请举一例子并说明现象____________ 。
已知:
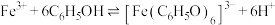 ;
;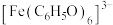 为紫色配合物。
为紫色配合物。(1)配制
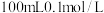 苯酚溶液,需要用到的玻璃仪器有:烧杯、胶头滴管、玻璃棒、
苯酚溶液,需要用到的玻璃仪器有:烧杯、胶头滴管、玻璃棒、(2)
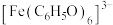 中,提供空轨道用以形成配位键的微粒是
中,提供空轨道用以形成配位键的微粒是(3)探究铁盐种类和pH对苯酚与
 显色反应的影响。
显色反应的影响。查阅资料:
ⅰ.
 对苯酚与
对苯酚与 的显色反应无影响;
的显色反应无影响;ⅱ.
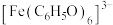 对特定波长光的吸收程度(用吸光度A表示)与
对特定波长光的吸收程度(用吸光度A表示)与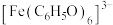 浓度在一定范围内成正比。
浓度在一定范围内成正比。提出猜想:猜想1:
 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响猜想2:
 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响猜想3:
 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响进行实验:
常温下,用盐酸调节pH,配制得到pH分别为a和b的
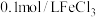 溶液(
溶液( );用硫酸调节pH,配制得到pH分别为a和b的
);用硫酸调节pH,配制得到pH分别为a和b的 溶液。取4支试管各加入
溶液。取4支试管各加入 苯酚溶液,按实验1~4分别再加入0.1mL含
苯酚溶液,按实验1~4分别再加入0.1mL含 的试剂,显色10min后用紫外一可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对
的试剂,显色10min后用紫外一可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对 水解程度的影响可忽略)。
水解程度的影响可忽略)。
| 序号 | 含 | 吸光度 | |
|
| |||
1 |
| / | A1 | |
2 |
| / | A2 | |
3 | / |
| A3 | |
4 | / |
| A4 | |

①根据实验结果,小组同学认为此结果不足以证明猜想3成立的理由是
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中试剂M为
 溶液、NaCl固体、
溶液、NaCl固体、 固体)。
固体)。
| 序号 | 含 | 再加入的试剂 | 吸光度 | |
|
| ||||
5 | / |
| NaCl固体 | A5 | |
6 |
| / | 试剂M | A6 | |
 对苯酚与
对苯酚与 的显色反应起抑制作用,得出此结论的依据是:
的显色反应起抑制作用,得出此结论的依据是: 、A1
、A1④根据实验1~6的结果,小组同学得出猜想3成立,且
 对
对 与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是
与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是(4)通过以上实验结论分析:与苯酚相比,对羟基苯甲酸(
 )与
)与 溶液发生显色反应
溶液发生显色反应(5)实验室中常用某些配合物的性质进行物质的检验,请举一例子并说明现象
您最近一年使用:0次
23-24高三上·广东·阶段练习
解题方法
3 . 一定条件下,利用R(g)制备M(g),反应为① ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示。下列说法正确的是
两个副反应,反应历程如图所示。下列说法正确的是
 ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示。下列说法正确的是
两个副反应,反应历程如图所示。下列说法正确的是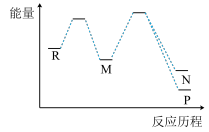
| A.反应③比反应①更快达到平衡 |
| B.温度越高,产物中M的纯度越高 |
| C.一定时间内,使用合适的催化剂可减少体系中P的含量 |
D.增大R的浓度,反应①②③的 增大, 增大, 减小 减小 |
您最近一年使用:0次
2023-12-02更新
|
425次组卷
|
4卷引用:化学(广东卷01)-2024年高考押题预测卷
(已下线)化学(广东卷01)-2024年高考押题预测卷广东省2024届普通高中毕业班高三上学期第二次调研考试化学试题2024届广东省茂名市化州市高三上学期第二次调研考试化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
23-24高三上·广东·阶段练习
解题方法
4 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 可用饱和 溶液浸泡生锈的青铜器 溶液浸泡生锈的青铜器 |  不稳定,易分解 不稳定,易分解 |
| B | 向蛋白质溶液中加入几滴醋酸铅溶液,有固体析出 | 蛋白质发生了盐析 |
| C | 向 溶液中滴加1滴 溶液中滴加1滴 溶液,再加入稀 溶液,再加入稀 溶液,溶液颜色变浅色 溶液,溶液颜色变浅色 | 其他条件不变,增大产物浓度,平衡向逆反应方向移动 |
| D | 向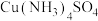 溶液中加入乙醇,析出蓝色晶体[ 溶液中加入乙醇,析出蓝色晶体[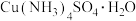 ] ] | 乙醇的极性比水的极性弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-02更新
|
519次组卷
|
3卷引用:化学(广东卷01)-2024年高考押题预测卷
名校
5 . 化学是以实验为基础的科学。下列实验操作和现象,能得出相应结论的是
| 选项 | 操作和现象 | 实验结论 |
| A | 向菠菜汁中加入少量稀硝酸,再滴入几滴 溶液,溶液变红 溶液,溶液变红 | 菠菜汁中含有 |
| B | 将收集满 的试管倒扣在盛有足量水的水槽中,试管中液面上升,试管顶部仍有少量气体 的试管倒扣在盛有足量水的水槽中,试管中液面上升,试管顶部仍有少量气体 | 收集的 气体中含有不溶于水的杂质气体 气体中含有不溶于水的杂质气体 |
| C | 向 溶液中加入 溶液中加入 固体,溶液由蓝变绿 固体,溶液由蓝变绿 | 增大反应物浓度, 平衡正向移动 平衡正向移动 |
| D | 向 固体中加入饱和碳酸钠溶液,过滤、洗涤后,向滤渣中滴加稀盐酸,产生无色气泡,滤渣大部分溶解 固体中加入饱和碳酸钠溶液,过滤、洗涤后,向滤渣中滴加稀盐酸,产生无色气泡,滤渣大部分溶解 | 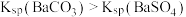 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-29更新
|
533次组卷
|
2卷引用:广东省华南师范大学附属中学2023届高三下学期第三次模拟考试化学试题
6 . “ 氧化法”和“光催化氧化法”常用于烟气脱硫、脱硝,对环境保护意义重大。回答下列问题:
氧化法”和“光催化氧化法”常用于烟气脱硫、脱硝,对环境保护意义重大。回答下列问题:
Ⅰ. 氧化法
氧化法
(1)用 氧化烟气中的
氧化烟气中的 时,体系中存在以下反应:
时,体系中存在以下反应:
a)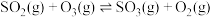

b)
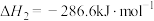
c)
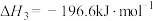
根据盖斯定律,
_______ 。
(2)在密闭容器中充入
 和
和
 ,发生以下反应:
,发生以下反应:
d)
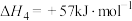
e)
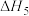
不同压强(p)下, 的平衡转化率
的平衡转化率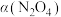 随反应温度(T)的变化关系如下图所示:
随反应温度(T)的变化关系如下图所示:
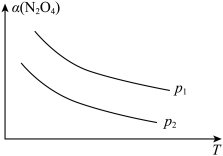
①由图可知,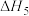
_______ 0(填“大于”或“小于”下同),
_______  。
。
②下列有关该反应体系的说法正确的是_______ (填标号)。
A.恒压下,混合气体的密度保持不变时,说明反应体系已达到平衡
B.任意时刻,存在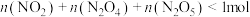
C.恒容下,升高温度,该体系中气体颜色变浅
D.恒容下,增大 的浓度,反应d、e的正反应速率均增大
的浓度,反应d、e的正反应速率均增大
③某温度下,平衡时 的物质的量分数为
的物质的量分数为 ,且
,且 与
与 的物质的量分数相等,此时
的物质的量分数相等,此时
_______ mol。
Ⅱ.光催化氧化法
光照条件下,催化剂 表面产生电子(
表面产生电子( )和空穴(
)和空穴( )。电子与
)。电子与 作用生成离子自由基(
作用生成离子自由基( ),空穴与水电离出的
),空穴与水电离出的 作用生成羟基自由基(
作用生成羟基自由基( ),
), 和
和 分别与
分别与 反应生成
反应生成 。变化过程如下图所示:
。变化过程如下图所示:

(3)一定范围内,NO脱除速率随烟气湿度的增大而增大,结合催化剂的作用机理,分析可能的原因_______ 。
(4)已知该过程中生成的 可继续与
可继续与 发生反应:
发生反应: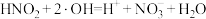 ;该反应可分两步进行,请补充反应ⅰ:
;该反应可分两步进行,请补充反应ⅰ:
ⅰ._______ ;
ⅱ.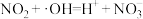 。
。
(5)理论上“光催化氧化法”中,消耗的 与生成的
与生成的 的物质的量之比为
的物质的量之比为_______ 。
 氧化法”和“光催化氧化法”常用于烟气脱硫、脱硝,对环境保护意义重大。回答下列问题:
氧化法”和“光催化氧化法”常用于烟气脱硫、脱硝,对环境保护意义重大。回答下列问题:Ⅰ.
 氧化法
氧化法(1)用
 氧化烟气中的
氧化烟气中的 时,体系中存在以下反应:
时,体系中存在以下反应:a)
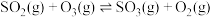

b)

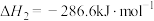
c)

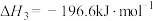
根据盖斯定律,

(2)在密闭容器中充入

 和
和
 ,发生以下反应:
,发生以下反应:d)

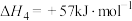
e)

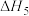
不同压强(p)下,
 的平衡转化率
的平衡转化率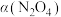 随反应温度(T)的变化关系如下图所示:
随反应温度(T)的变化关系如下图所示:
①由图可知,
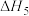

 。
。②下列有关该反应体系的说法正确的是
A.恒压下,混合气体的密度保持不变时,说明反应体系已达到平衡
B.任意时刻,存在
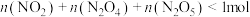
C.恒容下,升高温度,该体系中气体颜色变浅
D.恒容下,增大
 的浓度,反应d、e的正反应速率均增大
的浓度,反应d、e的正反应速率均增大③某温度下,平衡时
 的物质的量分数为
的物质的量分数为 ,且
,且 与
与 的物质的量分数相等,此时
的物质的量分数相等,此时
Ⅱ.光催化氧化法
光照条件下,催化剂
 表面产生电子(
表面产生电子( )和空穴(
)和空穴( )。电子与
)。电子与 作用生成离子自由基(
作用生成离子自由基( ),空穴与水电离出的
),空穴与水电离出的 作用生成羟基自由基(
作用生成羟基自由基( ),
), 和
和 分别与
分别与 反应生成
反应生成 。变化过程如下图所示:
。变化过程如下图所示:
(3)一定范围内,NO脱除速率随烟气湿度的增大而增大,结合催化剂的作用机理,分析可能的原因
(4)已知该过程中生成的
 可继续与
可继续与 发生反应:
发生反应: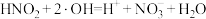 ;该反应可分两步进行,请补充反应ⅰ:
;该反应可分两步进行,请补充反应ⅰ:ⅰ.
ⅱ.
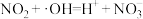 。
。(5)理论上“光催化氧化法”中,消耗的
 与生成的
与生成的 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
7 . 一定温度下,向2L密闭容器中加入
 发生反应①
发生反应①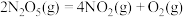 ,②
,② ,反应体系中
,反应体系中 、
、 、
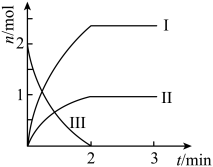
、 的物质的量随反应时间t的部分变化曲线如图所示,下列说法正确的是
的物质的量随反应时间t的部分变化曲线如图所示,下列说法正确的是

 发生反应①
发生反应①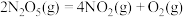 ,②
,② ,反应体系中
,反应体系中 、
、 、
、 的物质的量随反应时间t的部分变化曲线如图所示,下列说法正确的是
的物质的量随反应时间t的部分变化曲线如图所示,下列说法正确的是
A.曲线Ⅱ表示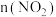 随t的变化 随t的变化 |
B. 内, 内,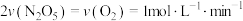 |
C. 后,充入 后,充入 ,容器的气体颜色先变深后变浅 ,容器的气体颜色先变深后变浅 |
D. 后,充入 后,充入 ,容器的气体颜色变浅 ,容器的气体颜色变浅 |
您最近一年使用:0次
解题方法
8 . 宏观辨识与微观探析是化学学科核心素养之一,下列关于次氯酸盐性质实验对应的反应方程式书写正确的是
A.将足量的二氧化碳通入 溶液中: 溶液中: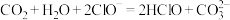 |
B.验证“84”消毒液与洁则剂不能混合的原因: |
C.用 溶液吸收废气中的 溶液吸收废气中的 制石膏乳: 制石膏乳: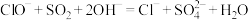 |
D.将硫酸铬溶液滴入含 的强碱性溶液中: 的强碱性溶液中: |
您最近一年使用:0次
名校
解题方法
9 . CuCl2是常见的化学试剂,某学习小组利用废铜屑“湿法”制备CuCl2·2H2O。

氯化铜在不同温度下结晶形成的结晶水合物
回答下列问题:
(1)仪器a的名称为_______ ,NaOH溶液的作用是_______ 。
(2)“湿法”制备CuCl2的离子方程式为_______ ,实验中,H2O2的实际用量要大于理论用量,原因是_______ 。
(3)为得到纯净的CuCl2·2H2O晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入HCl气体,加热蒸发浓缩,_______ ,过滤,洗涤,低温干燥,其中,持续通入HCl的作用是_______ 。
(4)查阅资料:[Cu(H2O)4]2+(蓝色)+4Cl- ⇌[CuCl4]2-(黄色)+4H2O,设计实验证明CuCl2溶液中存在上述平衡:取少量蓝色CuCl2稀溶液于试管中,_______ 。
(5)查阅资料:[CuCl4]2-比[Cu(H2O)4]2+更稳定:与Cu2+配位时,Cl-比H2O的配位能力更强,原因可能是_______ 。

氯化铜在不同温度下结晶形成的结晶水合物
| 温度 | 15℃以下 | 15~25.7℃ | 26~42℃ | 42℃以上 |
| 结晶水合物 | CuCl2·4H2O | CuCl2·3H2O | CuCl2·2H2O | CuCl2·H2O |
(1)仪器a的名称为
(2)“湿法”制备CuCl2的离子方程式为
(3)为得到纯净的CuCl2·2H2O晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入HCl气体,加热蒸发浓缩,
(4)查阅资料:[Cu(H2O)4]2+(蓝色)+4Cl- ⇌[CuCl4]2-(黄色)+4H2O,设计实验证明CuCl2溶液中存在上述平衡:取少量蓝色CuCl2稀溶液于试管中,
(5)查阅资料:[CuCl4]2-比[Cu(H2O)4]2+更稳定:与Cu2+配位时,Cl-比H2O的配位能力更强,原因可能是
您最近一年使用:0次
10 . 一定温度下,向2L恒温密闭容器中加入足量活性炭和2 mol NO2,发生反应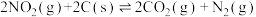 ,部分物质的物质的量随反应时间t的变化曲线如图所示,下列说法正确的是
,部分物质的物质的量随反应时间t的变化曲线如图所示,下列说法正确的是
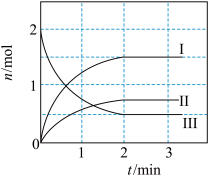
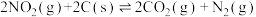 ,部分物质的物质的量随反应时间t的变化曲线如图所示,下列说法正确的是
,部分物质的物质的量随反应时间t的变化曲线如图所示,下列说法正确的是
| A.曲线Ⅱ表示c(CO2)随t的变化 |
B.0~2 min内,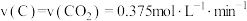 |
| C.3 min时,加入催化剂可同时增大NO2的生成速率和消耗速率 |
| D.3 min时。充入N2增大压强,该容器的气体颜色不变 |
您最近一年使用:0次