1 . 回答下列问题。
(1)已知下列热化学方程式:
Ⅰ.
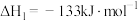
Ⅱ.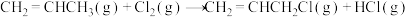
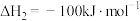
在相同条件下, 的正反应的活化能
的正反应的活化能 为
为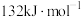 ,则逆反应的活化能
,则逆反应的活化能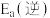 为
为___________  。
。
(2)查阅资料得知,反应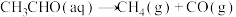 在含有少量I2的溶液中分两步进行:
在含有少量I2的溶液中分两步进行:
第Ⅰ步反应为 (慢反应);
(慢反应);
第Ⅱ步为快反应。
增大I2的浓度___________ (填“能”或“不能”)明显增大总反应的平均速率,理由为___________ 。
(3)氯化铜晶体( )常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
___________ (填字母,下同)。
a.KMnO4溶液 b.氯水 c.溴水 d.H2O2溶液
②溶液C中加入试剂y可以调节溶液pH,从而除去 而不引入杂质。试剂y可选用下列物质中的
而不引入杂质。试剂y可选用下列物质中的___________ 。
a.Cu b.CuO c. d.NaOH
d.NaOH
③SOCl2与水反应的化学方程式为___________ 。
④SOCl2与 混合并加热,可得到无水CuCl2的原因是
混合并加热,可得到无水CuCl2的原因是___________ 。
(1)已知下列热化学方程式:
Ⅰ.

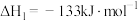
Ⅱ.
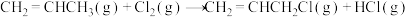
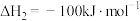
在相同条件下,
 的正反应的活化能
的正反应的活化能 为
为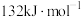 ,则逆反应的活化能
,则逆反应的活化能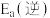 为
为 。
。(2)查阅资料得知,反应
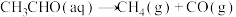 在含有少量I2的溶液中分两步进行:
在含有少量I2的溶液中分两步进行:第Ⅰ步反应为
 (慢反应);
(慢反应);第Ⅱ步为快反应。
增大I2的浓度
(3)氯化铜晶体(
 )常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下: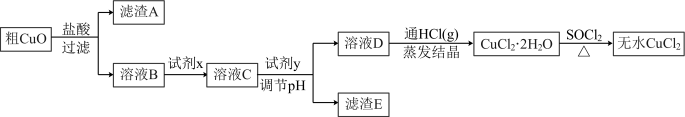
 |  |  | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全的pH | 3.2 | 9.0 | 6.7 |
已知:氯化亚砜(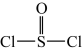 )熔点-105℃,沸点78.8℃,易水解。
)熔点-105℃,沸点78.8℃,易水解。
a.KMnO4溶液 b.氯水 c.溴水 d.H2O2溶液
②溶液C中加入试剂y可以调节溶液pH,从而除去
 而不引入杂质。试剂y可选用下列物质中的
而不引入杂质。试剂y可选用下列物质中的a.Cu b.CuO c.
 d.NaOH
d.NaOH③SOCl2与水反应的化学方程式为
④SOCl2与
 混合并加热,可得到无水CuCl2的原因是
混合并加热,可得到无水CuCl2的原因是
您最近半年使用:0次
解题方法
2 . 已知:无CO时反应 、有CO时反应
、有CO时反应 。在容积为
。在容积为 的容器中,相同时间下测得
的容器中,相同时间下测得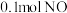 转化为
转化为 的转化率随温度变化如图所示。下列说法不正确的是
的转化率随温度变化如图所示。下列说法不正确的是
 、有CO时反应
、有CO时反应 。在容积为
。在容积为 的容器中,相同时间下测得
的容器中,相同时间下测得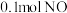 转化为
转化为 的转化率随温度变化如图所示。下列说法不正确的是
的转化率随温度变化如图所示。下列说法不正确的是
A.反应 的 的 |
| B.有CO时,该反应在低温条件下自发进行 |
C.Y点再通入CO、 各 各 ,此时v(CO,正)<v(CO,逆) ,此时v(CO,正)<v(CO,逆) |
D.达平衡后,其他条件不变改变物料使 ,CO转化率下降 ,CO转化率下降 |
您最近半年使用:0次
解题方法
3 . 在实验室中进行下列实验,下列操作能实现实验目的的是
| 选项 | 实验目的 | 操作 |
| A | 检验甲酸中是否含有羧基 | 取其水溶液于试管中,向其中加入少量金属钠,观察溶液中有无气泡产生 |
| B | 检验某溶液中是否含有 | 取少量待测液于试管中,向其中滴加浓氨水,生成白色沉淀,继续滴加浓氨水,观察沉淀是否溶解 |
| C | 检验牺牲阳极法对钢铁防腐的效果 | 将镀层有破损的镀锌铁片放入酸化的3%NaCl溶液中,一段时间后,取少量溶液向其中加入 溶液,观察有无蓝色沉淀生成 溶液,观察有无蓝色沉淀生成 |
| D | 探究氢离子浓度对 、 、 互相转化影响 互相转化影响 | 向 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-01-02更新
|
361次组卷
|
2卷引用:山西省三重教育2023-2024学年高三上学期联考理科综合试题
名校
4 . NOx(主要指NO和NO2)是大气主要污染物之一,有效去除大气中的NOx是环保工作者的重要研究课题。回答下列问题:
(1)已知:
①2NO2(g)+H2O(l)=HNO3 (aq) + HNO2(aq) △H1=-116.1 kJ·mol-1;
②3HNO2 (aq)=HNO3(aq) +2NO(g)+H2O(l) △H2=+75.9 kJ·mol-1。
则3NO2(g)+ H2O(l)=2HNO3 (aq)+NO(g)的△H为___________ 。
(2)在400 °C、催化剂存在条件下,NH3可以将NO还原为N2和H2O,反应为4NH3(g)+6NO(g) 5N2(g) +6H2O(g) △H<0。在该条件下,向体积为1 L的恒容密闭容器中通入4 mol NH3和6 mol NO发生上述反应,5 min末达到平衡, NO的平衡转化率为90%。
5N2(g) +6H2O(g) △H<0。在该条件下,向体积为1 L的恒容密闭容器中通入4 mol NH3和6 mol NO发生上述反应,5 min末达到平衡, NO的平衡转化率为90%。
①该反应的平衡常数表达式为Kc=___________ ,0~5 min用N2表示该反应的平均速率为___________ mol· L-1·min-1
②400 °C时,为提高NO的转化率,应选择的反应条件为___________ (填“增大压强”或“减小压强”)。
(3)NO和H2反应的化学方程式为2NO(g) +2H2(g) N2(g) + 2H2O(g),在T °C时,1 L恒容密闭容器里,充入0.003molNO和0.006molH2,测得体系的总压强p随时间t的变化如下表所示:
N2(g) + 2H2O(g),在T °C时,1 L恒容密闭容器里,充入0.003molNO和0.006molH2,测得体系的总压强p随时间t的变化如下表所示:
t=20 min时,体系中H2的分压p(H2)=___________ kPa,NO的平衡转化率为___________ %(保留一位小数)。
(4)温度为T° C,向体积不等的恒容密闭容器中分别加入足量活性炭和1 mol NO2,发生反应:2C(s)+2NO2(g) N2(g) +2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
N2(g) +2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
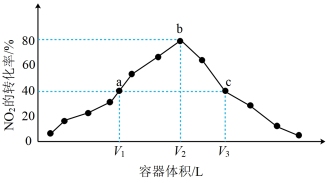
①c点时,反应___________ (填“是”或“否”)达到平衡状态。
②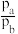
___________ (填“>”“=”或“<”) 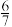 。
。
(1)已知:
①2NO2(g)+H2O(l)=HNO3 (aq) + HNO2(aq) △H1=-116.1 kJ·mol-1;
②3HNO2 (aq)=HNO3(aq) +2NO(g)+H2O(l) △H2=+75.9 kJ·mol-1。
则3NO2(g)+ H2O(l)=2HNO3 (aq)+NO(g)的△H为
(2)在400 °C、催化剂存在条件下,NH3可以将NO还原为N2和H2O,反应为4NH3(g)+6NO(g)
 5N2(g) +6H2O(g) △H<0。在该条件下,向体积为1 L的恒容密闭容器中通入4 mol NH3和6 mol NO发生上述反应,5 min末达到平衡, NO的平衡转化率为90%。
5N2(g) +6H2O(g) △H<0。在该条件下,向体积为1 L的恒容密闭容器中通入4 mol NH3和6 mol NO发生上述反应,5 min末达到平衡, NO的平衡转化率为90%。①该反应的平衡常数表达式为Kc=
②400 °C时,为提高NO的转化率,应选择的反应条件为
(3)NO和H2反应的化学方程式为2NO(g) +2H2(g)
 N2(g) + 2H2O(g),在T °C时,1 L恒容密闭容器里,充入0.003molNO和0.006molH2,测得体系的总压强p随时间t的变化如下表所示:
N2(g) + 2H2O(g),在T °C时,1 L恒容密闭容器里,充入0.003molNO和0.006molH2,测得体系的总压强p随时间t的变化如下表所示:| t/ min | 0 | 10 | 20 | 30 | 40 |
| p/kPa | 36 | 33.8 | 32 | 30.4 | 30.4 |
t=20 min时,体系中H2的分压p(H2)=
(4)温度为T° C,向体积不等的恒容密闭容器中分别加入足量活性炭和1 mol NO2,发生反应:2C(s)+2NO2(g)
 N2(g) +2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
N2(g) +2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
①c点时,反应
②
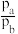
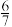 。
。
您最近半年使用:0次
2022-06-10更新
|
342次组卷
|
2卷引用:山西省吕梁市交城县2022届高三下学期第一次模拟考试理科综合化学试题
名校
解题方法
5 . 已知反应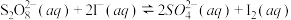 ,若往该溶液中加入含
,若往该溶液中加入含 的某溶液,反应机理:
的某溶液,反应机理:
①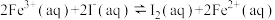
②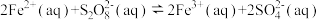
下列说法错误的是
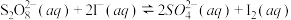 ,若往该溶液中加入含
,若往该溶液中加入含 的某溶液,反应机理:
的某溶液,反应机理:①
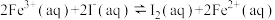
②
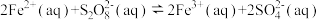
下列说法错误的是

A. 是该反应的催化剂,加入 是该反应的催化剂,加入 后降低了该反应的活化能 后降低了该反应的活化能 |
| B.往该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深 |
C.步骤①中 和 和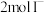 的总能量低于 的总能量低于 和 和 的总能量 的总能量 |
D.增大 浓度或 浓度或 浓度,反应①、反应②的反应速率均加快 浓度,反应①、反应②的反应速率均加快 |
您最近半年使用:0次
2020-12-18更新
|
1469次组卷
|
8卷引用:山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题
山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题山东省菏泽市2020-2021学年高二上学期期中考试化学试题(A)(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)(已下线)2.4 化学反应的调控-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)河南省南阳市第一中学校2022-2023学年高二上学期开学考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】60(已下线)【2022】【高二化学】【期中考】-179北京市第五十五中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
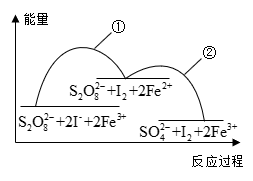
6 . 已知反应S2O (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )

①2Fe3+(aq)+2I-(aq) I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)
②2Fe2+(aq)+S2O (aq)
(aq) 2Fe3+(aq)+2SO
2Fe3+(aq)+2SO (aq)
(aq)
 (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
①2Fe3+(aq)+2I-(aq)
 I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)②2Fe2+(aq)+S2O
 (aq)
(aq) 2Fe3+(aq)+2SO
2Fe3+(aq)+2SO (aq)
(aq)| A.Fe3+是该反应的催化剂,加入Fe3+后降低了该反应的活化能 |
| B.反应①比反应②所需活化能大 |
| C.向该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深 |
| D.该反应可设计成原电池 |
您最近半年使用:0次
2020-09-25更新
|
1721次组卷
|
14卷引用:山西省大同市2021届高三上学期学情调研测试化学试题
山西省大同市2021届高三上学期学情调研测试化学试题辽宁省六校协作体2021届高三第一次联考化学试题江西省赣州市会昌县七校2021届高三联合9月月考化学试题辽宁省开原市中固镇第二中学2021届高三上学期9月月考化学试题内蒙古自治区赤峰二中2020-2021学年高二上学期第一次月考化学试题江西省红色七校(分宜中学、会昌中学、莲花中学、南城一中、任弼时中学、瑞金一中、遂川中学)2021届高三上学期第一次联考化学试题陕西省西安市长安区第一中学2021届高三上学期第三次月考化学试题江西省吉安县立中学2020-2021学年高二上学期12月月考化学(B班)试题江苏省苏州市姑苏区苏州中学2020-2021学年高二下学期期中考试化学试题江西省景德镇一中2020-2021学年高一下学期期中考试化学(1班)试题吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题黑龙江省双鸭山市第一中学2021-2022学年高二上学期第一次月考化学试题吉林省汪清县第六中学2021-2022学年高二12月月考化学试题吉林省乾安县第七中学2021-2022学年高二上学期第一次质量检测化学试题
名校
7 . 下列图示与对应的叙述相符的是( )
A.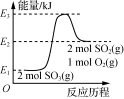 由图可知,2SO3(g)===2SO2(g)+O2(g) ΔH=(E1-E2)kJ·mol-1 由图可知,2SO3(g)===2SO2(g)+O2(g) ΔH=(E1-E2)kJ·mol-1 |
B.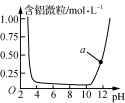 表示Al3+与OH-反应时溶液中含铝微粒浓度变化曲线,a点溶液中存在大量Al3+ 表示Al3+与OH-反应时溶液中含铝微粒浓度变化曲线,a点溶液中存在大量Al3+ |
C.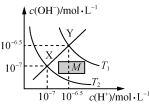 温度在T1和T2时水溶液中c(H+)和c(OH-)的关系,则阴影部分M内任意一点均满足c(H+)>c(OH-) 温度在T1和T2时水溶液中c(H+)和c(OH-)的关系,则阴影部分M内任意一点均满足c(H+)>c(OH-) |
D.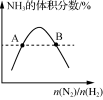 表示反应N2(g)+3H2(g)=2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2) 表示反应N2(g)+3H2(g)=2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2) |
您最近半年使用:0次
2019-03-28更新
|
1546次组卷
|
3卷引用:山西运城市运康中学校2019-2020学年高三12月月考化学试题
名校
8 . 一定条件下,体积为2L的密闭容器中,2mol X和3mol Y进行反应:X(g)+Y(g) Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是
Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是
 Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是
Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是| A.以X浓度变化表示的反应速率为0.05 mol/(L•s) |
| B.其他条件不变,增大X的浓度,平衡右移,X的转化率增大 |
| C.其他条件不变,12s后将容器体积扩大为10L,Z的平衡浓度变为0.06mol/L |
| D.其他条件不变,若移走1molX和1.5molY,再达平衡时Z的物质的量小于0.3mol |
您最近半年使用:0次
2019-02-19更新
|
512次组卷
|
4卷引用:山西省运城市芮城县2018-2019学年高二上学期期末考试化学试题
名校
9 . 将BaO2放入密闭真空容器中,反应2BaO2(s) 2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
 2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同 | A.保持体积和温度不变,充入一定量的氧气 | B.保持温度不变,缩小容器的体积 |
| C.保持体积不变,升高温度 | D.保持体积和温度不变,加入BaO2 |
您最近半年使用:0次
2017-10-22更新
|
351次组卷
|
6卷引用:【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期10月模块诊断化学试题
2010·山西太原·一模
10 . 在相同温度和压强下,对反应CO2(g)+H2(g) CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
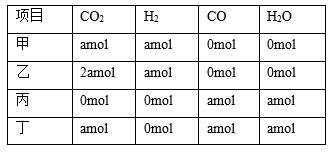
上述四种情况达到平衡后,n(CO)的大小顺序是
 CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
上述四种情况达到平衡后,n(CO)的大小顺序是
| A.乙=丁>丙=甲 | B.乙>丁>甲>丙 | C.丁>乙>丙=甲 | D.丁>丙>乙>甲 |
您最近半年使用:0次
2016-12-09更新
|
911次组卷
|
7卷引用:山西省太原五中2010届高三5月末考试试题理综化学
(已下线)山西省太原五中2010届高三5月末考试试题理综化学(已下线)2011-2012学年贵州省凯里一中高二上学期期中考试化学试卷(已下线)2014年高中化学苏教版选修四专题2 反应速率与化学平衡练习卷(已下线)2011-2012贵州省凯里一中第一学期期末考试高二化学试卷云南省德宏州芒市第一中学2017-2018学年高二上学期期中考试化学试题吉林省蛟河市一中2018-2019学年高一下学期第三次测试化学试题河南省安阳县第三高级中学2020-2021学年高二上学期第一次阶段考试化学试题



