名校
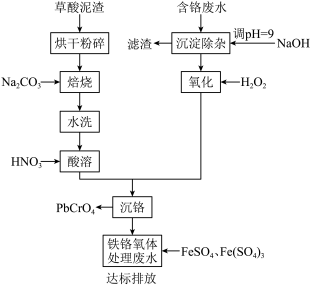
1 . 铬酸铅俗称铬黄,主要用于油漆、油墨、塑料以及橡胶等行业。一种以含铬废水(含Cr3+、Fe3+、Cu2+)和草酸泥渣(含草酸铅、硫酸铅)为原料制备铬酸铅的工艺流程如下:
回答下列问题
(1)草酸泥渣“粉碎”的目的是___________ ,“焙烧”时加入碳酸钠是为了将硫酸铅转化为PbO,同时放出CO2,该转化过程的化学方程式为___________ 。
(2)滤渣的主要成分为___________ 、___________ 。(填化学式)
(3)“沉淀除杂”所得滤液中含铬化合物主要为___________ 。(填化学式)
(4)“氧化”工序中发生反应的离子方程式为___________ 。
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因:___________ 。
(6)处理含 的废水时,Cr(Ⅵ)被还原成Cr(Ⅲ)。若投入10molFeSO4,使金属阳离子恰好完全形成铁铬氧体(FeO·FexCryO3,其中FexCryO3中Fe为+3价)沉淀,理论上还需要投入Fe2(SO4)3的物质的量为
的废水时,Cr(Ⅵ)被还原成Cr(Ⅲ)。若投入10molFeSO4,使金属阳离子恰好完全形成铁铬氧体(FeO·FexCryO3,其中FexCryO3中Fe为+3价)沉淀,理论上还需要投入Fe2(SO4)3的物质的量为___________ mol。

回答下列问题
(1)草酸泥渣“粉碎”的目的是
(2)滤渣的主要成分为
(3)“沉淀除杂”所得滤液中含铬化合物主要为
(4)“氧化”工序中发生反应的离子方程式为
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因:
(6)处理含
 的废水时,Cr(Ⅵ)被还原成Cr(Ⅲ)。若投入10molFeSO4,使金属阳离子恰好完全形成铁铬氧体(FeO·FexCryO3,其中FexCryO3中Fe为+3价)沉淀,理论上还需要投入Fe2(SO4)3的物质的量为
的废水时,Cr(Ⅵ)被还原成Cr(Ⅲ)。若投入10molFeSO4,使金属阳离子恰好完全形成铁铬氧体(FeO·FexCryO3,其中FexCryO3中Fe为+3价)沉淀,理论上还需要投入Fe2(SO4)3的物质的量为
您最近半年使用:0次
2024-04-13更新
|
217次组卷
|
4卷引用:2024届江西省吉安市第一中学高三下学期一模化学试题
2024届江西省吉安市第一中学高三下学期一模化学试题(已下线)东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题东北三省四市2024届高三教研联合体高考模拟(一)化学试卷东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题
2 . 一定温度下,把0.3molM(g)和0.1molN(s)加入容积为1L的恒容密闭容器中,发生反应 ,经5s反应达到平衡,0~5s内P(g)的平均反应速率为
,经5s反应达到平衡,0~5s内P(g)的平均反应速率为 ,同时生成0.1molQ(g)。下列叙述中错误的是
,同时生成0.1molQ(g)。下列叙述中错误的是
 ,经5s反应达到平衡,0~5s内P(g)的平均反应速率为
,经5s反应达到平衡,0~5s内P(g)的平均反应速率为 ,同时生成0.1molQ(g)。下列叙述中错误的是
,同时生成0.1molQ(g)。下列叙述中错误的是A.反应达到平衡状态时, 的体积分数为 的体积分数为 |
B.该温度下,反应的平衡常数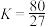 |
C.反应达到平衡后,再通入一定量的 ,再次达到平衡时 ,再次达到平衡时 的平衡浓度增大 的平衡浓度增大 |
D.若起始时加入 和 和 ,平衡时 ,平衡时 的体积分数为 的体积分数为 |
您最近半年使用:0次
名校
解题方法
3 . 下列有关实验现象和解释或结论都正确的组合是
| 选项 | 实验操作 | 现象 | 解释或结论 |
A | 相同条件下,分别测量0.1molL1和0.01molL1醋酸溶液的导电性 | 前者的导电性强 | 醋酸浓度越大,电离程度越大 |
B | 向FeCl3和KSCN的混合溶液中加入KCl固体 | 血红色溶液变浅 | 增大KCl的浓度,使得平衡逆向移动 |
C | 两支试管各盛4mL0.1mol/L酸性高锰酸钾溶液,分别加入2mL0.1mol/L草酸溶液和2mL0.2mol/L草酸溶液 | 加入0.2mol/L草酸溶液的试管中,高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
D | 把充有NO2和N2O4的平衡球装置分别放入热水和冷水中 | 热水中颜色更深 | 其他条件不变时,温度升高,平衡向吸热反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-09-04更新
|
591次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高三上学期11月期中考试化学试题
名校
4 . 某学习小组欲利用 平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
 溶液和20 mL 0.015 mol⋅L
溶液和20 mL 0.015 mol⋅L KSCN溶液混合,得血红色溶液X,进行下列实验:
KSCN溶液混合,得血红色溶液X,进行下列实验:
实验Ⅰ.改变 、
、 、
、 、
、 等离子浓度对平衡的影响
等离子浓度对平衡的影响
(1)取2 mL溶液X,加入5滴0.01 mol⋅L KSCN溶液,溶液红色
KSCN溶液,溶液红色_______ (填“变深”、“变浅”或“不变”,下同);取2 mL溶液X,插入经砂纸打磨过的铁丝,溶液红色_______ 。基于上述两个实验可以得到的结论是_______ 。
(2)取2 mL溶液X,加入5滴0.03 mol⋅L KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是
KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是_______ 或者不直接参与平衡体系的 或
或 对平衡产生了影响。
对平衡产生了影响。
实验Ⅱ.探究KCl对 平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
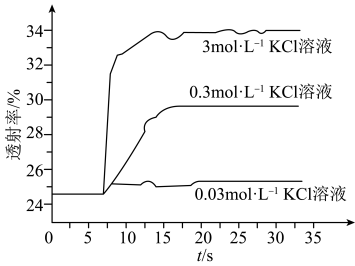
(3)上述实验可以得到以下结论:一是KCl对 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响_______ 。二是_______ 。
(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。
产生的影响。
猜想②: 产生的影响。
产生的影响。
猜想③:_______ 。
实验Ⅲ.探究盐对 和
和 平衡体系产生的影响
平衡体系产生的影响
资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在 溶液中存在反应
溶液中存在反应 。
。
(5)根据上述信息,学习小组同学各取2 mL溶液X,分别加入5滴①去离子水、②0.3 mol⋅L KCl溶液、③0.3 mol⋅L
KCl溶液、③0.3 mol⋅L NaCl溶液、④0.3 mol⋅L
NaCl溶液、④0.3 mol⋅L
 溶液、⑤3 mol⋅L
溶液、⑤3 mol⋅L HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。

上述实验能证明阳离子盐效应影响 平衡体系的实验组是
平衡体系的实验组是_______ 。盐效应影响较大的阳离子是_______ 。
A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:_______ 。
 平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
 溶液和20 mL 0.015 mol⋅L
溶液和20 mL 0.015 mol⋅L KSCN溶液混合,得血红色溶液X,进行下列实验:
KSCN溶液混合,得血红色溶液X,进行下列实验:实验Ⅰ.改变
 、
、 、
、 、
、 等离子浓度对平衡的影响
等离子浓度对平衡的影响(1)取2 mL溶液X,加入5滴0.01 mol⋅L
 KSCN溶液,溶液红色
KSCN溶液,溶液红色(2)取2 mL溶液X,加入5滴0.03 mol⋅L
 KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是
KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是 或
或 对平衡产生了影响。
对平衡产生了影响。实验Ⅱ.探究KCl对
 平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
(3)上述实验可以得到以下结论:一是KCl对
 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①:
 产生的影响。
产生的影响。猜想②:
 产生的影响。
产生的影响。猜想③:
实验Ⅲ.探究盐对
 和
和 平衡体系产生的影响
平衡体系产生的影响资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在
 溶液中存在反应
溶液中存在反应 。
。(5)根据上述信息,学习小组同学各取2 mL溶液X,分别加入5滴①去离子水、②0.3 mol⋅L
 KCl溶液、③0.3 mol⋅L
KCl溶液、③0.3 mol⋅L NaCl溶液、④0.3 mol⋅L
NaCl溶液、④0.3 mol⋅L
 溶液、⑤3 mol⋅L
溶液、⑤3 mol⋅L HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
上述实验能证明阳离子盐效应影响
 平衡体系的实验组是
平衡体系的实验组是A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:
您最近半年使用:0次
2023-05-21更新
|
320次组卷
|
2卷引用:江西省萍乡中学、新余市第一中学2023-2024学年高二上学期10月创新班联考化学试题
名校
解题方法
5 . 已知:Ag++NH3 Ag(NH3)+ K1=103.12
Ag(NH3)+ K1=103.12
Ag(NH3)++NH3 [Ag(NH3)2]+ K2
[Ag(NH3)2]+ K2
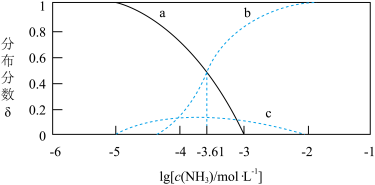
Ag+、Ag(NH3)+、[Ag(NH3)2]+的分布分数δ与lgc(NH3)关系如图所示,下列说法正确的是
{例如:分布分数δ(Ag+)= }
}
 Ag(NH3)+ K1=103.12
Ag(NH3)+ K1=103.12Ag(NH3)++NH3
 [Ag(NH3)2]+ K2
[Ag(NH3)2]+ K2Ag+、Ag(NH3)+、[Ag(NH3)2]+的分布分数δ与lgc(NH3)关系如图所示,下列说法正确的是
{例如:分布分数δ(Ag+)=
 }
}
| A.曲线c代表[Ag(NH3)2]+ |
| B.K2的数量级为105 |
C.[Ag(NH3)2]+ Ag++2NH3的平衡常数K=10-7.22 Ag++2NH3的平衡常数K=10-7.22 |
| D.当c(NH3)<0.01mol•L-1时,银元素主要以[Ag(NH3)2]+形式存在 |
您最近半年使用:0次
2023-04-30更新
|
264次组卷
|
2卷引用:江西省鹰潭市2023届高三下学期二模理综化学试题
名校
解题方法
6 . 某小组同学探究盐对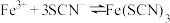 平衡体系的影响。
平衡体系的影响。
实验Ⅰ:探究KCl对 和
和 平衡体系的影响
平衡体系的影响
将等体积、低浓度的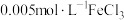 溶液(已用稀盐酸酸化)和
溶液(已用稀盐酸酸化)和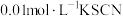 溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
② 在水溶液中由于水解而显黄色;
在水溶液中由于水解而显黄色; 溶液中存在
溶液中存在 (黄色)。
(黄色)。
(1)稀盐酸酸化 溶液的目的是
溶液的目的是___________ 。采用浓度较低的 溶液制备
溶液制备 和
和 平衡体系,是为了避免
平衡体系,是为了避免___________ (填离子符号)的颜色对实验干扰。
(2)从实验结果来看,KCl溶液确实对 和
和 平衡体系有影响,且随着KCl浓度增大,
平衡体系有影响,且随着KCl浓度增大, 平衡向
平衡向___________ (填“正”或“逆”)反应方向移动。
同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使 和
和 平衡状态因盐效应而发生变化。
平衡状态因盐效应而发生变化。
原因2:溶液中存在副反应 ,离子浓度发生变化,导致
,离子浓度发生变化,导致 和
和 平衡状态发生变化。
平衡状态发生变化。
(3)基于以上分析,该组同学取等体积的溶液a,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
①上述实验可证明盐效应影响了 和
和 平衡体系的是
平衡体系的是___________ (填字母序号)。
a.1和2 b.1和3 c.1和4
②选择实验___________ (填序号)可得出结论: 的盐效应弱于
的盐效应弱于 的盐效应。
的盐效应。
(4)取等体积的溶液a继续进行实验,结果如下表。
上述实验可证明副反应影响了 和
和 平衡体系,结合实验现象及化学用语分析副反应对
平衡体系,结合实验现象及化学用语分析副反应对 和
和 平衡体系有影响的原因:
平衡体系有影响的原因:___________ 。
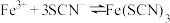 平衡体系的影响。
平衡体系的影响。实验Ⅰ:探究KCl对
 和
和 平衡体系的影响
平衡体系的影响将等体积、低浓度的
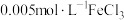 溶液(已用稀盐酸酸化)和
溶液(已用稀盐酸酸化)和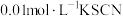 溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
②
 在水溶液中由于水解而显黄色;
在水溶液中由于水解而显黄色; 溶液中存在
溶液中存在 (黄色)。
(黄色)。(1)稀盐酸酸化
 溶液的目的是
溶液的目的是 溶液制备
溶液制备 和
和 平衡体系,是为了避免
平衡体系,是为了避免(2)从实验结果来看,KCl溶液确实对
 和
和 平衡体系有影响,且随着KCl浓度增大,
平衡体系有影响,且随着KCl浓度增大, 平衡向
平衡向同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使
 和
和 平衡状态因盐效应而发生变化。
平衡状态因盐效应而发生变化。原因2:溶液中存在副反应
 ,离子浓度发生变化,导致
,离子浓度发生变化,导致 和
和 平衡状态发生变化。
平衡状态发生变化。(3)基于以上分析,该组同学取等体积的溶液a,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
| 序号 | 加入少量盐 | 溶液颜色 |
| 1 | 无 | 红色 |
| 2 | KCl | 变浅 |
| 3 |  | 略变浅 |
| 4 | NaCl | 变浅程度较大 |
 和
和 平衡体系的是
平衡体系的是a.1和2 b.1和3 c.1和4
②选择实验
 的盐效应弱于
的盐效应弱于 的盐效应。
的盐效应。(4)取等体积的溶液a继续进行实验,结果如下表。
| 序号 | 加入溶液 | 溶液颜色 |
| 5 | 1mL浓盐酸 | 明显变浅,溶液偏黄 |
| 6 | 1mL去离子水 | 略变浅 |
 和
和 平衡体系,结合实验现象及化学用语分析副反应对
平衡体系,结合实验现象及化学用语分析副反应对 和
和 平衡体系有影响的原因:
平衡体系有影响的原因:
您最近半年使用:0次
2023-04-20更新
|
117次组卷
|
4卷引用:江西省五校2022-2023学年高一下学期直升班联考化学试题
名校
7 . 下列叙述与图对应的是
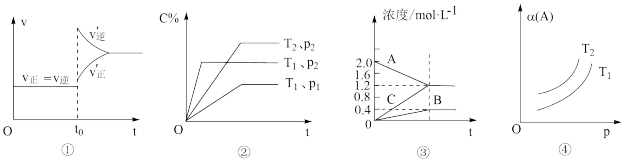

A.已达平衡状态的反应:N2(g)+3H2(g)  2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 |
B.由图②可知,P2>P1、T1>T2满足反应:2A(g)+B(g)  2C(g) ΔH<0 2C(g) ΔH<0 |
| C.图③表示的反应方程式为:2A(g)=B(g)+3C(g) |
D.由图④可知,对于反应aA(g) bB(g)+cC(g),该反应用于工业生产时,采用的压强越大越好 bB(g)+cC(g),该反应用于工业生产时,采用的压强越大越好 |
您最近半年使用:0次
2023-02-02更新
|
396次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高二上学期9月月考化学试题
名校
8 . 1776年,法国化学家LaVoisier首次确定硫元素。自然界天然的硫单质主要存在于火山区,发生反应如下(a、b均大于0):ⅰ.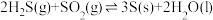
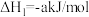 ;
;
ⅱ. 。回答下列问题:
。回答下列问题:
(1)根据上述信息, )
) 
_______ kJ/mol。推测a____ b或(填“>”“<”或“=”)。
(2)一定温度下,在恒容密闭容器中充入适量的 、
、 和
和 气体,仅发生上述反应。下列叙述正确的是_______(填字母)。
气体,仅发生上述反应。下列叙述正确的是_______(填字母)。
(3)一定温度下,向2L密闭容器中充入 和
和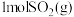 ,仅发生反应①,达到平衡后,测得
,仅发生反应①,达到平衡后,测得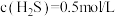 。温度保持不变,压缩容器至1L且保持体积不变,达到新平衡时
。温度保持不变,压缩容器至1L且保持体积不变,达到新平衡时
_______ mol/L。
(4)在恒容密闭容器中充入一定量 和
和 气体,测得
气体,测得 的平衡转化率与温度、投料比
的平衡转化率与温度、投料比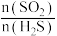 关系如图所示。
关系如图所示。
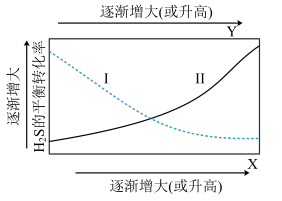
①代表 的平衡转化率随温度变化的曲线为
的平衡转化率随温度变化的曲线为_______ 。
②解释曲线Ⅱ变化趋势:_______ 。
(5)一定温度下,向密闭容器中充入 、
、 和
和 ,达到平衡时测得平衡体系中有
,达到平衡时测得平衡体系中有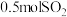 和
和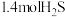 ,平衡时总压强为21kPa。该温度下,反应②的平衡常数
,平衡时总压强为21kPa。该温度下,反应②的平衡常数
_______ 。(不要求带单位,可用分数表示,提示:用分压计算的平衡常数为 ,分压等于总压×物质的量分数)。
,分压等于总压×物质的量分数)。
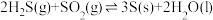
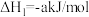 ;
;ⅱ.
 。回答下列问题:
。回答下列问题:(1)根据上述信息,
 )
) 
(2)一定温度下,在恒容密闭容器中充入适量的
 、
、 和
和 气体,仅发生上述反应。下列叙述正确的是_______(填字母)。
气体,仅发生上述反应。下列叙述正确的是_______(填字母)。| A.混合气体密度不再随时间变化时达到平衡状态 |
| B.增大硫单质的质量,逆反应速率会增大 |
C.达到平衡后,适当升温, 的平衡转化率减小 的平衡转化率减小 |
| D.平衡后充入少量惰性气体(不反应),平衡向左移动 |
 和
和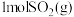 ,仅发生反应①,达到平衡后,测得
,仅发生反应①,达到平衡后,测得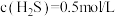 。温度保持不变,压缩容器至1L且保持体积不变,达到新平衡时
。温度保持不变,压缩容器至1L且保持体积不变,达到新平衡时
(4)在恒容密闭容器中充入一定量
 和
和 气体,测得
气体,测得 的平衡转化率与温度、投料比
的平衡转化率与温度、投料比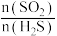 关系如图所示。
关系如图所示。
①代表
 的平衡转化率随温度变化的曲线为
的平衡转化率随温度变化的曲线为②解释曲线Ⅱ变化趋势:
(5)一定温度下,向密闭容器中充入
 、
、 和
和 ,达到平衡时测得平衡体系中有
,达到平衡时测得平衡体系中有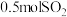 和
和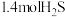 ,平衡时总压强为21kPa。该温度下,反应②的平衡常数
,平衡时总压强为21kPa。该温度下,反应②的平衡常数
 ,分压等于总压×物质的量分数)。
,分压等于总压×物质的量分数)。
您最近半年使用:0次
2022-12-15更新
|
356次组卷
|
3卷引用:江西省2022-2023学年高二上学期12月统一调研测试(联考)化学试题
名校
9 . 如图所示,三个烧瓶中分别充满NO2气体并分别装在盛有水的三个烧杯中,在①烧杯中加入CaO,在②烧杯中不加其他任何物质,在③烧杯中加入NH4Cl晶体,发现①中红棕色变深,③中红棕色变浅。已知:2NO2(红棕色) N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是
 N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是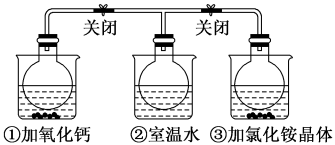
A.2NO2 N2O4是吸热反应 N2O4是吸热反应 |
| B.NH4Cl溶于水时吸收热量 |
| C.①烧瓶中平衡时混合气体的平均相对分子质量增大 |
| D.③烧瓶中气体的压强增大 |
您最近半年使用:0次
2022-08-28更新
|
1130次组卷
|
23卷引用:江西省上饶市2020-2021学年高二上学期期末教学质量测试化学试题
江西省上饶市2020-2021学年高二上学期期末教学质量测试化学试题江西省赣州市第一中学2020-2021学年高二下学期开学测试化学试题(已下线)2010年北京市八一中学高二第二学期期末考试化学试卷2018版化学(苏教版)高考总复习专题七课时跟踪训练--化学平衡的移动新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题【全国百强校】辽宁省鞍山市第一中学2018-2019学年高二下学期开学考试化学试题新疆自治区生产建设兵团第二中学2018-2019学年高二第一次月考化学试题陕西省延安市第一中学2019-2020学年高二上学期期中考试化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》云南省普洱市江城县第一中学2019—2020学年高二上学期期末考试化学试题四川省泸州市泸县第二中学2019-2020学年高二下学期第一次在线月考化学试题黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题(已下线)2.3.2+影响化学平衡状态的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题河南省信阳高级中学2020-2021学年高二下学期回顾测试化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷(已下线)2.2.2 浓度商、温度对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题广东省深圳市宝安区宝安中学2022-2023学年高一上学期期中考试化学试题新疆奇台县第一中学2022-2023学年高二上学期期中考试化学试题山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题(已下线)选择题11-15
名校
10 . 研究氮氧化物、碳氧化物的产生及利用有重要的化学意义。回答下列问题:
(1)汽车燃料中不含氮元素,汽车尾气中所含NO产生的原因是_______ 。
(2)将SrCO3放入密闭的真空容器中,发生反应SrCO3(s)⇌SrCO3(s)+CO2(g),反应达到平衡时c(CO2)为x mol/L,如反应温度不变,将反应体系的体积快速压缩为原来的一半,则c(CO2)的变化范围为_______ 。
(3)用CO2和H2在一定条件下可转化生成甲醇蒸气和水蒸气:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ∆H
已知部分化学键键能如表所示:
①∆H=_______ kJ∙mol-1;
②一定条件下,在相同体积的恒容密闭容器中充入1.0mol CO2和3.0mol H2,相同时间段内测得CO2的转化率随温度变化如图所示:
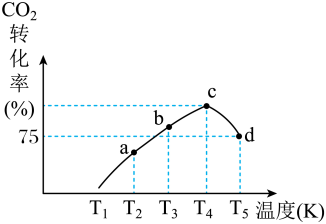
d点v正_______ v逆(填“>”“<”或“=”)。已知容器内的起始压强为160kPa,则图中d点对应温度下反应的平衡常数Kp=_______ kPa-2(KP为以分压表示的平衡常数,分压=总压×物质的量分数)
(1)汽车燃料中不含氮元素,汽车尾气中所含NO产生的原因是
(2)将SrCO3放入密闭的真空容器中,发生反应SrCO3(s)⇌SrCO3(s)+CO2(g),反应达到平衡时c(CO2)为x mol/L,如反应温度不变,将反应体系的体积快速压缩为原来的一半,则c(CO2)的变化范围为
(3)用CO2和H2在一定条件下可转化生成甲醇蒸气和水蒸气:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ∆H
已知部分化学键键能如表所示:
| 化学键 | H-H | C=O | C-O | H-O | C-H |
| E/(kJ·mol-1) | 436 | 745 | 351 | 463 | 413 |
②一定条件下,在相同体积的恒容密闭容器中充入1.0mol CO2和3.0mol H2,相同时间段内测得CO2的转化率随温度变化如图所示:

d点v正
您最近半年使用:0次



