1 . 利用含钴废料(主要成分为 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: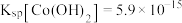 ;
;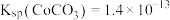 。
。
请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为 和
和___________ 。“酸浸”时 发生反应的总离子方程式为
发生反应的总离子方程式为___________ 。
(2)“萃取”时 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)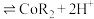 ,若萃取剂的量一定时,
,若萃取剂的量一定时,___________ (填“一次萃取”或“少量多次萃取”)的萃取效率更高。若“酸浸”后浸出液的 ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为___________ (结果保留一位小数,溶液体积变化忽略不计)。
(3)“沉锰”时, 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为___________ 。
(4)可以通过电解 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是___________ 。若Ⅱ室溶液中溶质的质量增加了 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为___________ 。
 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: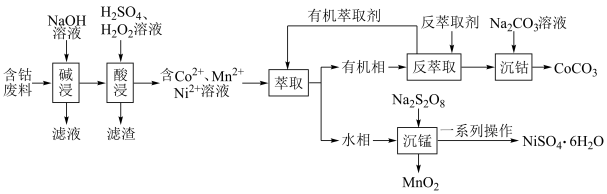
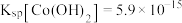 ;
;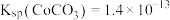 。
。请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为
 和
和 发生反应的总离子方程式为
发生反应的总离子方程式为(2)“萃取”时
 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)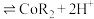 ,若萃取剂的量一定时,
,若萃取剂的量一定时, ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为(3)“沉锰”时,
 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为(4)可以通过电解
 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为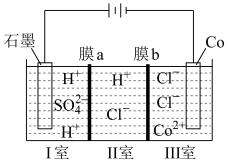
您最近一年使用:0次
名校
2 . 环己烯是工业常用的化工原料。工业上通过热铂基催化剂重整将环己烷脱氢制备环己烯,其热化学方程式为
 。
。
(1)几种共价键的键能数据如下:
则a=_______  。
。
(2)在恒温恒容密闭容器中充入环己烷气体,仅发生上述反应。下列叙述正确的是_______ (填字母)。
a.混合气体的密度不随时间变化时说明该反应达到平衡状态
b.平衡后再充入环己烷气体,平衡向右移动
c.加入高效催化剂,单位时间内环己烯的产率可能会增大
d.增大固体催化剂的质量,一定能提高正、逆反应速率
(3)环己烷的平衡转化率和环己烯的选择性(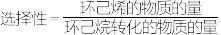 )随温度的变化如图所示:
)随温度的变化如图所示:
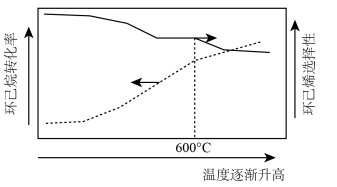
①随着温度升高,环己烷平衡转化率增大的原因是_______ 。
②当温度高于600℃时,可能的副产物有_______ (任写出其中一种结构简式)。
(4)在873K、100kPa条件下,向反应器中充入氩气和环己烷的混合气体,仅发生反应: 。
。
①环己烷的平衡转化率随 的增大而
的增大而_______ (填“升高”或“降低”或“不变”),其原因是_______ 。
②当 时,达到平衡所需时间为20min,环己烷的平衡转化率为
时,达到平衡所需时间为20min,环己烷的平衡转化率为 ,则平衡时环己烷的分压为
,则平衡时环己烷的分压为_______ kPa(保留2位小数),该环己烷脱氢反应的压强平衡常数
_______ kPa(保留2位小数)。[注:用分压计算的平衡常数为压强平衡常数( ),分压=总压×物质的量分数]
),分压=总压×物质的量分数]

 。
。(1)几种共价键的键能数据如下:
| 共价键 |  |  |  |  |
键能/ | 436 | 413 | 348 | a |
 。
。(2)在恒温恒容密闭容器中充入环己烷气体,仅发生上述反应。下列叙述正确的是
a.混合气体的密度不随时间变化时说明该反应达到平衡状态
b.平衡后再充入环己烷气体,平衡向右移动
c.加入高效催化剂,单位时间内环己烯的产率可能会增大
d.增大固体催化剂的质量,一定能提高正、逆反应速率
(3)环己烷的平衡转化率和环己烯的选择性(
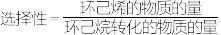 )随温度的变化如图所示:
)随温度的变化如图所示:
①随着温度升高,环己烷平衡转化率增大的原因是
②当温度高于600℃时,可能的副产物有
(4)在873K、100kPa条件下,向反应器中充入氩气和环己烷的混合气体,仅发生反应:
 。
。①环己烷的平衡转化率随
 的增大而
的增大而②当
 时,达到平衡所需时间为20min,环己烷的平衡转化率为
时,达到平衡所需时间为20min,环己烷的平衡转化率为 ,则平衡时环己烷的分压为
,则平衡时环己烷的分压为
 ),分压=总压×物质的量分数]
),分压=总压×物质的量分数]
您最近一年使用:0次
真题
名校
3 . 在恒温恒容密闭容器中充入一定量 ,发生如下反应:
,发生如下反应: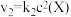 和
和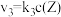 ,其中
,其中 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。
下列说法正确的是
 ,发生如下反应:
,发生如下反应: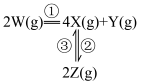
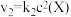 和
和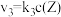 ,其中
,其中 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。 | 0 | 1 | 2 | 3 | 4 | 5 |
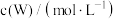 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 |
A. 内,X的平均反应速率为 内,X的平均反应速率为 |
| B.若增大容器容积,平衡时Y的产率增大 |
C.若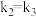 ,平衡时 ,平衡时 |
D.若升高温度,平衡时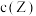 减小 减小 |
您最近一年使用:0次
2023-11-29更新
|
2946次组卷
|
4卷引用:陕西省西安中学2023-2024学年高三(实验版)上学期12月练考理科综合试题
名校
4 . 为减少大气污染,科学家采取多种措施处理工业废气中排放的氮氧化物(NOx)、SO2等。回答下列问题:
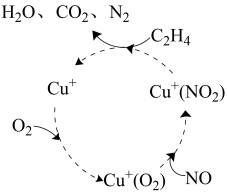
(1)某脱硝反应机理如图所示,Cu+的作用为____ ,C2H4参与的反应方程式为____ 。
(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
①若有3molNO参与反应,则被NO氧化的NH3的物质的量为____ 。
②催化还原时应控制反应温度在315~400℃之间,反应温度不宜过高的原因是____ 。
③350℃时NO的百分含量与氨氮比的关系如图所示,若只改变氨气的投放量,当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是____ (用化学方程式表示)。

(3)烟气脱硫、脱硝一体化技术是大气污染防治研究的热点,ClO2在酸性条件下稳定,是性能优良的脱硫脱硝试剂。
①ClO 也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为
也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为____ 。
②某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。
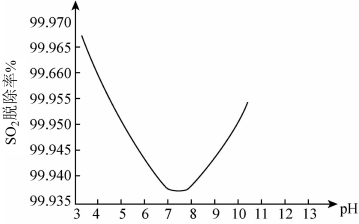
当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是:____ ;在pH约7.8之后,随pH的增大,SO2脱除率又开始升高,其原因是____ 。
(1)某脱硝反应机理如图所示,Cu+的作用为

(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
4N2(g)+6H2O(g) △H=-1627kJ·mol-1。①若有3molNO参与反应,则被NO氧化的NH3的物质的量为
②催化还原时应控制反应温度在315~400℃之间,反应温度不宜过高的原因是
③350℃时NO的百分含量与氨氮比的关系如图所示,若只改变氨气的投放量,当
 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是
(3)烟气脱硫、脱硝一体化技术是大气污染防治研究的热点,ClO2在酸性条件下稳定,是性能优良的脱硫脱硝试剂。
①ClO
 也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为
也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为②某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。

当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是:
您最近一年使用:0次
2022-08-29更新
|
240次组卷
|
4卷引用:陕西省咸阳高新一中2023届高三上学期第一次质量检测化学试题
名校
5 . 如图所示,三个烧瓶中分别充满NO2气体并分别装在盛有水的三个烧杯中,在①烧杯中加入CaO,在②烧杯中不加其他任何物质,在③烧杯中加入NH4Cl晶体,发现①中红棕色变深,③中红棕色变浅。已知:2NO2(红棕色) N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是
 N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是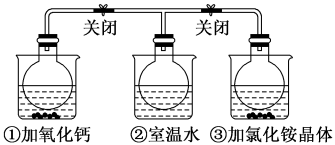
A.2NO2 N2O4是吸热反应 N2O4是吸热反应 |
| B.NH4Cl溶于水时吸收热量 |
| C.①烧瓶中平衡时混合气体的平均相对分子质量增大 |
| D.③烧瓶中气体的压强增大 |
您最近一年使用:0次
2022-08-28更新
|
1132次组卷
|
23卷引用:陕西省延安市第一中学2019-2020学年高二上学期期中考试化学试题
陕西省延安市第一中学2019-2020学年高二上学期期中考试化学试题(已下线)2010年北京市八一中学高二第二学期期末考试化学试卷2018版化学(苏教版)高考总复习专题七课时跟踪训练--化学平衡的移动新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题【全国百强校】辽宁省鞍山市第一中学2018-2019学年高二下学期开学考试化学试题新疆自治区生产建设兵团第二中学2018-2019学年高二第一次月考化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》云南省普洱市江城县第一中学2019—2020学年高二上学期期末考试化学试题四川省泸州市泸县第二中学2019-2020学年高二下学期第一次在线月考化学试题黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题(已下线)2.3.2+影响化学平衡状态的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题江西省上饶市2020-2021学年高二上学期期末教学质量测试化学试题江西省赣州市第一中学2020-2021学年高二下学期开学测试化学试题河南省信阳高级中学2020-2021学年高二下学期回顾测试化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷(已下线)2.2.2 浓度商、温度对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题广东省深圳市宝安区宝安中学2022-2023学年高一上学期期中考试化学试题新疆奇台县第一中学2022-2023学年高二上学期期中考试化学试题山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题(已下线)选择题11-15
名校
6 . 工业上采用高浓度含砷废水制取 ,工艺流程如下:
,工艺流程如下:

已知含砷废水中砷元素以+3价的形式存在。不同pH时,三价砷的物种分布如下图所示:

(1) 第一步电离方程式
第一步电离方程式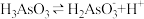 的电离常数为
的电离常数为 ,则
,则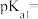
___________ (已知 )
)
(2)“调pH”时,控制溶液的pH=6,“沉砷”时会生成 沉淀。写出“沉砷”时反应的离子方程式:
沉淀。写出“沉砷”时反应的离子方程式:___________
(3)“沉砷”时会发生副反应: ,从而降低砷元素的沉淀率。为减少副反应的发生,采取的方法是加入
,从而降低砷元素的沉淀率。为减少副反应的发生,采取的方法是加入 的同时加入少量
的同时加入少量 ,生成的
,生成的 沉淀中会混有FeS。加入少量
沉淀中会混有FeS。加入少量 能抑制副反应的原因是(用平衡移动原理解释)
能抑制副反应的原因是(用平衡移动原理解释)___________
(4)“焙烧”含少量FeS的 可以得到
可以得到 和
和 的混合物。
的混合物。 是一种酸性氧化物,选择合适的溶液X,将砷元素转化为
是一种酸性氧化物,选择合适的溶液X,将砷元素转化为 从混合物中浸出。写出“浸出”反应的离子方程式:
从混合物中浸出。写出“浸出”反应的离子方程式:___
(5)保持溶液X的浓度不变,为了提高焙烧后固体中砷元素的浸出速率,可以采取的方法有(填两条):
①________
②________
 ,工艺流程如下:
,工艺流程如下:
已知含砷废水中砷元素以+3价的形式存在。不同pH时,三价砷的物种分布如下图所示:

(1)
 第一步电离方程式
第一步电离方程式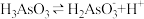 的电离常数为
的电离常数为 ,则
,则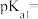
 )
)(2)“调pH”时,控制溶液的pH=6,“沉砷”时会生成
 沉淀。写出“沉砷”时反应的离子方程式:
沉淀。写出“沉砷”时反应的离子方程式:(3)“沉砷”时会发生副反应:
 ,从而降低砷元素的沉淀率。为减少副反应的发生,采取的方法是加入
,从而降低砷元素的沉淀率。为减少副反应的发生,采取的方法是加入 的同时加入少量
的同时加入少量 ,生成的
,生成的 沉淀中会混有FeS。加入少量
沉淀中会混有FeS。加入少量 能抑制副反应的原因是(用平衡移动原理解释)
能抑制副反应的原因是(用平衡移动原理解释)(4)“焙烧”含少量FeS的
 可以得到
可以得到 和
和 的混合物。
的混合物。 是一种酸性氧化物,选择合适的溶液X,将砷元素转化为
是一种酸性氧化物,选择合适的溶液X,将砷元素转化为 从混合物中浸出。写出“浸出”反应的离子方程式:
从混合物中浸出。写出“浸出”反应的离子方程式:(5)保持溶液X的浓度不变,为了提高焙烧后固体中砷元素的浸出速率,可以采取的方法有(填两条):
①
②
您最近一年使用:0次
2021-11-15更新
|
300次组卷
|
2卷引用:陕西省西安市西北工业大学附属中学2022-2023学年高三上学期期末考试化学试题
名校
解题方法
7 . 已知反应S2O (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )

①2Fe3+(aq)+2I-(aq) I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)
②2Fe2+(aq)+S2O (aq)
(aq) 2Fe3+(aq)+2SO
2Fe3+(aq)+2SO (aq)
(aq)
 (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
①2Fe3+(aq)+2I-(aq)
 I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)②2Fe2+(aq)+S2O
 (aq)
(aq) 2Fe3+(aq)+2SO
2Fe3+(aq)+2SO (aq)
(aq)| A.Fe3+是该反应的催化剂,加入Fe3+后降低了该反应的活化能 |
| B.反应①比反应②所需活化能大 |
| C.向该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深 |
| D.该反应可设计成原电池 |
您最近一年使用:0次
2020-09-25更新
|
1721次组卷
|
14卷引用:陕西省西安市长安区第一中学2021届高三上学期第三次月考化学试题
陕西省西安市长安区第一中学2021届高三上学期第三次月考化学试题山西省大同市2021届高三上学期学情调研测试化学试题辽宁省六校协作体2021届高三第一次联考化学试题江西省赣州市会昌县七校2021届高三联合9月月考化学试题辽宁省开原市中固镇第二中学2021届高三上学期9月月考化学试题内蒙古自治区赤峰二中2020-2021学年高二上学期第一次月考化学试题江西省红色七校(分宜中学、会昌中学、莲花中学、南城一中、任弼时中学、瑞金一中、遂川中学)2021届高三上学期第一次联考化学试题江西省吉安县立中学2020-2021学年高二上学期12月月考化学(B班)试题江苏省苏州市姑苏区苏州中学2020-2021学年高二下学期期中考试化学试题江西省景德镇一中2020-2021学年高一下学期期中考试化学(1班)试题吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题黑龙江省双鸭山市第一中学2021-2022学年高二上学期第一次月考化学试题吉林省汪清县第六中学2021-2022学年高二12月月考化学试题吉林省乾安县第七中学2021-2022学年高二上学期第一次质量检测化学试题
名校
8 . 已知反应: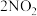 (红棕色)
(红棕色)
 (无色),分别进行如下两个实验:
(无色),分别进行如下两个实验:
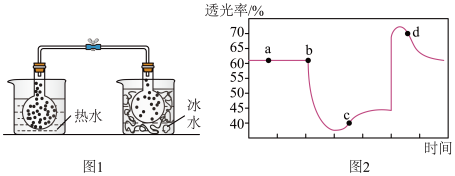
实验ⅰ:将 球分别浸泡在热水和冰水中,现象如图1。
球分别浸泡在热水和冰水中,现象如图1。
实验ⅱ:将一定量的 充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(
充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(气体颜色越深,透光率越小 ),如图2。下列说法不正确 的是( )
 (红棕色)
(红棕色)
 (无色),分别进行如下两个实验:
(无色),分别进行如下两个实验:实验ⅰ:将
 球分别浸泡在热水和冰水中,现象如图1。
球分别浸泡在热水和冰水中,现象如图1。实验ⅱ:将一定量的
 充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(
充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(
| A.图1现象说明该反应为放热反应 |
| B.图2中b点的操作是压缩注射器 |
C.d点: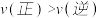 |
| D.若不忽略体系温度变化,且没有能量损失,则T(b)<T(c) |
您最近一年使用:0次
2020-09-06更新
|
166次组卷
|
2卷引用:陕西省安康市安康中学2023-2024学年高二上学期10月月考化学试题
名校
9 . 硫酰氯(SO2Cl2)可用于有机合成和药物制造等。实验室利用SO2和Cl2在活性炭作用下制取SO2Cl2[SO2(g)+Cl2(g) SO2Cl2(l) ΔH=-97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,有强腐蚀性,不宜接触碱、醇、纤维素等许多无机物和有机物,遇水能发生剧烈反应并产生白雾。回答下列问题:
SO2Cl2(l) ΔH=-97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,有强腐蚀性,不宜接触碱、醇、纤维素等许多无机物和有机物,遇水能发生剧烈反应并产生白雾。回答下列问题:
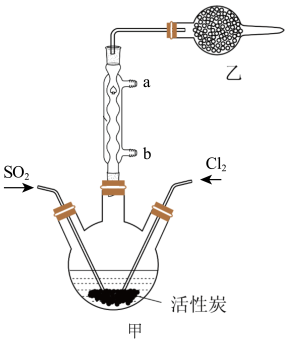
I.SO2Cl2的制备
(1)水应从___ (选填“a”或“b”)口进入。
(2)制取SO2的最佳组合是___ (填标号)。
①Fe+18.4mol/LH2SO4
②Na2SO3+70%H2SO4
③Na2SO3+3mo/LHNO3
(3)乙装置中盛放的试剂是___ 。
(4)制备过程中需要将装置甲置于冰水浴中,原因是___ 。
(5)反应结束后,分离甲中混合物的最佳实验操作是___ 。
II.测定产品中SO2Cl2的含量,实验步骤如下:
①取1.5g产品加入足量Ba(OH)2溶液,充分振荡、过滤、洗涤,将所得溶液均放入锥形瓶中;
②向锥形瓶中加入硝酸酸化,再加入0.2000mol·L-1的AgNO3溶液l00.00mL;
③向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
④加入NH4Fe(SO4)2指示剂,用0.1000mol·L-1NH4SCN溶液滴定过量Ag+,终点所用体积为10.00mL。
已知:Ksp(AgCl)=3.2×10-10 Ksp(AgSCN)=2×10-12
(6)滴定终点的现象为___ 。
(7)产品中SO2Cl2的质量分数为___ %,若步骤③不加入硝基苯则所测SO2Cl2含量将___ (填“偏高”、“偏低”或“无影响”)。
 SO2Cl2(l) ΔH=-97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,有强腐蚀性,不宜接触碱、醇、纤维素等许多无机物和有机物,遇水能发生剧烈反应并产生白雾。回答下列问题:
SO2Cl2(l) ΔH=-97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,有强腐蚀性,不宜接触碱、醇、纤维素等许多无机物和有机物,遇水能发生剧烈反应并产生白雾。回答下列问题:
I.SO2Cl2的制备
(1)水应从
(2)制取SO2的最佳组合是
①Fe+18.4mol/LH2SO4
②Na2SO3+70%H2SO4
③Na2SO3+3mo/LHNO3
(3)乙装置中盛放的试剂是
(4)制备过程中需要将装置甲置于冰水浴中,原因是
(5)反应结束后,分离甲中混合物的最佳实验操作是
II.测定产品中SO2Cl2的含量,实验步骤如下:
①取1.5g产品加入足量Ba(OH)2溶液,充分振荡、过滤、洗涤,将所得溶液均放入锥形瓶中;
②向锥形瓶中加入硝酸酸化,再加入0.2000mol·L-1的AgNO3溶液l00.00mL;
③向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
④加入NH4Fe(SO4)2指示剂,用0.1000mol·L-1NH4SCN溶液滴定过量Ag+,终点所用体积为10.00mL。
已知:Ksp(AgCl)=3.2×10-10 Ksp(AgSCN)=2×10-12
(6)滴定终点的现象为
(7)产品中SO2Cl2的质量分数为
您最近一年使用:0次
2019-12-10更新
|
482次组卷
|
3卷引用:陕西省西安市长安区第一中学2020-2021学年高三第七次质量检测理综化学试题
10 . 还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下: Cr2O72-(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有
Cr2O72-(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有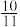 转化为Cr2O72-,下列说法不正确的是( )
转化为Cr2O72-,下列说法不正确的是( )
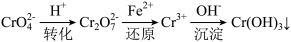
 Cr2O72-(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有
Cr2O72-(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6g/L,CrO42-有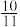 转化为Cr2O72-,下列说法不正确的是( )
转化为Cr2O72-,下列说法不正确的是( )| A.溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B.若用FeSO4作还原剂,处理1L废水,至少需要1.65mol |
| C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5 |
| D.常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
您最近一年使用:0次



