1 . 下列实验操作及现象、对应结论不正确的是
选项 | 实验操作及现象 | 结论 |
A | 向重铬酸钾溶液中加水,溶液颜色变浅 | 增加水的用量,平衡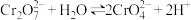 向右移动 向右移动 |
B | 向含酚酞的 溶液中加入 溶液中加入 固体,溶液红色变浅 固体,溶液红色变浅 |  溶液中存在水解平衡 溶液中存在水解平衡 |
C | 向硫酸铜溶液中滴加浓氨水至过量,溶液先产生蓝色沉淀,然后沉淀溶解变为深蓝色溶液 |  转化为 转化为 |
D |  时,向 时,向 溶液中滴加甲基橙溶液,溶液变红 溶液中滴加甲基橙溶液,溶液变红 | 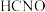 的电离平衡常数大于 的电离平衡常数大于 的电离平衡常数 的电离平衡常数 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 在体积为1 L的恒温密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应: CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ,测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
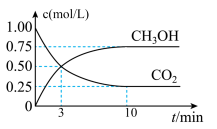
| A.该化学反应在3 min时达到平衡状态 |
| B.保持其他条件不变,降低温度,平衡时c(CH3OH)=0.85 mol·L-1,则该反应的ΔH >0 |
| C.相同温度下,起始时向上述容器中充入0.5 mol CO2、1.5 mol H2,平衡时CO2的转化率为75% |
| D.12 min时,向上述容器中再充入0.25 mol CO2、0.25 mol H2O(g),此时反应将向正反应方向进行 |
您最近一年使用:0次
2023-12-23更新
|
122次组卷
|
3卷引用:河北省衡水市安平中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
3 . 在某密闭容器中投入碳粉和一定量的 ,发生反应:
,发生反应: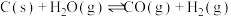
 ,下列措施能增大化学反应速率的是
,下列措施能增大化学反应速率的是
 ,发生反应:
,发生反应: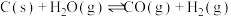
 ,下列措施能增大化学反应速率的是
,下列措施能增大化学反应速率的是A.增加 的质量 的质量 | B.升高温度 |
C.移除部分 | D.扩大容器体积 |
您最近一年使用:0次
2023-03-16更新
|
118次组卷
|
2卷引用:河北省2022-2023学年高二下学期开学考试化学试题
解题方法
4 . 制造航天飞船的主要材料是铝,工业上制铝时用冰晶石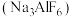 做助熔剂,已知
做助熔剂,已知 微溶于水。某工厂采用含氟矿石(主要成分为
微溶于水。某工厂采用含氟矿石(主要成分为 、
、 )和含铝废渣(主要成分为
)和含铝废渣(主要成分为 、
、 ,含有
,含有 、
、 杂质)联合制备冰晶石的流程如下:
杂质)联合制备冰晶石的流程如下:

回答下列问题:
(1)基态 原子的价层电子排布式是
原子的价层电子排布式是_______ ,基态 原子核外有
原子核外有_______ 个未成对电子。
(2)“酸浸1”得到 和
和 的化学方程式为
的化学方程式为_______ 。
(3)“氧化”时反应的离子方程式为_______ ; 也可用
也可用 代替,
代替, 的电子式为
的电子式为_______ 。
(4)“萃取”过程可表示为 (水层)
(水层) (有机层)
(有机层) (有机层)
(有机层) (水层)。在实验室中模拟由“有机层”获取
(水层)。在实验室中模拟由“有机层”获取 溶液的具体操作是
溶液的具体操作是_______ 。
(5)“合成”时反应的化学方程式为_______ [另一生成物为 ]。
]。
(6)“系列操作”包含过滤、_______ 、_______ 。
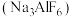 做助熔剂,已知
做助熔剂,已知 微溶于水。某工厂采用含氟矿石(主要成分为
微溶于水。某工厂采用含氟矿石(主要成分为 、
、 )和含铝废渣(主要成分为
)和含铝废渣(主要成分为 、
、 ,含有
,含有 、
、 杂质)联合制备冰晶石的流程如下:
杂质)联合制备冰晶石的流程如下:
回答下列问题:
(1)基态
 原子的价层电子排布式是
原子的价层电子排布式是 原子核外有
原子核外有(2)“酸浸1”得到
 和
和 的化学方程式为
的化学方程式为(3)“氧化”时反应的离子方程式为
 也可用
也可用 代替,
代替, 的电子式为
的电子式为(4)“萃取”过程可表示为
 (水层)
(水层) (有机层)
(有机层) (有机层)
(有机层) (水层)。在实验室中模拟由“有机层”获取
(水层)。在实验室中模拟由“有机层”获取 溶液的具体操作是
溶液的具体操作是(5)“合成”时反应的化学方程式为
 ]。
]。(6)“系列操作”包含过滤、
您最近一年使用:0次
名校
5 .  的配位化合物较稳定且运用广泛。
的配位化合物较稳定且运用广泛。 可与
可与 、
、 、
、 、
、 等配体形成使溶液呈浅紫色的
等配体形成使溶液呈浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验:
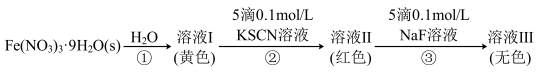
已知: 与
与 、
、 的反应在溶液中存在以下平衡:
的反应在溶液中存在以下平衡:




下列说法不正确 的是
 的配位化合物较稳定且运用广泛。
的配位化合物较稳定且运用广泛。 可与
可与 、
、 、
、 、
、 等配体形成使溶液呈浅紫色的
等配体形成使溶液呈浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验:
已知:
 与
与 、
、 的反应在溶液中存在以下平衡:
的反应在溶液中存在以下平衡:



下列说法
A.I中溶液呈黄色可能是由于 水解产物的颜色引起的 水解产物的颜色引起的 |
B.向溶液II中加入NaF后,溶液颜色变为无色,说明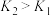 |
C.为了能观察到溶液I中 的颜色,可向该溶液中加入稀盐酸 的颜色,可向该溶液中加入稀盐酸 |
| D.向溶液III中加入足量的KSCN固体,溶液可能再次变为红色 |
您最近一年使用:0次
2023-01-09更新
|
801次组卷
|
8卷引用:河北省石家庄市第二中学2022-2023学年高三下学期开学考试化学试题
名校
解题方法
6 . 下列事实能用勒夏特列原理来解释的是
A.SO2被氧化为SO3,往往需要使用催化剂:2SO2(g)+O2(g)  2SO3(g) 2SO3(g) |
B.500 ℃温度比室温更有利于合成氨反应:N2(g)+3H2(g)  2NH3(g)△H<0 2NH3(g)△H<0 |
C.H2、I2、HI平衡混合气体加压后颜色加深:H2(g)+I2(g)  2HI(g) 2HI(g) |
D.实验室采用排饱和食盐水的方法收集氯气:Cl2+H2O  H++Cl-+HClO H++Cl-+HClO |
您最近一年使用:0次
2022-10-06更新
|
842次组卷
|
40卷引用:河北省张家口市宣化一中2020-2021学年高二下学期期初考试化学试题
河北省张家口市宣化一中2020-2021学年高二下学期期初考试化学试题河北省邯郸市大名县第一中学2022-2023学年高二上学期第一次月考化学试题河北省石家庄市第十八中学2022-2023学年高二上学期10月月考化学试题2015-2016学年湖北省黄冈市高二上学期期末考试化学试卷2015-2016学年内蒙古包头九中高一下期末化学试题【校级联考】福建省晋江市(安溪一中、养正中学、惠安一中、泉州实验中学四校)2018-2019学年高二上学期期中考试化学试题江西省赣州市南康中学2019-2020学年高二上学期第一次月考化学试题山东省师范大学附属中学2019-2020学年高二上学期第五次学分认定考试化学试题山东省实验中学2019-2020学年高二上学期期中考试化学试题(已下线)考点12 化学反应速率化学平衡——《备战2020年高考精选考点专项突破题集》山西省怀仁市重点中学2019-2020学年高二上学期期末考试化学试题吉林省白城市洮南市第一中学2020-2021学年高二上学期第一次月考化学试题江西省南昌市第十中学2020-2021学年高二上学期第一次月考化学试题(已下线)【南昌新东方】7. 南昌十中 徐钢 刘惠文.(已下线)第七章 能力提升检测卷-2021年高考化学一轮复习讲练测山东省临沂市第四中学2020-2021学年高二11月份阶段检测化学试题新疆生产建设兵团第四师第一中学2020-2021学年高二上学期期中考试化学试题四川省成都新津为明学校2020-2021学年高二上学期期中测试化学试题陕西省咸阳市实验中学2020-2021学年高二上学期第二次月考化学试题湖南省湘潭市第一中学2020-2021学年高二下学期期中考试(水平测试)化学试卷天津市滨海新区大港油田第三中学2020-2021学年高二上学期期中考试化学试题重庆市第七中学2020-2021学年高二上学期第一次月考化学试题湖南省长沙宁乡市第十高级中学2020-2021学年高二上学期10月月考化学试题(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题七 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题23 化学平衡的移动和化学反应进行的方向(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练重庆市育才中学校2021-2022学年高二上学期第一次月考化学试题四川省广安市武胜烈面中学校2021-2022学年高二10月月考化学试题新疆伊犁市奎屯市第一高级中学2019-2020学年高二上学期期中考试化学试题湖北省石首市第一中学2021-2022学年高二上学期10月月考化学试题(已下线)卷11 化学反应速率和平衡选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)第21讲 化学平衡状态 化学平衡的移动(讲)-2023年高考化学一轮复习讲练测(全国通用)天津市咸水沽第二中学2021-2022学年高二上学期期中化学试题甘肃省张掖市高台县第一中学2022-2023学年高三上学期期中检测化学试题广东省佛山市顺德区第一中学2022-2023学年高二上学期期中考试化学试题广东省佛山市三水中学2022-2023学年高二上学期11月第二次统测化学试题(已下线)第2讲 化学平衡状态及化学平衡的移动广东省肇庆市封开县广信中学、四会中学2023-2024学年高二上学期第一次联考化学试题天津市实验中学滨海学校2022-2023学年高二上学期期中质量调查化学试题广东省湛江市第二十一中学2023-2024学年高二上学期期中考试化学试题
名校
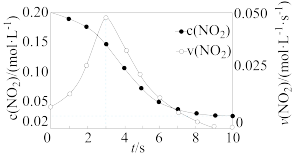
7 . 容积均为1L的甲、乙两个刚性容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入 ,发生反应
,发生反应 。甲容器中
。甲容器中 的相关量随时间变化关系如下图所示。下列说法正确的是
的相关量随时间变化关系如下图所示。下列说法正确的是
 ,发生反应
,发生反应 。甲容器中
。甲容器中 的相关量随时间变化关系如下图所示。下列说法正确的是
的相关量随时间变化关系如下图所示。下列说法正确的是
| A.3s时甲容器中反应达到化学平衡状态 |
B.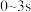 内,甲容器中 内,甲容器中 反应速率增大说明该反应的速率与 反应速率增大说明该反应的速率与 浓度无关 浓度无关 |
C.3s时乙容器中c( )小于0.20mol/L,乙容器中该反应的化学平衡常数大于225 )小于0.20mol/L,乙容器中该反应的化学平衡常数大于225 |
D.甲、乙两容器均达平衡后,欲使两者 的体积分数相等,可向乙容器中再充入少量 的体积分数相等,可向乙容器中再充入少量 气体 气体 |
您最近一年使用:0次
2022-07-28更新
|
613次组卷
|
3卷引用:河北省滦南县第四中学2023届高三上学期开学考试化学试题
河北省滦南县第四中学2023届高三上学期开学考试化学试题江苏省南京市第十三中学2022届高三下学期适应性考试化学试题(已下线)第七章 化学反应速率和化学平衡(测)-2023年高考化学一轮复习讲练测(全国通用)
8 . K2Cr2O7溶液中存在平衡:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+。现在用K2Cr2O7溶液进行下列实验:
(黄色)+2H+。现在用K2Cr2O7溶液进行下列实验:

已知:C2H5OH遇到强氧化剂可被氧化。结合实验,下列说法不正确的是
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+。现在用K2Cr2O7溶液进行下列实验:
(黄色)+2H+。现在用K2Cr2O7溶液进行下列实验:
已知:C2H5OH遇到强氧化剂可被氧化。结合实验,下列说法不正确的是
| A.①中溶液橙色加深,③中溶液变黄 |
B.②中Cr2O 被C2H5OH还原 被C2H5OH还原 |
| C.对比②和④可知K2Cr2O7酸性溶液氧化性弱 |
| D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色 |
您最近一年使用:0次
9 . 下列实验方案能够达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究生成物浓度改变FeCl3+3KSCN Fe(SCN)3+3KCl化学平衡的影响 Fe(SCN)3+3KCl化学平衡的影响 | 在平衡体系中加入KCl晶体,观察并比较实验现象 |
| B | 探究草酸浓度对反应速率的影响 | 向两支试管中分别加入2mL0.01mol/L的酸性KMnO4溶液,再同时分别向两支试管加入2mL0.1mol/L的H2C2O4溶液和2mL0.05mol/L的H2C2O4溶液,观察KMnO4溶液褪色所需时间 |
| C | 比较H2CO3和HClO酸性强弱 | 相同温度下,用pH试纸测定等浓度的NaHCO3和NaClO溶液的pH |
| D | 比较AgCl和AgI的Ksp大小 | 向盛有1mL0.1mol·L-1AgNO3溶液的试管中滴加2滴0.1mol·L-1NaCl溶液,有白色沉淀生成,向其中继续滴加几滴0.1mol/LKI溶液,有黄色沉淀产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 如图是关于反应A2(g)+3B2(g)⇌2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是


| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |
您最近一年使用:0次
2021-09-02更新
|
868次组卷
|
52卷引用:河北省定州中学2017-2018学年高二上学期开学考试化学试题
河北省定州中学2017-2018学年高二上学期开学考试化学试题(已下线)2014秋河北省唐山一中高二上学期期中化学试卷2015-2016学年河北省成安一中高二上学期10月月考化学试卷安徽省六安市第一中学2017-2018学年高二上学期开学考试化学试题河南省林州市第一中学分校(林虑中学)2017-2018学年高二上学期开学检测化学试题河北省深州中学2016-2017学年高二下学期期末考试化学试题河北省故城县高级中学2018届高三12月月考化学试题(已下线)2010—2011学年海南省洋浦中学高二上学期期末考试化学试卷(已下线)2011-2012年吉林省长春外国语学校高二上学期第一次月考化学试卷(已下线)2011-2012学年云南省蒙自县文澜高级中学高二上学期期中考试化学试卷(已下线)2011-2012学年贵州省凯里一中高二上学期期中考试化学试卷(已下线)2011-2012学年云南蒙自高中高二上学期期中考试化学试卷(已下线)2012-2013学年安徽省舒城晓天中学高二上学期第一次月考化学试卷(已下线)2012-2013学年浙江省宁海县正学中学高二下学期第一次阶段性测试化学试卷(已下线)2012-2013学年山东省临沭一中高二10月学情调查化学试卷(已下线)2014年高二化学人教版选修四 8化学平衡移动练习卷(已下线)2013-2014四川省雅安中学下学期期中考试高二化学试卷(已下线)2011-2012贵州省凯里一中第一学期期末考试高二化学试卷(已下线)2014-2015学年云南省玉溪市第一中学高二上学期期中考试化学试卷(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷(已下线)2014-2015学年湖北省部分重点中学高二上学期期中考试化学试卷(已下线)2014-2015学年辽宁师范大学附中高二10月模考化学试卷2015届吉林省东北师大附中高三上学期第三次摸底化学试卷2014-2015学年山东省微山一中高二下学期期末考试化学试卷2015-2016学年江苏省海安实验中学高二上学期期中选修化学试卷2015-2016学年四川省成都市六校高二上学期期中联考化学试卷2015-2016学年山东省泰安市高二上学期期末考试化学试卷2016-2017学年贵州省安顺平坝第一高级中学高二上期中化学卷2016-2017学年浙江省余姚中学高二上期中化学试卷云南省姚安县第一中学2017-2018学年高二10月月考化学试题甘肃省武威市第十八中2018-2019学年高二上学期第一次月考化学试题【区级联考】山东省济南市莱芜区2019届高三第一学期期末质量检测化学试题步步为赢 高二化学寒假作业:作业五 化学平衡的图像分析2020届人教版高三专题基础复习专题7《化学反应速率与化学平衡》测试卷黑龙江桦南二中2019-2020学年高二上学期期中考试化学试题天津市和平区2018-2019高二期末考试化学试题黑龙江省海林市朝鲜族中学2020-2021学年高二上学期第一次月考化学试题江苏省宿迁市沭阳县潼阳中学2020-2021学年高二下学期第一次月考化学试题山西省运城市稷山中学2022届高三上学期月考(一)化学试题(已下线)第19讲 化学平衡 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省长沙市周南中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)考向22 化学平衡状态 化学平衡的移动-备战2022年高考化学一轮复习考点微专题(已下线)章末培优2 专题2 化学反应速率与化学平衡-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)湖南省怀化市第五中学2021-2022学年高二上学期期中考试化学试题云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题(已下线)第6章 化学反应速率和化学平衡复习-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)上海市嘉定区第一中学2021-2022学年高一下学期期期末考试化学试题(已下线)第19讲 化学平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)甘肃省武威市凉州区2020-2021学年高二上学期期末考试化学试题浙江省嘉兴市海盐第二高级中学2021-2022学年高二上学期(10月)阶段检测化学试题新疆乌鲁木齐八一中学2023-2024学年高二上学期11月期中化学试题



