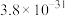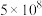1 . 某兴趣小组以重铬酸钾( )溶液为研究对象,改变条件使其发生“色彩变幻”。
)溶液为研究对象,改变条件使其发生“色彩变幻”。
已知:① 溶液存在平衡:
溶液存在平衡: 。
。
②含铬元素的离子在溶液中的颜色: (橙色);
(橙色); (黄色);Cr3+(绿色)。
(黄色);Cr3+(绿色)。 的正反应是
的正反应是_____ (填“吸热”或“放热”)反应。
(2)ⅱ是验证“只降低生成物的浓度,该平衡正向移动”,试剂a是_____ (填化学式)。
(3)ⅲ的目的是要验证“增大生成物的浓度,该平衡逆向移动”,此实验不能达到预期目的,理由是______ 。
(4)根据实验Ⅱ中不同现象,可以得出的结论是______ 。
(5)继续实验Ⅲ:______ 。
②第二步溶液变绿色:该反应的离子方程式是_______ 。
 )溶液为研究对象,改变条件使其发生“色彩变幻”。
)溶液为研究对象,改变条件使其发生“色彩变幻”。已知:①
 溶液存在平衡:
溶液存在平衡: 。
。②含铬元素的离子在溶液中的颜色:
 (橙色);
(橙色); (黄色);Cr3+(绿色)。
(黄色);Cr3+(绿色)。
 的正反应是
的正反应是(2)ⅱ是验证“只降低生成物的浓度,该平衡正向移动”,试剂a是
(3)ⅲ的目的是要验证“增大生成物的浓度,该平衡逆向移动”,此实验不能达到预期目的,理由是
(4)根据实验Ⅱ中不同现象,可以得出的结论是
(5)继续实验Ⅲ:
实验Ⅲ: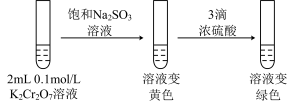
②第二步溶液变绿色:该反应的离子方程式是
您最近半年使用:0次
2 .  溶液中存在平衡:
溶液中存在平衡: ,加入下列物质能够使溶液橙色明显加深的是
,加入下列物质能够使溶液橙色明显加深的是
 溶液中存在平衡:
溶液中存在平衡: ,加入下列物质能够使溶液橙色明显加深的是
,加入下列物质能够使溶液橙色明显加深的是| A.3~5滴浓硫酸 | B.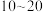 滴浓 滴浓 溶液 溶液 |
| C.1mLC2H5OH | D.1mLH2O |
您最近半年使用:0次
3 . 下列实验操作及现象、对应结论不正确的是
选项 | 实验操作及现象 | 结论 |
A | 向重铬酸钾溶液中加水,溶液颜色变浅 | 增加水的用量,平衡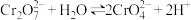 向右移动 向右移动 |
B | 向含酚酞的 溶液中加入 溶液中加入 固体,溶液红色变浅 固体,溶液红色变浅 |  溶液中存在水解平衡 溶液中存在水解平衡 |
C | 向硫酸铜溶液中滴加浓氨水至过量,溶液先产生蓝色沉淀,然后沉淀溶解变为深蓝色溶液 |  转化为 转化为 |
D |  时,向 时,向 溶液中滴加甲基橙溶液,溶液变红 溶液中滴加甲基橙溶液,溶液变红 | 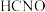 的电离平衡常数大于 的电离平衡常数大于 的电离平衡常数 的电离平衡常数 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
4 . 近年来我国大力加强温室气体 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题。
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题。
(1)已知:

写出 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式:________________________________ ;形成甲醇中的 键需要
键需要________ (填“吸收”或“释放”)能量。
(2)为提高 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是________ (填字母)。
a.高温、高压 b.低温、低压 c.高温、低压 d.低温、高压
(3)在 时,在某恒容密闭容器中进行由
时,在某恒容密闭容器中进行由 催化氢化合成
催化氢化合成 的反应。如图为不同投料比
的反应。如图为不同投料比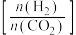 时某反应物
时某反应物 的平衡转化率的变化曲线,则反应物
的平衡转化率的变化曲线,则反应物 是
是________ (填“ ”或“
”或“ ”)。
”)。

(4)在 时,在
时,在 的恒容密闭容器中加入
的恒容密闭容器中加入 、
、 及催化剂,
及催化剂, 时反应达到平衡,测得
时反应达到平衡,测得 。
。
①前 内
内 的平均反应速率
的平均反应速率
________  。
。
②化学平衡常数
________________________ 。
③下列描述中能说明上述反应已达平衡的是________ (填字母)。
a.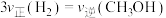
b.单位时间内生成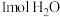 的同时生成
的同时生成
c.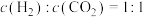
d.容器中气体的平均相对分子质量不随时间而变化
④催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下表四组实验数据。
根据上表所给数据,用 生产甲醇的最优条件为
生产甲醇的最优条件为________ (填实验编号)。
 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题。
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题。(1)已知:


写出
 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式: 键需要
键需要(2)为提高
 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是a.高温、高压 b.低温、低压 c.高温、低压 d.低温、高压
(3)在
 时,在某恒容密闭容器中进行由
时,在某恒容密闭容器中进行由 催化氢化合成
催化氢化合成 的反应。如图为不同投料比
的反应。如图为不同投料比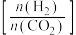 时某反应物
时某反应物 的平衡转化率的变化曲线,则反应物
的平衡转化率的变化曲线,则反应物 是
是 ”或“
”或“ ”)。
”)。
(4)在
 时,在
时,在 的恒容密闭容器中加入
的恒容密闭容器中加入 、
、 及催化剂,
及催化剂, 时反应达到平衡,测得
时反应达到平衡,测得 。
。①前
 内
内 的平均反应速率
的平均反应速率
 。
。②化学平衡常数

③下列描述中能说明上述反应已达平衡的是
a.
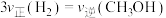
b.单位时间内生成
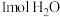 的同时生成
的同时生成
c.
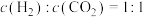
d.容器中气体的平均相对分子质量不随时间而变化
④催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下表四组实验数据。
实验编号 | 温度 | 催化剂 |
| 甲醇的选择性 |
| 543 |
| 12.3 | 42.3 |
| 543 |
| 11.9 | 72.7 |
| 553 |
| 15.3 | 39.1 |
| 553 |
| 12.0 | 70.6 |
 生产甲醇的最优条件为
生产甲醇的最优条件为
您最近半年使用:0次
2024-02-23更新
|
37次组卷
|
2卷引用:河北省百师联盟2023-2024学年高二上学期1月期末大联考化学试题
5 . 下列说法正确的是
A.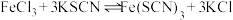 ,向 ,向 与KSCN混合液中加入KCl固体,溶液红色变浅 与KSCN混合液中加入KCl固体,溶液红色变浅 |
B. , , ,加热氯化铜溶液,溶液变成蓝绿色 ,加热氯化铜溶液,溶液变成蓝绿色 |
C.可通过观察气泡产生的快慢,探究影响 与稀硫酸反应速率的因素 与稀硫酸反应速率的因素 |
D.可通过测定单位时间内生成 的体积,比较Zn与不同浓度硫酸溶液反应速率的快慢 的体积,比较Zn与不同浓度硫酸溶液反应速率的快慢 |
您最近半年使用:0次
6 . 一定条件下,可逆反应
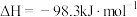 。下列有关叙述错误的是
。下列有关叙述错误的是

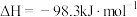 。下列有关叙述错误的是
。下列有关叙述错误的是A.相同条件下, 和 和 反应生成2mol 反应生成2mol ,放出的热量为 ,放出的热量为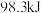 |
B.恒容条件下,向平衡体系中通入一定量 , , 的平衡转化率减小 的平衡转化率减小 |
C.恒压条件下,向平衡体系中通入一定量 ,平衡不移动 ,平衡不移动 |
D.及时分离出 ,平衡正向移动,平衡常数不变 ,平衡正向移动,平衡常数不变 |
您最近半年使用:0次
名校
解题方法
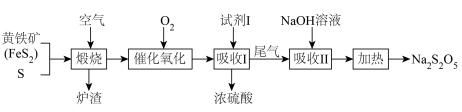
7 . 以黄铁矿和硫黄为原料生产硫酸,并将产生的尾气综合利用制备焦亚硫酸钠( )的流程如图所示。下列说法错误的是
)的流程如图所示。下列说法错误的是
 )的流程如图所示。下列说法错误的是
)的流程如图所示。下列说法错误的是
A.黄铁矿煆烧的化学方程式为 |
B.催化氧化过程中,为提高 的利用率,可加大氧气的通入量 的利用率,可加大氧气的通入量 |
C.为提高 的吸收效率,试剂I宜采用水进行吸收 的吸收效率,试剂I宜采用水进行吸收 |
D.吸收Ⅱ后得到 溶液,则生成焦亚硫酸钠的化学方程式为 溶液,则生成焦亚硫酸钠的化学方程式为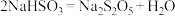 |
您最近半年使用:0次
名校
8 . 在体积为1 L的恒温密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应: CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ,测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
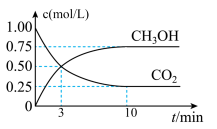
| A.该化学反应在3 min时达到平衡状态 |
| B.保持其他条件不变,降低温度,平衡时c(CH3OH)=0.85 mol·L-1,则该反应的ΔH >0 |
| C.相同温度下,起始时向上述容器中充入0.5 mol CO2、1.5 mol H2,平衡时CO2的转化率为75% |
| D.12 min时,向上述容器中再充入0.25 mol CO2、0.25 mol H2O(g),此时反应将向正反应方向进行 |
您最近半年使用:0次
2023-12-23更新
|
117次组卷
|
3卷引用:河北省衡水市安平中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
9 . 根据实验目的,下列有关实验方案、现象及结论均正确的是
| 选项 | 实验目的 | 实验方案 | 现象及结论 |
| A | 比较金属活动性 | 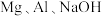 溶液构成原电池装置 溶液构成原电池装置 | 若Mg片上冒气泡,证明活动性: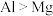 |
| B | 探究浓度对平衡移动的影响 |  溶液中存在反应: 溶液中存在反应: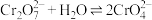 (黄色) (黄色) ,向溶液中加入少量 ,向溶液中加入少量 溶液 溶液 | 若溶液变为黄色,说明在其他条件不变时,减小生成物浓度,平衡向正反应方向移动 |
| C | 探究 和 和 的反应是否为可逆反应 的反应是否为可逆反应 | 取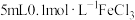 溶液,向其中滴加 溶液,向其中滴加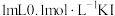 溶液,取上层溶液滴加 溶液,取上层溶液滴加 溶液 溶液 | 若溶液变成血红色,说明该反应是可逆反应 |
| D | 探究浓度对反应速率的影响 | 常温下向表面积相同的铁片上分别滴加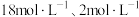 的硫酸溶液 的硫酸溶液 | 若相同时间内 的硫酸中产生的气泡多,说明浓度越大,速率越快 的硫酸中产生的气泡多,说明浓度越大,速率越快 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
10 . 反应①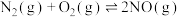 、②
、②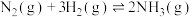 在不同温度时的化学平衡常数(K)值如下表所示。
在不同温度时的化学平衡常数(K)值如下表所示。
下列说法正确的是
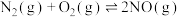 、②
、②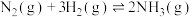 在不同温度时的化学平衡常数(K)值如下表所示。
在不同温度时的化学平衡常数(K)值如下表所示。反应 | ① | ② | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K |
| 0.1 |
| 0.507 | 0.152 |
| A.升高温度,反应①、②的正反应速率增大程度均大于逆反应速率增大程度 |
B.一定温度下,反应①、②分别达到平衡,压缩容器体积(加压)均可使 的转化率增大 的转化率增大 |
C.提高反应②中 与 与 的投料比 的投料比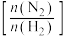 可增大 可增大 的转化率 的转化率 |
D.已知①、②的 ,可以求算反应 ,可以求算反应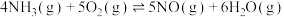 的△H 的△H |
您最近半年使用:0次



 纳米棒
纳米棒