1 . 下列说法正确的是
A.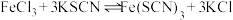 ,向 ,向 与KSCN混合液中加入KCl固体,溶液红色变浅 与KSCN混合液中加入KCl固体,溶液红色变浅 |
B. , , ,加热氯化铜溶液,溶液变成蓝绿色 ,加热氯化铜溶液,溶液变成蓝绿色 |
C.可通过观察气泡产生的快慢,探究影响 与稀硫酸反应速率的因素 与稀硫酸反应速率的因素 |
D.可通过测定单位时间内生成 的体积,比较Zn与不同浓度硫酸溶液反应速率的快慢 的体积,比较Zn与不同浓度硫酸溶液反应速率的快慢 |
您最近一年使用:0次
2 . 一定条件下,可逆反应
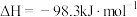 。下列有关叙述错误的是
。下列有关叙述错误的是

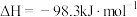 。下列有关叙述错误的是
。下列有关叙述错误的是A.相同条件下, 和 和 反应生成2mol 反应生成2mol ,放出的热量为 ,放出的热量为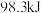 |
B.恒容条件下,向平衡体系中通入一定量 , , 的平衡转化率减小 的平衡转化率减小 |
C.恒压条件下,向平衡体系中通入一定量 ,平衡不移动 ,平衡不移动 |
D.及时分离出 ,平衡正向移动,平衡常数不变 ,平衡正向移动,平衡常数不变 |
您最近一年使用:0次
名校
解题方法
3 . 根据实验目的,下列有关实验方案、现象及结论均正确的是
| 选项 | 实验目的 | 实验方案 | 现象及结论 |
| A | 比较金属活动性 | 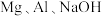 溶液构成原电池装置 溶液构成原电池装置 | 若Mg片上冒气泡,证明活动性: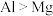 |
| B | 探究浓度对平衡移动的影响 |  溶液中存在反应: 溶液中存在反应: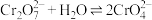 (黄色) (黄色) ,向溶液中加入少量 ,向溶液中加入少量 溶液 溶液 | 若溶液变为黄色,说明在其他条件不变时,减小生成物浓度,平衡向正反应方向移动 |
| C | 探究 和 和 的反应是否为可逆反应 的反应是否为可逆反应 | 取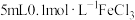 溶液,向其中滴加 溶液,向其中滴加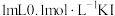 溶液,取上层溶液滴加 溶液,取上层溶液滴加 溶液 溶液 | 若溶液变成血红色,说明该反应是可逆反应 |
| D | 探究浓度对反应速率的影响 | 常温下向表面积相同的铁片上分别滴加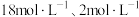 的硫酸溶液 的硫酸溶液 | 若相同时间内 的硫酸中产生的气泡多,说明浓度越大,速率越快 的硫酸中产生的气泡多,说明浓度越大,速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
真题
名校
4 . 在恒温恒容密闭容器中充入一定量 ,发生如下反应:
,发生如下反应: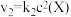 和
和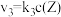 ,其中
,其中 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。
下列说法正确的是
 ,发生如下反应:
,发生如下反应: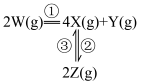
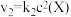 和
和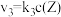 ,其中
,其中 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。 | 0 | 1 | 2 | 3 | 4 | 5 |
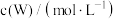 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 |
A. 内,X的平均反应速率为 内,X的平均反应速率为 |
| B.若增大容器容积,平衡时Y的产率增大 |
C.若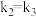 ,平衡时 ,平衡时 |
D.若升高温度,平衡时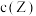 减小 减小 |
您最近一年使用:0次
2023-11-29更新
|
2931次组卷
|
4卷引用:河北省衡水市武邑中学2023-2024学年高三上学期12月期中考试化学试题
名校
5 . 下列说法正确的是
A.稀氨水中存在平衡NH3•H2O NH NH +OH-,若要使平衡逆向移动且c(OH-)增大,可加入NH4Cl固体 +OH-,若要使平衡逆向移动且c(OH-)增大,可加入NH4Cl固体 |
| B.某固体化合物M不导电,但熔融时能完全电离,则M一定是强电解质 |
| C.熵值增大的反应都能自发进行 |
D.溶液中存在平衡FeCl3+3KSCN Fe(SCN)3+3KCl,平衡时加入KCl固体时,平衡逆向移动 Fe(SCN)3+3KCl,平衡时加入KCl固体时,平衡逆向移动 |
您最近一年使用:0次
名校
解题方法
6 . 为探究 在盐酸中与
在盐酸中与 、
、 的反应,某实验小组设计如图实验。
的反应,某实验小组设计如图实验。
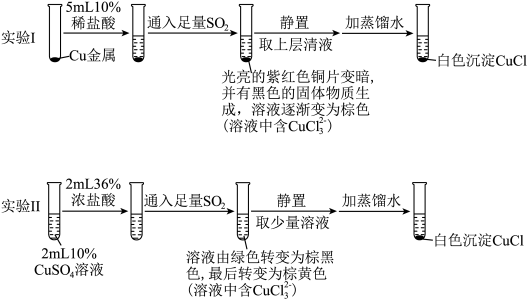
已知: ,实验Ⅰ中得到的黑色固体为
,实验Ⅰ中得到的黑色固体为 。下列说法正确的是
。下列说法正确的是
 在盐酸中与
在盐酸中与 、
、 的反应,某实验小组设计如图实验。
的反应,某实验小组设计如图实验。
已知:
 ,实验Ⅰ中得到的黑色固体为
,实验Ⅰ中得到的黑色固体为 。下列说法正确的是
。下列说法正确的是A.实验Ⅰ、Ⅱ中生成 白色沉淀的原理不相同 白色沉淀的原理不相同 |
B. 在实验Ⅰ、Ⅱ中呈现的化学性质一致 在实验Ⅰ、Ⅱ中呈现的化学性质一致 |
C.实验Ⅰ通入 时反应的离子方程式为 时反应的离子方程式为 |
D.实验Ⅱ若消耗 ,则生成 ,则生成 个 个 |
您最近一年使用:0次
2023-09-27更新
|
192次组卷
|
7卷引用:河北省部分学校2023-2024学年高三上学期9月月考化学试题
名校
7 . 电池正极片由镍钴锰酸锂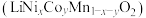 正极材料和铝片组成,以其为原料回收各金属工艺流程如下:
正极材料和铝片组成,以其为原料回收各金属工艺流程如下:
(1)滤液1中含铝微粒为___________ 。
(2)“碱浸”后需进行过滤、洗涤,简述洗涤的操作过程:___________ 。
(3)“还原”时,参加反应的
___________ 。
(4)“分离”过程包含萃取和反萃取,萃取时必须使用的仪器是___________ ;萃取时利用有机物HT将Co2+从水溶液中萃取出来,该过程可表示为Co2+(水层)+2HT(有机层) CoT2(有机层)+2H+(水层)。向CoT2(有机层)中加入稀硫酸能获得较纯的含Co2+的水溶液,从平衡角度解释其原因:
CoT2(有机层)+2H+(水层)。向CoT2(有机层)中加入稀硫酸能获得较纯的含Co2+的水溶液,从平衡角度解释其原因:___________ 。
(5)“氧化”过程中MnSO4发生反应生成MnO2、(NH4)2SO4和H2SO4的化学方程式为___________ 。
(6)“沉钴”后获得CoC2O4·2H2O,取mgCoC2O4·2H2O进行“高温分解”,测得固体的失重率( )与温度的关系曲线如图所示。写出加热到160℃时反应的化学方程式:
)与温度的关系曲线如图所示。写出加热到160℃时反应的化学方程式:___________ ;“高温分解”需控制的最低温度为___________ 。
 正极材料和铝片组成,以其为原料回收各金属工艺流程如下:
正极材料和铝片组成,以其为原料回收各金属工艺流程如下:
(1)滤液1中含铝微粒为
(2)“碱浸”后需进行过滤、洗涤,简述洗涤的操作过程:
(3)“还原”时,参加反应的

(4)“分离”过程包含萃取和反萃取,萃取时必须使用的仪器是
 CoT2(有机层)+2H+(水层)。向CoT2(有机层)中加入稀硫酸能获得较纯的含Co2+的水溶液,从平衡角度解释其原因:
CoT2(有机层)+2H+(水层)。向CoT2(有机层)中加入稀硫酸能获得较纯的含Co2+的水溶液,从平衡角度解释其原因:(5)“氧化”过程中MnSO4发生反应生成MnO2、(NH4)2SO4和H2SO4的化学方程式为
(6)“沉钴”后获得CoC2O4·2H2O,取mgCoC2O4·2H2O进行“高温分解”,测得固体的失重率(
 )与温度的关系曲线如图所示。写出加热到160℃时反应的化学方程式:
)与温度的关系曲线如图所示。写出加热到160℃时反应的化学方程式:
您最近一年使用:0次
8 . 科学家研究高效催化剂对汽车尾气进行无害化处理,其反应原理为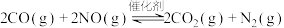
 。回答下列问题:
。回答下列问题:
(1)某温度下,在密闭容器中该反应达到化学平衡后,只改变一种条件对该反应的正、逆反应速率的影响如图甲所示。

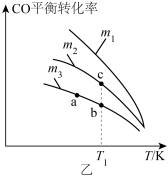
①加催化剂对反应速率影响的图像是______ (填字母,下同)。
②适当升高温度对反应速率影响的图像是A,该反应的正反应是__________ 反应(填“吸热”或“放热”)。
③图像D改变的条件是__________ (任写一条)。
(2)在 密闭容器中充入CO和NO共
密闭容器中充入CO和NO共 ,发生反应
,发生反应
 ,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比
,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比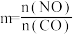 ]。
]。
①该反应的化学平衡常数表达式是__________ 。
②图中a、b、c三点对应的平衡常数 、
、 、
、 相对大小关系是
相对大小关系是__________ , 、
、 、
、 相对大小关系是
相对大小关系是__________ 。
③若 ,温度为
,温度为 ,反应达到平衡所用的时间为
,反应达到平衡所用的时间为 ,CO的平衡转化率为40%。达平衡过程中平均反应速率
,CO的平衡转化率为40%。达平衡过程中平均反应速率
__________  ,平衡时混合气体总物质的量=
,平衡时混合气体总物质的量=__________  ;若
;若 时,该容器中此四种物质均为
时,该容器中此四种物质均为 ,则此时v(正)
,则此时v(正)______ (填“>”“<”或“=”)v(逆)。
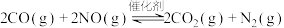
 。回答下列问题:
。回答下列问题:(1)某温度下,在密闭容器中该反应达到化学平衡后,只改变一种条件对该反应的正、逆反应速率的影响如图甲所示。


①加催化剂对反应速率影响的图像是
②适当升高温度对反应速率影响的图像是A,该反应的正反应是
③图像D改变的条件是
(2)在
 密闭容器中充入CO和NO共
密闭容器中充入CO和NO共 ,发生反应
,发生反应
 ,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比
,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比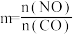 ]。
]。①该反应的化学平衡常数表达式是
②图中a、b、c三点对应的平衡常数
 、
、 、
、 相对大小关系是
相对大小关系是 、
、 、
、 相对大小关系是
相对大小关系是③若
 ,温度为
,温度为 ,反应达到平衡所用的时间为
,反应达到平衡所用的时间为 ,CO的平衡转化率为40%。达平衡过程中平均反应速率
,CO的平衡转化率为40%。达平衡过程中平均反应速率
 ,平衡时混合气体总物质的量=
,平衡时混合气体总物质的量= ;若
;若 时,该容器中此四种物质均为
时,该容器中此四种物质均为 ,则此时v(正)
,则此时v(正)
您最近一年使用:0次
名校
解题方法
9 . 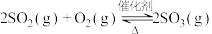
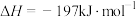 该反应在工业制备硫酸中有重要应用。下列叙述正确的是
该反应在工业制备硫酸中有重要应用。下列叙述正确的是
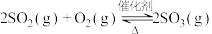
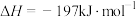 该反应在工业制备硫酸中有重要应用。下列叙述正确的是
该反应在工业制备硫酸中有重要应用。下列叙述正确的是| A.达到反应限度时,反应放出197kJ的热量 |
B.提高反应温度,可实现 的完全转化 的完全转化 |
C.工业生产中可通过增大 浓度来提升 浓度来提升 转化率 转化率 |
D.工业制备硫酸过程中将生成的 用水吸收制得 用水吸收制得 |
您最近一年使用:0次
2023-05-17更新
|
341次组卷
|
2卷引用:河北省石家庄市第一中学2022-2023学年高一下学期7月期末化学试题
2023·浙江·二模
解题方法
10 . 下列方案设计、现象和结论不正确的是
| 实验方案 | 现象 | 结论 | |
| A | 试管中依次加入3mL乙醇2mL浓硫酸、2mL乙酸及沸石后连接好装置并加热 | 饱和碳酸钠液面上出现有香味的无色油状液体 | 有酯类物质生成 |
| B | 将 液体和 液体和 固体分别暴露在潮湿空气中 固体分别暴露在潮湿空气中 | 只有前者会冒“白烟” | 相同条件下水解程度: |
| C | 室温下,将 溶液和稀 溶液和稀 混合 混合 | 溶液变浑浊且有刺激性气味的气体生成 |  既体现还原性又体现氧化性 既体现还原性又体现氧化性 |
| D | 向 溶液中加入5滴 溶液中加入5滴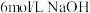 溶液 溶液 | 溶液由橙色变黄色 |  减小,平衡向 减小,平衡向 减小的方向移动 减小的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



