解题方法
1 . 下列方案设计、现象和结论不正确的是
| 实验方案 | 现象 | 结论 | |
| A | 试管中依次加入3mL乙醇2mL浓硫酸、2mL乙酸及沸石后连接好装置并加热 | 饱和碳酸钠液面上出现有香味的无色油状液体 | 有酯类物质生成 |
| B | 将 液体和 液体和 固体分别暴露在潮湿空气中 固体分别暴露在潮湿空气中 | 只有前者会冒“白烟” | 相同条件下水解程度: |
| C | 室温下,将 溶液和稀 溶液和稀 混合 混合 | 溶液变浑浊且有刺激性气味的气体生成 |  既体现还原性又体现氧化性 既体现还原性又体现氧化性 |
| D | 向 溶液中加入5滴 溶液中加入5滴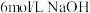 溶液 溶液 | 溶液由橙色变黄色 |  减小,平衡向 减小,平衡向 减小的方向移动 减小的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023·全国·模拟预测
名校
2 . 下列实验操作、现象、结论均正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向平衡体系FeCl3+3KSCN Fe(SCN)3+3KCl中加入适量KCl固体 Fe(SCN)3+3KCl中加入适量KCl固体 | 溶液的颜色变浅 | 平衡逆向移动 |
| B | 对平衡体系2NO2(g) N2O4(g)压缩体积,增大压强 N2O4(g)压缩体积,增大压强 | 混合气体的颜色变深 | 平衡逆向移动 |
| C | 2mL0.1mol•L-1K2Cr2O7溶液中存在:Cr2O +H2O +H2O 2CrO 2CrO +2H+,向其中滴加5~10滴6mol•L-1NaOH溶液 +2H+,向其中滴加5~10滴6mol•L-1NaOH溶液 | 溶液由橙色变为黄色 | 平衡正向移动 |
| D | CuCl2溶液中存在:[Cu(H2O)4]2+(蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O △H>0,对CuCl2溶液加热 [CuCl4]2-(黄色)+4H2O △H>0,对CuCl2溶液加热 | 溶液由蓝色变为黄色 | 平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列说法正确的是
| A.升高温度,会使单位体积内分子数增多,从而加快化学反应速率 |
B. (蓝色) (蓝色)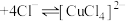 (黄色) (黄色)  , , 稀溶液受热颜色变黄 稀溶液受热颜色变黄 |
C.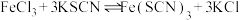 达平衡后,加入少量KCl固体,溶液红色变浅 达平衡后,加入少量KCl固体,溶液红色变浅 |
D. (橙色) (橙色) (黄色) (黄色) ,向 ,向 溶液中滴加几滴浓硫酸,溶液变为黄色 溶液中滴加几滴浓硫酸,溶液变为黄色 |
您最近一年使用:0次
2023-02-20更新
|
232次组卷
|
3卷引用:河北省石家庄市新乐市第一中学2022-2023学年高二上学期期末考试化学试题
河北省石家庄市新乐市第一中学2022-2023学年高二上学期期末考试化学试题河北省石家庄市第二十四中学2023-2024学年高二上学期10月月考化学试题(已下线)专题04 化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
4 . 二氧化硫的催化氧化反应: 是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是
是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是
 是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是
是工业制硫酸中的重要反应。某温度下,在一密闭容器中探究二氧化硫的催化氧化反应,下列叙述正确的是A.加入合适催化剂可以提高 的平衡产率 的平衡产率 |
| B.缩小容器容积可以增大活化分子百分含量 |
C.扩大容器容积可以提高 的平衡产率 的平衡产率 |
| D.缩小容器容积可以增大反应速率 |
您最近一年使用:0次
名校
5 . 可逆反应2SO2+O2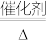 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
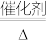 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是| A.升高温度平衡向正反应方向移动 |
| B.增大压强SO2的转化率增大 |
| C.加入催化剂平衡不发生移动,但反应速率加快 |
| D.只增大SO2浓度平衡不移动 |
您最近一年使用:0次
名校
6 . 下列叙述中错误的是
| A.常温下,2A(s)+B(g)=2C(g)+D(g)不能自发进行,则该反应△H一定大于0 |
B.常温下,Fe3+(aq)+3SCN-(aq) Fe(SCN)3(aq)达到平衡后,加水稀释至原溶液体积的2倍,平衡逆向移动 Fe(SCN)3(aq)达到平衡后,加水稀释至原溶液体积的2倍,平衡逆向移动 |
C.CO、O2与人体血液中的血红蛋白(Hb)建立如下平衡:CO+HbO2 HbCO+O2,当CO中毒时,应将中毒患者转移至高压氧仓吸氧 HbCO+O2,当CO中毒时,应将中毒患者转移至高压氧仓吸氧 |
D.硫酸工业生产中,2SO2(g)+O2(g) 2SO3(g)在高温、高压条件下进行 2SO3(g)在高温、高压条件下进行 |
您最近一年使用:0次
2022-11-02更新
|
218次组卷
|
4卷引用:河北省张家口市部分学校2022-2023学年高二上学期期中考试化学试题
名校
解题方法
7 . 乙烯水合法是工业制乙醇的方法: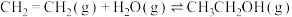 ,该反应在密闭容器中进行,下列说法错误的是
,该反应在密闭容器中进行,下列说法错误的是
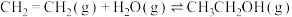 ,该反应在密闭容器中进行,下列说法错误的是
,该反应在密闭容器中进行,下列说法错误的是A.恒温恒容,充入 , ,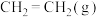 的转化率增大 的转化率增大 |
B.若升高温度,平衡常数减小,则该反应 |
| C.压缩容积,活化分子百分数增大,反应速率加快 |
D.恒温恒压,通入 ,平衡向左移动 ,平衡向左移动 |
您最近一年使用:0次
2022-10-29更新
|
581次组卷
|
7卷引用:选择题11-15
(已下线)选择题11-15四川省雅安市2023届高三上学期零诊考试化学试题(已下线)专题13 化学反应速率和化学平衡(已下线)查补易混易错04 化学反应原理部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)湖南省衡阳市第一中学2023届高三下学期5月月考化学试题(已下线)2019年高考海南卷化学试题变式题(单选题)辽宁省锦州市渤海大学附属高级中学2023-2024学年高三上学期第三次考试化学试题
名校
解题方法
8 . 下列有关说法不正确的是
| A.盐酸与锌粉反应时,若加入少量CuSO4溶液,能加快H2产生速率 |
| B.增大反应物的浓度,平衡向右移动,生成物的体积分数不一定增大 |
| C.钢铁浸泡于食盐水中发生电化学腐蚀时的正极反应为:2H2O+2e-=H2↑+2OH- |
| D.已知:S(g)+O2(g)=SO2(g) ΔH1;S(s)+O2(g)=SO2(g) ΔH2,则ΔH1<ΔH2 |
您最近一年使用:0次
2022-09-27更新
|
175次组卷
|
2卷引用:河北省昌黎第一中学2023届高三下学期第七次调研考试化学试题
9 . CO2是一种温室气体,对人类的生存环境产生巨大的影响,将CO2作为原料转化为有用化学品,对实现碳中和及生态环境保护有着重要意义。
Ⅰ.工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为:2NH3(l)+CO2(l)=H2O(l)+NH2CONH2(l) △H=___________ kJ/mol。
(2)在恒容密闭容器中发生反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) △H<0。下列说法正确的是
Ⅱ.可利用CO2和CH4催化制备合成气(CO、H2),在一定温度下容积为1 L密闭容器中,充入等物质的量CH4和CO2,加入Ni/Al2O3使其发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)
(3)反应达平衡后,平衡常数K=81,此时测得c(CO)为3 mol/L,则CH4的转化率为___________ (保留2位有效数字)。
(4)制备“合成气”反应历程分两步:
上述反应中C(ads)为吸附性活性炭,反应历程的能量图变化如下图所示:

①反应速率快慢比较:反应①___________ 反应②(填“>”“<”或“=”),请依据有效碰撞理论微观探析其原因___________ 。
②一定温度下,反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的平衡常数K=
2CO(g)+2H2(g)的平衡常数K=___________ (用k1、k2、k3、k4表示)。
(5)制备合成气(CO、H2)过程中发生副反应:CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.0 kJ/mol,在刚性密闭容器中,进料比
CO(g)+H2O(g) △H2=+41.0 kJ/mol,在刚性密闭容器中,进料比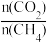 分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中,
分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中, 随温度变化的关系如图所示:
随温度变化的关系如图所示:

随着进料比 的增加,
的增加, 的值
的值___________ (填“增大”、“不变”或“减小”),其原因是___________ 。
Ⅰ.工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为:2NH3(l)+CO2(l)=H2O(l)+NH2CONH2(l) △H=
(2)在恒容密闭容器中发生反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) △H<0。下列说法正确的是
| A.增大CO2的浓度,有利于NH3的转化率增大 |
| B.反应在任何温度下都能自发进行 |
| C.当混合气体的密度不再发生改变时反应达平衡状态 |
| D.充入He,压强增大,平衡向正反应移动 |
Ⅱ.可利用CO2和CH4催化制备合成气(CO、H2),在一定温度下容积为1 L密闭容器中,充入等物质的量CH4和CO2,加入Ni/Al2O3使其发生反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g)
2CO(g)+2H2(g)(3)反应达平衡后,平衡常数K=81,此时测得c(CO)为3 mol/L,则CH4的转化率为
(4)制备“合成气”反应历程分两步:
| 步骤 | 反应 | 正反应速率方程 | 逆反应速率方程 |
| 反应① | CH4(g) C(ads)+2H2(g) C(ads)+2H2(g) | v正=k1·c(CH4) | v逆=k2·c2(H2) |
| 反应② | C(ads)+CO2(g) 2CO(g) 2CO(g) | v正=k3·c(CO2) | v逆=k4·c2(CO) |

①反应速率快慢比较:反应①
②一定温度下,反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的平衡常数K=
2CO(g)+2H2(g)的平衡常数K=(5)制备合成气(CO、H2)过程中发生副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.0 kJ/mol,在刚性密闭容器中,进料比
CO(g)+H2O(g) △H2=+41.0 kJ/mol,在刚性密闭容器中,进料比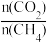 分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中,
分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中, 随温度变化的关系如图所示:
随温度变化的关系如图所示:
随着进料比
 的增加,
的增加, 的值
的值
您最近一年使用:0次
10 . 碳酸锶(SrCO3)难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶(含少量Ba2+、Ca2+、Mg2+、 Pb2+等)制备高纯碳酸锶的工艺流程如下:
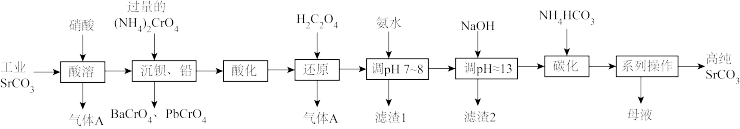
已知:I. Cr(OH)3为两性氢氧化物;
II.常温下,各物质的溶度积常数如下表所示。
回答下列问题:
(1)气体A的电子式为_______ 。
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为_______ (用离子方程式解释);“还原”时发生反应的离子方程式为_______ 。
(3)“滤渣1”的主要成分为_______ (填化学式)。
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为_______ 。
(5)“调pH ≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为_______ 。
(6)已知:碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,则“碳化”时,反应Sr2+(aq)+2HCO (aq)
(aq) SrCO3(s)+H2CO3(aq)的平衡常数K=
SrCO3(s)+H2CO3(aq)的平衡常数K=_______ (保留两位有效数字)。
(7)“系列操作”中包含“200°C烘干”操作,烘干过程中除蒸发水分外,还能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能为_______ (填化学式)。

已知:I. Cr(OH)3为两性氢氧化物;
II.常温下,各物质的溶度积常数如下表所示。
| 化合物 | Cr(OH)3 | Ca(OH)2 | Mg(OH)2 | SrCO3 |
| Ksp近似值 | 1×10-31 | 5.5×10-6 | 1.8×10-11 | 5.6×10-10 |
(1)气体A的电子式为
(2)“除钡、铅”时,pH过低会导致(NH4)2CrO4的利用率降低,原因为
(3)“滤渣1”的主要成分为
(4)用氨水和NaOH分步调节pH,而不是直接调节溶液的pH≈13的原因为
(5)“调pH ≈13”后需对溶液进行煮沸并趁热过滤出滤渣2,煮沸并趁热过滤的原因为
(6)已知:碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,则“碳化”时,反应Sr2+(aq)+2HCO
 (aq)
(aq) SrCO3(s)+H2CO3(aq)的平衡常数K=
SrCO3(s)+H2CO3(aq)的平衡常数K=(7)“系列操作”中包含“200°C烘干”操作,烘干过程中除蒸发水分外,还能够除去SrCO3中的微量可溶性杂质,该杂质除NH4HCO3外还可能为
您最近一年使用:0次
2022-04-09更新
|
1200次组卷
|
13卷引用:河北省石家庄市2022届高三毕业班教学质量检测二(一模)化学试题
河北省石家庄市2022届高三毕业班教学质量检测二(一模)化学试题(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(工业流程题)(已下线)秘籍17 工艺流程的条件控制与计算-备战2022年高考化学抢分秘籍(全国通用)(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学-2022年高考押题预测卷01(山东卷)(已下线)化学-2022年高考考前押题密卷(湖南卷)(已下线)化学-2022年高考考前押题密卷(重庆卷)湖北省宜昌市夷陵中学2022届高三5月第二次限时训练(四模)化学试题辽宁省抚顺市第二中学2021-2022学年高三上学期10月月考化学试题山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题湖南省株洲市九方中学2022-2023学年高三上学期第一次月考化学试题湖南省邵阳市第一中学2023届高三第五次月考化学试题



