名校
解题方法
1 . 在某密闭容器中投入碳粉和一定量的 ,发生反应:
,发生反应: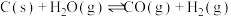
 ,下列措施能增大化学反应速率的是
,下列措施能增大化学反应速率的是
 ,发生反应:
,发生反应: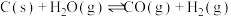
 ,下列措施能增大化学反应速率的是
,下列措施能增大化学反应速率的是A.增加 的质量 的质量 | B.升高温度 |
C.移除部分 | D.扩大容器体积 |
您最近半年使用:0次
2023-03-16更新
|
118次组卷
|
2卷引用:河北省2022-2023学年高二下学期开学考试化学试题
名校
2 . 四钼酸铵[(NH4)2 Mo4O13·2H2O]微溶于水,常用作石油工业的催化剂、微量元素肥料、织物防火及阻燃剂等。从富钼精矿中(主要成分为MoS2,还含有少量NiS、SiO2、As2O3)制备四钼酸铵的一种流程如图所示:

已知:“浸出”所得浸出液中主要存在的离子为Na+、OH-、MoO 、SO
、SO 、SiO
、SiO 、AsO
、AsO
(1)钼(Mo)在周期表中位于第五周期ⅥB族,画出钼的价电子轨道表示式____________
(2)氧化焙烧时,MoS2发生反应的化学方程式为__________________________________
(3)“滤渣Ⅱ”的主要成分为__________________ (写化学式)
(4)实验室进行萃取分液操作时,需要用到的玻璃仪器主要有_________ 、_________ 。
(5)“萃取”的原理为2R3N(叔胺N-235)+2H++MoO ⇌(R3NH)2MoO4 ,则“反萃取”工序中的试剂X最适宜选用
⇌(R3NH)2MoO4 ,则“反萃取”工序中的试剂X最适宜选用__________ (填选项字母)
a.NaOH溶液 b.氨水 c.稀硫酸 d.(NH4)2SO4溶液
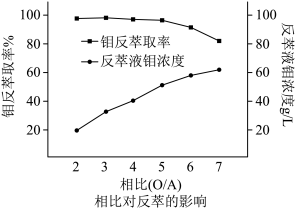
(6)在“反萃取”工序中相比(有机相与水相的体积比)如图所示。则反萃取时应选择的相比为____________ 。
(7)在“酸沉结晶”前,钼酸铵溶液中c(MoO )=0.80mol·L-1,c(SO
)=0.80mol·L-1,c(SO )=0.05mol·L-1,在结晶前应加入Ba(OH)2固体以除去溶液中的SO
)=0.05mol·L-1,在结晶前应加入Ba(OH)2固体以除去溶液中的SO 。当BaMoO4开始沉淀时,SO
。当BaMoO4开始沉淀时,SO 的去除率是
的去除率是__________ %(保留1位小数)。[Ksp(BaSO4)=1.1×10-10、Ksp(BaMoO4)=4.0×10-8,忽略溶液体积变化]

已知:“浸出”所得浸出液中主要存在的离子为Na+、OH-、MoO
 、SO
、SO 、SiO
、SiO 、AsO
、AsO
(1)钼(Mo)在周期表中位于第五周期ⅥB族,画出钼的价电子轨道表示式
(2)氧化焙烧时,MoS2发生反应的化学方程式为
(3)“滤渣Ⅱ”的主要成分为
(4)实验室进行萃取分液操作时,需要用到的玻璃仪器主要有
(5)“萃取”的原理为2R3N(叔胺N-235)+2H++MoO
 ⇌(R3NH)2MoO4 ,则“反萃取”工序中的试剂X最适宜选用
⇌(R3NH)2MoO4 ,则“反萃取”工序中的试剂X最适宜选用a.NaOH溶液 b.氨水 c.稀硫酸 d.(NH4)2SO4溶液
(6)在“反萃取”工序中相比(有机相与水相的体积比)如图所示。则反萃取时应选择的相比为

(7)在“酸沉结晶”前,钼酸铵溶液中c(MoO
 )=0.80mol·L-1,c(SO
)=0.80mol·L-1,c(SO )=0.05mol·L-1,在结晶前应加入Ba(OH)2固体以除去溶液中的SO
)=0.05mol·L-1,在结晶前应加入Ba(OH)2固体以除去溶液中的SO 。当BaMoO4开始沉淀时,SO
。当BaMoO4开始沉淀时,SO 的去除率是
的去除率是
您最近半年使用:0次
名校
3 . 下列实验中,对现象的解释不正确 的是
| 选项 | A | B |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 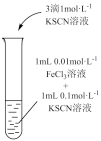 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 |
| 选项 | C | D |
| 装置及操作 |  分别测定20℃和80℃蒸馏水的电导率 |  |
| 现象 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在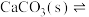  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列实验操作、现象及相应的结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将两个完全相同的 球分别浸泡在冰水和热水中 球分别浸泡在冰水和热水中 | 热水中 球气体颜色更深 球气体颜色更深 |  正反应为放热反应,升温平衡逆向移动 正反应为放热反应,升温平衡逆向移动 |
| B | 向重铬酸钾溶液中,滴入少量氢氧化钠溶液 | 溶液由黄色变为橙色 |  , , 中和 中和 使平衡正向移动 使平衡正向移动 |
| C | 用温度计测定锥形瓶中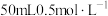 盐酸与适当过量的NaOH溶液反应的最高温度 盐酸与适当过量的NaOH溶液反应的最高温度 | 温度升高,利用最高温度计算实验放出热量为 | 中和热 |
| D | 向某无色溶液中滴加稀硫酸 | 产生有刺激性气味气体和淡黄色沉淀 | 该无色溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-02-22更新
|
156次组卷
|
2卷引用:四川省乐山市2022-2023学年高二下学期开学考试化学试题
5 . 恒容密闭容器中发生反应: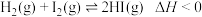 ,达平衡后只改变一个条件一定能增大正反应速率且使平衡正向移动的是
,达平衡后只改变一个条件一定能增大正反应速率且使平衡正向移动的是
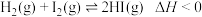 ,达平衡后只改变一个条件一定能增大正反应速率且使平衡正向移动的是
,达平衡后只改变一个条件一定能增大正反应速率且使平衡正向移动的是| A.升高温度 | B.使用催化剂 | C.及时分离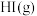 | D.充入一定量 |
您最近半年使用:0次
名校
6 . 某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能高选择性吸附NO2。废气中的NO2被吸附后,经处理能全部转化为HNO3。原理如图。已知: ,△H<0,下列说法不正确的是
,△H<0,下列说法不正确的是
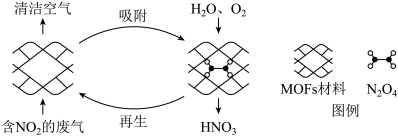
 ,△H<0,下列说法不正确的是
,△H<0,下列说法不正确的是
| A.气体温度升高后有利于N2O4的固定 |
B.使用多孔材料不能改变 的焓变 的焓变 |
C.使用多孔材料能促进 平衡正向移动,有利于NO2的去除 平衡正向移动,有利于NO2的去除 |
D.加入 H2O和O2,发生化学反应方程式为: |
您最近半年使用:0次
2023-02-22更新
|
311次组卷
|
2卷引用:河南省周口市川汇区周口恒大中学2023-2024学年高二下学期开学化学试题
名校
7 . 根据实验测定,某容器中同时发生甲和乙两个反应:
反应甲:

反应乙:
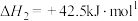
该容器中的反应达到平衡后,下列措施中一定能提高平衡体系中CH3OH的百分含量的是
反应甲:


反应乙:

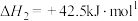
该容器中的反应达到平衡后,下列措施中一定能提高平衡体系中CH3OH的百分含量的是
| A.降低温度 | B.使用催化剂 |
| C.扩大容器体积 | D.在原料气中加入H2O(g) |
您最近半年使用:0次
2023-02-15更新
|
201次组卷
|
2卷引用: 上海交通大学附属中学2022-2023学年高三下学期开学摸底考试化学试题
名校
8 . 以反应 为例,探究影响平衡移动的因素。取相同浓度的
为例,探究影响平衡移动的因素。取相同浓度的 溶液,分别进行下列实验,对实验现象的分析
溶液,分别进行下列实验,对实验现象的分析不正确 的是
 为例,探究影响平衡移动的因素。取相同浓度的
为例,探究影响平衡移动的因素。取相同浓度的 溶液,分别进行下列实验,对实验现象的分析
溶液,分别进行下列实验,对实验现象的分析| 操作和现象 | 分析 | |
| A | 观察溶液为绿色 |  和 和 同时存在 同时存在 |
| B | 升高温度,溶液变为黄绿色 | 平衡正移, 的浓度增大 的浓度增大 |
| C | 加少量 片,静置, 片,静置, 片上覆盖红色固体 片上覆盖红色固体 |  的浓度增大 的浓度增大 |
| D | 加几滴 溶液,静置,上层清液为蓝色 溶液,静置,上层清液为蓝色 | 平衡逆移, 的浓度减小 的浓度减小 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-02-13更新
|
285次组卷
|
13卷引用:重庆市南开中学校2022-2023学年高二下学期开学考试化学试题
重庆市南开中学校2022-2023学年高二下学期开学考试化学试题北京市朝阳区2021-2022学年高二上学期期末考试化学试题北京市房山区2022届高三一模化学试题北京市第二十二中学 2021-2022 学年高二下学期期中考试化学试题广东省广州市第六中学2022-2023学年高二上学期期中考试化学试题北京市顺义区顺义第一中学2022-2023学年高二上学期期中考试化学试题北京市第八中学2022-2023学年高二上学期期末考试化学试题北京市昌平区第一中学2022-2023学年高二上学期期末考试化学试题天津市南开区2022~2023 学年高三上学期阶段性质量监测 (二) 化学试题河南省信阳市2022-2023学年高二上学期期末考试化学试题北京交通大学附属中学2023-2024学年高三上学期10月月考化学试题北京市日坛中学2023-2024学年高三上学期10月检测化学试题重庆市万州第二高级中学2023-2024学年高二上学期期中考试化学试题
9 . 氨的催化氧化是工业制硝酸的基础:
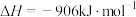 。下列叙述正确的是
。下列叙述正确的是

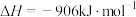 。下列叙述正确的是
。下列叙述正确的是A.增加 的量,有利于提高 的量,有利于提高 的转化率 的转化率 |
B.将 和 和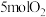 混合,充分反应能放出906kJ的热量 混合,充分反应能放出906kJ的热量 |
C.当 时,反应达到平衡状态 时,反应达到平衡状态 |
| D.升高温度,正反应速率增大、逆反应速率减小 |
您最近半年使用:0次
名校
10 . CuCl2溶液中存在如下平衡:[Cu(H2O)4]2+(蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O △H>0。取相同浓度的CuCl2溶液,分别进行下列实验,下列对实验现象的分析中错误的是
[CuCl4]2-(黄色)+4H2O △H>0。取相同浓度的CuCl2溶液,分别进行下列实验,下列对实验现象的分析中错误的是
 [CuCl4]2-(黄色)+4H2O △H>0。取相同浓度的CuCl2溶液,分别进行下列实验,下列对实验现象的分析中错误的是
[CuCl4]2-(黄色)+4H2O △H>0。取相同浓度的CuCl2溶液,分别进行下列实验,下列对实验现象的分析中错误的是| 操作和现象 | 分析 | |
| A | 观察溶液为绿色 | [Cu(H2O)4]2+和[CuCl4]2-同时存在 |
| B | 升高温度,溶液变为黄绿色 | 平衡正移,[CuCl4]2-的浓度增大 |
| C | 加水稀释,振荡后静置,溶液变为蓝色 | 平衡逆移,[Cu(H2O)4]2+的浓度增大 |
| D | 加几滳AgNO3溶液,静置,上层清液为蓝色 | 平衡逆移,[CuCl4]2-的浓度减小 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-02-11更新
|
140次组卷
|
2卷引用:吉林省长春外国语学校2022-2023学年高二下学期开学考试化学试题



