解题方法
1 . 在恒容容器中发生CH4(g)燃烧。写出1molCH4(g)完全燃烧的热化学方程式____  达到平衡后,若向其中加入H2O后,平衡
达到平衡后,若向其中加入H2O后,平衡____ (选填:向右移动,向左移动,不移动),加入O2后,甲烷转化率____ 。
 达到平衡后,若向其中加入H2O后,平衡
达到平衡后,若向其中加入H2O后,平衡
您最近半年使用:0次
名校
2 . KSCN是实验室常用的化学试剂。
(1)探究KCl浓度对Fe3+与SCN-显色反应的影响
将25mL0.005mol•L-1FeCl3与25mL0.01mol•L-1KSCN溶液混合得红色溶液,各取3mL溶液分别加KCl晶体进行透光实验,结果如图所示。
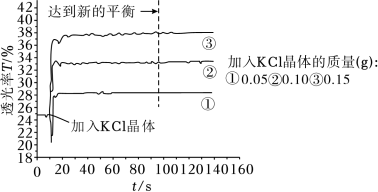
已知:i.溶液颜色越浅,透光率(T)越高;
ii.FeCl3溶液中存在Fe3++4Cl- [FeCl4]-(黄色)。
[FeCl4]-(黄色)。
①采用FeCl3稀溶液是为了避免_______ (填离子符号)的颜色对实验干扰。
②由实验结果分析,随着KCl浓度增大,Fe(SCN)3的浓度_______ (填“增大”“减小”或“不变”),从平衡移动的角度分析可能的原因_______ 。
(2)探究KSCN在铜含量测定过程中的作用
步骤如下:取1.0g铜盐样品溶于稀盐酸配成250mL溶液,取10.00mL加入过量KI充分反应,用0.0100mol•L-1的Na2S2O3标准液滴定至终点。
已知:i.2Cu2++4I-=2CuI↓+I2;2S2O +I2=S4O
+I2=S4O +2I-;
+2I-;
ii.I2+I- I
I ,CuI沉淀强烈吸附I
,CuI沉淀强烈吸附I ;
;
iii.Ksp(CuI)=1.0×10-12;Ksp(CuSCN)=4.8×10-15
①以淀粉为指示剂,滴定终点的颜色变化为_______ ;根据信息预测最终测定的结果将_______ (填“偏大”“偏小”或“无影响”)。
②通过实验探究,在滴定过程中加入KSCN可使测定结果更准确,写出发生反应的离子方程式_______ ;到达滴定终点时消耗标准液20.00mL,样品中铜元素质量分数为_______ ,滴定后仍存在少量CuI沉淀,测得溶液中c(I-)=0.2mol•L-1,则c(SCN-)=_______ 。
(1)探究KCl浓度对Fe3+与SCN-显色反应的影响
将25mL0.005mol•L-1FeCl3与25mL0.01mol•L-1KSCN溶液混合得红色溶液,各取3mL溶液分别加KCl晶体进行透光实验,结果如图所示。

已知:i.溶液颜色越浅,透光率(T)越高;
ii.FeCl3溶液中存在Fe3++4Cl-
 [FeCl4]-(黄色)。
[FeCl4]-(黄色)。①采用FeCl3稀溶液是为了避免
②由实验结果分析,随着KCl浓度增大,Fe(SCN)3的浓度
(2)探究KSCN在铜含量测定过程中的作用
步骤如下:取1.0g铜盐样品溶于稀盐酸配成250mL溶液,取10.00mL加入过量KI充分反应,用0.0100mol•L-1的Na2S2O3标准液滴定至终点。
已知:i.2Cu2++4I-=2CuI↓+I2;2S2O
 +I2=S4O
+I2=S4O +2I-;
+2I-;ii.I2+I-
 I
I ,CuI沉淀强烈吸附I
,CuI沉淀强烈吸附I ;
;iii.Ksp(CuI)=1.0×10-12;Ksp(CuSCN)=4.8×10-15
①以淀粉为指示剂,滴定终点的颜色变化为
②通过实验探究,在滴定过程中加入KSCN可使测定结果更准确,写出发生反应的离子方程式
您最近半年使用:0次
2024-04-05更新
|
51次组卷
|
3卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题
名校
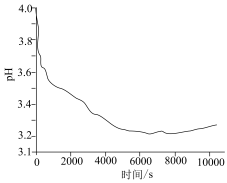
3 . 某兴趣小组将4g铁钉放入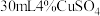 溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
已知:
①CuSCN:白色固体,不溶于水;
②室温下,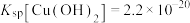 ,
, ,
, 。
。
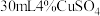 溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
溶液中,溶液pH变化如下图所示。一段时间后,取出铁钉,过滤,取反应后的滤液,加适量KSCN溶液,溶液立即变红,但红色很快褪去,产生白色沉淀。下列说法不正确的是
已知:
①CuSCN:白色固体,不溶于水;
②室温下,
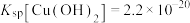 ,
, ,
, 。
。A. 溶液 溶液 的原因是 的原因是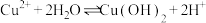 |
B.0~6000s,随着反应进行,溶液pH下降的原因可能是 被 被 氧化为 氧化为 |
C.反应后期溶液pH略有上升的可能原因是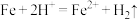 |
D.溶液先变红后又褪色的可能原因是 的反应速率快, 的反应速率快,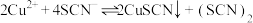 的反应限度大 的反应限度大 |
您最近半年使用:0次
2024-03-17更新
|
104次组卷
|
2卷引用:北京市第一七一中学2023-2024学年高三下学期开学考试化学试题
名校
解题方法
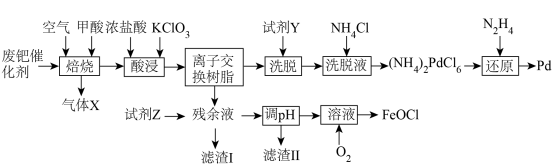
4 . 钯(Pd)见一种银白色过渡金属,质软、有良好的延展性和可塑性,他锻造、压延和拉丝。块状金属钯能吸收大量氢气,使体积显著胀大、变脆乃至破裂成碎片。一种从废钯催化剂(杂质主要含有机物、活性炭及少量Fe、Cu、Al等元素)中回收钯和类芬顿催化剂 的工艺流程如图所示:
的工艺流程如图所示:
已知:①常温下,钯不溶于盐酸;Pd易被氧化为难溶于酸的 而失去催化活性;
而失去催化活性;
②阴、阳离子交换树脂的基本工作原理分别为 、
、 (R—表示树脂的有机成分);
(R—表示树脂的有机成分);
③常温下,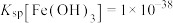 ;
;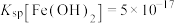 ;
; ;当溶液中某离子浓度小于等于
;当溶液中某离子浓度小于等于 时,可认为该离子沉淀完全;
时,可认为该离子沉淀完全;
④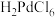 是一种二元强酸,
是一种二元强酸, 在溶液中存在配位平衡:
在溶液中存在配位平衡: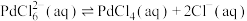
 ;
;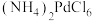 在水中溶解度小。
在水中溶解度小。
回答下列问题:
(1)废钯催化剂“焙烧”时,先通入空气进行逆流式焙烧,其主要目的是___________ ,再通入甲酸继续焙烧的目的是___________ 。
(2)“酸浸”过程需要升高温度至70℃左右,则主要反应的离子方程式为___________ ,实现浸取Pd的同时,还可能会存在的缺陷是___________ 。
(3)“洗脱”时,加入最佳“试剂Y”的名称是___________ ,“洗脱液”中要加入过量 的目的是
的目的是___________ 。
(4)“还原”过程中,不生成污染环境的气体,则被氧化的元素与被还原的元素物质的量之比为___________ 。“调pH”步骤中,若铁元素和铝元素浓度均为 ,则调pH的范围为
,则调pH的范围为___________ (lg2=0.3)。
 的工艺流程如图所示:
的工艺流程如图所示:
已知:①常温下,钯不溶于盐酸;Pd易被氧化为难溶于酸的
 而失去催化活性;
而失去催化活性;②阴、阳离子交换树脂的基本工作原理分别为
 、
、 (R—表示树脂的有机成分);
(R—表示树脂的有机成分);③常温下,
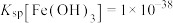 ;
;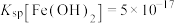 ;
; ;当溶液中某离子浓度小于等于
;当溶液中某离子浓度小于等于 时,可认为该离子沉淀完全;
时,可认为该离子沉淀完全;④
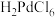 是一种二元强酸,
是一种二元强酸, 在溶液中存在配位平衡:
在溶液中存在配位平衡: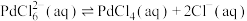
 ;
;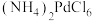 在水中溶解度小。
在水中溶解度小。回答下列问题:
(1)废钯催化剂“焙烧”时,先通入空气进行逆流式焙烧,其主要目的是
(2)“酸浸”过程需要升高温度至70℃左右,则主要反应的离子方程式为
(3)“洗脱”时,加入最佳“试剂Y”的名称是
 的目的是
的目的是(4)“还原”过程中,不生成污染环境的气体,则被氧化的元素与被还原的元素物质的量之比为
 ,则调pH的范围为
,则调pH的范围为
您最近半年使用:0次
名校
解题方法
5 . 下列实验操作、现象及相应结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 用pH 计测定浓度均为0.1mol/L的 、 、 溶液的酸碱性 溶液的酸碱性 |  溶液显碱性, 溶液显碱性, 溶液显酸性 溶液显酸性 | 可以确定 是弱酸,无法判断 是弱酸,无法判断 是否为弱酸 是否为弱酸 |
B | 铬酸钾溶液中存在平衡: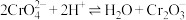 ,向铬酸钾溶液中加水稀释 ,向铬酸钾溶液中加水稀释 | 溶液黄色加深 | 平衡逆向移动 |
C | 向肉桂醛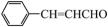 中加入溴水 中加入溴水 | 溴水溶液褪色 | 证明肉桂醛中含有碳碳双键 |
D | 取少量 溶液于试管中,先加入足量稀硝酸,再加足量 溶液于试管中,先加入足量稀硝酸,再加足量 溶液 溶液 | 有白色沉淀生成 | 证明 溶液已经被氧化变质 溶液已经被氧化变质 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
6 . 恒容密闭容器中发生反应
 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是A.室温下能自发进行,表明该反应的 |
| B.保持温度一定,充入氩气使反应速率加快 |
| C.加入合适的催化剂,既能改变反应历程又能降低活化能 |
D.其他条件一定,再通入适量 , , 和 和 的转化率都将增大 的转化率都将增大 |
您最近半年使用:0次
2024-02-29更新
|
76次组卷
|
2卷引用:四川省眉山市彭山区第一中学2023-2024学年高二下学期开学考试化学试题
解题方法
7 . 下列实验方案对应的实验操作、目的或现象均正确的是
| 选项 | 实验方案 | 现象或目的 |
| A. | 在一支试管中先加入2 mL 0.1 mol/L K2Cr2O7溶液,再滴入5~10滴6 mol/L H2SO4溶液 | 溶液橙色变深 |
| B. | 在试管中先加入2 mL 0.1 mol/L Na2CO3溶液,然后加热,利用pH传感器测量溶液pH | 溶液pH不断上升 |
| C. | 在盛有甲苯和苯酚混合溶液的试管中滴加少量酸性KMnO4溶液,溶液褪色 | 甲苯中含有苯酚 |
| D. | 向试管中先加C2H5CH2-X再加入NaOH溶液并加热,最后滴加AgNO3溶液 | 验证X为氯原子 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
8 . 利用某矿渣(含 )制备
)制备 的工艺流程如下:
的工艺流程如下:

已知:① ;
;
②
 。
。
回答下列问题:
(1)为提高焙烧效率可采取的操作有___________ (至少写两条,温度改变除外)。
(2)“滤液”中 元素的主要存在形式为
元素的主要存在形式为 ,“焙烧”时
,“焙烧”时 发生反应的化学方程式为
发生反应的化学方程式为___________ ;“滤渣”的主要成分为___________ 。
(3)“调 ”后溶液中
”后溶液中 的浓度是
的浓度是 ,则
,则 的浓度是
的浓度是___________  。
。
(4)在“转化”过程中淀粉水解液起___________ 作用。
(5)室温下,加入石灰乳调节 ,当
,当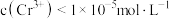 时,
时,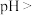
___________ 。
 )制备
)制备 的工艺流程如下:
的工艺流程如下:
已知:①
 ;
;②

 。
。回答下列问题:
(1)为提高焙烧效率可采取的操作有
(2)“滤液”中
 元素的主要存在形式为
元素的主要存在形式为 ,“焙烧”时
,“焙烧”时 发生反应的化学方程式为
发生反应的化学方程式为(3)“调
 ”后溶液中
”后溶液中 的浓度是
的浓度是 ,则
,则 的浓度是
的浓度是 。
。(4)在“转化”过程中淀粉水解液起
(5)室温下,加入石灰乳调节
 ,当
,当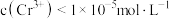 时,
时,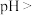
您最近半年使用:0次
2023-12-03更新
|
230次组卷
|
4卷引用:黑龙江省双鸭山市第一中学2023-2024学年高二下学期开学化学试题
名校
9 . 已知: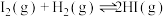
 ,下列说法错误的是
,下列说法错误的是
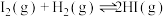
 ,下列说法错误的是
,下列说法错误的是| A.断键吸收的能量小于成键放出的能量 |
B.其它条件不变,升高温度,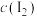 增大 增大 |
| C.其它条件不变,压缩体积加压,混合体系颜色不变 |
D.其它条件不变,增大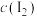 , , 的转化率增大 的转化率增大 |
您最近半年使用:0次
名校
解题方法
10 . 三氯化六氨合钴(III) 是一种典型的维尔纳配合物,实验室常以活性炭为催化剂来制备,化学方程式为
是一种典型的维尔纳配合物,实验室常以活性炭为催化剂来制备,化学方程式为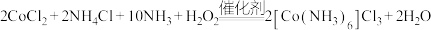 。
。
【配制氯化铵溶液】
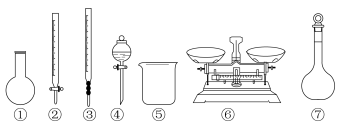
(1)实验欲用 固体配制
固体配制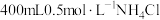 溶液,需要称取
溶液,需要称取 固体的质量为
固体的质量为_______ ;图中有四种仪器是不需要的,还需要的玻璃仪器除量筒以外还有_______ 。
【制备 】
】
设计小组设计如图装置(夹持仪器及加热装置已省略),回答下列问题:
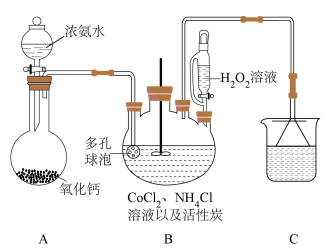
(2)装置A中发生反应的化学方程式为_______ 。
(3)装置B中盛放H2O2的实验仪器名称为_______ ,反应温度不宜超过50℃,除H2O2会分解外,另一原因是_______ 。
(4)装置C中漏斗的作用是_______ 。
(5)装置B中反应结束后,用冰水浴冷却后过滤,把沉淀溶解于沸水中,……,再慢慢加入适量浓盐酸于滤液中,有大量橙黄色 晶体析出。
晶体析出。
①除去活性炭的实验操作是_______ 。
②用平衡移动原理解释析出大量橙黄色晶体的原因:_______ 。
 是一种典型的维尔纳配合物,实验室常以活性炭为催化剂来制备,化学方程式为
是一种典型的维尔纳配合物,实验室常以活性炭为催化剂来制备,化学方程式为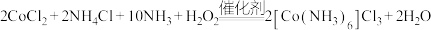 。
。【配制氯化铵溶液】

(1)实验欲用
 固体配制
固体配制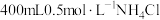 溶液,需要称取
溶液,需要称取 固体的质量为
固体的质量为【制备
 】
】设计小组设计如图装置(夹持仪器及加热装置已省略),回答下列问题:

(2)装置A中发生反应的化学方程式为
(3)装置B中盛放H2O2的实验仪器名称为
(4)装置C中漏斗的作用是
(5)装置B中反应结束后,用冰水浴冷却后过滤,把沉淀溶解于沸水中,……,再慢慢加入适量浓盐酸于滤液中,有大量橙黄色
 晶体析出。
晶体析出。①除去活性炭的实验操作是
②用平衡移动原理解释析出大量橙黄色晶体的原因:
您最近半年使用:0次



