1 . 回答下列问题
(1)能够使化学平衡移动的因素有________ 、________ 、________ 。
(2)可逆反应A(g)+2B(g) 2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡______ 移动(填正向、逆向、不),B的转化率_______ , v(正) ________ 。(填增大、减小、不变)。
(1)能够使化学平衡移动的因素有
(2)可逆反应A(g)+2B(g)
 2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
您最近半年使用:0次
名校
2 . 甲醇是重要的化工原料,发展前景广阔。研究表明, 加氢可以合成甲醇,反应如下:
加氢可以合成甲醇,反应如下: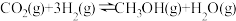
(1)反应的平衡常数表达式为K=___________ 。
(2)有利于提高平衡时 转化率的措施有
转化率的措施有___________ (填字母)。
a.使用催化剂
b.加压
c.增大 和H2的初始投料比
和H2的初始投料比
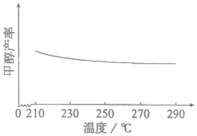
(3)研究温度对甲醇产率的影响时发现,在210~290℃,保持原料气中 和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
___________ 0(填“>”“=”或“<”),依据是___________ 。
 加氢可以合成甲醇,反应如下:
加氢可以合成甲醇,反应如下: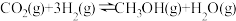
(1)反应的平衡常数表达式为K=
(2)有利于提高平衡时
 转化率的措施有
转化率的措施有a.使用催化剂
b.加压
c.增大
 和H2的初始投料比
和H2的初始投料比(3)研究温度对甲醇产率的影响时发现,在210~290℃,保持原料气中
 和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的

您最近半年使用:0次
2021-12-02更新
|
788次组卷
|
4卷引用:甘肃省白银市白银区大成学校2022-2023学年高二下学期开学考试(上期末)化学试题
名校
解题方法
3 . Ⅰ.磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为________ 。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
_______CuSO4+_______PH3+_______H2O=_______Cu3P↓+_______H3PO4+_______H2SO4_______
(3)工业制备PH3的流程如图所示。

①白磷和烧碱溶液反应的化学方程式为:_________________ 。
②若起始时有1 mol P4参加反应,则整个工业流程中共生成________ mol PH3。
II. 、
、 、
、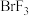 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是__________ 。
(2)溴化碘( )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为_______ ;
(3)已知某些离子的还原性强弱顺序为 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_________ ;
(1)AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
_______CuSO4+_______PH3+_______H2O=_______Cu3P↓+_______H3PO4+_______H2SO4
(3)工业制备PH3的流程如图所示。

①白磷和烧碱溶液反应的化学方程式为:
②若起始时有1 mol P4参加反应,则整个工业流程中共生成
II.
 、
、 、
、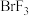 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是
(2)溴化碘(
 )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为(3)已知某些离子的还原性强弱顺序为
 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
您最近半年使用:0次
4 . I.等物质的量的A、B、C、D四种物质混合,发生如下反应:aA(?)+bB(?) cC(s)+dD(?),当反应达到平衡时,测得A减少nmol,B减少
cC(s)+dD(?),当反应达到平衡时,测得A减少nmol,B减少 mol,C增加
mol,C增加 mol,D增加nmol。
mol,D增加nmol。
(1)该反应的各系数a=_________ ,b=________ ,c=________ ,d=________ 。
(2)若只改变压强,反应速率发生变化,但平衡不移动,该反应中物质的聚集状是A_____________ 态、B_____________ 态、D_____________ 态。
(3)若只升高温度,反应一段时间后,测得四种物质的量又达到相等,则ΔH__________ 0。(填“>”、“<”)
II.在一定条件下,xA+yB⇌zC的可逆反应达到平衡,
(4)已知A、B、C均为气体,在减压后平衡向逆反应方向移动,则x、y、z的关系是__________ .
(5)已知C是气体且x+y=z,在加压时如果平衡发生移动,则平衡必向__________ 方向移动.(填“正反应”或“逆反应”)
(6)已知B、C是气体,现增加A的物质的量(其他条件不变),平衡不移动,则A是__________ 态.
 cC(s)+dD(?),当反应达到平衡时,测得A减少nmol,B减少
cC(s)+dD(?),当反应达到平衡时,测得A减少nmol,B减少 mol,C增加
mol,C增加 mol,D增加nmol。
mol,D增加nmol。(1)该反应的各系数a=
(2)若只改变压强,反应速率发生变化,但平衡不移动,该反应中物质的聚集状是A
(3)若只升高温度,反应一段时间后,测得四种物质的量又达到相等,则ΔH
II.在一定条件下,xA+yB⇌zC的可逆反应达到平衡,
(4)已知A、B、C均为气体,在减压后平衡向逆反应方向移动,则x、y、z的关系是
(5)已知C是气体且x+y=z,在加压时如果平衡发生移动,则平衡必向
(6)已知B、C是气体,现增加A的物质的量(其他条件不变),平衡不移动,则A是
您最近半年使用:0次
5 . 现有反应:mA(g) + nB(g)⇌pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为________ 热反应,且m+n_____ p(填>、=、<)。
(2)若加入B(体积不变),则A的转化率_________ ,B的转化率_________ 。(填增大、减小或不变)
(3)若升高温度,则平衡时B、C的浓度之比将_________ 。(填增大、减小或不变)
(4) 若加入催化剂,平衡时气体混合物的总物质的量_________ 。(填增大、减小或不变)
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______ ,而维持容器内压强不变,充入氖气时,混合物颜色_______ (填变深、变浅或不变)。
(1)该反应的逆反应为
(2)若加入B(体积不变),则A的转化率
(3)若升高温度,则平衡时B、C的浓度之比将
(4) 若加入催化剂,平衡时气体混合物的总物质的量
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色
您最近半年使用:0次
6 . 在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系:Cr2O72-+H2O 2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液是橙色的。
2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液是橙色的。
(1)向上述溶液中加入NaOH溶液,溶液呈__________ 色,因为_________ 。
(2)向已加入NaOH溶液的1中再加入过量稀硫酸,则溶液呈__________ 色,因为__________ 。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡____________________ ,溶液颜色将____________________ 。
 2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液是橙色的。
2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液是橙色的。(1)向上述溶液中加入NaOH溶液,溶液呈
(2)向已加入NaOH溶液的1中再加入过量稀硫酸,则溶液呈
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡
您最近半年使用:0次
2019-12-02更新
|
89次组卷
|
10卷引用:2016-2017学年甘肃省兰州一中高二上期中理化学试卷
2016-2017学年甘肃省兰州一中高二上期中理化学试卷(已下线)2012-2013学年辽宁省辽河油田第二高中高一下学期期末考试化学试卷【校级联考】安徽省滁州市定远县西片区2018-2019学年高二上学期期中考试化学试题河北省石家庄市普通高中2019-2020学年高二10月月考化学(高考)试题安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题海南省海南鑫源高级中学2019-2020学年高二上学期期末考试化学试题(已下线)2.3.1 浓度、压强变化对化学平衡的影响(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)作业(十一) 温度、浓度对化学平衡的影响第二章 化学反应速率与化学平衡 第二节 化学平衡 第3课时 影响化学平衡的因素
名校
7 . 现有反应aA(g)+bB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应是________ 热反应,且a+b________ p(填“>”“<”或“=”)。
(2)减压时,A的质量分数________ (填“增大”“减小”或“不变”,下同),正反应速率________ 。
(3)若加入B(体积不变),则A的转化率________ ,B的转化率________ 。
(4)若升高温度,则平衡时,B、C的浓度之比c(B)/c(C) 将________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量________ 。
(6)若B是有色物质, A、C均为无色物质,则加入C(体积不变)时混合物的颜色________ ,而维持容器内气体的压强不变,充入氖气时,混合物的颜色________ 。(填“变浅”“变深”或“不变”)
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应的逆反应是
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若升高温度,则平衡时,B、C的浓度之比c(B)/c(C) 将
(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若B是有色物质, A、C均为无色物质,则加入C(体积不变)时混合物的颜色
您最近半年使用:0次
2018-11-30更新
|
234次组卷
|
4卷引用:甘肃省白银市靖远县第四中学2018-2019学年高二上学期期中考试化学试题
名校
解题方法
8 . 红矾钠(Na2Cr2O7·2H2O)是重要的化工原料,工业上用铬铁矿(主要成分是FeO·Cr2O3)制备红矾钠的过程中会发生如下反应:
4FeO(s)+4Cr2O3(s)+8Na2CO3(s)+7O2(g) 8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ΔH<0
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ΔH<0
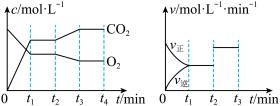
(1)如图为上述反应的浓度—时间图象,由图象判断反应进行至t2时刻时,改变的条件是_________________________ ,如图为上述反应的速率—时间图象,表示上述反应在t1时达到平衡, 在t2时因改变某个条件而使曲线发生变化。由图判断,t2时刻曲线变化的原因可能是________ (填写序号)。
a.升高温度 b.加催化剂
c.通入O2 d.缩小容器体积
(2)工业上可利用上述反应的副产物CO2来生产甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
①一定温度下,在容积为1L的密闭容器中,充入2 mol CO2和4 mol H2,一段时间后达到平衡,测得CH3OH的物质的量浓度为1mol/L,则该温度下此反应的平衡常数为_________ ,某时刻测得CO2、H2、CH3OH和H2O的物质的量分别为2mol,1mol,1mol,1mol,则这一时刻v(正)___________ v(逆)
②在T1温度时,将1 mol CO2和3 mol H2充入一密闭容器中,充分反应达到平衡后,CO2转化率为α,则容器内的压强与起始压强之比为_______________ 。
4FeO(s)+4Cr2O3(s)+8Na2CO3(s)+7O2(g)
 8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ΔH<0
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ΔH<0(1)如图为上述反应的浓度—时间图象,由图象判断反应进行至t2时刻时,改变的条件是
a.升高温度 b.加催化剂
c.通入O2 d.缩小容器体积

(2)工业上可利用上述反应的副产物CO2来生产甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。①一定温度下,在容积为1L的密闭容器中,充入2 mol CO2和4 mol H2,一段时间后达到平衡,测得CH3OH的物质的量浓度为1mol/L,则该温度下此反应的平衡常数为
②在T1温度时,将1 mol CO2和3 mol H2充入一密闭容器中,充分反应达到平衡后,CO2转化率为α,则容器内的压强与起始压强之比为
您最近半年使用:0次
2018-11-09更新
|
84次组卷
|
2卷引用:【全国百强校】甘肃省会宁县第一中学2018-2019学年高二(理科)上学期期中考试化学试题
名校
9 . 在水溶液中橙红色的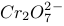 与黄色的
与黄色的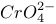 有下列平衡关系:
有下列平衡关系:

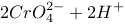 ,把重铬酸钾(
,把重铬酸钾( )溶于水配成稀溶液是橙色的。
)溶于水配成稀溶液是橙色的。
(1)向上述溶液中加入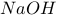 溶液,溶液呈
溶液,溶液呈__________ 色,因为_________ 。
(2)向已加入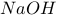 溶液的1中再加入过量稀硫酸,则溶液呈
溶液的1中再加入过量稀硫酸,则溶液呈__________ 色,因为__________ 。
(3)向原溶液中加入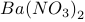 溶液(已知
溶液(已知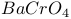 为黄色沉淀)则平衡
为黄色沉淀)则平衡________ ,溶液颜色将________ 。
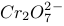 与黄色的
与黄色的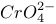 有下列平衡关系:
有下列平衡关系:

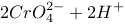 ,把重铬酸钾(
,把重铬酸钾( )溶于水配成稀溶液是橙色的。
)溶于水配成稀溶液是橙色的。(1)向上述溶液中加入
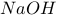 溶液,溶液呈
溶液,溶液呈(2)向已加入
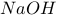 溶液的1中再加入过量稀硫酸,则溶液呈
溶液的1中再加入过量稀硫酸,则溶液呈(3)向原溶液中加入
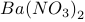 溶液(已知
溶液(已知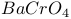 为黄色沉淀)则平衡
为黄色沉淀)则平衡
您最近半年使用:0次
10 . 现有反应mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
(1)该反应的逆反应是________ 热反应,且m+n______ (填“>”“<”或“=”)p。
(2)减压时,A的质量分数________ (填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则A的转化率________ ,B的转化率________ 。
(4)若升高温度,则平衡时,B、C的浓度之比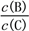 将
将________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则(1)该反应的逆反应是
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若升高温度,则平衡时,B、C的浓度之比
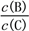 将
将
您最近半年使用:0次



