解题方法
1 . K2Cr2O7溶液中存在平衡: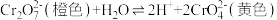 。
。
(1)向2mL0.1mol/LK2Cr2O7溶液中滴加5滴6mol/LNaOH溶液。可观察到的现象是_______ ;得出的结论是:_______ 。
(2)向上述溶液中再滴加10滴6mol/LH2SO4溶液。可观察到的现象是_______ ;得出的结论是_______ 。
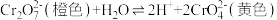 。
。(1)向2mL0.1mol/LK2Cr2O7溶液中滴加5滴6mol/LNaOH溶液。可观察到的现象是
(2)向上述溶液中再滴加10滴6mol/LH2SO4溶液。可观察到的现象是
您最近半年使用:0次
2 . 探究外界条件变化化学平衡的影响。向一密闭容器中通入1 mol N2、3 mol H2发生反应N2(g)+3H2(g) 2NH3(g) ΔH<0,一段时间后达到平衡。
2NH3(g) ΔH<0,一段时间后达到平衡。
(1)若增大N2的浓度,平衡移动的方向是_____________ ;达新平衡时,氮气的浓度与改变时相比较,其变化是________ 。
(2)若升高温度,平衡移动的方向是__________ ;达新平衡时的温度与改变时相比较,其变化是________ 。
(3)若增大压强,平衡移动的方向是__________ ;达新平衡时的压强与改变时相比较,其变化是________ 。
 2NH3(g) ΔH<0,一段时间后达到平衡。
2NH3(g) ΔH<0,一段时间后达到平衡。(1)若增大N2的浓度,平衡移动的方向是
(2)若升高温度,平衡移动的方向是
(3)若增大压强,平衡移动的方向是
您最近半年使用:0次
2023-07-15更新
|
68次组卷
|
2卷引用:陕西省渭南市蒲城县蒲城中学2023-2024学年高二上学期期中考试化学试题
名校
3 . 现有反应mA(g)+nB(g)⇌pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
(1)m+n_______ (填“>”“<”或“=”)p。
(2)减压时,A的质量分数_______ (填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则B的转化率_______ 。
(4)若升高温度,则平衡时,B、C的浓度之比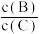 将
将_______ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量_______ 。
(6)若反应体系平衡后,再加入C(体积不变),则B的体积分数_______ ,而维持容器内气体的压强不变,充入氖气时,混合物的颜色_______ (填“变浅”“变深”或“不变”)。
(1)m+n
(2)减压时,A的质量分数
(3)若加入B(体积不变),则B的转化率
(4)若升高温度,则平衡时,B、C的浓度之比
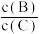 将
将(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若反应体系平衡后,再加入C(体积不变),则B的体积分数
您最近半年使用:0次
4 . I、在水溶液中橙色的Cr2O 与黄色的CrO
与黄色的CrO 有平衡关系: Cr2O
有平衡关系: Cr2O + H2O
+ H2O 2CrO
2CrO + 2H+,把重铬酸钾溶于水配成稀溶液呈橙色。
+ 2H+,把重铬酸钾溶于水配成稀溶液呈橙色。
(1)向上述溶液中加入NaOH溶液,则平衡___________ (向左移或向右移),溶液呈___________ 色。
(2)向已加入NaOH溶液的溶液中再加入过量稀硫酸,则溶液应是___________ 色,因为___________ 。
(3)向原溶液中加入硝酸钡溶液(已知BaCrO4为黄色沉淀),则平衡___________ (向左移或向右移),溶液颜色将___________ 。
II、 在一定条件下,反应xA 十yB zC达到平衡。
zC达到平衡。
(4)若A、B、C都是气体,在增压后平衡向逆反应方向移动,则x、,y、,z之间的关系是___________ 。
(5)若C是气体,且x + y=z,增大压强如果平衡发生移动,则A的转化率将___________ (填“增大”、“减小”或“不变”)
 与黄色的CrO
与黄色的CrO 有平衡关系: Cr2O
有平衡关系: Cr2O + H2O
+ H2O 2CrO
2CrO + 2H+,把重铬酸钾溶于水配成稀溶液呈橙色。
+ 2H+,把重铬酸钾溶于水配成稀溶液呈橙色。(1)向上述溶液中加入NaOH溶液,则平衡
(2)向已加入NaOH溶液的溶液中再加入过量稀硫酸,则溶液应是
(3)向原溶液中加入硝酸钡溶液(已知BaCrO4为黄色沉淀),则平衡
II、 在一定条件下,反应xA 十yB
 zC达到平衡。
zC达到平衡。(4)若A、B、C都是气体,在增压后平衡向逆反应方向移动,则x、,y、,z之间的关系是
(5)若C是气体,且x + y=z,增大压强如果平衡发生移动,则A的转化率将
您最近半年使用:0次
5 . 铬是硬度最高的金属,具有良好的抗腐蚀性的耐磨性,常用于制造不锈钢和仪器仪表的金属表面镀铬,用途十分广泛。
(1)铬的常见的氧化——三氧化二铬( ),既能与KOH溶液反应生成
),既能与KOH溶液反应生成 ,又能与硫酸反应生成
,又能与硫酸反应生成 。
。 是
是___________ (填“酸性”“碱性”或“两性”)氧化物, 与过量KOH溶液反应的离子方程式为
与过量KOH溶液反应的离子方程式为___________ 。
(2)已知: ,Cr(Ⅲ)体现还原性生成
,Cr(Ⅲ)体现还原性生成 或
或 。在碱性介质中Cr(Ⅲ)有较强的还原性,可使
。在碱性介质中Cr(Ⅲ)有较强的还原性,可使 —淀粉溶液褪色,反应过程中铬元素由
—淀粉溶液褪色,反应过程中铬元素由___________ 转化为___________ (填离子符号);在酸性介质中Cr(Ⅲ)还原性较差,可与强氧化剂反应,可将 还原为
还原为 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(3) 中铬元素的化合价为
中铬元素的化合价为___________ ;将 溶液滴加到淀粉——KI溶液中,溶液变蓝;可使
溶液滴加到淀粉——KI溶液中,溶液变蓝;可使 、
、 和
和 在不同酸碱性条件下氧化性的大小关系是
在不同酸碱性条件下氧化性的大小关系是___________ 。
(1)铬的常见的氧化——三氧化二铬(
 ),既能与KOH溶液反应生成
),既能与KOH溶液反应生成 ,又能与硫酸反应生成
,又能与硫酸反应生成 。
。 是
是 与过量KOH溶液反应的离子方程式为
与过量KOH溶液反应的离子方程式为(2)已知:
 ,Cr(Ⅲ)体现还原性生成
,Cr(Ⅲ)体现还原性生成 或
或 。在碱性介质中Cr(Ⅲ)有较强的还原性,可使
。在碱性介质中Cr(Ⅲ)有较强的还原性,可使 —淀粉溶液褪色,反应过程中铬元素由
—淀粉溶液褪色,反应过程中铬元素由 还原为
还原为 ,其反应的离子方程式为
,其反应的离子方程式为(3)
 中铬元素的化合价为
中铬元素的化合价为 溶液滴加到淀粉——KI溶液中,溶液变蓝;可使
溶液滴加到淀粉——KI溶液中,溶液变蓝;可使 、
、 和
和 在不同酸碱性条件下氧化性的大小关系是
在不同酸碱性条件下氧化性的大小关系是
您最近半年使用:0次
6 . (1)向盛有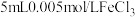 溶液的试管中加入
溶液的试管中加入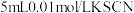 溶液,溶液呈红色。在这个反应体系中存在下述平衡:
溶液,溶液呈红色。在这个反应体系中存在下述平衡: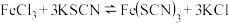
①向上述平衡体系中加入5滴浓的 溶液,溶液颜色
溶液,溶液颜色______ (填“变深”“变浅”或“不变”)。
②向上述平衡体系中加入少量 固体,溶液颜色
固体,溶液颜色______ (填“变深”“变浅”或“不变”)。
(2)氨是一种重要的化工原料,合成氨的反应: ,反应过程如图所示:
,反应过程如图所示:
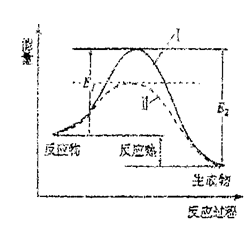
①

______ (用含 、
、 的式子表示)。
的式子表示)。
②加催化剂的曲线______ (填“Ⅰ”或“Ⅱ”)。
③在一定条件下,能说明反应 一定达到平衡的是
一定达到平衡的是______ (填字母代号)。
A.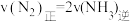
B.单位时间内消耗 的同时消耗
的同时消耗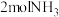
C.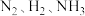 的物质的量之比为
的物质的量之比为
D.混合气体中 保持不变
保持不变
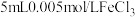 溶液的试管中加入
溶液的试管中加入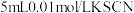 溶液,溶液呈红色。在这个反应体系中存在下述平衡:
溶液,溶液呈红色。在这个反应体系中存在下述平衡: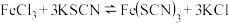
①向上述平衡体系中加入5滴浓的
 溶液,溶液颜色
溶液,溶液颜色②向上述平衡体系中加入少量
 固体,溶液颜色
固体,溶液颜色(2)氨是一种重要的化工原料,合成氨的反应:
 ,反应过程如图所示:
,反应过程如图所示:
①


 、
、 的式子表示)。
的式子表示)。②加催化剂的曲线
③在一定条件下,能说明反应
 一定达到平衡的是
一定达到平衡的是A.
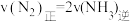
B.单位时间内消耗
 的同时消耗
的同时消耗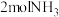
C.
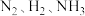 的物质的量之比为
的物质的量之比为
D.混合气体中
 保持不变
保持不变
您最近半年使用:0次
7 . 在一个2L的恒容密闭容器中,加入3molA和1molB发生如下反应:3A(g)+B(g) 2C(g)+3D(?)。5min后达到平衡,C的浓度为0.6mol·L-1。达到平衡后,当升高温度时,A的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
2C(g)+3D(?)。5min后达到平衡,C的浓度为0.6mol·L-1。达到平衡后,当升高温度时,A的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的正反应是___ 反应(填“吸热”或“放热”),D的状态是__ (填“气态”或“非气态”)。
(2)达到平衡时,A的转化率为___ ,此温度下的平衡常数K=__ (保留两位小数)。
(3)若加入适量B,则A的转化率将__ (填“增大”“减小”或“不变”,下同),化学平衡常数将__ 。
 2C(g)+3D(?)。5min后达到平衡,C的浓度为0.6mol·L-1。达到平衡后,当升高温度时,A的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
2C(g)+3D(?)。5min后达到平衡,C的浓度为0.6mol·L-1。达到平衡后,当升高温度时,A的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的正反应是
(2)达到平衡时,A的转化率为
(3)若加入适量B,则A的转化率将
您最近半年使用:0次
8 . 甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。__ PB(填“>、<、=”)。
②A、B、C三点的平衡常数KA,KB,KC的大小关系是__ 。
③下列叙述能说明上述反应能达到化学平衡状态的是__ (填代号)。
a.H2的消耗速率是CH3OH消耗速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,该反应的平衡常数K=__ ,再加入1.0molCO后重新到达平衡,则CO的转化率__ (填“增大,不变或减小”)。
(3)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)__ v(逆)(填“>、<或=”)。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。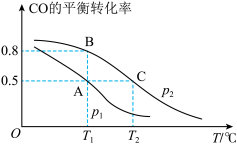
②A、B、C三点的平衡常数KA,KB,KC的大小关系是
③下列叙述能说明上述反应能达到化学平衡状态的是
a.H2的消耗速率是CH3OH消耗速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,该反应的平衡常数K=
(3)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)
您最近半年使用:0次
2020-10-19更新
|
182次组卷
|
21卷引用:陕西省宝鸡市金台区2019-2020学年高二上学期期中检测化学试题
陕西省宝鸡市金台区2019-2020学年高二上学期期中检测化学试题陕西省西安市长安区2023-2024学年高二上学期10月份月考化学试题【校级联考】福建省福州市八县(市)协作校2018-2019学年高二上学期期末联考化学试题黑龙江省双鸭山市第一中学2019-2020学年高二上学期第一次月考化学试题湖北省随州市曾都一中2020-2021学年高二上学期9月月考化学试题河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学(实验班)试题内蒙古包头市第一中学2020-2021学年高二上学期第一次月考化学试题山东省惠民县第二中学致远部2020-2021学年高二上学期10月月考化学试题内蒙古通辽市开鲁县第一中学2021届高三上学期第二次阶段性考试化学试题重庆市铁路中学校2020-2021学年高二上学期11月月考化学试题重庆育才中学2021-2022学年高二上学期第四次定时练习化学试题湖南师范大学附属中学2022-2023学年高二上学期期中考试化学试题四川省广安代市中学校2021-2022学年高二上学期9月考化学试题湖南省怀化市第三中学2022-2023学年高二上学期期中考试化学试题江西省永修县第一中学2023-2024学年高二上学期开学考试化学试题河南省濮阳市2023-2024学年高二上学期9月月考化学试题江西省宜春市宜丰中学2023-2024学年高二上学期开学考试化学试题四川省仁寿第一中学校(北校区)2023-2024学年高二上学期10月月考化学试题海南省琼海市嘉积中学2023-2024学年高二上学期第一次月考化学试题四川省泸州市泸县第四中学2023-2024学年高二上学期12月月考化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题
9 . 研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
2NO(g)+Cl2(g) 2NOCl(g) K2 ΔH2<0 (Ⅱ)
2NOCl(g) K2 ΔH2<0 (Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________ (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(NOCl)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=________ mol,NO的转化率α1=________ 。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2________ α1(填“>”“<”或“=”),平衡常数K2________ (填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是____________ 。
2NO2(g)+NaCl(s)
 NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)2NO(g)+Cl2(g)
 2NOCl(g) K2 ΔH2<0 (Ⅱ)
2NOCl(g) K2 ΔH2<0 (Ⅱ)(1)4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(NOCl)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=
您最近半年使用:0次
2018-09-26更新
|
235次组卷
|
10卷引用:陕西省城固县第一中学2019届高三上学期第一次月考化学试题
陕西省城固县第一中学2019届高三上学期第一次月考化学试题2015-2016学年北京大学附属中学分校高二上抽考化学试卷2015-2016学年河北省望都中学高二上学期第二次月考化学试卷2015-2016学年贵州省思南中学高二上二次月考化学试卷湖南省岳阳市第一中学2018届高三12月月考化学试题(已下线)2018年9月22日 《每日一题》人教选修4-周末培优(已下线)2018年9月28日《每日一题》一轮复习化学平衡常数和转化率(已下线)2019年9月27日 《每日一题》2020年高考一轮复习-化学平衡常数和转化率江西省新余市分宜中学2019-2020学年高二上学期第一次段考化学试题广东名校联盟(广州二中,珠海一中,中山纪中)2019-2020学年高二上学期期中考试化学试题
名校
解题方法
10 . 尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)工业上用CO2和NH3在一定条件下合成,其反应方程式__________ 。
(2)在一个2L的密闭容器内,当起始投入量氨碳比 ,CO2的转化率随时间的变化关系如下图所示。
,CO2的转化率随时间的变化关系如下图所示。
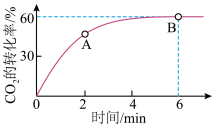
① A点的逆反应速率v逆(CO2)__________________ B点的正反应速率为v正(CO2)(填“大于”、“小于”或“等于”)
②假设氨的起始投入量为8mol,求从开始到达到平衡状态这段时间内v(NH3)=_________________ 。
③NH3的平衡转化率为____________________ 。
④单纯从制备的成本角度考虑,我们希望氨碳比 尽可能
尽可能__________ (“大”、“小”)因为_________ 。
(1)工业上用CO2和NH3在一定条件下合成,其反应方程式
(2)在一个2L的密闭容器内,当起始投入量氨碳比
 ,CO2的转化率随时间的变化关系如下图所示。
,CO2的转化率随时间的变化关系如下图所示。
① A点的逆反应速率v逆(CO2)
②假设氨的起始投入量为8mol,求从开始到达到平衡状态这段时间内v(NH3)=
③NH3的平衡转化率为
④单纯从制备的成本角度考虑,我们希望氨碳比
 尽可能
尽可能
您最近半年使用:0次
2017-08-21更新
|
326次组卷
|
2卷引用:陕西省武功县普集高级中学2023-2024学年高二上学期10月月考化学试题



