名校
1 . 相同条件下,草酸根(C2O )的还原性强于Fe2+。为检验这一结论,进行以下实验:
)的还原性强于Fe2+。为检验这一结论,进行以下实验:
资料:i.工业上,向炽热铁屑中通入氯化氢生产无水氯化亚铁。
ii.K3[Fe(C2O4)3]・3H2O(三草酸合铁酸钾)为亮绿色晶体,光照易分解。其水溶液中存在[Fe(C2O4)3]3- Fe3++3C2O
Fe3++3C2O K=6.3×10-21
K=6.3×10-21
(实验1)用以下装置制取无水氯化亚铁

(1)仪器a的名称为___________ ,B的作用为___________ 。
(2)欲制得纯净的FeCl2,实验过程中点燃A、C酒精灯的先后顺序是___________ 。
(3)D中用NaOH溶液进行尾气处理,存在的问题是___________ 、___________ 。
(实验2)通过Fe3+和C2O 在溶液中的反应比较Fe2+和C2O
在溶液中的反应比较Fe2+和C2O 的还原性强弱。
的还原性强弱。
(4)取实验2中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是___________ 。
(5)经检验,亮绿色晶体为K3Fe(C2O4)3・3H2O。设计实验,确认实验2中没有发生氧化还原反应的操作和现象是___________ 。
(6)取实验2中的亮绿色溶液光照一段时间,产生黄色浑浊且有气泡产生。补全反应的离子方程式:___________ [Fe(C2O4)3]3-
___________ FeC2O4↓+___________ ↑+___________
(实验3)又设计以下装置直接比较Fe2+和C2O 的还原性强弱,并达到了预期的目的。
的还原性强弱,并达到了预期的目的。
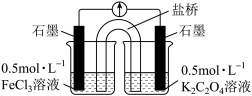
(7)描述达到预期目的可能产生的现象:___________ 。
 )的还原性强于Fe2+。为检验这一结论,进行以下实验:
)的还原性强于Fe2+。为检验这一结论,进行以下实验:资料:i.工业上,向炽热铁屑中通入氯化氢生产无水氯化亚铁。
ii.K3[Fe(C2O4)3]・3H2O(三草酸合铁酸钾)为亮绿色晶体,光照易分解。其水溶液中存在[Fe(C2O4)3]3-
 Fe3++3C2O
Fe3++3C2O K=6.3×10-21
K=6.3×10-21(实验1)用以下装置制取无水氯化亚铁

(1)仪器a的名称为
(2)欲制得纯净的FeCl2,实验过程中点燃A、C酒精灯的先后顺序是
(3)D中用NaOH溶液进行尾气处理,存在的问题是
(实验2)通过Fe3+和C2O
 在溶液中的反应比较Fe2+和C2O
在溶液中的反应比较Fe2+和C2O 的还原性强弱。
的还原性强弱。操作 | 现象 |
| 在避光处,向10mL 0.5 mol·L-1FeCl3溶液中缓慢加入0.5 mol·L-1K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤 | 得到亮绿色溶液和亮绿色晶体 |
(5)经检验,亮绿色晶体为K3Fe(C2O4)3・3H2O。设计实验,确认实验2中没有发生氧化还原反应的操作和现象是
(6)取实验2中的亮绿色溶液光照一段时间,产生黄色浑浊且有气泡产生。补全反应的离子方程式:

(实验3)又设计以下装置直接比较Fe2+和C2O
 的还原性强弱,并达到了预期的目的。
的还原性强弱,并达到了预期的目的。
(7)描述达到预期目的可能产生的现象:
您最近一年使用:0次
2020-12-11更新
|
1229次组卷
|
4卷引用:黑龙江省哈尔滨市第三中学2021届高三上学期第四次验收考试化学试题
黑龙江省哈尔滨市第三中学2021届高三上学期第四次验收考试化学试题黑龙江省哈尔滨市第九中学2021届高三上学期第四次验收化学试卷(已下线)培优01 无机制备类实验 基础训练-2021年高考化学大题培优练(新高考地区专用)重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题
名校
解题方法
2 . 某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:

已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2 2CuO+TeO2。
2CuO+TeO2。
(1)煅烧时,Cr2O3发生反应的化学方程式为_________ 。
(2)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有____ (填化学式)。
(3)用平衡移动原理解释酸化过程中可以得到Na2Cr2O7溶液________________ ,写出还原过程中的化学反应方程式_______________ ,此工艺流程中可以循环利用的物质___________ 。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50 g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定。(已知Cr2O 被还原为Cr3+)
被还原为Cr3+)
①氧化还原滴定过程中的离子方程式为___________ 。
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00 mL,则所得产品中K2Cr2O7的纯度为__________ 。[已知M(K2Cr2O7)=294 g·mol-1]

已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2
 2CuO+TeO2。
2CuO+TeO2。(1)煅烧时,Cr2O3发生反应的化学方程式为
(2)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有
(3)用平衡移动原理解释酸化过程中可以得到Na2Cr2O7溶液
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50 g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定。(已知Cr2O
 被还原为Cr3+)
被还原为Cr3+)①氧化还原滴定过程中的离子方程式为
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00 mL,则所得产品中K2Cr2O7的纯度为
您最近一年使用:0次
3 . 碳酸钴( )是一种红色粉末,主要用作催化剂、选矿剂和陶瓷釉.以含钴废料 (主要成分为
)是一种红色粉末,主要用作催化剂、选矿剂和陶瓷釉.以含钴废料 (主要成分为 、
、 还含少量
还含少量 、Zn等杂质)为原料制备
、Zn等杂质)为原料制备 的一种工艺如下:
的一种工艺如下:

常温下,Ksp[Al(OH)3]≈1.0×10-34。
回答下列问题:
(1)“酸浸”前常将含钴废料粉碎,其主要目的是__________________ 。
(2)“还原”过程中还原 理论上需消耗
理论上需消耗 的体积为
的体积为___________ L(标准状况)。
(3)已知“萃取” 的原理为
的原理为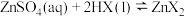 (有机层)
(有机层)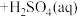 ,从有机层中获得
,从有机层中获得 溶液的操作是加入
溶液的操作是加入____________ (填试剂名称),其作用是__________________ (从平衡移动原理角度分析)。
(4)常温下“除铝”过程中,调节 为5.0时,溶液中c(Al3+)=
为5.0时,溶液中c(Al3+)=_____________ 。
(5)“沉钴”中,其他条件相同时, 产品纯度与
产品纯度与 溶液浓度、反应温度的关系如图所示,
溶液浓度、反应温度的关系如图所示,
__________ (填“>”或“<”) 。
。

 )是一种红色粉末,主要用作催化剂、选矿剂和陶瓷釉.以含钴废料 (主要成分为
)是一种红色粉末,主要用作催化剂、选矿剂和陶瓷釉.以含钴废料 (主要成分为 、
、 还含少量
还含少量 、Zn等杂质)为原料制备
、Zn等杂质)为原料制备 的一种工艺如下:
的一种工艺如下:
常温下,Ksp[Al(OH)3]≈1.0×10-34。
回答下列问题:
(1)“酸浸”前常将含钴废料粉碎,其主要目的是
(2)“还原”过程中还原
 理论上需消耗
理论上需消耗 的体积为
的体积为(3)已知“萃取”
 的原理为
的原理为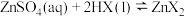 (有机层)
(有机层)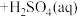 ,从有机层中获得
,从有机层中获得 溶液的操作是加入
溶液的操作是加入(4)常温下“除铝”过程中,调节
 为5.0时,溶液中c(Al3+)=
为5.0时,溶液中c(Al3+)=(5)“沉钴”中,其他条件相同时,
 产品纯度与
产品纯度与 溶液浓度、反应温度的关系如图所示,
溶液浓度、反应温度的关系如图所示,
 。
。
您最近一年使用:0次
2020-11-06更新
|
133次组卷
|
2卷引用:黑吉两省十校2020-2021学年高二上学期期中联考(其他8校用)化学试题
名校
解题方法
4 . 氮是地球上含量较丰富的一种元素,氮的化合物在工业生产和生活中有重要的作用。
I.已知298K时,发生反应:N2O4(g) 2NO2(g)△H>0
2NO2(g)△H>0
(1)在密闭容器内,一定条件下该反应达到平衡,当分别改变下列条件时,填写下列空白:
①达到平衡时,升高温度,平衡将________ 移动。(填“正向”、“逆向”或“不”)
②达到平衡时,充入Ar气,并保持体积不变,平衡将_________ 移动。(填“正向”、“逆向"或“不”)
③保持容器容积不变,再通入一定量N2O4,,达到平衡时NO2的百分含量________ (填“增大”“减小”或“不变”,下同)。
④保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时N2O4的转化率_____ 。
(2)恒容密闭容器中发生上述反应,已知v正=k正·p(N2O4),v逆=k逆·p2(NO2),Kp=__________ (用k正、k逆表示)。若初始压强为100kPa,k正=2.7×104s-1,当NO2的物质的量分数为50%时,v正=_________ kPa·s-1。[其中Kp为平衡常数,用平衡分压代替平衡浓度计算,p(N2O4)和p(NO2)分别是N2O4和NO2的分压,分压=p总×物质的量分数,k正、k逆为速率常数]
II.在催化剂作用下,H2可以还原NO消除污染,反应为:2NO(g)+2H2(g) N2(g)+2H2O(g)△H=-664kJ/mol
N2(g)+2H2O(g)△H=-664kJ/mol
(3)将2molNO和1molH2充入一个恒容的密闭容器中,经相同时间测得N2的体积分数与温度的关系如图所示。

低于900K时,N2的体积分数_______ (填“是”或“不是")对应温度下平衡时的体积分数,原因是_______________________________ 。高于900K时,Nz的体积分数降低的可能原因是__________________________________________________________ (答出两点)。
I.已知298K时,发生反应:N2O4(g)
 2NO2(g)△H>0
2NO2(g)△H>0(1)在密闭容器内,一定条件下该反应达到平衡,当分别改变下列条件时,填写下列空白:
①达到平衡时,升高温度,平衡将
②达到平衡时,充入Ar气,并保持体积不变,平衡将
③保持容器容积不变,再通入一定量N2O4,,达到平衡时NO2的百分含量
④保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时N2O4的转化率
(2)恒容密闭容器中发生上述反应,已知v正=k正·p(N2O4),v逆=k逆·p2(NO2),Kp=
II.在催化剂作用下,H2可以还原NO消除污染,反应为:2NO(g)+2H2(g)
 N2(g)+2H2O(g)△H=-664kJ/mol
N2(g)+2H2O(g)△H=-664kJ/mol(3)将2molNO和1molH2充入一个恒容的密闭容器中,经相同时间测得N2的体积分数与温度的关系如图所示。

低于900K时,N2的体积分数
您最近一年使用:0次
5 . 某小组同学对FeCl3与KI的反应进行探究。
【初步探究】室温下进行下表所列实验。
(1)证明实验Ⅰ中有Fe2+ 生成,加入的试剂为____________________________ 。
(2)写出实验Ⅰ反应的离子方程式:_____________________________________ 。
(3)上述实验现象可以证明Fe3+与I−发生可逆反应,实验Ⅰ在用量上的用意是__________
(4)在实验I的溶液中加入CCl4,实验现象是____________________________ ,取其上层清液中滴加KSCN溶液,并未看到明显的红色,其原因为(从平衡移动的角度解释)_________________________________________________________ 。
【深入探究】20min后继续观察实验现象:实验Ⅰ溶液棕黄色变深;实验Ⅱ溶液红色变浅。
(5)已知在酸性较强的条件下,I−可被空气氧化为I2,故甲同学提出假设:该反应条件下空气将I−氧化为I2,使实验Ⅰ中溶液棕黄色变深。甲同学设计实验:____________________________________ ,20min内溶液不变蓝,证明该假设不成立,导致溶液不变蓝的因素可能是__________________________ 。
【初步探究】室温下进行下表所列实验。
| 序号 | 操作 | 现象 |
| 实验Ⅰ | 取5mL 0.1mol/L KI溶液,滴加0.1mol/L FeCl3溶液5∼6滴(混合溶液pH=5) | 溶液变为棕黄色 |
| 实验Ⅱ | 取2mL实验Ⅰ反应后的溶液,滴加2滴0.1mol⋅L−1 KSCN溶液 | 溶液呈红色 |
(2)写出实验Ⅰ反应的离子方程式:
(3)上述实验现象可以证明Fe3+与I−发生可逆反应,实验Ⅰ在用量上的用意是
(4)在实验I的溶液中加入CCl4,实验现象是
【深入探究】20min后继续观察实验现象:实验Ⅰ溶液棕黄色变深;实验Ⅱ溶液红色变浅。
(5)已知在酸性较强的条件下,I−可被空气氧化为I2,故甲同学提出假设:该反应条件下空气将I−氧化为I2,使实验Ⅰ中溶液棕黄色变深。甲同学设计实验:
您最近一年使用:0次
名校
解题方法
6 . 科学家积极探索新技术对CO2进行综合利用, CO2可用来合成低碳烃。
CO2(g) +4H2(g) CH4(g) + 2H2O(g) ΔH= a kJ/mol
CH4(g) + 2H2O(g) ΔH= a kJ/mol
(1)已知:①4H2(g)+ 2O2(g)=4H2O(g) △H=-967.2kJ/mol.
②CH4(g) + 2O2(g) =CO2(g) + 2H2O(g) ΔH=-802.0 kJ/mol.
请回答:①②这两个反应在热力学上趋势均很大,其原因是__________________ ; a=____________ kJ/mol。
(2)在体积为1L的密闭刚性容器中,充入4mol H2和1mol CO2,测得温度对CO2的平衡转化率和催化剂催化效率的影响如图1所示。
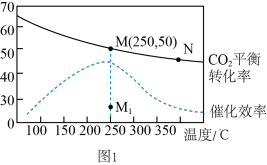
①已知M点总压为1MPa,该反应在此温度下的平衡常数Kp=______ MPa-2。(Kp是用平衡分压代替平衡浓度表示的化学平衡常数,气体分压=气体总压×体积分数。)
②欲增加二氧化碳的平衡转化率,可采取的措施有__________ 。
A.通入惰性气体 B.提高温度
C.增加二氧化碳浓度 D.增加氢气浓度
③下列说法正确的是_________ 。
A.平衡常数大小:KN>KM
B.其他条件不变,若不使用催化剂,则250℃ 时CO2的平衡转化率可能位于点M1
C.图1中M点时,甲烷的体积分数为12.5%
D.当压强或n( H2)/n(CO2)不变时均可证明化学反应已达到平衡状态
(3)新型高效的甲烷燃料电池工作时总反应式:CH4+2O2=CO2+2H2O。
①该电池的负极是___________ (填a或b),②负极电极反应式为___________ ;
CO2(g) +4H2(g)
 CH4(g) + 2H2O(g) ΔH= a kJ/mol
CH4(g) + 2H2O(g) ΔH= a kJ/mol (1)已知:①4H2(g)+ 2O2(g)=4H2O(g) △H=-967.2kJ/mol.
②CH4(g) + 2O2(g) =CO2(g) + 2H2O(g) ΔH=-802.0 kJ/mol.
请回答:①②这两个反应在热力学上趋势均很大,其原因是
(2)在体积为1L的密闭刚性容器中,充入4mol H2和1mol CO2,测得温度对CO2的平衡转化率和催化剂催化效率的影响如图1所示。

①已知M点总压为1MPa,该反应在此温度下的平衡常数Kp=
②欲增加二氧化碳的平衡转化率,可采取的措施有
A.通入惰性气体 B.提高温度
C.增加二氧化碳浓度 D.增加氢气浓度

③下列说法正确的是
A.平衡常数大小:KN>KM
B.其他条件不变,若不使用催化剂,则250℃ 时CO2的平衡转化率可能位于点M1
C.图1中M点时,甲烷的体积分数为12.5%
D.当压强或n( H2)/n(CO2)不变时均可证明化学反应已达到平衡状态
(3)新型高效的甲烷燃料电池工作时总反应式:CH4+2O2=CO2+2H2O。
①该电池的负极是
您最近一年使用:0次
名校
7 . CrO42-和Cr2O72-在溶液中可相互转化。室温下,1.0×10-3mol/L的Na2CrO4溶液中c(Cr2O72-)随pH的变化如图所示。
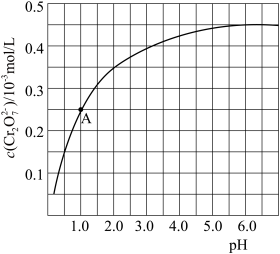
(1)用离子方程式表示Na2CrO4溶液中的可逆反应________________ 。
(2)调节该溶液的酸碱性使pH减小,观察到实验现象为_______________ 根据图示中A点数据,计算出该转化反应的平衡常数________ ;
(3)温度升高,溶液中CrO42-的平衡转化率减小,则该反应的ΔH____ 0(填“大于”、“等于”或“小于”)。
(4)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定待测液中的Cl-,利用Ag+与CrO42-生成砖红色沉淀,作为滴定终点标志。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,溶液中c(Ag+)为____ mol/L,此时溶液中c(CrO42-)等于____ mol/L。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。

(1)用离子方程式表示Na2CrO4溶液中的可逆反应
(2)调节该溶液的酸碱性使pH减小,观察到实验现象为
(3)温度升高,溶液中CrO42-的平衡转化率减小,则该反应的ΔH
(4)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定待测液中的Cl-,利用Ag+与CrO42-生成砖红色沉淀,作为滴定终点标志。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,溶液中c(Ag+)为
您最近一年使用:0次
名校
8 . (1)高温下,C(s)+H2O(g) CO(g)+H2(g) ΔH>0,反应的化学平衡常数表达式K=
CO(g)+H2(g) ΔH>0,反应的化学平衡常数表达式K=____ ,该反应随温度升高,K值___ (填增大、减小或不变),该反应在高温下自发进行的原因是_____ 。
(2)向重铬酸钾溶液中加入氢氧化钠固体,溶液的颜色变化为____ ,原因是(请从平衡的角度用化学用语及必要的文字说明)____ 。
(3)密闭容器中充入N2O4达化学平衡,压缩体积达新平衡,整个过程的现象为____ 。
(4)多元弱酸的逐级电离平衡常数为K1、K2、K3……,则K1、K2、K3的大小关系为___ 。
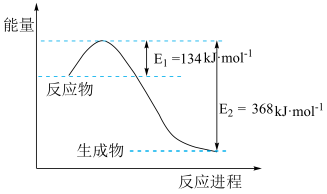
(5)1molNO2和1molCO反应生成CO2和NO过程中的能量变化如图,请写出NO2和CO反应的热化学方程式___ ,向上述可逆反应中加入催化剂,则E1____ (填增大、减小或不变,下同);此反应的ΔH____ 。
 CO(g)+H2(g) ΔH>0,反应的化学平衡常数表达式K=
CO(g)+H2(g) ΔH>0,反应的化学平衡常数表达式K=(2)向重铬酸钾溶液中加入氢氧化钠固体,溶液的颜色变化为
(3)密闭容器中充入N2O4达化学平衡,压缩体积达新平衡,整个过程的现象为
(4)多元弱酸的逐级电离平衡常数为K1、K2、K3……,则K1、K2、K3的大小关系为
(5)1molNO2和1molCO反应生成CO2和NO过程中的能量变化如图,请写出NO2和CO反应的热化学方程式

您最近一年使用:0次
真题
名校
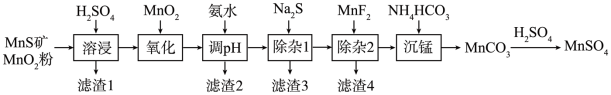
9 . 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
(1)“滤渣1”含有S和__________________________ ;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________ 。
(2)“氧化”中添加适量的MnO2的作用是将________________________ 。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______ ~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________ 。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________ 。
(6)写出“沉锰”的离子方程式___________________________________________________ 。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y= 时,z=
时,z=___________ 。
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和
(2)“氧化”中添加适量的MnO2的作用是将
(3)“调pH”除铁和铝,溶液的pH范围应调节为
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(6)写出“沉锰”的离子方程式
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=
 时,z=
时,z=
您最近一年使用:0次
2019-06-09更新
|
19601次组卷
|
29卷引用:黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题
黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题2019年全国统一高考化学试题(新课标Ⅲ)河北省张家口市第四中学2018-2019学年高二下学期6月月考理科综合化学试题 河北省辛集中学2020届高三上学期入学考试化学试题安徽省阜阳市颍上二中等三校2020届高三上学期入学考试化学试题甘肃省高台县第一中学2020届高三上学期期中考试化学试题山东省滕州市第一中学2020届高三3月线上模拟考试化学试题(已下线)专题七 工艺流程题(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训河北省承德市围场卉原中学2020届高三模拟自测联考试卷理综化学试卷2020届四川省成都市第七中学高三三月份网络教学质量监测卷化学试题(已下线)专题6.1 无机化工流程题(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升四川省宜宾市叙州区第一中学校2020届高三下学期第四学月考试理综化学试题四川省宜宾市叙州区第二中学校2020届高三第一次高考适应性考试理综化学试题河南省信阳市罗山县2021届高三第一次调研(8月联考)化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三章素养检测黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题(已下线)押全国卷理综第27题 工业流程-备战2021年高考化学临考题号押题(课标全国卷)江西省宜春市第九中学2021-2022学年高三上学期10月月考化学试题天津市第二十五中学2021-2022学年高三上学期第一次月考化学试题(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)押全国卷理综第27题 工业流程-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题16工艺流程题-五年(2018~2022)高考真题汇编(全国卷)四川省泸州市泸县第五中学2022届高三高考适应性考试理综化学试题(已下线)专题18 工艺流程题(已下线)T26-工业流程题陕西省西安市周至县第六中学2023-2024学年高三上学期11月期中化学试题河南省济源市高级中学2023-2024学年高三上学期高考模拟检测(10月)理科综合试题-高中化学
名校
10 . 某同学在实验室进行铁盐与亚铁盐相互转化实验。
实验Ⅰ:将Fe3+转化为Fe2+
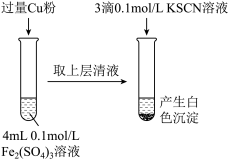
(1)Fe3+与Cu粉发生反应的离子方程式为_________________________________ 。
(2)某学生用对比实验法探究白色沉淀产生的原因,请填写实验万案:
查阅资料:
已知①SCN-的化学性质与I-相似 ②2Cu2++4I-=2CuI↓+I2
Cu2+与SCN-反应的离子方程式为③___________________________________ 。
实验Ⅱ:将Fe2+转化为Fe3+
探究上述现象出现的原因:
查阅资料:Fe2++NO Fe(NO)2+(棕色)
Fe(NO)2+(棕色)
(3)用离子方程式解释NO产生的原因___________________________________ 。
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应Ⅰ:Fe2+与HNO3反应;反应Ⅱ:Fe2+与NO反应
①反应Ⅰ是一个不可逆反应,设计实验方案加以证明_____________________________ 。
②请用化学平衡移动原理解释溶液由棕色变为黄色的原因_____________________________ 。
实验Ⅰ:将Fe3+转化为Fe2+

(1)Fe3+与Cu粉发生反应的离子方程式为
(2)某学生用对比实验法探究白色沉淀产生的原因,请填写实验万案:
| 实验方案 | 现象 | 结论 |
| 步骤1:取4mL① | 产生白色沉淀 | CuSO4溶液与KSCN溶液反应产生了白色沉淀 |
| 步骤2:取4mL② | 无明显现象 |
查阅资料:
已知①SCN-的化学性质与I-相似 ②2Cu2++4I-=2CuI↓+I2
Cu2+与SCN-反应的离子方程式为③
实验Ⅱ:将Fe2+转化为Fe3+
| 实验方案 | 现象 |
| 向3mL0.1mol/LFeSO4溶液中加入 3mL0.5mol/L稀硝酸 | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
探究上述现象出现的原因:
查阅资料:Fe2++NO
 Fe(NO)2+(棕色)
Fe(NO)2+(棕色)(3)用离子方程式解释NO产生的原因
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应Ⅰ:Fe2+与HNO3反应;反应Ⅱ:Fe2+与NO反应
①反应Ⅰ是一个不可逆反应,设计实验方案加以证明
②请用化学平衡移动原理解释溶液由棕色变为黄色的原因
您最近一年使用:0次
2018-04-25更新
|
400次组卷
|
4卷引用:黑龙江省鹤岗市第一中学2020届高三11月月考化学试题



