解题方法
1 . 烯烃催化裂解是制备短链烯烃的重要途径。研究表明,1-丁烯[CH3CH2CH=CH2(g)]催化裂解时,发生两个平行竞争反应生成丙烯和乙烯,两反应的热化学方程式为:
①3CH3CH2CH=CH2(g)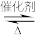 4CH3CH=CH2(g) △H=+579 kJ·mol-1
4CH3CH=CH2(g) △H=+579 kJ·mol-1
②CH3CH2CH=CH2(g)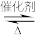 2CH2=CH2(g) △H=+283 kJ·mol-1
2CH2=CH2(g) △H=+283 kJ·mol-1
回答下列问题:
(1)若1-丁烯的燃烧热为2539 kJ·mol-1,则表示乙烯燃烧热的热化学方程式为____ ;1-丁烯转化为丙烯反应的化学平衡常数表达式为_____ 。
(2)有利于提高1-丁烯平衡转化率的措施有_______ 。
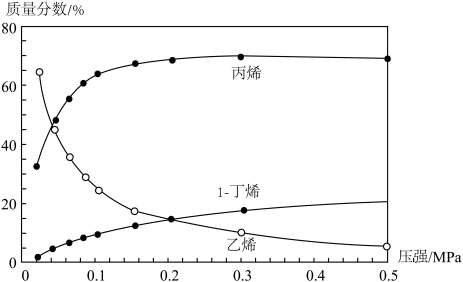
(3)550℃和0.02~0.5 MPa下,①②两个反应均建立平衡,测得平衡混合物里各组分的质量分数随压强变化的曲线如下图所示。由图可知,1-丁烯的质量分数随压强的增大而增大,主要原因是______ 。
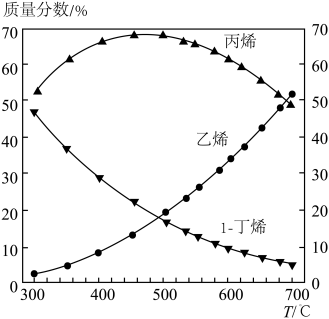
(4)在1-丁烯裂解的实际生产中,为了提高产物中丙烯的含量,除了选择合适的温度和压强之外,还有一条关键措施是_____ 。0.1 MPa和300~700℃下,1-丁烯裂解产物中各组分比例变化的曲线如下图所示。由图可知,生产过程中提高丙烯质量分数的最佳温度为___ ℃,在该温度之前各温度对应的组成______ (填“一定是”、“可能是”或“一定不是”)平衡态,理由是____________ 。
①3CH3CH2CH=CH2(g)
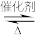 4CH3CH=CH2(g) △H=+579 kJ·mol-1
4CH3CH=CH2(g) △H=+579 kJ·mol-1②CH3CH2CH=CH2(g)
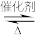 2CH2=CH2(g) △H=+283 kJ·mol-1
2CH2=CH2(g) △H=+283 kJ·mol-1回答下列问题:
(1)若1-丁烯的燃烧热为2539 kJ·mol-1,则表示乙烯燃烧热的热化学方程式为
(2)有利于提高1-丁烯平衡转化率的措施有
(3)550℃和0.02~0.5 MPa下,①②两个反应均建立平衡,测得平衡混合物里各组分的质量分数随压强变化的曲线如下图所示。由图可知,1-丁烯的质量分数随压强的增大而增大,主要原因是

(4)在1-丁烯裂解的实际生产中,为了提高产物中丙烯的含量,除了选择合适的温度和压强之外,还有一条关键措施是

您最近半年使用:0次
解题方法
2 . 在一定条件下,一定量的X在恒容密闭容器中发生反应: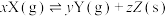
 ,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
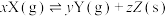
 ,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
,达到平衡时,Y的浓度与温度和容器容积的关系如图所示,下列判断正确的是
A. |
B. |
| C.在M点,投入适量Z,逆反应速率增大 |
| D.在M点,增大X的浓度,X的平衡质量分数增大 |
您最近半年使用:0次
解题方法
3 . 环氧乙烷(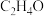 )被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯(
)被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯( )直接氧化法制取环氧乙烷,体系中发生的反应如下:
)直接氧化法制取环氧乙烷,体系中发生的反应如下:
主反应:


副反应: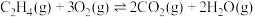

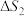
回答下列问题:
(1)已知几种化学键的键能如表所示:
试计算
___________ 。
(2)主反应与副反应的吉布斯自由能变( )与温度T的关系如图所示,则副反应的
)与温度T的关系如图所示,则副反应的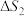
___________ (填“>”“<”或“=”)0,
___________ (填“>”“<”或“=”)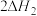 。
。

(3)在250℃、101kPa下,向某密闭容器中充入一定量的 和
和 ,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是
,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是 ,增大压强,
,增大压强, 的含量将
的含量将___________ (填“增大”“减小”或“不变”)。工业生产中常采用的反应条件为250℃、2.0MPa,并选择Ag作催化剂,充分反应后体系中含碳组分含量最高的是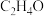 ,则Ag所起的作用可能为
,则Ag所起的作用可能为___________ 。
(4)一定条件下,用富氧空气(只含 和
和 ,且
,且 的体积分数为55%)代替
的体积分数为55%)代替 ,将
,将 、
、 、
、 按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa,
按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa, 的体积分数为31.25%,
的体积分数为31.25%,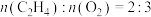 ,则
,则 和
和 的平衡转化率之比为
的平衡转化率之比为___________ ,该条件下主反应的压强平衡常数
___________  (
( 为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
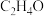 )被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯(
)被广泛地应用于洗涤、制药、印染等行业。工业上通常采用乙烯( )直接氧化法制取环氧乙烷,体系中发生的反应如下:
)直接氧化法制取环氧乙烷,体系中发生的反应如下:主反应:



副反应:
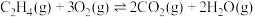

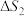
回答下列问题:
(1)已知几种化学键的键能如表所示:
| 化学键 | C-H | C=C | C-C | C-O | O=O |
键能 | 423 | 682 | 368 | 335 | 498 |

(2)主反应与副反应的吉布斯自由能变(
 )与温度T的关系如图所示,则副反应的
)与温度T的关系如图所示,则副反应的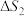

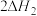 。
。
(3)在250℃、101kPa下,向某密闭容器中充入一定量的
 和
和 ,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是
,同时发生上述两个反应,充分反应后,体系中含碳组分含量最高的是 ,增大压强,
,增大压强, 的含量将
的含量将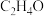 ,则Ag所起的作用可能为
,则Ag所起的作用可能为(4)一定条件下,用富氧空气(只含
 和
和 ,且
,且 的体积分数为55%)代替
的体积分数为55%)代替 ,将
,将 、
、 、
、 按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa,
按物质的量之比为11:11:1通入某恒容密闭容器中,发生上述两个反应,平衡时测得容器内总压为2.0MPa, 的体积分数为31.25%,
的体积分数为31.25%,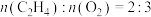 ,则
,则 和
和 的平衡转化率之比为
的平衡转化率之比为
 (
( 为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
为用分压代替浓度的平衡常数,各组分分压=各组分物质的量分数×总压)。
您最近半年使用:0次
4 . T0时,向容积为5L的恒容密闭容器中充入一定量的A(g)和B(g),发生反应: △H<0。反应过程中的部分数据如下表,下列说法错误的是
△H<0。反应过程中的部分数据如下表,下列说法错误的是
 △H<0。反应过程中的部分数据如下表,下列说法错误的是
△H<0。反应过程中的部分数据如下表,下列说法错误的是| t/min | n(A)/mol | n(B)/mol |
| 0 | 4.0 | 2.0 |
| 5 | 2.0 | 1.0 |
| 10 | 2.0 | 1.0 |
| A.其他条件不变,温度变为T1时,平衡时测得C的浓度为0.8mol/L,则T1>T0 |
B.8min时,该反应的 (正)= (正)= (逆) (逆) |
| C.平衡时,D的体积分数约为14.3% |
| D.5min时,向该容器中再充入4.0molA和2.0molB,达新平衡后,B的百分含量变大 |
您最近半年使用:0次
2024-03-23更新
|
249次组卷
|
2卷引用:河北省唐山市2023-2024学年高三一模化学试题
解题方法
5 . 综合利用CH4和CO2对构建低碳社会、促进工业可持续发展有重要意义。
(1)CH4与Cl2光照下反应有多种产物。其中有机产物(图1)的电子式是_______ 。有人认为CH4是四棱锥型,碳原子位于四棱锥的顶点(图2),判断CH4不是四棱锥型分子的依据是_______ 。(选填编号)
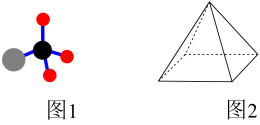
a.CH4是非极性分子
b.一氯甲烷只有一种结构
c.二氯甲烷只有一种沸点
d.CH4中碳的质量分数75%
实验室对(CH4-CO2)催化重整,反应原理为:CH4(g)+CO2(g) 2CO(g)+2H2(g)。在1L固定容积的密闭容器中,充入0.1mol CO2、0.1mol CH4,分别在p1、p2、p3三种压强和不同温度下进行(CH4-CO2)催化重整,测得平衡时甲烷的转化率、温度和压强的关系如图。
2CO(g)+2H2(g)。在1L固定容积的密闭容器中,充入0.1mol CO2、0.1mol CH4,分别在p1、p2、p3三种压强和不同温度下进行(CH4-CO2)催化重整,测得平衡时甲烷的转化率、温度和压强的关系如图。
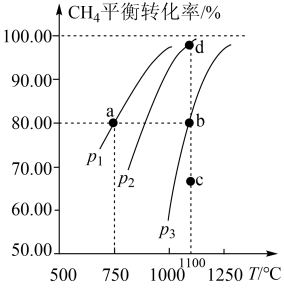
(2)750℃、p1时,反应经20min达到平衡。则平衡后CO的物质的量为_______ 。图中c点时,v正_______ v逆(选填:<、>、=)。
(3)该反应正反应为_______ 热反应(选填:吸、放);在p1、p2、p3中,压强最大的是_______ 。
(4)已知a点时的平衡常数Ka=1.64,则d点时的平衡常数Kd_______ 1.64(选填:<、>、=),理由是_______ 。
(1)CH4与Cl2光照下反应有多种产物。其中有机产物(图1)的电子式是

a.CH4是非极性分子
b.一氯甲烷只有一种结构
c.二氯甲烷只有一种沸点
d.CH4中碳的质量分数75%
实验室对(CH4-CO2)催化重整,反应原理为:CH4(g)+CO2(g)
 2CO(g)+2H2(g)。在1L固定容积的密闭容器中,充入0.1mol CO2、0.1mol CH4,分别在p1、p2、p3三种压强和不同温度下进行(CH4-CO2)催化重整,测得平衡时甲烷的转化率、温度和压强的关系如图。
2CO(g)+2H2(g)。在1L固定容积的密闭容器中,充入0.1mol CO2、0.1mol CH4,分别在p1、p2、p3三种压强和不同温度下进行(CH4-CO2)催化重整,测得平衡时甲烷的转化率、温度和压强的关系如图。
(2)750℃、p1时,反应经20min达到平衡。则平衡后CO的物质的量为
(3)该反应正反应为
(4)已知a点时的平衡常数Ka=1.64,则d点时的平衡常数Kd
您最近半年使用:0次
名校
6 . 某恒容密闭容器中,只改变温度(T)或压强(p),水蒸气百分含量随时间的变化趋势符合下图所示的反应是
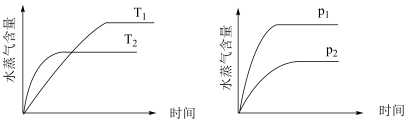

A.  |
B.  |
C.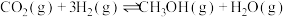  |
D.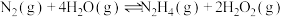  |
您最近半年使用:0次
2023-08-21更新
|
475次组卷
|
3卷引用:浙江省精诚联盟2022-2023学年高三上学期12月适应性联考化学试题
名校
7 . 碳热还原氧化锌反应可用于循环制氢。碳热还原氧化锌的主要反应如下:
反应I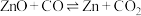 ;
;
反应Ⅱ
在不同容器中分别发生反应I、反应Ⅱ,不同压强(P1或P2)下分别达平衡时,两个反应中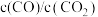 随温度变化的关系如图所示。下列说法正确的是
随温度变化的关系如图所示。下列说法正确的是
反应I
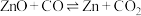 ;
;反应Ⅱ

在不同容器中分别发生反应I、反应Ⅱ,不同压强(P1或P2)下分别达平衡时,两个反应中
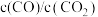 随温度变化的关系如图所示。下列说法正确的是
随温度变化的关系如图所示。下列说法正确的是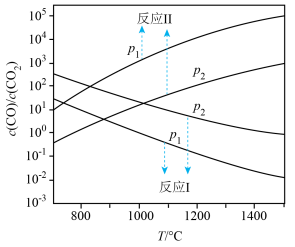
A.压强大小: |
B.在如图所示条件下,反应I可表示为  |
C.选择反应Ⅱ的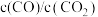 小于反应I的条件,将C与ZnO置于同一密闭容器中,碳热还原氧化锌反应能顺利进行 小于反应I的条件,将C与ZnO置于同一密闭容器中,碳热还原氧化锌反应能顺利进行 |
D.一定条件下将C与ZnO置于同一密闭容器中反应,当 时,增大 时,增大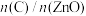 的值,可减少平衡时气体中 的值,可减少平衡时气体中 的含量 的含量 |
您最近半年使用:0次
2023-06-02更新
|
648次组卷
|
3卷引用:江苏省扬州市2023届高三下学期三模化学试题
8 . 已知 催化加氢合成乙醇的反应原理为
催化加氢合成乙醇的反应原理为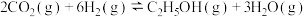 。设
。设 为起始时的投料比,即
为起始时的投料比,即 。
。 的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是

 催化加氢合成乙醇的反应原理为
催化加氢合成乙醇的反应原理为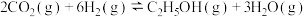 。设
。设 为起始时的投料比,即
为起始时的投料比,即 。
。 的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
的平衡转化率与压强、温度和投料比的关系如图所示,下列有关说法错误的是
A.图1中投料比相同,温度从高到低的顺序为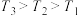 |
B.图2中投料比由大到小的顺序为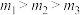 |
C.若图1中投料比 ,a点时乙醇的分压为 ,a点时乙醇的分压为 |
D.若图2中投料比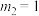 ,随着温度的升高,该平衡体系中 ,随着温度的升高,该平衡体系中 的百分含量逐渐减小 的百分含量逐渐减小 |
您最近半年使用:0次
9 . 在一密闭容器中,反应 aA(g) bB(g)+cC(s)达平衡后容器体积为 2L,保持温度不变,将容器的体积由2L 变为3L,当达到新的平衡时,B 的浓度是原来的 50%,下列说法正确的是
bB(g)+cC(s)达平衡后容器体积为 2L,保持温度不变,将容器的体积由2L 变为3L,当达到新的平衡时,B 的浓度是原来的 50%,下列说法正确的是
 bB(g)+cC(s)达平衡后容器体积为 2L,保持温度不变,将容器的体积由2L 变为3L,当达到新的平衡时,B 的浓度是原来的 50%,下列说法正确的是
bB(g)+cC(s)达平衡后容器体积为 2L,保持温度不变,将容器的体积由2L 变为3L,当达到新的平衡时,B 的浓度是原来的 50%,下列说法正确的是| A.平衡向正反应方向移动 | B.物质C 的浓度减小 |
| C.物质B 的质量分数增加 | D.体系的熵增大 |
您最近半年使用:0次
2020-12-16更新
|
629次组卷
|
2卷引用:浙江省精诚联盟2020届高三适应性联考化学试题
名校
10 . 在一密闭容器中,反应 aA(气) bB(气)达平衡后,保持温度不变,把容器体积压缩到原来的一半且达到新平衡时,A的浓度是原来的1.5倍,则下列说法
bB(气)达平衡后,保持温度不变,把容器体积压缩到原来的一半且达到新平衡时,A的浓度是原来的1.5倍,则下列说法不正确 的是
 bB(气)达平衡后,保持温度不变,把容器体积压缩到原来的一半且达到新平衡时,A的浓度是原来的1.5倍,则下列说法
bB(气)达平衡后,保持温度不变,把容器体积压缩到原来的一半且达到新平衡时,A的浓度是原来的1.5倍,则下列说法| A.平衡向正反应方向移动 | B.物质A的转化率变小 |
| C.物质B的质量分数增加了 | D.a>b |
您最近半年使用:0次
2020-11-06更新
|
516次组卷
|
12卷引用:浙江省衢州、湖州、丽水2021届高三11月教学质量检测化学试题
浙江省衢州、湖州、丽水2021届高三11月教学质量检测化学试题(已下线)浙江省湖州、衢州、丽水2021届高三11月教学质量检测化学试题(已下线)【浙江新东方】【2020】【高三上】【期中】【HD-LP418】【化学】浙江省绍兴市上虞区2020-2021学年高二上学期期末教学质量调测化学试题浙江省丽水外国语学校高中部2021-2022学年高二上学期第一次月考(10月)化学试题浙江省嘉兴市2021-2022学年高二上学期期末检测化学试题浙江省湖州市三贤联盟2021-2022学年高二上学期期中考试化学试题浙江省杭州市S9联盟2022-2023学年高二上学期期中联考化学试题浙江省湖州市吴兴高级中学2023-2024学年高二上学期10月阶段性测试化学试题黑龙江省鸡西市密山市高级中学2023-2024学年高二上学期期末联考化学试题湖南省衡阳县第四中学2023-2024学年高二上学期11月期中化学试题湖南省衡阳县第四中学2023-2024年高二上学期期中考试化学B卷



