名校
1 . 研究 之间的转化具有重要意义。
之间的转化具有重要意义。
已知:

将一定量 气体充入恒容的密闭容器中,控制反应温度为
气体充入恒容的密闭容器中,控制反应温度为 。
。
(1)下列可以作为反应达到平衡的判据是___________(填编号)。
(2)反应温度 时,体系中
时,体系中 、
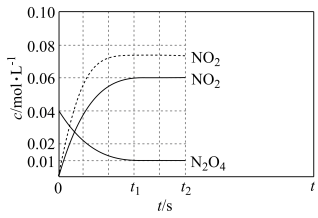
、 随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为
随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为 ,
, 随t(时间)变化曲线如图虚线所示。
随t(时间)变化曲线如图虚线所示。
①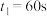 ,在0~60s时段,反应速率
,在0~60s时段,反应速率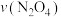 为
为___________ 
②反应温度为
___________ (填“大于”或“小于”) 。
。
③温度 时反应达平衡后,将反应容器的容积减少一半,平衡向
时反应达平衡后,将反应容器的容积减少一半,平衡向___________ (填“正反应”或“逆反应”)方向移动。
④ 时刻反应达到平衡,混合气体平衡总压强为p,
时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为75%,则反应
气体的平衡转化率为75%,则反应 的平衡常数
的平衡常数
___________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
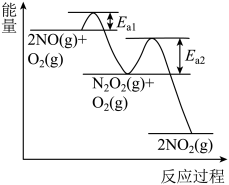
(3)NO氧化反应: 分两步进行,其反应过程能量变化示意图如图。
分两步进行,其反应过程能量变化示意图如图。
Ⅰ.

Ⅱ.

决定NO氧化反应速率的步骤是___________ (填“Ⅰ”或“Ⅱ”)。
 之间的转化具有重要意义。
之间的转化具有重要意义。已知:


将一定量
 气体充入恒容的密闭容器中,控制反应温度为
气体充入恒容的密闭容器中,控制反应温度为 。
。(1)下列可以作为反应达到平衡的判据是___________(填编号)。
| A.气体的压强不变 | B. |
| C.K不变 | D.容器内颜色不变 |
(2)反应温度
 时,体系中
时,体系中 、
、 随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为
随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为 ,
, 随t(时间)变化曲线如图虚线所示。
随t(时间)变化曲线如图虚线所示。
①
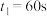 ,在0~60s时段,反应速率
,在0~60s时段,反应速率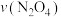 为
为
②反应温度为

 。
。③温度
 时反应达平衡后,将反应容器的容积减少一半,平衡向
时反应达平衡后,将反应容器的容积减少一半,平衡向④
 时刻反应达到平衡,混合气体平衡总压强为p,
时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为75%,则反应
气体的平衡转化率为75%,则反应 的平衡常数
的平衡常数
(3)NO氧化反应:
 分两步进行,其反应过程能量变化示意图如图。
分两步进行,其反应过程能量变化示意图如图。
Ⅰ.


Ⅱ.


决定NO氧化反应速率的步骤是
您最近一年使用:0次
名校
2 . 氨是最重要的氮肥,是产量最大的化工产品之一。其合成原理为:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ•mol-1。
2NH3(g) △H=-92.4kJ•mol-1。
(1)在密闭容器中,投入1molN2和3molH2在催化剂作用下发生反应,测得反应放出的热量_______ 92.4kJ(填“小于”、“大于”或“等于”)。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量_______ (填“变大”、“变小”或“不变”)。
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将_______ (填“正向”、“逆向”或“不移动”)。
(4)若容器恒容绝热,加热使容器内温度迅速升至原来的2倍,平衡将_______ (填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________ (填“大于”、“小于”或“等于”)原来的2倍。
(5)若该反应在一密闭容器中发生,如图是某一时间段反应速率与反应进程的关系曲线图。
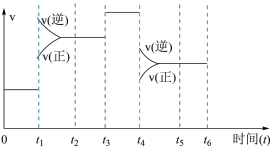
t1、t3、t4时刻体系中反应条件分别发生了什么变化?
t1:________ 。
t3:________ 。
t4:________ 。
 2NH3(g) △H=-92.4kJ•mol-1。
2NH3(g) △H=-92.4kJ•mol-1。(1)在密闭容器中,投入1molN2和3molH2在催化剂作用下发生反应,测得反应放出的热量
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将
(4)若容器恒容绝热,加热使容器内温度迅速升至原来的2倍,平衡将
(5)若该反应在一密闭容器中发生,如图是某一时间段反应速率与反应进程的关系曲线图。

t1、t3、t4时刻体系中反应条件分别发生了什么变化?
t1:
t3:
t4:
您最近一年使用:0次
9-10高一下·黑龙江鹤岗·期末
名校
解题方法
3 . 在一定条件下,可逆反应mA+nB pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减小压强,平衡正向移动,则m+n和p的关系是___ 。
(2)A、C是气体,增加B的量,平衡不移动,则B为___ 。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是___ 。
(4)加热后,可使 的质量增加,则正反应是
的质量增加,则正反应是___ (填“放热”或“吸热”)反应。
 pC达到平衡,若:
pC达到平衡,若:(1)A、B、C都是气体,减小压强,平衡正向移动,则m+n和p的关系是
(2)A、C是气体,增加B的量,平衡不移动,则B为
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
(4)加热后,可使
 的质量增加,则正反应是
的质量增加,则正反应是
您最近一年使用:0次
2021-10-24更新
|
108次组卷
|
31卷引用:2010-2011学年广东省深圳高级中学高二下学期期中考试化学试卷
(已下线)2010-2011学年广东省深圳高级中学高二下学期期中考试化学试卷(已下线)2011-2012学年广东始兴县风度中学高二下学期期中考试理综化学试卷(已下线)2011-2012学年广东省始兴县风度中学高二下学期期末考试理综化学卷(已下线)2010年江苏省启东中学高二上学期期中考试化学卷(已下线)2010-2011学年江苏省启东中学高二上学期期中考试化学试题(理)(已下线)2011-2012年河北省南宫中学高二上学期9月份月考化学(理)试卷(已下线)2011-2012学年黑龙江省绥棱县第一中学高二上学期期末考试化学试卷(已下线)2011-2012年安徽红星中安工大附中高二下学期期中联考理科化学试卷(已下线)2012-2013学年甘肃省兰州一中高二上学期期末考试化学试卷(已下线)2012-2013学年山东省临沂市高二上学期期中考试化学试卷(已下线)2013-2014学年陕西省岐山县高二上学期期中质量检测理科化学试卷2014-2015学年天津市宝坻区四校高二11月联考化学试卷2015-2016学年陕西省西安一中高二上10月月考化学试卷2015-2016学年湖南省株洲十八中高二上学期期中(理)化学试卷2015-2016学年天津市和平区高二上学期期末考试化学试卷2015-2016学年湖南省怀化市会同三中高二上12月月考化学试卷2016-2017学年吉林省汪清六中高二上第一次月考化学试卷内蒙古阿拉善左旗高级中学2017-2018学年高二上学期期末考试化学试题甘肃省武威第五中学2017-2018学年高二下学期第二次月考化学试题甘肃省武威第五中学2018-2019学年高二上学期期末考试化学试题黑龙江省齐齐哈尔市龙江二中2019-2020学年高二12月月考化学试题湖南省湘西土家族苗族自治州花垣县边城高级中学2020-2021学年高二上学期9月月考化学试题西藏自治区拉萨市第二高级中学2019-2020学年高二上学期期末考试化学试题河北省衡水市武邑武罗学校2020-2021学年高二上学期期中考试化学试题黑龙江省绥化市望奎县第一中学2021-2022学年高二上学期第一次月考化学试题黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题甘肃省兰州市西固区三校2021-2022学年高二上学期期中联考化学(理科)试题陕西省汉滨区五里高级中学2022-2023学年高二上学期期中考试化学试题河南省许昌市鄢陵县职业教育中心2021-2022学年高二上学期第一次月考化学试题(已下线)09~10年鹤岗一中高一下学期期末考试化学卷2014-2015学年辽宁实验分校高一下6月阶段测试化学试卷
名校
4 . 在一定条件下,xA+yB⇌zC的反应达到平衡.
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是___ 。
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则向____ 移动.(填“正向”、“逆向”、“无法判断”)
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不移动,则A是_____ 态.(填“气”、“液”、“固”)
(4)加热后C的质量分数减少,则正反应是_____ 热反应。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则向
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不移动,则A是
(4)加热后C的质量分数减少,则正反应是
您最近一年使用:0次
2021-01-09更新
|
146次组卷
|
5卷引用:2015-2016学年广东省清远市第一中学高二上学期10月月考化学试卷
名校
解题方法
5 . 现有反应mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)若加入B(容器体积不变),则A的转化率______ (填增大、减小或不变,下同),B的转化率______ 。
(2)若升高温度,则平衡时B、C的浓度之比c(B)/c(C)将______ (填增大、减小或不变)。
(3)若B是有色物质,A、C均无色,则加入C(容积不变)时混合物颜色________ (填变深、变浅或不变,下同),而维持容器内压强不变,充入Ne时,混合物的颜色_________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)若加入B(容器体积不变),则A的转化率
(2)若升高温度,则平衡时B、C的浓度之比c(B)/c(C)将
(3)若B是有色物质,A、C均无色,则加入C(容积不变)时混合物颜色
您最近一年使用:0次
名校
解题方法
6 . 在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),2min末反应达到平衡状态,此时测得D、C的浓度均为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态,此时测得D、C的浓度均为0.4mol/L,请填写下列空白:
(1)x值等于_____________ 。
(2)A的转化率为_______________ 。
(3)生成D的反应速率为_____________ 。
(4)如果增大反应体系的压强,则平衡体系中C的质量分数_________ (增大、减小或不变)。
(5)在此温度下,该化学反应的平衡常数k=__________
 xC(g)+2D(g),2min末反应达到平衡状态,此时测得D、C的浓度均为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态,此时测得D、C的浓度均为0.4mol/L,请填写下列空白:(1)x值等于
(2)A的转化率为
(3)生成D的反应速率为
(4)如果增大反应体系的压强,则平衡体系中C的质量分数
(5)在此温度下,该化学反应的平衡常数k=
您最近一年使用:0次
名校
7 . 工业上可利用“甲烷蒸气转化法”生产氢气,反应的热化学方程式为CH4(g)+H2O(g)⇌CO2(g)+3H2(g) △H=+161.1kJ·mol-1
(1)已知温度、压强对甲烷平衡时的体积分数的影响如图1,请回答:
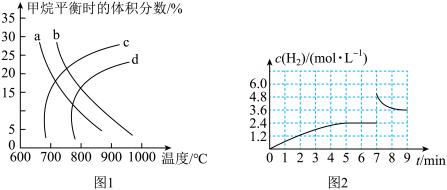
①图1中a、b、c、d四条曲线中的两条代表压强分别为1MPa、2MPa时甲烷体积分数的曲线,其中表示1MPa的是_____ 。
②该反应的平衡常数:K(600℃)___ (填“>”“<”或“=”)K(700℃)。
(2)①已知:在700℃、1MPa时,1molCH4与1molH2O在1L的密闭容器中反应,6min时达到平衡(如图2),此时CH4的转化率为__ ,该温度下反应的平衡常数为____ (结果保留小数点后一位数字)。
②从图2分析,由第一次平衡到第二次平衡,平衡移动的方向是____ (填“向正反应方向”或“向逆反应方向”)移动,采取的措施可能是____ 。
(1)已知温度、压强对甲烷平衡时的体积分数的影响如图1,请回答:

①图1中a、b、c、d四条曲线中的两条代表压强分别为1MPa、2MPa时甲烷体积分数的曲线,其中表示1MPa的是
②该反应的平衡常数:K(600℃)
(2)①已知:在700℃、1MPa时,1molCH4与1molH2O在1L的密闭容器中反应,6min时达到平衡(如图2),此时CH4的转化率为
②从图2分析,由第一次平衡到第二次平衡,平衡移动的方向是
您最近一年使用:0次
2019-06-11更新
|
412次组卷
|
3卷引用:广东省中山市第一中学2018-2019学年高二上学期第一次段考化学试题
8 . 已知SO3分解反应为2SO3(g)⇌2SO2(g)+O2(g)。在1.0L密闭容器中加入10mol SO3(g),在一定温度进行上述反应,反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)欲提高SO3的平衡转化率,应采取的措施为_____ (填字母)。
a.增大压强 b.通入SO3 c.降低压强
(2)平衡时SO3的转化率为_____ ,该温度下的平衡常数Kw=_____
(3)研究表明,SO3(g)分解速率v=4×10﹣3×pSO3(kPa•min﹣1),t=6h时,测得体系中pO2=55kPa,则此时的pSO3=_____ kPa,v(SO3)=_____ kPa•min﹣1。
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/kPa | 400 | 412 | 422 | 440 | 469 | 518 | 538 | 560 | 560 |
回答下列问题:
(1)欲提高SO3的平衡转化率,应采取的措施为
a.增大压强 b.通入SO3 c.降低压强
(2)平衡时SO3的转化率为
(3)研究表明,SO3(g)分解速率v=4×10﹣3×pSO3(kPa•min﹣1),t=6h时,测得体系中pO2=55kPa,则此时的pSO3=
您最近一年使用:0次
解题方法
9 . 已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
(1)开展实验1和实验2的目的是:____________________ 。
(2)180℃、反应到40min时,体系______ (填“达到”或“未达到”)平衡状态,理由是:______________ ;此时CH4的平衡转化率为:_________ 。
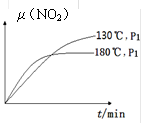
(3)在一定条件下,反应时间t与转化率μ(NO2)的关系如图所示,请在图象中画出180℃时,压强为P2(设压强P2>P1)的变化曲线,并做必要的标注_____ 。
 N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:| 实验 编号 | 温度 | 时间 min 物质 的量mol | 0 | 10 | 20 | 40 | 50 |
| 1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 |
(1)开展实验1和实验2的目的是:
(2)180℃、反应到40min时,体系
(3)在一定条件下,反应时间t与转化率μ(NO2)的关系如图所示,请在图象中画出180℃时,压强为P2(设压强P2>P1)的变化曲线,并做必要的标注

您最近一年使用:0次
解题方法
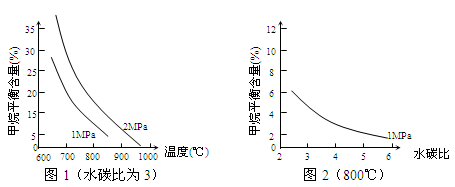
10 . 工业上可利用“甲烷蒸气转化法生产氢气”,反应为:CH4(g)+H2O(g) CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
(1)CH4(g)+H2O(g) CO(g)+3H2(g) 的△H
CO(g)+3H2(g) 的△H_______ 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将_____________ 移动(填“向正应方向”、“向逆反应方向”或“不”)。
(2)温度对该反应的反应速率和平衡移动的影响是_______________________ 。
(3)其他条件不变,请在图2中画出 压强为2 MPa时,甲烷平衡含量(%)与水碳比之间关系曲线___________ 。(只要求画出大致的变化曲线)
(4)已知:在700℃,1MPa时,1mol CH4与1mol H2O在2L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少________ ?(写出计算过程,结果保留小数点后一位数字。)
 CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
CO(g)+3H2(g)。已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
(1)CH4(g)+H2O(g)
 CO(g)+3H2(g) 的△H
CO(g)+3H2(g) 的△H(2)温度对该反应的反应速率和平衡移动的影响是
(3)其他条件不变,请在图2中
(4)已知:在700℃,1MPa时,1mol CH4与1mol H2O在2L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少
您最近一年使用:0次
2016-12-09更新
|
336次组卷
|
3卷引用:广东省阳东广雅学校2017-2018学年高二11月月考化学试题



