1 . 尿素[CO(NH2)2][s]是首个由无机物人工合成的有机物。
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g) NH2COONH4(l)
NH2COONH4(l)  H1=-119.2 kJ∙mol-1;NH2COONH4(l)
H1=-119.2 kJ∙mol-1;NH2COONH4(l) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)  H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g)
H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)  H3=
H3=___________ kJ∙mol-1,下列图象能表示尿素合成塔中发生反应的能量变化历程的是___________ (填标号)。
A .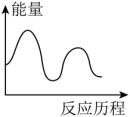 B.
B. 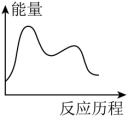 C.
C. 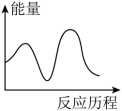 D.
D.
(2)T℃,在2L的密闭容器中,通入2molNH3和1molCO2,保持体积不变,发生反应,2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
①NH3的平衡转化率为___________ 。
②能说明上述反应达到平衡状态的是___________ (填标号)。
A.n(CO2):n(NH3)=1:2
B.混合气体的密度不再发生变化
C.CO2的体积分数在混合气体中保持不变
D.单位时间内消耗2molNH3,同时生成1molH2O
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),若原料气中
CO(NH2)2(s)+H2O(g),若原料气中 =m,测得m与CO2的平衡转化率(α)的关系如图所示:
=m,测得m与CO2的平衡转化率(α)的关系如图所示:
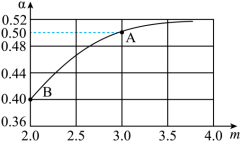
若平衡时A点容器内总压强为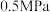 ,则上述反应的平衡常数Kp=
,则上述反应的平衡常数Kp=___________  。(用平衡分压代平衡浓度计算,分压=总压×物质的量分数)
。(用平衡分压代平衡浓度计算,分压=总压×物质的量分数)
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g)
 NH2COONH4(l)
NH2COONH4(l)  H1=-119.2 kJ∙mol-1;NH2COONH4(l)
H1=-119.2 kJ∙mol-1;NH2COONH4(l) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)  H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g)
H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)  H3=
H3=A .
 B.
B.  C.
C.  D.
D.
(2)T℃,在2L的密闭容器中,通入2molNH3和1molCO2,保持体积不变,发生反应,2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:①NH3的平衡转化率为
②能说明上述反应达到平衡状态的是
A.n(CO2):n(NH3)=1:2
B.混合气体的密度不再发生变化
C.CO2的体积分数在混合气体中保持不变
D.单位时间内消耗2molNH3,同时生成1molH2O
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g),若原料气中
CO(NH2)2(s)+H2O(g),若原料气中 =m,测得m与CO2的平衡转化率(α)的关系如图所示:
=m,测得m与CO2的平衡转化率(α)的关系如图所示:
若平衡时A点容器内总压强为
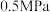 ,则上述反应的平衡常数Kp=
,则上述反应的平衡常数Kp= 。(用平衡分压代平衡浓度计算,分压=总压×物质的量分数)
。(用平衡分压代平衡浓度计算,分压=总压×物质的量分数)
您最近一年使用:0次
2 . 在T℃条件下,向1L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应:2X(g) + Y(g) a Z(g) + W(g)
a Z(g) + W(g)  H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)化学计量数a的值为___________ ;此反应的逆反应 S
S___________ 0 (填﹤,﹥,﹦)。
(2)下列说法中能说明该反应达到了化学平衡状态的是___________ 。
A.容器内压强一定
B.v(X)正=2 v (Y)逆
C.容器内Z分子数一定
D.容器内气体的质量一定
E.容器内气体的密度一定
F.X、Y、Z、W的浓度之比为2∶1∶a∶1
(3)维持温度不变,若起始时向容器中加入4mol X和6 mol Y,若达平衡时容器内的压强减小到开始时的85%,则反应中放出的热量为___________ kJ。
(4)已知:该反应的平衡常数随温度的变化如下表:
若在某温度下,2 mol X和1 mol Y在该容器中反应达平衡,X的平衡转化率为50%,则该温度为___________ ℃。
 a Z(g) + W(g)
a Z(g) + W(g)  H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则(1)化学计量数a的值为
 S
S(2)下列说法中能说明该反应达到了化学平衡状态的是
A.容器内压强一定
B.v(X)正=2 v (Y)逆
C.容器内Z分子数一定
D.容器内气体的质量一定
E.容器内气体的密度一定
F.X、Y、Z、W的浓度之比为2∶1∶a∶1
(3)维持温度不变,若起始时向容器中加入4mol X和6 mol Y,若达平衡时容器内的压强减小到开始时的85%,则反应中放出的热量为
(4)已知:该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 150 | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 | 0.21 |
您最近一年使用:0次
名校
解题方法
3 . 已知下列反应的平衡常数: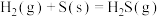 ,
, ;
; ,
, ;则反应
;则反应 的平衡常数是
的平衡常数是
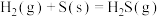 ,
, ;
; ,
, ;则反应
;则反应 的平衡常数是
的平衡常数是A. | B. | C. | D.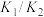 |
您最近一年使用:0次
2024-03-05更新
|
157次组卷
|
65卷引用:甘肃省兰州第一中学2017-2018学年高二上学期期中考试化学(理)试题
甘肃省兰州第一中学2017-2018学年高二上学期期中考试化学(理)试题甘肃省兰州市教育局第四片区联考2023-2024学年高二上学期期中考试化学试题2015-2016学年重庆市第一中学高二上期中测试化学试卷江西省九江市同文中学2018-2019学年高二上学期期中考试化学试题甘肃省甘谷第一中学2019-2020学年高二上学期第一次月考化学试题新疆乌鲁木齐市第四中学2019-2020学年高二上学期期中考试化学试题广东省梅州市水寨中学2019-2020学年高二上学期期中考试化学试题湖南省长沙市长郡中学2019-2020学年高二上学期期中考试化学试题安徽省黄山市“八校联盟”2019-2020学年高二上学期期中考试化学试题(已下线)【南昌新东方】江西省九江市同文中学2018-2019学年高二上学期期中考试化学试题江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高二下学期期中考试化学试题福建省福州黎明中学2021-2022学年高二上学期期中考试化学试题山东省济宁市泗水县2021-2022学年高二上学期期中考试化学试题福建省建瓯市芝华中学2021-2022学年高二上学期期中考试化学试题福建省建瓯市芝华中学2022-2023学年高二上学期期中考试化学试题黑龙江省佳木斯市四校联考2023-2024学年高二上学期11月期中化学考试试题广东省台山市某校2023-2024学年高二上学期期中考试化学试题甘肃省武威市民勤县第一中学2023-2024学高二下学期开学考试化学试题湖南省衡阳县第四中学2023-2024学年高二上学期11月期中化学试题2016届湖南省衡阳县第四中学高三9月月考试化学试卷2015-2016学年内蒙古巴彦淖尔高二上10月月考化学试卷2015-2016学年吉林省松原市油田高中高一下期末化学试卷2016-2017学年四川省成都外国语学校高二上10月月考化学试卷辽宁省庄河市高级中学2016-2017学年高一下学期期末考试化学试题陕西省渭南市尚德中学2017-2018学年高二第一次教学质量检测化学试题湖南省娄底市第四中学2018-2019学年高二上学期10月月考化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高二上学期期末考试化学试题四川省遂宁市2018-2019学年高二下学期期末考试化学试题(已下线)2019年9月16日《每日一题》选修4—— 化学平衡常数山东省日照市第一中学2019-2020学年高二10月月考化学试题吉林省吉化第一高级中学校2019-2020学年高二9月月考化学试题四川省自贡市田家炳中学2019-2020学年高二下学期开学考试化学试题安徽省亳州市涡阳县第九中学2019-2020学年高一7月月考化学试题广东省广州大学附属中学2019-2020学年高一下学期期末考试化学试题广东省广州大学附属中学等三校2019~2020学年高一下学期期末联考化学试题福建省泰宁第一中学2019-2020学年高二上学期第一阶段考试化学(选考)试题(已下线)2.3.3+化学平衡常数-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)2.3.3化学平衡常数(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)安徽省舒城中学2020-2021学年高二上学期第二次月考化学试题河北省鸡泽县第一中学2020-2021学年高二上学期第一次月考化学试题河北省张家口市宣化区宣化第一中学2020-2021学年高二上学期10月月考化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高二上学期第一次月考化学试题辽宁省大连市一〇三中学2020-2021学年高二10月月考化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时1 化学平衡常数 平衡转化率人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时2 化学平衡常数及相关计算(已下线)【浙江新东方】绍兴qw122选择性必修1(SJ)专题2第二单元课时3 化学平衡常数平衡转化率(已下线)第20讲 化学平衡常数及转化率的计算(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向23 化学平衡常数及其应用-备战2022年高考化学一轮复习考点微专题湖南省武冈市第二中学2021-2022学年高二上学期开学摸底考试化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题黑龙江省绥化市望奎县第一中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.2.3 化学平衡常数(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)重庆市清华中学校2021—2022学年上学期高二10月月考化学试题(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)广东省揭阳华侨高级中学2021-2022学年高二上学期第一次阶段考试化学试题(已下线)2.2.1 化学平衡状态 化学平衡常数 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)广西柳州市第三中学2022-2023学年高二上学期10月月考化学试题陕西省宝鸡市千阳县中学2022-2023学年高二上学期第一次月考(理)化学试题福建省福州第十五中学2022-2023学年高二上学期11月线上限时训练化学试题2.2.3化学平衡常数 课中第二章 化学反应速率与化学平衡 第二节 化学平衡 第2课时 化学平衡常数河北省石家庄市第四十二中学2023-2024学年高二上学期第一次月考化学试题(已下线)第3讲 化学平衡计算 平衡常数河南省焦作市博爱县第一中学2023-2024学年高三上学期9月月考化学试题
名校
4 . 在一定温度下,将1mol  和3mol
和3mol  充入体积为2L的恒容密闭容器中发生反应并达到平衡:
充入体积为2L的恒容密闭容器中发生反应并达到平衡:
 ,测得平衡混合气体中
,测得平衡混合气体中 的物质的量分数为25%。下列说法不正确的是
的物质的量分数为25%。下列说法不正确的是
 和3mol
和3mol  充入体积为2L的恒容密闭容器中发生反应并达到平衡:
充入体积为2L的恒容密闭容器中发生反应并达到平衡:
 ,测得平衡混合气体中
,测得平衡混合气体中 的物质的量分数为25%。下列说法不正确的是
的物质的量分数为25%。下列说法不正确的是| A.平衡混合气体中C原子的物质的量是1mol |
| B.达平衡后若升高温度,正反应速率增大的程度比逆反应速率增大的程度小 |
C.该反应的化学平衡常数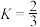 ,达平衡时 ,达平衡时 转化率为50% 转化率为50% |
D.其他条件相同时,若起始充入2mol  和6mol 和6mol  ,达到平衡时 ,达到平衡时 的物质的量分数大于25% 的物质的量分数大于25% |
您最近一年使用:0次
名校
5 . 2018年是哈伯因发明用氮气和氢气合成氨的方法而获得诺贝尔奖100周年。氨是重要的化学品之一,我国目前的生产能力位居世界首位,回答下列问题:
(1)工业上通常采用铁触媒作催化剂,在400℃~500℃、10~30MPa,原料气中 和
和 物质的量之比为1∶2.8的条件下合成氨。分析说明原料气中
物质的量之比为1∶2.8的条件下合成氨。分析说明原料气中 过量的理由是
过量的理由是___________ 。
(2)若在1L的密闭容器中,一定量的氮气和氢气进行如下反应:
 ,其化学平衡常数K与温度T的关系如表所示。
,其化学平衡常数K与温度T的关系如表所示。
①试比较 、
、 的大小,
的大小,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②400℃时,反应 的化学平衡常数为
的化学平衡常数为___________ 。
③400℃时, 反应中,当测得
反应中,当测得 、
、 和
和 物质的量分别为3mol、2mol和1mol时,则该反应
物质的量分别为3mol、2mol和1mol时,则该反应___________ (填“达到平衡状态”或“正向进行”或“逆向进行”)。
(3)在一定条件下,甲、乙体积相同的密闭容器中,开始均投入1mol 和3mol
和3mol 。相对于乙,甲容器中仅改变一个条件,测得甲、乙体积中
。相对于乙,甲容器中仅改变一个条件,测得甲、乙体积中 的转化率与时间关系如图所示。
的转化率与时间关系如图所示。

①相对于乙,甲改变的条件是___________ (填字母),判断依据是___________ 。
A.加入催化剂 B.升高温度 C.增大压强 D.分离氨
②在甲条件下,平衡时体积为0.5L,则该反应的平衡常数K为________ (结果保留两位有效数字)。
(1)工业上通常采用铁触媒作催化剂,在400℃~500℃、10~30MPa,原料气中
 和
和 物质的量之比为1∶2.8的条件下合成氨。分析说明原料气中
物质的量之比为1∶2.8的条件下合成氨。分析说明原料气中 过量的理由是
过量的理由是(2)若在1L的密闭容器中,一定量的氮气和氢气进行如下反应:

 ,其化学平衡常数K与温度T的关系如表所示。
,其化学平衡常数K与温度T的关系如表所示。| T/℃ | 200 | 300 | 400 |
| K |  |  | 0.5 |
 、
、 的大小,
的大小,
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②400℃时,反应
 的化学平衡常数为
的化学平衡常数为③400℃时,
 反应中,当测得
反应中,当测得 、
、 和
和 物质的量分别为3mol、2mol和1mol时,则该反应
物质的量分别为3mol、2mol和1mol时,则该反应(3)在一定条件下,甲、乙体积相同的密闭容器中,开始均投入1mol
 和3mol
和3mol 。相对于乙,甲容器中仅改变一个条件,测得甲、乙体积中
。相对于乙,甲容器中仅改变一个条件,测得甲、乙体积中 的转化率与时间关系如图所示。
的转化率与时间关系如图所示。
①相对于乙,甲改变的条件是
A.加入催化剂 B.升高温度 C.增大压强 D.分离氨
②在甲条件下,平衡时体积为0.5L,则该反应的平衡常数K为
您最近一年使用:0次
2023-11-05更新
|
167次组卷
|
2卷引用:甘肃省酒泉市四校联考2023-2024学年高二上学期11月期中化学试题
名校
6 . 300℃时,将2molX和2molY两种气体混合于2L密闭容器中,发生如下反应: ,2min末达到平衡,生成0.8molW。下列说法错误的是
,2min末达到平衡,生成0.8molW。下列说法错误的是
 ,2min末达到平衡,生成0.8molW。下列说法错误的是
,2min末达到平衡,生成0.8molW。下列说法错误的是| A.300℃时,该反应的平衡常数K=0.5 |
B.在2min末时,Y的平衡浓度为0.8 |
C.0~2min,W的平均反应速率为0.2 |
| D.若温度不变,缩小容器容积,则X的转化率减小 |
您最近一年使用:0次
2023-11-05更新
|
94次组卷
|
2卷引用:甘肃省酒泉市四校联考2023-2024学年高二上学期11月期中化学试题
11-12高二下·广东·期中
名校
解题方法
7 . 一定温度下,反应N2(g)+3H2(g) ⇌2NH3(g)的反应热和化学平衡常数分别为ΔH和K,则相同温度时反应4NH3(g)⇌2N2(g)+6H2(g)的反应热和化学平衡常数为
| A.2ΔH和2K | B.-2ΔH和K2 | C.2ΔH和-2K | D.-2ΔH和 |
您最近一年使用:0次
2023-09-05更新
|
250次组卷
|
21卷引用:甘肃省兰州市联片办学2019-2020学年高二上学期期中考试化学(理)试题
甘肃省兰州市联片办学2019-2020学年高二上学期期中考试化学(理)试题(已下线)2011-2012学年广东省三校高二下学期联考化学试卷2014-2015学年山东省济南一中高二上学期期中化学试卷2014-2015学年云南省曲靖市陆良县二中高二下期中化学试卷陕西省黄陵中学2019-2020学年高二上学期期中考试化学试题重庆市万州纯阳中学2020-2021学年高二上学期期中考试化学试题甘肃省镇原县第二中学2021-2022学年高二上学期第一次月考化学试题福建省南安市柳城中学2021-2022学年高二上学期期中考试化学试题2015-2016学年安徽省郎溪中学高二上学期第一次月考化学试卷河北省张家口市第一中学2016-2017学年高一(衔接班)6月月考(理)化学试题黑龙江省鹤岗市第一中学2018-2019学年高一下学期期末化学试题江西省宜春市上高二中2019-2020学年高二上学期第二次月考化学试题湖南省长郡中学2019-2020学年高二上学期第三次月考化学试题贵州省毕节市民族中学2019-2020学年高二上学期第二次月考化学试题安徽省合肥市2019-2020学年高二上学期期末考试化学试题江西省赣州市会昌县会昌中学2020-2021学年高二上学期第一次月考化学试题吉林省汪清县汪清四中2021-2022学年高二上学期第一次阶段考试化学试题湖北省宜昌英杰学校2022-2023学年高二上学期10月测试化学试题新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题四川省绵阳南山中学2023-2024学年高二上学期开学考试化学试题四川省南充市南部县第二中学2023-2024学年高二上学期10月月考化学试题
解题方法
8 . 回答下列问题:
(1)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应化学方程式为:C2H5OH(g)+IB(g)=ETBE(g)△H。反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=_______ kJ/mol。反应历程的最优途径是_______ (填C1、C2或C3)。

C1表示先吸附乙醇,C2表示先吸附异丁烯,C3表示乙醇和异丁烯同时吸附
(2)用NH3可消除NO污染,反应原理为:4NH3+6NO 5N2+6H2O,以n(NH3):n(NO)分别为4:1、3:1、1:3投料,得到NO脱除率随温度变化的曲线如图所示。
5N2+6H2O,以n(NH3):n(NO)分别为4:1、3:1、1:3投料,得到NO脱除率随温度变化的曲线如图所示。

①曲线a对应的n(NH3):n(NO)=______ 。
②曲线c中NO的起始浓度为4×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为_______ 。
③由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降,可能的原因是_______ (至少写两条)。
(3)二氧化硫的催化氧化是工业上生产硫酸的主要反应O2(g)+2SO2(g) 2SO3(g)。
2SO3(g)。
已知:标准平衡常数Kθ= ,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=
,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=_______ (用含ω的最简式表示)。
(1)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应化学方程式为:C2H5OH(g)+IB(g)=ETBE(g)△H。反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=

C1表示先吸附乙醇,C2表示先吸附异丁烯,C3表示乙醇和异丁烯同时吸附
(2)用NH3可消除NO污染,反应原理为:4NH3+6NO
 5N2+6H2O,以n(NH3):n(NO)分别为4:1、3:1、1:3投料,得到NO脱除率随温度变化的曲线如图所示。
5N2+6H2O,以n(NH3):n(NO)分别为4:1、3:1、1:3投料,得到NO脱除率随温度变化的曲线如图所示。
①曲线a对应的n(NH3):n(NO)=
②曲线c中NO的起始浓度为4×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为
③由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降,可能的原因是
(3)二氧化硫的催化氧化是工业上生产硫酸的主要反应O2(g)+2SO2(g)
 2SO3(g)。
2SO3(g)。已知:标准平衡常数Kθ=
 ,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=
,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=
您最近一年使用:0次
解题方法
9 . 在2L密闭容器中加入适量的氮气和氢气,发生反应N2(g)+3H2(g)  2NH3(g),10min后,在密闭容器中达到平衡,平衡时n(N2)=3mol,n(H2)=1mol,n(NH3)=4mol,求:
2NH3(g),10min后,在密闭容器中达到平衡,平衡时n(N2)=3mol,n(H2)=1mol,n(NH3)=4mol,求:
(1)N2的转化率和这段时间内NH3的化学反应速率分别是:____ 、____ ;
(2)平衡时压强与开始时压强的比值_______ ;
(3)该温度下反应的平衡常数_________ 。
 2NH3(g),10min后,在密闭容器中达到平衡,平衡时n(N2)=3mol,n(H2)=1mol,n(NH3)=4mol,求:
2NH3(g),10min后,在密闭容器中达到平衡,平衡时n(N2)=3mol,n(H2)=1mol,n(NH3)=4mol,求:(1)N2的转化率和这段时间内NH3的化学反应速率分别是:
(2)平衡时压强与开始时压强的比值
(3)该温度下反应的平衡常数
您最近一年使用:0次
2022-12-03更新
|
150次组卷
|
2卷引用:甘肃省临夏州临夏县中学2021-2022学年高二上学期期中考试化学(A卷)试题
10 . Ⅰ.化学反应速率和化学平衡影响因素较多,经常采用变量控制思想分析问题。某小组利用 溶液和酸性
溶液和酸性 溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
请回答:
(1)已知 酸性溶液与
酸性溶液与 溶液反应有
溶液反应有 生成,用化学方程式表示该实验的实验原理:
生成,用化学方程式表示该实验的实验原理:___________ 。
(2)根据表中的实验数据,可以得到的结论是___________ 。
(3)利用实验3中数据计算,用 溶液的浓度变化表示的反应速率为
溶液的浓度变化表示的反应速率为
___________ 。
Ⅱ.研究 的综合利用对促进“低碳经济”的发展有重要意义。工业上以
的综合利用对促进“低碳经济”的发展有重要意义。工业上以 、,为原料生产尿素
、,为原料生产尿素 ,
,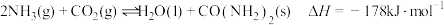 ,
,
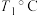 时,在1L的密闭容器中充入
时,在1L的密闭容器中充入 和模拟工业生产,
和模拟工业生产, ,图中是
,图中是 平衡转化率
平衡转化率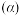 与
与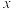 的关系。
的关系。
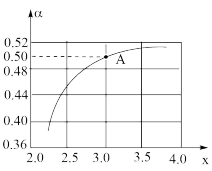
(4)图中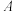 点
点 的平衡转化率
的平衡转化率
___________ %(结果保留3位有效数字)。
(5)当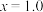 时,若起始的压强为
时,若起始的压强为 ,水为液态平衡时压强变为起始的
,水为液态平衡时压强变为起始的 ,则该反应的平衡常数
,则该反应的平衡常数 =
=___________ ( 为以分压表示的平衡常数,分压=总压
为以分压表示的平衡常数,分压=总压 体积分数)。
体积分数)。
 溶液和酸性
溶液和酸性 溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
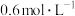  溶液 溶液 |  |   溶液 溶液 |  稀硫酸 稀硫酸 | ||
| 1 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
请回答:
(1)已知
 酸性溶液与
酸性溶液与 溶液反应有
溶液反应有 生成,用化学方程式表示该实验的实验原理:
生成,用化学方程式表示该实验的实验原理:(2)根据表中的实验数据,可以得到的结论是
(3)利用实验3中数据计算,用
 溶液的浓度变化表示的反应速率为
溶液的浓度变化表示的反应速率为
Ⅱ.研究
 的综合利用对促进“低碳经济”的发展有重要意义。工业上以
的综合利用对促进“低碳经济”的发展有重要意义。工业上以 、,为原料生产尿素
、,为原料生产尿素 ,
,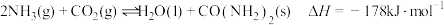 ,
,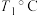 时,在1L的密闭容器中充入
时,在1L的密闭容器中充入 和模拟工业生产,
和模拟工业生产, ,图中是
,图中是 平衡转化率
平衡转化率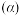 与
与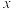 的关系。
的关系。
(4)图中
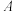 点
点 的平衡转化率
的平衡转化率
(5)当
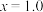 时,若起始的压强为
时,若起始的压强为 ,水为液态平衡时压强变为起始的
,水为液态平衡时压强变为起始的 ,则该反应的平衡常数
,则该反应的平衡常数 =
= 为以分压表示的平衡常数,分压=总压
为以分压表示的平衡常数,分压=总压 体积分数)。
体积分数)。
您最近一年使用:0次



