解题方法
1 . 已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
(1)计算H2S的平衡转化率a=_____ (写出计算过程)。
(2)计算浓度平衡常数K=_____ 。(写出计算过程)。
 COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。(1)计算H2S的平衡转化率a=
(2)计算浓度平衡常数K=
您最近一年使用:0次
2 . 一氧化氮可用作人造丝的漂白剂及丙烯和二甲醚的安定剂。一定温度下,在2L恒容密闭容器中充入1molNO、1mol ,发生反应
,发生反应 ,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得
,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得 的物质的量分数为25%。
的物质的量分数为25%。
(1)平衡时,体系压强p=___________ MPa。
(2)平衡时,
___________ 。
(3)该反应平衡常数表达式为___________ ,该温度下时,平衡常数K=___________ 。
 ,发生反应
,发生反应 ,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得
,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得 的物质的量分数为25%。
的物质的量分数为25%。(1)平衡时,体系压强p=
(2)平衡时,

(3)该反应平衡常数表达式为
您最近一年使用:0次
名校
3 . 化学科学家采用丙烯歧化法制取乙烯和丁烯的反应原理为2C3H6(g) C2H4(g)+C4H8(g) ∆H。回答下列问题:
C2H4(g)+C4H8(g) ∆H。回答下列问题:
(1)向恒温恒容反应器中加入一定量的C3H6,生成C2H4的物质的量与时间的关系如表所示:
①a=_______ ,p初始:p5min=_______ 。
②其他条件不变,若缩小反应器的体积,则C3H6转化率_______ (填“增大”“减小”或“不变”)。
(2)将2 mol C3H6置于体积为1 L的恒容反应器中,反应进行15min时丙烯的转化率与温度的关系如图所示:
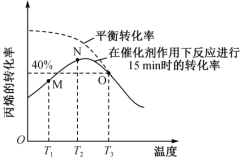
①N点_______ (填“有”或“没有”)达到平衡状态,原因是_______ 。
②M→N过程中C3H6转化率升高的原因是_______ 。
③T3时Kc=_______ ,若其他条件不变,往反应器中再加入2 mol C3H6,反应重新达到平衡时混合体系中乙烯的体积分数为_______ 。
 C2H4(g)+C4H8(g) ∆H。回答下列问题:
C2H4(g)+C4H8(g) ∆H。回答下列问题:(1)向恒温恒容反应器中加入一定量的C3H6,生成C2H4的物质的量与时间的关系如表所示:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| C2H4的物质的量/mol | 0 | 0.8 | 1.2 | 1.5 | a | 1.5 |
①a=
②其他条件不变,若缩小反应器的体积,则C3H6转化率
(2)将2 mol C3H6置于体积为1 L的恒容反应器中,反应进行15min时丙烯的转化率与温度的关系如图所示:

①N点
②M→N过程中C3H6转化率升高的原因是
③T3时Kc=
您最近一年使用:0次
2021-03-21更新
|
212次组卷
|
3卷引用:安徽省江淮名校2020-2021学年高二下学期开学联考化学试题
解题方法
4 . 在密闭容器中,将 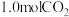 与
与 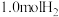 混合加热到800 ℃,发生下列反应:
混合加热到800 ℃,发生下列反应: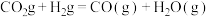 ,一段时间后该反应达到平衡,测得CO的物质的量为
,一段时间后该反应达到平衡,测得CO的物质的量为  。求:
。求:
 达到平衡时
达到平衡时 的体积(标准状况下)
的体积(标准状况下)___ 和该反应的化学平衡常数___ ;
 达到平衡后向该平衡体系中通入
达到平衡后向该平衡体系中通入 水蒸气,达到新的平衡状态时,求
水蒸气,达到新的平衡状态时,求  的物质的量分数。
的物质的量分数。___
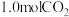 与
与 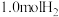 混合加热到800 ℃,发生下列反应:
混合加热到800 ℃,发生下列反应: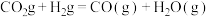 ,一段时间后该反应达到平衡,测得CO的物质的量为
,一段时间后该反应达到平衡,测得CO的物质的量为  。求:
。求: 达到平衡时
达到平衡时 的体积(标准状况下)
的体积(标准状况下) 达到平衡后向该平衡体系中通入
达到平衡后向该平衡体系中通入 水蒸气,达到新的平衡状态时,求
水蒸气,达到新的平衡状态时,求  的物质的量分数。
的物质的量分数。
您最近一年使用:0次
5 . 已知反应2CH3OH(g)=CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
(1)比较此时正、逆反应速率的大小:v(正)____ v(逆)(填“>”“<”或“=”)。
(2)若加入CH3OH后,经10min反应达到平衡,此时CH3OH的转化率__ ,该时间内反应速率v(CH3OH)=____ mol·L-1·min-1。
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
(1)比较此时正、逆反应速率的大小:v(正)
(2)若加入CH3OH后,经10min反应达到平衡,此时CH3OH的转化率
您最近一年使用:0次
6 . 用CO2来生产燃料甲醇是工业上一种有效开发利用CO2的方法。为探究反应原理,进行如下实验,在体积为1 L的恒容密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
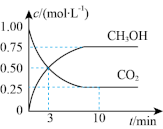
(1)从反应开始到平衡,CO2的平均反应速率v(CO2)=__ mol·L-1·min-1。
(2)氢气的转化率=__ 。
(3)求此温度下该反应的平衡常数K=__ 。
(4)下列措施中能使平衡体系中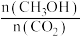 增大的是
增大的是__ 。
A.将H2O(g)从体系中分离出去 B.充入He(g),使体系压强增大
C.升高温度 D.再充入1mol H2
(5)当反应进行到3min末时,下列说法正确的是___ (填字母)。
A.CO和CH3OH(g)的物质的量浓度相等
B.用CO和CH3OH(g)表示的化学反应速率相等
C.上述反应达到平衡状态
D.3 min后该反应的正反应速率逐渐增大
(6)当反应达到平衡时,CO2的物质的量浓度为c1,然后向容器中再加入一定量CO2,待反应再一次达到平衡后,CO2的物质的量浓度为c2,则c1___ c2(填“>”“<”或“=”)。
 CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)从反应开始到平衡,CO2的平均反应速率v(CO2)=
(2)氢气的转化率=
(3)求此温度下该反应的平衡常数K=
(4)下列措施中能使平衡体系中
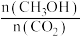 增大的是
增大的是A.将H2O(g)从体系中分离出去 B.充入He(g),使体系压强增大
C.升高温度 D.再充入1mol H2
(5)当反应进行到3min末时,下列说法正确的是
A.CO和CH3OH(g)的物质的量浓度相等
B.用CO和CH3OH(g)表示的化学反应速率相等
C.上述反应达到平衡状态
D.3 min后该反应的正反应速率逐渐增大
(6)当反应达到平衡时,CO2的物质的量浓度为c1,然后向容器中再加入一定量CO2,待反应再一次达到平衡后,CO2的物质的量浓度为c2,则c1
您最近一年使用:0次
7 . 已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g) ==COS(g)+H2O(g),在610K时,将0.1mol CO2加入与0.40molH2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①H2S的平衡转化率a1=_______ %,反应平衡常数K=___________ 。
②在620K重复实验,平衡后水的物质的量分数为003,H2S的转化率a2____ a1,该反应的ΔH___ 0。(填“>”“<”或“=”)
①H2S的平衡转化率a1=
②在620K重复实验,平衡后水的物质的量分数为003,H2S的转化率a2
您最近一年使用:0次



