名校
1 . 把7 molA气体和5 molB气体混合放入2 L密闭容器中,在一定条件下发生反应:3A(g)+B(g)⇌2C(s)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.2 mol·(L·min)-1,求:
(1)B的转化率_______
(2)x的值_______
(3)平衡时压强与初始时压强之比_______
(4)该温度下此反应的平衡常数_______
(1)B的转化率
(2)x的值
(3)平衡时压强与初始时压强之比
(4)该温度下此反应的平衡常数
您最近一年使用:0次
2021-01-06更新
|
1427次组卷
|
6卷引用:山西运城盐湖五中2022-2023学年高二上学期阶段性测试化学试题
山西运城盐湖五中2022-2023学年高二上学期阶段性测试化学试题广东省雷州市第二中学2020-2021学年高二上学期期中考试化学试题吉林省长春市第二十九中学2021-2022学年高二上学期第一学程考试化学试题(已下线)2.2.2 化学平衡常数(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)专题04 可逆反应、化学平衡状态、化学平衡常数【考题猜想】(5大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
解题方法
2 . 在一定温度下,将4.0molSO2与2.0molO2的混合气体充入容积为2L的密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g),经过2min达到平衡状态,SO2的平衡转化率为90.0%。
2SO3(g),经过2min达到平衡状态,SO2的平衡转化率为90.0%。
(1)0~2min内O2的平均反应速率v(O2)=___ 。
(2)该温度下此反应的化学平衡常数的值K=___ 。
(3)在相同温度下,某容器内c(SO2)=c(O2)=c(SO3)=1.0mol·L-1,则此时反应速率v正___ v逆(填“>”、“<”或“=”)。
(4)在一定温度下,下列措施可以提高SO2转化率的是___ (填字母)。
A.增大SO2的浓度
B.容积不变,充入氖气
C.增大O2的浓度
D.容积不变,再充入4.0molSO2与2.0molO2
 2SO3(g),经过2min达到平衡状态,SO2的平衡转化率为90.0%。
2SO3(g),经过2min达到平衡状态,SO2的平衡转化率为90.0%。(1)0~2min内O2的平均反应速率v(O2)=
(2)该温度下此反应的化学平衡常数的值K=
(3)在相同温度下,某容器内c(SO2)=c(O2)=c(SO3)=1.0mol·L-1,则此时反应速率v正
(4)在一定温度下,下列措施可以提高SO2转化率的是
A.增大SO2的浓度
B.容积不变,充入氖气
C.增大O2的浓度
D.容积不变,再充入4.0molSO2与2.0molO2
您最近一年使用:0次
名校
3 . 利用水煤气合成二甲醚( )所涉及的反应如下:
)所涉及的反应如下:
①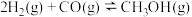 ,平衡常数
,平衡常数 ;
;
② ,平衡常数
,平衡常数 ;
;
③ ,平衡常数
,平衡常数 。
。
(1)总反应 的平衡常数
的平衡常数
_____________ (用 、
、 、
、 表示)。
表示)。
(2)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施有_________ (填字母代号)。
a.加压 b.加入催化剂 c.增大H2的浓度 d.增加CO的浓度 e.分离出二甲醚
(3)已知反应② 在某温度下的平衡常数为400。此温度下,在密闭容器中加入
在某温度下的平衡常数为400。此温度下,在密闭容器中加入 ,反应到某时刻测得各组分的浓度如下:
,反应到某时刻测得各组分的浓度如下:
若经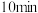 反应达到平衡,则
反应达到平衡,则
__________________________ 。
 )所涉及的反应如下:
)所涉及的反应如下:①
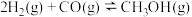 ,平衡常数
,平衡常数 ;
;②
 ,平衡常数
,平衡常数 ;
;③
 ,平衡常数
,平衡常数 。
。(1)总反应
 的平衡常数
的平衡常数
 、
、 、
、 表示)。
表示)。(2)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施有
a.加压 b.加入催化剂 c.增大H2的浓度 d.增加CO的浓度 e.分离出二甲醚
(3)已知反应②
 在某温度下的平衡常数为400。此温度下,在密闭容器中加入
在某温度下的平衡常数为400。此温度下,在密闭容器中加入 ,反应到某时刻测得各组分的浓度如下:
,反应到某时刻测得各组分的浓度如下:物质 |
|
|
|
浓度/( |
|
|
|
 反应达到平衡,则
反应达到平衡,则
您最近一年使用:0次
2020-10-11更新
|
137次组卷
|
2卷引用:山西省太原市第五中学校2023-2024学年高二上学期10月月考化学试题
4 . 800K时,将0.1moA(g)和0.2molB(g)充入体积为1L的固定容积反应器中,发生如下反应:A(g)+2B(g)⇌2C(g)+D(g),达到平衡时A的物质的量分数为20%。
(1)求达平衡时B的转化率α(B)_____ 。
(2)求该温度下的平衡常数K______ (分数表示)。
(3)若起始A的分压为10kPa,求Kp(分数表示)_____ 。
(1)求达平衡时B的转化率α(B)
(2)求该温度下的平衡常数K
(3)若起始A的分压为10kPa,求Kp(分数表示)
您最近一年使用:0次
名校
解题方法
5 . T℃ 时,在一容积为 2 L 的恒容密闭容器中加入 2 mol A 和 3 mol B,压强为 P0, 在催化剂存在的条件下进行下列反应:2A(g)+3B(g) ⇌3C(g),2 分钟达到平衡,平衡混合气中 C 的体积分数为 37.5%。 已知该反应某一时刻的瞬时速率计算公式为v正=k正·[A]2·[B]3,v逆=k逆·[C]3,其中 k正、k逆为速率常数。
(1)计算上述条件下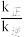 的值。 (写出必要的计算过程,下同)
的值。 (写出必要的计算过程,下同)_____
(2)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数,记作 Kp。已知某气体分压(P分)=气体总压(P总) ×该气体的物质的量分数,计算 T℃ 时上述反应 Kp 的值(用含 P0 的数值表示)。____________
(1)计算上述条件下
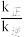 的值。 (写出必要的计算过程,下同)
的值。 (写出必要的计算过程,下同)(2)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数,记作 Kp。已知某气体分压(P分)=气体总压(P总) ×该气体的物质的量分数,计算 T℃ 时上述反应 Kp 的值(用含 P0 的数值表示)。
您最近一年使用:0次
2020-03-27更新
|
348次组卷
|
3卷引用:山西省汾阳市汾阳中学2020-2021学年高二下学期开学考试化学试题
名校
6 . 在压强为0.1MPa、10L恒容的密闭容器中,将2molCO与5molH2的混合气体在催化剂作用下能生成甲醇CO(g)+2H2(g)=CH3OH(g)△H<0请回答下列问题:
(1)该反应的熵变ΔS_________________ 0(填“>”、“<”或“=”).
(2)若温度T2时,5min后反应达到平衡,CO的转化率为75%,则:
①平衡时体系总的物质的量为_________________ mol
②反应的平衡常数K=_________________ ;
③反应0-5min在区间的平均反应速率v(H2)=_________________
(3)向反应器中再分别充入下列气体,能使CO转化率增大的是_________________
A.CO B.H2 C.CH3OH D.He
(1)该反应的熵变ΔS
(2)若温度T2时,5min后反应达到平衡,CO的转化率为75%,则:
①平衡时体系总的物质的量为
②反应的平衡常数K=
③反应0-5min在区间的平均反应速率v(H2)=
(3)向反应器中再分别充入下列气体,能使CO转化率增大的是
A.CO B.H2 C.CH3OH D.He
您最近一年使用:0次
名校
解题方法
7 . 工业上已经实现CO2与H2反应合成甲醇。在一恒温、恒容密闭容器中充入2 mol CO2和6 mol H2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。 请回答:
CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。 请回答:
‘
(1)该密闭容器的容积是______________ L。
(2)达到平衡状态的时刻是_______________ min(填“3”或“10”)。
(3)在前10min内,用CO2浓度的变化表示的反应速率 (CO2)=
(CO2)=_____________ mol/(L·min)。
(4)10min时体系的压强与开始时压强之比为______ 。
(5)该温度下,反应的化学平衡常数数值是____ 。
(6)已知: ① CO(g)+2H2(g) CH3OH(g) ΔH= -90.1 kJ·mol-1 ②CO(g) +H2O(g)
CH3OH(g) ΔH= -90.1 kJ·mol-1 ②CO(g) +H2O(g)  CO2(g)+H2(g) ΔH= -41.1 kJ·mol-1,则CO2与H2反应合成CH3OH(g)的热化学方程式为
CO2(g)+H2(g) ΔH= -41.1 kJ·mol-1,则CO2与H2反应合成CH3OH(g)的热化学方程式为_____ ,反应在10 min内所放出的热量为_____ kJ.
 CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。 请回答:
CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。 请回答:‘

(1)该密闭容器的容积是
(2)达到平衡状态的时刻是
(3)在前10min内,用CO2浓度的变化表示的反应速率
 (CO2)=
(CO2)=(4)10min时体系的压强与开始时压强之比为
(5)该温度下,反应的化学平衡常数数值是
(6)已知: ① CO(g)+2H2(g)
 CH3OH(g) ΔH= -90.1 kJ·mol-1 ②CO(g) +H2O(g)
CH3OH(g) ΔH= -90.1 kJ·mol-1 ②CO(g) +H2O(g)  CO2(g)+H2(g) ΔH= -41.1 kJ·mol-1,则CO2与H2反应合成CH3OH(g)的热化学方程式为
CO2(g)+H2(g) ΔH= -41.1 kJ·mol-1,则CO2与H2反应合成CH3OH(g)的热化学方程式为
您最近一年使用:0次
2019-09-30更新
|
266次组卷
|
3卷引用:山西省古县第一中学2020-2021学年高二上学期期中化学试题
8 . 某温度下,在容积为2L的密闭容器中充入5mol气体A和3mol气体B,发生反应:3A(g)+B(g) 2C(g)+2D(g),5分钟后反应达到平衡状态,测得生成2molD,计算以下量(写出计算过程):
2C(g)+2D(g),5分钟后反应达到平衡状态,测得生成2molD,计算以下量(写出计算过程):
(1)计算A的转化率。
(2)计算该温度下该反应的化学平衡常数。
 2C(g)+2D(g),5分钟后反应达到平衡状态,测得生成2molD,计算以下量(写出计算过程):
2C(g)+2D(g),5分钟后反应达到平衡状态,测得生成2molD,计算以下量(写出计算过程):(1)计算A的转化率。
(2)计算该温度下该反应的化学平衡常数。
您最近一年使用:0次
12-13高二上·黑龙江哈尔滨·期末
9 . 在某温度下,将H2和I2各0.10mol的气态混合物充入l0L的密闭容器中,充分反应,达到平衡后,测得c(H2)=0.0080mol/L。则氢气的转化率为________ ;该温度下,反应的平衡常数为____________ ;已知该反应为放热反应,当降低温度时,反应的平衡常数会_________ (填“变大”、“变小”或“不变”)。
您最近一年使用:0次
2016-12-09更新
|
539次组卷
|
3卷引用:山西省晋中市平遥综合职业技术学校2020-2021学年高二上学期10月月考化学试题
山西省晋中市平遥综合职业技术学校2020-2021学年高二上学期10月月考化学试题(已下线)黑龙江省哈尔滨市第十二中学2012-2013学年高二上学期期末考试化学试卷2016-2017学年黑龙江省鸡西市第十九中学高二上学期期末考试化学试卷


 )
)