解题方法
1 . 已知常温下部分弱电解质的电离常数如表:
回答下列问题:
(1)常温下,物质的量浓度相同的三种溶液:① ②HClO③
②HClO③ ,其pH由大到小的顺序是
,其pH由大到小的顺序是_______ (填序号)。
(2)25℃时, 的NaClO溶液中各离子浓度由大到小的顺序为
的NaClO溶液中各离子浓度由大到小的顺序为_______ 。
(3) 溶液中的电荷守恒关系式为
溶液中的电荷守恒关系式为_______ (用离子浓度表示) 。
(4)热的 溶液可以洗涤油污的原因是
溶液可以洗涤油污的原因是_______ °
(5)25℃时,若测得某 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: 为
为_______ 。
(6)25℃时,若测得某 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: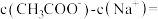
_______ mol/L(列出计算式即可,不需要计算准确值)。
| 弱电解质 | HClO |  |  |  |
| 电离常数 | 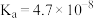 | 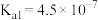 、 、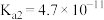 | 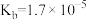 | 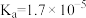 |
(1)常温下,物质的量浓度相同的三种溶液:①
 ②HClO③
②HClO③ ,其pH由大到小的顺序是
,其pH由大到小的顺序是(2)25℃时,
 的NaClO溶液中各离子浓度由大到小的顺序为
的NaClO溶液中各离子浓度由大到小的顺序为(3)
 溶液中的电荷守恒关系式为
溶液中的电荷守恒关系式为(4)热的
 溶液可以洗涤油污的原因是
溶液可以洗涤油污的原因是(5)25℃时,若测得某
 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: 为
为(6)25℃时,若测得某
 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: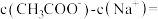
您最近一年使用:0次
2 . 常温下,若在实验室中配制500mL 溶液,为使配制过程中不出现浑浊现象,至少需要
溶液,为使配制过程中不出现浑浊现象,至少需要 的盐酸的体积是
的盐酸的体积是_______ (已知 的
的 为
为 )。
)。
 溶液,为使配制过程中不出现浑浊现象,至少需要
溶液,为使配制过程中不出现浑浊现象,至少需要 的盐酸的体积是
的盐酸的体积是 的
的 为
为 )。
)。
您最近一年使用:0次
名校
解题方法
3 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属化学平衡。根据要求回答问题:
(1)写出工业上用 制备
制备 的化学方程式:
的化学方程式:_______ 。
(2)常温下, 通入
通入 溶液中,所得溶液
溶液中,所得溶液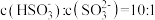 ,则溶液的pH=
,则溶液的pH=_______ (已知 :
: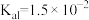 、
、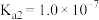 )。
)。
(3)某温度下,水的离子积常数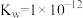 。将此温度下pH=11的
。将此温度下pH=11的 溶液a L与pH=1的b L
溶液a L与pH=1的b L 溶液混合,若所得混合液pH=2,则
溶液混合,若所得混合液pH=2,则
_______ 。
(4)常温下,若在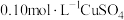 溶液中加入
溶液中加入 稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,
稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,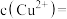
_______  。
。
(1)写出工业上用
 制备
制备 的化学方程式:
的化学方程式:(2)常温下,
 通入
通入 溶液中,所得溶液
溶液中,所得溶液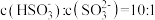 ,则溶液的pH=
,则溶液的pH= :
: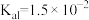 、
、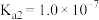 )。
)。(3)某温度下,水的离子积常数
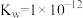 。将此温度下pH=11的
。将此温度下pH=11的 溶液a L与pH=1的b L
溶液a L与pH=1的b L 溶液混合,若所得混合液pH=2,则
溶液混合,若所得混合液pH=2,则
(4)常温下,若在
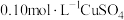 溶液中加入
溶液中加入 稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,
稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,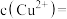
 。
。
您最近一年使用:0次
名校
4 . 根据要求,回答下列问题:
(1)已知甲烷的燃烧热为 ,
,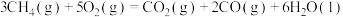
 。写出CO燃烧的热化学方程式:
。写出CO燃烧的热化学方程式:_______ ,若 、
、 键的键能分别为
键的键能分别为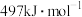 、
、 ,则使1molCO转化为相应的原子时需要的能量是
,则使1molCO转化为相应的原子时需要的能量是_______ ;1mol 按上述方式燃烧时损失的热能是
按上述方式燃烧时损失的热能是_______ (保留1位小数)。
(2)煤的气化反应之一为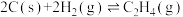

已知:①

②
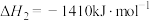
③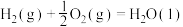

则上述煤的生成 的气化反应的
的气化反应的
_______ 。实际生产中该气化反应需要加入催化剂,其主要原因是_______ (填“速率问题”或“平衡问题”)。
(1)已知甲烷的燃烧热为
 ,
,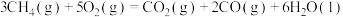
 。写出CO燃烧的热化学方程式:
。写出CO燃烧的热化学方程式: 、
、 键的键能分别为
键的键能分别为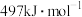 、
、 ,则使1molCO转化为相应的原子时需要的能量是
,则使1molCO转化为相应的原子时需要的能量是 按上述方式燃烧时损失的热能是
按上述方式燃烧时损失的热能是(2)煤的气化反应之一为
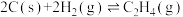

已知:①


②

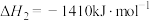
③
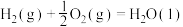

则上述煤的生成
 的气化反应的
的气化反应的
您最近一年使用:0次
2022-12-13更新
|
210次组卷
|
2卷引用:山西省晋城市第二中学校2022-2023学年高二上学期12月月考化学试题
解题方法
5 . 在化学分析中,以AgNO3标准溶液滴定溶液中的Cl-时,采用K2CrO4为指示剂,利用Ag+与CrO 反应生成砖红色沉淀指示滴定终点。当溶液中的Cl-恰好沉淀完全时(浓度等于1.0×10-5mol/L),(已知25℃时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)。求:
反应生成砖红色沉淀指示滴定终点。当溶液中的Cl-恰好沉淀完全时(浓度等于1.0×10-5mol/L),(已知25℃时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)。求:
(1)溶液中c(Ag+)=_______ 。
(2)溶液中c(CrO )=
)=_______ (写出具体计算过程)。
 反应生成砖红色沉淀指示滴定终点。当溶液中的Cl-恰好沉淀完全时(浓度等于1.0×10-5mol/L),(已知25℃时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)。求:
反应生成砖红色沉淀指示滴定终点。当溶液中的Cl-恰好沉淀完全时(浓度等于1.0×10-5mol/L),(已知25℃时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)。求:(1)溶液中c(Ag+)=
(2)溶液中c(CrO
 )=
)=
您最近一年使用:0次
解题方法
6 . 在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。
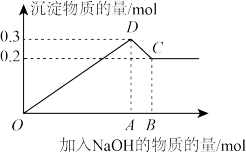
(1)写出下列线段内发生反应的离子方程式:
OD段__________________ 。
CD段__________________ 。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为____________ 。
(3)图中C点表示当加入__________ mol NaOH时,Al3+已经__________ ,Mg2+已经________ 。

(1)写出下列线段内发生反应的离子方程式:
OD段
CD段
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为
(3)图中C点表示当加入
您最近一年使用:0次
2022高三·全国·专题练习
7 . 哈伯合成氨在较高温度下以氢气做氢源,氢气可由天然气制备。CH4(g)+H2O(g) CO(g)+3H2(g)。如表列出了几种化学键的键能:
CO(g)+3H2(g)。如表列出了几种化学键的键能:
298K时,上述反应的ΔH=____ 。
 CO(g)+3H2(g)。如表列出了几种化学键的键能:
CO(g)+3H2(g)。如表列出了几种化学键的键能:| 化学键 | H—H | C—H | H—O | C≡O |
| 键能kJ/mol | 436 | 413 | 467 | 1072 |
您最近一年使用:0次
8 . 依据事实,写出下列反应的热化学方程式。
(1)0.25molC2H5OH完全燃烧生成液态水时放出341.7kJ热量,则表示C2H5OH燃烧热的热化学方程式。___________
(2)工业上用H2和Cl2反应制HCl,各键能为:H﹣H:436 kJ·mol-1,Cl﹣Cl:243 kJ·mol-1,H﹣Cl:431 kJ·mol-1.该反应的热化学方程式是___________ 。
(3)已知①C4H10(g)=C4H8(g)+H2(g) ΔH1
②C4H10(g)+ O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ O2(g)=H2O(g) ΔH3=-242 kJ·mol-1
O2(g)=H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为___________ kJ·mol-1。
(4)已知化学反应N2+3H2 2NH3的能量变化如图所示。
2NH3的能量变化如图所示。
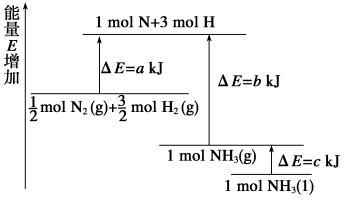
①1 mol N和3 mol H生成1 mol NH3(g)是___________ 能量的过程(填“吸收”或“释放”)。由 mol N2(g)和
mol N2(g)和 mol H2(g)生成1 mol NH3(g)过程
mol H2(g)生成1 mol NH3(g)过程___________ (填“吸收”或“释放”)能量。
② mol N2(g)和
mol N2(g)和 mol H2(g)反应生成1 mol NH3(l)的△H =
mol H2(g)反应生成1 mol NH3(l)的△H = ___________
(1)0.25molC2H5OH完全燃烧生成液态水时放出341.7kJ热量,则表示C2H5OH燃烧热的热化学方程式。
(2)工业上用H2和Cl2反应制HCl,各键能为:H﹣H:436 kJ·mol-1,Cl﹣Cl:243 kJ·mol-1,H﹣Cl:431 kJ·mol-1.该反应的热化学方程式是
(3)已知①C4H10(g)=C4H8(g)+H2(g) ΔH1
②C4H10(g)+
 O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1③H2(g)+
 O2(g)=H2O(g) ΔH3=-242 kJ·mol-1
O2(g)=H2O(g) ΔH3=-242 kJ·mol-1反应①的ΔH1为
(4)已知化学反应N2+3H2
 2NH3的能量变化如图所示。
2NH3的能量变化如图所示。
①1 mol N和3 mol H生成1 mol NH3(g)是
 mol N2(g)和
mol N2(g)和 mol H2(g)生成1 mol NH3(g)过程
mol H2(g)生成1 mol NH3(g)过程②
 mol N2(g)和
mol N2(g)和 mol H2(g)反应生成1 mol NH3(l)的△H =
mol H2(g)反应生成1 mol NH3(l)的△H =
您最近一年使用:0次
2021-10-15更新
|
466次组卷
|
2卷引用:山西运城盐湖五中2022-2023学年高二上学期阶段性测试化学试题
名校
9 . 一定量的Cu与足量浓硫酸混合加热,充分反应后生成2.24LSO2气体(标准状况下),反应后溶液体积为500mL。试计算:
(1)参加反应的Cu的质量___ 。
(2)反应后溶液中CuSO4的物质的量浓度___ 。
(1)参加反应的Cu的质量
(2)反应后溶液中CuSO4的物质的量浓度
您最近一年使用:0次
2021-05-27更新
|
633次组卷
|
4卷引用:2020年山西省普通高中学业水平考试化学试题
10 . 实验室常常用氯化铵与足量熟石灰混合加热制取氨气。现欲制取4.48L(标准状况)氨气,至少需要称取氯化铵的质量是___________ 。
您最近一年使用:0次
2021-05-24更新
|
976次组卷
|
2卷引用:山西省2020年普通高中学业水平考试化学试题



