名校
1 . 在2 L密闭容器中进行反应:mX(g)+nY(g) pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
已知2 min内v(Q)=0.075 mol·L-1·min-1, =0.5
=0.5
(1)试确定以下物质的相关量:起始时n(Y)=___________ ,n(Q)=___________ ;
(2)方程式中m=___________ ,n=___________ ,p=___________ ,q=___________ ;
(3)用Z表示2 min内的反应速率___________ 。
 pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:| 物质 时间 | X | Y | Z | Q |
| 起始/mol | 0.7 | 1 | ||
| 2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3 min末/mol | 0.8 |
 =0.5
=0.5(1)试确定以下物质的相关量:起始时n(Y)=
(2)方程式中m=
(3)用Z表示2 min内的反应速率
您最近一年使用:0次
解题方法
2 . 根据晶胞结构示意图,计算晶胞的体积或密度。
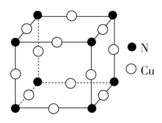
(1)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为____ 。该化合物的相对分子质量为M,NA为阿伏加德罗常数的值。若该晶胞的边长为a cm,则该晶体的密度是______ g·cm-3。
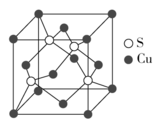
(2)S与Cu形成化合物晶体的晶胞如图所示。已知该晶体的密度为a g·cm-3,则该晶胞中硫原子的个数为______ 的体积为______ cm3(NA表示阿伏加德罗常数的值)。
(1)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为

(2)S与Cu形成化合物晶体的晶胞如图所示。已知该晶体的密度为a g·cm-3,则该晶胞中硫原子的个数为

您最近一年使用:0次
名校
3 . (1)2 mol CO2的质量为____________ g
(2)在标准状况下2 mol O2所占有的体积约为____________ L,含氧原子的物质的量为____________ mol。
(3)1 L 0.2 mol/L的KI溶液中,含溶质KI的物质的量是____________ mol。K+____________ mol
(2)在标准状况下2 mol O2所占有的体积约为
(3)1 L 0.2 mol/L的KI溶液中,含溶质KI的物质的量是
您最近一年使用:0次
2021-05-18更新
|
706次组卷
|
2卷引用:海南省儋州市川绵中学2022-2023学年高二下学期期末考试化学试题
4 . 化学平衡常数只与温度有关,与反应物或生成物的浓度无关。
已知可逆反应:M(g)+N(g) P(g)+Q(g),△H>0
P(g)+Q(g),△H>0
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol·L-1,c(N)=2.4mol·L-1;达到平衡后,M的转化率为60%,此时N的转化率为___ ;
(2)若反应温度升高,M的转化率___ (填“增大”“减小”或“不变”;)
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4mol·L-1,c(N)=amol·L-1;达到平衡后,c(P)=2mol·L-1,a=___ ;
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=1mol•L-1,达到平衡后,M的转化率为___ 。
已知可逆反应:M(g)+N(g)
 P(g)+Q(g),△H>0
P(g)+Q(g),△H>0请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol·L-1,c(N)=2.4mol·L-1;达到平衡后,M的转化率为60%,此时N的转化率为
(2)若反应温度升高,M的转化率
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4mol·L-1,c(N)=amol·L-1;达到平衡后,c(P)=2mol·L-1,a=
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=1mol•L-1,达到平衡后,M的转化率为
您最近一年使用:0次
5 . 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,据此回答:

(1)该反应的化学方程式为______ 。
(2)从开始至2min,X的平均反应速率为______ mol/(L·min)、Z的平均反应速率为______ mol/(L·min)。
(3)改变下列条件,可以加快化学反应速率的有______ 。
A.升高温度
B.减小物质X的物质的量
C.增加物质Z的物质的量
D.减小压强

(1)该反应的化学方程式为
(2)从开始至2min,X的平均反应速率为
(3)改变下列条件,可以加快化学反应速率的有
A.升高温度
B.减小物质X的物质的量
C.增加物质Z的物质的量
D.减小压强
您最近一年使用:0次
解题方法
6 . 根据所学知识,回答下列问题:
(1)标准状况下,1.7 g NH3的体积为___ L;它与标准状况下____ L CH4含有的氢原子数目相同。
(2)等质量的CO和N2所含分子数之比为____ 。
(3)将11.7 g NaCl固体配成10 L溶液,从中取出50 mL,这50 mL溶液中NaCl的物质的量浓度为____ mol·L-1
(4)34 g某二价金属的氯化物中含有0.5 mol Cl-,则该金属氯化物的摩尔质量为_____ g·mol-1,该金属的相对原子质量为_____ 。
(5)已知SO2、O2混合气体的质量共11.2 g,在标准状况下的体积为4.48 L,则混合气体中SO2的物质的量为_____ 。
(1)标准状况下,1.7 g NH3的体积为
(2)等质量的CO和N2所含分子数之比为
(3)将11.7 g NaCl固体配成10 L溶液,从中取出50 mL,这50 mL溶液中NaCl的物质的量浓度为
(4)34 g某二价金属的氯化物中含有0.5 mol Cl-,则该金属氯化物的摩尔质量为
(5)已知SO2、O2混合气体的质量共11.2 g,在标准状况下的体积为4.48 L,则混合气体中SO2的物质的量为
您最近一年使用:0次
名校
解题方法
7 . 将等物质的量的A、B两种气体混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g)。经4 min达到化学平衡。此时测得D的浓度为0.5mol/L,且c(A):c(B)=3:5,C的平均速率为0.125mol/(L·min),则:
(1)此时A的物质的量浓度为_______ ;
(2)B的平均速率为_______ ;
(3)x的值为_______ ;
(4)平衡混合物中C和D的物质的量之比为_______ ;
(5)平衡混合物中D的体积分数为_______ 。
(1)此时A的物质的量浓度为
(2)B的平均速率为
(3)x的值为
(4)平衡混合物中C和D的物质的量之比为
(5)平衡混合物中D的体积分数为
您最近一年使用:0次
2021-02-23更新
|
173次组卷
|
2卷引用:海南省海口市灵山中学2019—2020学年高二上学期期中测试化学试题
8 . 已知一定温度和压强下,在容积为VL的密闭容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g)+ B(g)⇌C(g) ∆H<0。达到平衡时,C的体积分数为40%。试回答有关问题:
(1)升温时,C的反应速率_______ (填“加快”、“减慢”或“不变”);
(2)若平衡时,保持容器容积不变,使容器内压强增大,则平衡_______ ;
A.一定向正反应方向移动 B.一定向逆反应方向移动
C.一定不移动 D.不一定移动
(3)若使温度、压强都保持和题干中的一样不变,在密闭容器中充入2 mol A和2 mol B,则反应达到平衡时:A的转化率为_______ (精确到0.01%),容器的容积为_______ L。
(1)升温时,C的反应速率
(2)若平衡时,保持容器容积不变,使容器内压强增大,则平衡
A.一定向正反应方向移动 B.一定向逆反应方向移动
C.一定不移动 D.不一定移动
(3)若使温度、压强都保持和题干中的一样不变,在密闭容器中充入2 mol A和2 mol B,则反应达到平衡时:A的转化率为
您最近一年使用:0次
9 . 在某温度下,将H2和I2各0.1 mol的气态混合物充入10 L的密闭容器中,发生反应H2(g)+I2(g)⇌2HI(g),连续测定c(I2)的变化,5 s 时测定c(I2)=0.008 0 mol·L-1并保持不变。则:
(1)反应的平衡常数的表达式是K=_______ 。
(2)此温度下,平衡常数值为_______ 。
(3)若在此温度下,在10 L的密闭容器充入0.2 mol HI气体,达到平衡时,HI的转化率为_______ 。
(1)反应的平衡常数的表达式是K=
(2)此温度下,平衡常数值为
(3)若在此温度下,在10 L的密闭容器充入0.2 mol HI气体,达到平衡时,HI的转化率为
您最近一年使用:0次
10 . 在一个10L的恒容密闭容器中,已知SO2与O2的反应: 2SO2(g)+O2(g)  2SO3(g),如果反应开始时充入4mol SO2和2mol O2,5min后反应到达平衡,此时,SO3的浓度是0.2 mol/L,求:
2SO3(g),如果反应开始时充入4mol SO2和2mol O2,5min后反应到达平衡,此时,SO3的浓度是0.2 mol/L,求:
(1)到达平衡时SO2的转化率_______ ?
(2)到达平衡时O2的浓度_______ ?
(3)SO2的反应速率_______ ?
(4)该反应的平衡常数_______ ?
 2SO3(g),如果反应开始时充入4mol SO2和2mol O2,5min后反应到达平衡,此时,SO3的浓度是0.2 mol/L,求:
2SO3(g),如果反应开始时充入4mol SO2和2mol O2,5min后反应到达平衡,此时,SO3的浓度是0.2 mol/L,求:(1)到达平衡时SO2的转化率
(2)到达平衡时O2的浓度
(3)SO2的反应速率
(4)该反应的平衡常数
您最近一年使用:0次



