23-24高二下·全国·课前预习
1 . 某种含C、H、O三种元素的未知物A,经燃烧分析实验测得其中碳的质量分数为52.16%,氢的质量分数为13.14%。则:
(1)氧的质量分数为___________ 。
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈___________ 。
(3)该未知物A的实验式为___________ 。
(1)氧的质量分数为
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈
(3)该未知物A的实验式为
您最近一年使用:0次
23-24高二·全国·假期作业
2 . 已知由C、H、O元素组成的某化合物9.2 g完全燃烧后可以得到17.6 g CO2和10.8 g H2O,通过计算确定该化合物的实验式_______ 。(写出解题过程)
您最近一年使用:0次
23-24高二上·全国·期中
解题方法
3 . 某温度下,在2 L密闭容器中进行反应:mX(g)+nY(g)⇌ pZ(g)+qQ(g),式中m、n、p、q为物质的化学计量数。在0~3 min内,各物质的物质的量变化如表所示:
已知2 min内v(Q)=0.075 mol·L-1·min-1,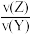 =1/2。
=1/2。
(1)试确定以下物质的相关量:起始时n(Y)=_______ ,n(Q)=_______ 。
(2)化学方程式中m=_______ ,n=_______ ,p=_______ ,q=_______ 。
(3)用Z表示2 min内的反应速率:_______ 。
(4)2 min末Q的转化率为_______ 。
物质 时间 | X | Y | Z | Q |
| 起始/mol | 0.7 | 1 | ||
| 2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3 min末/mol | 0.8 |
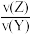 =1/2。
=1/2。(1)试确定以下物质的相关量:起始时n(Y)=
(2)化学方程式中m=
(3)用Z表示2 min内的反应速率:
(4)2 min末Q的转化率为
您最近一年使用:0次
解题方法
4 . 某温度(t℃)时,纯水中c(H+)=1.0×10-6.5mol∙L-1。
(1)则该温度下水的离子积常数KW=___________ ;t℃___________ (填“>”、“<”或“=”) 25℃。
(2)将此温度下pH=12的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为___________ ,溶液中由水电离出的c(H+)=___________ (忽略溶液混合时体积的变化)
(3)室温下,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合后混合液的pH=10,则所用H2SO4溶液与NaOH溶液的体积之比是___________ (忽略溶液混合时体积的变化)。
(1)则该温度下水的离子积常数KW=
(2)将此温度下pH=12的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为
(3)室温下,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合后混合液的pH=10,则所用H2SO4溶液与NaOH溶液的体积之比是
您最近一年使用:0次
解题方法
5 . 一定温度下,向容积为 的密闭容器中通入
的密闭容器中通入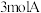 和
和 ,混合气体起始压强为
,混合气体起始压强为 。发生反应:
。发生反应: ,反应进行到
,反应进行到 时测得剩余
时测得剩余 ,此时
,此时 的浓度为
的浓度为 。反应进行到
。反应进行到 时该容器内混合气体总压强为p,5min后反应达到平衡。
时该容器内混合气体总压强为p,5min后反应达到平衡。
(1)x为___________ 。
(2)反应在 内,B的平均反应速率为
内,B的平均反应速率为___________ 。
(3)请用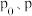 来表示
来表示 时反应物B的转化率为
时反应物B的转化率为___________ 。
(4)在四种不同的条件下测定得到以下反应速率,其中表示的反应速率最快的是___________。
 的密闭容器中通入
的密闭容器中通入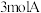 和
和 ,混合气体起始压强为
,混合气体起始压强为 。发生反应:
。发生反应: ,反应进行到
,反应进行到 时测得剩余
时测得剩余 ,此时
,此时 的浓度为
的浓度为 。反应进行到
。反应进行到 时该容器内混合气体总压强为p,5min后反应达到平衡。
时该容器内混合气体总压强为p,5min后反应达到平衡。(1)x为
(2)反应在
 内,B的平均反应速率为
内,B的平均反应速率为(3)请用
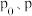 来表示
来表示 时反应物B的转化率为
时反应物B的转化率为(4)在四种不同的条件下测定得到以下反应速率,其中表示的反应速率最快的是___________。
A. | B.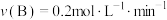 |
C. | D.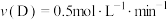 |
您最近一年使用:0次
6 . 计算填空:
(1)在 时,
时, 在
在 中完全燃烧生成
中完全燃烧生成 放出
放出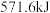 的热量,则
的热量,则 的燃烧热为
的燃烧热为____________________ 。
(2)已知: 的燃烧热为
的燃烧热为 ,
, 和
和 的混合气体
的混合气体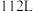 (标准状况下)完全燃烧生成
(标准状况下)完全燃烧生成 和液态水时放出的热量为
和液态水时放出的热量为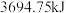 ,则混合气体中
,则混合气体中 和
和 的体积比为
的体积比为____________________ 。
(1)在
 时,
时, 在
在 中完全燃烧生成
中完全燃烧生成 放出
放出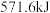 的热量,则
的热量,则 的燃烧热为
的燃烧热为(2)已知:
 的燃烧热为
的燃烧热为 ,
, 和
和 的混合气体
的混合气体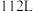 (标准状况下)完全燃烧生成
(标准状况下)完全燃烧生成 和液态水时放出的热量为
和液态水时放出的热量为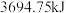 ,则混合气体中
,则混合气体中 和
和 的体积比为
的体积比为
您最近一年使用:0次
解题方法
7 . 顺1,2二甲基环丙烷和反1,2二甲基环丙烷可发生如下转化:

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=_______ 。

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=
您最近一年使用:0次
解题方法
8 . 某些化学键的键能(kJ·mol-1)如下表:
(1)1 mol H2在2 mol Cl2中燃烧,生成2 mol HCl放出的热量为_______ kJ。
(2)在一定条件下,1 mol H2分别与足量的Cl2、Br2、I2完全反应,放出热量由多到少的顺序是_______ 。
| 键 | H—H | Br—Br | I—I | Cl—Cl | H—Cl | H—I | H—Br |
| 键能 | 436 | 193 | 151 | 247 | 431 | 299 | 366 |
(2)在一定条件下,1 mol H2分别与足量的Cl2、Br2、I2完全反应,放出热量由多到少的顺序是
您最近一年使用:0次
解题方法
9 . 以甲烷为原料制取氢气是工业上常用的制氢方法。已知有关化学反应的能量变化如图所示:
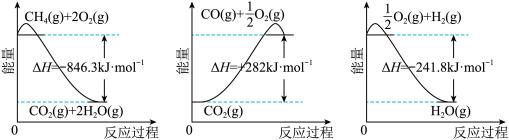
(1)下列说法正确的是___________(填字母)。
(2)CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________ 。

(1)下列说法正确的是___________(填字母)。
| A.CH4的摩尔燃烧焓为846.3 kJ·mol-1 |
| B.CO的摩尔燃烧焓为282 kJ·mol-1 |
| C.H2的摩尔燃烧焓为241.8 kJ·mol-1 |
| D.CO(g)+H2O(g)=CO2(g)+H2(g)为放热反应 |
您最近一年使用:0次
10 . 二甲醚(CH3OCH3)重整制取氢气,具有无毒性、无刺激性等优点,发生反应:CH3OCH3(g)=CO(g)+H2(g)+CH4(g) ΔH。已知部分化学键的键能如下表所示:
计算该反应的ΔH值。_________
| 化学键 | C-H | C-O | H-H | C≡O(CO) |
| 键能/(kJ·mol-1) | 413 | 356 | 436 | 1 075 |
您最近一年使用:0次



