1 . 可逆反应 ⇌
⇌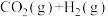 在密闭容器中建立了平衡。当温度为749 K时,
在密闭容器中建立了平衡。当温度为749 K时,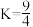 ,问:
,问:
(1)当CO和H2O的起始浓度为2mol/L时,CO的转化率为多少?_____
(2)当CO和H2O的起始浓度分别为2mol/L和6mol/L时,CO的转化率为多少_____
 ⇌
⇌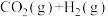 在密闭容器中建立了平衡。当温度为749 K时,
在密闭容器中建立了平衡。当温度为749 K时,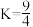 ,问:
,问:(1)当CO和H2O的起始浓度为2mol/L时,CO的转化率为多少?
(2)当CO和H2O的起始浓度分别为2mol/L和6mol/L时,CO的转化率为多少
您最近一年使用:0次
2 . 化学反应2SO2(g)+O2(g) 2SO3(g)是硫酸制造工业的基本反应。将0.050 mol SO2(g)和0.030mol O2(g)注入体积为1.0L的密闭反应器,并置于某较高温度下的恒温环境中,达化学平衡后,测得反应器中有0.040 mol SO3(g),求该温度下反应的平衡常数及SO2、O2的平衡转化率
2SO3(g)是硫酸制造工业的基本反应。将0.050 mol SO2(g)和0.030mol O2(g)注入体积为1.0L的密闭反应器,并置于某较高温度下的恒温环境中,达化学平衡后,测得反应器中有0.040 mol SO3(g),求该温度下反应的平衡常数及SO2、O2的平衡转化率________ 。
 2SO3(g)是硫酸制造工业的基本反应。将0.050 mol SO2(g)和0.030mol O2(g)注入体积为1.0L的密闭反应器,并置于某较高温度下的恒温环境中,达化学平衡后,测得反应器中有0.040 mol SO3(g),求该温度下反应的平衡常数及SO2、O2的平衡转化率
2SO3(g)是硫酸制造工业的基本反应。将0.050 mol SO2(g)和0.030mol O2(g)注入体积为1.0L的密闭反应器,并置于某较高温度下的恒温环境中,达化学平衡后,测得反应器中有0.040 mol SO3(g),求该温度下反应的平衡常数及SO2、O2的平衡转化率
您最近一年使用:0次
3 . 830 K时,在密闭容器中发生下列可逆反应: CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH<0 。请回答下列问题:
(1)若起始时c(CO) =2 mol·L-1,c(H2O) =3 mol·L-1,4 s后达到平衡,此时CO的转化率为60%,则在该温度下,该反应的平衡常数K=____ ;用H2O表示的化学反应速率为_____ 。
(2)在相同温度下,若起始时c(CO) =1 mol·L-1,c(H2O) =2 mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,此时v(正)______ v(逆) (填“大于”“小于”或“等于”)。
(3)若降低温度,该反应的K值可能为______ 。
a.1 b.2 c.0.5
(1)若起始时c(CO) =2 mol·L-1,c(H2O) =3 mol·L-1,4 s后达到平衡,此时CO的转化率为60%,则在该温度下,该反应的平衡常数K=
(2)在相同温度下,若起始时c(CO) =1 mol·L-1,c(H2O) =2 mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,此时v(正)
(3)若降低温度,该反应的K值可能为
a.1 b.2 c.0.5
您最近一年使用:0次
名校
4 . (1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式: ___________ 。
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应N2+3H2 2NH3 △H=a kJ·mol-1。试根据表中所列键能数据计算a 的数值:
2NH3 △H=a kJ·mol-1。试根据表中所列键能数据计算a 的数值:__________ 。
(3)以CO作还原剂与磷石膏反应,不同反应温度下可得到不同的产物。向盛有CaSO4的真空恒容密闭容器中充入CO,且c初始(CO)=1×10-4mol·L-1,反应体系起始总压强为0.1a MPa, 1150℃下,反应:CaSO4(s) + CO(g) CaO(s) + CO2(g) + SO2(g)达到平衡时, CO的转化率为80%,该反应的压强平衡常数Kp=
CaO(s) + CO2(g) + SO2(g)达到平衡时, CO的转化率为80%,该反应的压强平衡常数Kp=________ MPa(用含a的代数式表示;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;忽略副反应)。
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
已知反应N2+3H2
 2NH3 △H=a kJ·mol-1。试根据表中所列键能数据计算a 的数值:
2NH3 △H=a kJ·mol-1。试根据表中所列键能数据计算a 的数值:(3)以CO作还原剂与磷石膏反应,不同反应温度下可得到不同的产物。向盛有CaSO4的真空恒容密闭容器中充入CO,且c初始(CO)=1×10-4mol·L-1,反应体系起始总压强为0.1a MPa, 1150℃下,反应:CaSO4(s) + CO(g)
 CaO(s) + CO2(g) + SO2(g)达到平衡时, CO的转化率为80%,该反应的压强平衡常数Kp=
CaO(s) + CO2(g) + SO2(g)达到平衡时, CO的转化率为80%,该反应的压强平衡常数Kp=
您最近一年使用:0次
2019-11-03更新
|
129次组卷
|
2卷引用:河北省张家口市宣化区宣化第一中学2020-2021学年高二上学期10月月考化学试题
名校
5 . 已知可逆反应: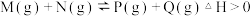 ,请回答下列问题:
,请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为: ,
,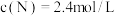 ;达到平衡后,M的转化率为
;达到平衡后,M的转化率为 ,求此时N的转化率
,求此时N的转化率____ 。
(2)若反应温度不变,反应物的起始浓度分别为: ,
,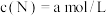 ,达到平衡后,
,达到平衡后,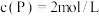 ,求a的值
,求a的值____ 。
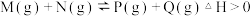 ,请回答下列问题:
,请回答下列问题:(1)在某温度下,反应物的起始浓度分别为:
 ,
,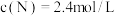 ;达到平衡后,M的转化率为
;达到平衡后,M的转化率为 ,求此时N的转化率
,求此时N的转化率(2)若反应温度不变,反应物的起始浓度分别为:
 ,
,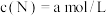 ,达到平衡后,
,达到平衡后,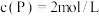 ,求a的值
,求a的值
您最近一年使用:0次
名校
6 . 已知2A2(g)+B2(g) 2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为wmol·L-1,放出热量bkJ。
2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为wmol·L-1,放出热量bkJ。
(1)a________ b(填“>”“=”或“<”)。
(2)该反应的平衡常数表达式为________ ,若将反应温度升高到700 ℃,该反应的平衡常数将________ (填“增大”“减小”或“不变”)。
(3)能说明该反应已经达到平衡状态的是________ 。
a.v(C)=2v(B2) b.容器内压强保持不变 c.v逆(A2)=2v正(B2) d.容器内的密度保持不变
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是________ 。
a.及时分离出C气体 b.适当升高温度 c.增大B2的浓度 d.选择高效的催化剂
(5)密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g) H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为________ 。
 2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为wmol·L-1,放出热量bkJ。
2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为wmol·L-1,放出热量bkJ。(1)a
(2)该反应的平衡常数表达式为
(3)能说明该反应已经达到平衡状态的是
a.v(C)=2v(B2) b.容器内压强保持不变 c.v逆(A2)=2v正(B2) d.容器内的密度保持不变
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是
a.及时分离出C气体 b.适当升高温度 c.增大B2的浓度 d.选择高效的催化剂
(5)密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g)
 H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为
您最近一年使用:0次
2019-01-07更新
|
454次组卷
|
2卷引用:河北省鸡泽县第一中学2019-2020学年高二12月月考化学试题
名校
7 . (1)800℃时,某密闭容器中存在如下反应:2NO2(g) 2NO(g) + O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的浓度随时间的变化如图曲线I所示
2NO(g) + O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的浓度随时间的变化如图曲线I所示
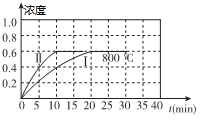
①反应Ⅱ相对于反应I而言,改变的条件可能是_______________ .
②800℃时,若开始时向容器中同时加入1mol/LNO、0.2mol/LO2、0.5mol/L NO2,则v正____________ v逆(填“<”、“>”或“=”)
(2)已知N2O4(g) 2NO2(g)△H=+57.20kJ/mol,t min时,将一定量的NO2、N2O4,充入一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
2NO2(g)△H=+57.20kJ/mol,t min时,将一定量的NO2、N2O4,充入一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
①c(X)代表__________ (填化学式)的浓度,该反应的平衡常数K=_____________ 。
②前10min内用NO2浓度变化表示的反应速率为___________ ,20min时改变的条件是_____________ ;重新达到平衡时,NO2的质量分数___________________ 。
a.增大b.减小
c.不变d.无法判断
 2NO(g) + O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的浓度随时间的变化如图曲线I所示
2NO(g) + O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的浓度随时间的变化如图曲线I所示
①反应Ⅱ相对于反应I而言,改变的条件可能是
②800℃时,若开始时向容器中同时加入1mol/LNO、0.2mol/LO2、0.5mol/L NO2,则v正
(2)已知N2O4(g)
 2NO2(g)△H=+57.20kJ/mol,t min时,将一定量的NO2、N2O4,充入一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
2NO2(g)△H=+57.20kJ/mol,t min时,将一定量的NO2、N2O4,充入一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/(mol/L) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)(mol/L) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
①c(X)代表
②前10min内用NO2浓度变化表示的反应速率为
a.增大b.减小
c.不变d.无法判断
您最近一年使用:0次
2017-11-30更新
|
120次组卷
|
2卷引用:河北省保定市博野中学2021-2022学年高二上学期11月月考化学试题
2016高二·全国·课时练习
名校
8 . 在一个容积为500 mL的密闭容器中,充入5 mol H2和2 mol CO。在一定温度和一定压强下,发生如下反应:2H2(g)+CO(g) CH3OH(g),经过5 min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2 mol·L-1,求:
CH3OH(g),经过5 min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2 mol·L-1,求:
(1)以H2的浓度变化表示的该反应的速率_____ 。
(2)达到平衡时CO的转化率_____ 。
(3)该温度下的K=_____ 。
 CH3OH(g),经过5 min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2 mol·L-1,求:
CH3OH(g),经过5 min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2 mol·L-1,求:(1)以H2的浓度变化表示的该反应的速率
(2)达到平衡时CO的转化率
(3)该温度下的K=
您最近一年使用:0次
2017-11-27更新
|
1035次组卷
|
5卷引用:河北省石家庄市第二十一中学2022-2023学年高二上学期十月月考化学试题
河北省石家庄市第二十一中学2022-2023学年高二上学期十月月考化学试题(已下线)同步君 选修4 第2章 第3节 化学平衡常数陕西省宝鸡市渭滨中学2020-2021学年度高二上学期期中考试化学试题(已下线)2.2.3 化学平衡常数(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第三节 化学平衡 化学平衡第三课时(化学平衡常数)
9 . T0C时,在一个体积为2L的容器中,A气体和B气体反应反应生成C气体,反应过程中A、B、C浓度变化如图所示.

(1) 写出该反应的方程式:_______________
(2) 计算该温度下该反应的平衡常数:_______________
(3) 已知:K(300℃)>K(350℃),该反应是____________ 热反应.
(4) 0~4分钟时,B的平均反应速率为:_______________
(5) 到达平衡时A的转化率为:_______________
(6) 恒容条件下,下列措施中能使n(A)/n(C)降低的有____________ .
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.

(1) 写出该反应的方程式:
(2) 计算该温度下该反应的平衡常数:
(3) 已知:K(300℃)>K(350℃),该反应是
(4) 0~4分钟时,B的平均反应速率为:
(5) 到达平衡时A的转化率为:
(6) 恒容条件下,下列措施中能使n(A)/n(C)降低的有
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
您最近一年使用:0次
10 . 工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为 计算:
计算:
(1)该条件下N2的平衡转化率______ ;(小数点后保留一位)
(2)该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数
N2(g)+3H2(g)的平衡常数_______ 。(不带单位)
 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为 计算:
计算:(1)该条件下N2的平衡转化率
(2)该条件下反应2NH3(g)
 N2(g)+3H2(g)的平衡常数
N2(g)+3H2(g)的平衡常数
您最近一年使用:0次
2015-11-26更新
|
267次组卷
|
4卷引用:2015-2016学年河北省望都中学高二上学期第二次月考化学试卷



